количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Теория
Применение БАД Уропрофит® при мочекаменной болезни: клиническая лекция
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Урология и Нефрология" №4
- Аннотация
- Статья
- Ссылки
В статье обсуждается место фитотерапии в лечении больных с камнями почек и мочеточников, в том числе при проведении дистанционной литотрипсии. На примере БАД Уропрофит® (производство компании «Экомир») подтверждена эффективность включения препаратов растительного происхождения в комплексную терапию мочекаменной болезни, а также их использования для профилактики мочекаменной болезни и ее инфекционно-воспалительных осложнений.
Комплекс биологически активных веществ, входящих в состав БАД Уропрофит®, обусловливает его противовоспалительное, диуретическое, легкое ощелачивающее, литокинетическое действие. Эффективность применения БАД Уропрофит® подтверждена успешными клиническими исследованиями, проведенными отечественными учеными.
По данным результатов исследований, прием БАД Уропрофит® способствует уменьшению лейкоцитурии и кристаллурии, увеличению суточного диуреза, что положительно влияет на течение воспалительного процесса в мочевых путях и отхождение осколков раздробленных конкрементов. Уропрофит® обладает хорошей переносимостью и может применяться длительно.
В статье обсуждается место фитотерапии в лечении больных с камнями почек и мочеточников, в том числе при проведении дистанционной литотрипсии. На примере БАД Уропрофит® (производство компании «Экомир») подтверждена эффективность включения препаратов растительного происхождения в комплексную терапию мочекаменной болезни, а также их использования для профилактики мочекаменной болезни и ее инфекционно-воспалительных осложнений.
Комплекс биологически активных веществ, входящих в состав БАД Уропрофит®, обусловливает его противовоспалительное, диуретическое, легкое ощелачивающее, литокинетическое действие. Эффективность применения БАД Уропрофит® подтверждена успешными клиническими исследованиями, проведенными отечественными учеными.
По данным результатов исследований, прием БАД Уропрофит® способствует уменьшению лейкоцитурии и кристаллурии, увеличению суточного диуреза, что положительно влияет на течение воспалительного процесса в мочевых путях и отхождение осколков раздробленных конкрементов. Уропрофит® обладает хорошей переносимостью и может применяться длительно.
Мочекаменная болезнь (МКБ) является многофакторным заболеванием и занимает второе место по распространенности после воспалительных заболеваний органов мочевой системы. Инфекция мочевых путей может стать как непосредственной причиной камнеобразования, так и осложнением МКБ. Высокая распространенность МКБ (30–40% всех урологических заболеваний), ее характерное сочетание с хроническими инфекционно-воспалительными заболеваниями почек и верхних мочевых путей, частые рецидивы камнеобразования обусловливают необходимость поиска новых медикаментозных и немедикаментозных средств лечения и профилактики [1].
Дистанционная литотрипсия (ДЛТ), которая сегодня является методом выбора для избавления от камней, позволила значительно сократить число открытых оперативных вмешательств на почке и мочевых путях при МКБ. Вторым по значимости современным малоинвазивным методом удаления конкрементов по праву является контактная литотрипсия (КЛТ). Несмотря на внедрение и совершенствование этих малоинвазивных методов удаления мочевых конкрементов, проблема консервативного лечения мочекаменной болезни остается актуальной.
Нефролитиаз часто осложняется инфекцией мочевых путей, которая усугубляет течение болезни, и может быть патогенетическим фактором возникновения конкрементов и рецидива камнеобразования. Арсенал уроантисептиков огромен, но их длительное постоянное применение ограничивается нежелательными побочными явлениями, дисбактериозом, ростом распространенности резистентных возбудителей, риском развития лекарственной аллергии, сопутствующими заболеваниями, а порой и значительной стоимостью лекарства. В этой связи для лечения уролитиаза и инфекционно-воспалительных заболеваний мочеполовой системы перспективным может быть применение растительных средств и фитопрепаратов, обладающих доказанными мочегонным, противовоспалительным, противомикробным и спазмолитическим свойствами. Давно зарекомендовали себя брусничный лист и брусничный морс, толокнянка, плоды шиповника, хвощ полевой, почечный чай, листья березы, комбинированные препараты Фитолизин, Цистон, Пролит и пр.
Многообразие средств растительного происхождения не исключает настойчивый поиск новых средств и их рациональных эффективных сочетаний. Таким образом, консервативная медикаментозная терапия МКБ должна быть комплексной и включать различные лекарственные препараты, в том числе растительного происхождения [2]. Фитотерапия может способствовать не только стимуляции самостоятельного отхождения конкрементов, но и оптимальному освобождению мочевых путей от осколков раздробленных камней при ДЛТ и КЛТ, а также профилактике обострений мочевой инфекции и нарушений функции почки. С этой целью создаются комплексы растительных средств, обладающие свойствами лекарственных препаратов, которые можно применять в комплексной терапии МКБ и ее инфекционно-воспалительных осложнений. В последнее время наблюдается отчетливая тенденция к широкому применению фитопрепаратов в комплексной литокинетической терапии и профилактике мочевой инфекции с целью сохранения функциональной способности почки после литотрипсии. При терапевтическом и профилактическом использовании весьма эффективны многокомпонентные растительные комплексы и биологически активные добавки к пище (БАД), содержащие биологически активные вещества, относящиеся к разным классам химических соединений и оказывающие комплексное фармакотерапевтическое воздействие на основные звенья патологических процессов при МКБ [3].
Таких препаратов много, но проводить адекватную терапевтическую оценку их эффективности довольно трудно. Причиной этого, прежде всего, является их огромное количество. Известно, что для полноценной жизни организм нуждается в большом количестве (около 600) различных питательных веществ, только немногие из них он может создавать самостоятельно, остальные получает с пищей. Это объясняет популярность потребления биологически активных пищевых добавок в мире. Их регулярно и успешно применяют более 80% населения США, около 90% населения Японии и порядка 65% населения Европы. В целом в развитых странах 70–90% населения применяло растительные препараты хотя бы однажды. Кроме того, в США продажи всех фитопрепаратов составляют ежегодно более 60 млрд долларов. В Африке фитопрепараты составляют 80% торговых марок, применяемых в здравоохранении, в Китае – 50% от общего числа продаж лекарственных средств. Современное здравоохранение справедливо считает, что специальное включение в рацион биологически активных веществ сегодня – насущная необходимость.
В России, по данным агентства «Фармэксперт», количество потребителей БАД за последние несколько лет достигло 20%, а количество зарегистрированных добавок, по разным данным, превысило 80 тысяч. Для того чтобы зарегистрировать в Министерстве здравоохранения России препарат растительного происхождения как лекарственное средство, необходимы значительные денежные средства и определенное, порой весьма продолжительное, время. Регистрация препарата растительного происхождения в качестве биологически активной добавки к пище (БАД) проще. Для этого необходимо представить в Министерство пищевой промышленности документы, подтверждающие, что средство не ядовито, может употребляться в пищу, и получить результаты простых токсикологических тестов, проведения развернутых клинических исследований при этом не требуется. Этим объясняется то, что сегодня для некоторых растительных препаратов понятия «лекарство» и «БАД» весьма относительны и определяют вовсе не их сущность, а путь на аптечный рынок.
Если лекарства химической природы при назначении требуют от врача соблюдения баланса между эффективной лечебной дозой и нежелательными явлениями, то для растительных средств имеется реальная возможность широкого выбора дозы, поскольку они реже обладают побочными действиями. Однако производстворастительных препаратов часто не стандартизовано, поэтому сравнение различных препаратов (торговых марок разных производителей), получаемых из одного и того же сырья, проблематично из-за различий в источниках сырья, способах и процессах экстракции, отсутствия уверенности в том, что активный компонент экстракта в адекватных количествах попадает в конечный продукт процесса, отличий в составе различных партий препарата. Тем не менее сторонники БАД в качестве преимуществ приема препаратов растительного происхождения отмечают:
- естественное «природное» происхождение компонентов;
- относительную безопасность и патогенетический характер фитотерапии;
- отсутствие лекарственных взаимодействий;
- отсутствие необходимости в титровании дозы и коррекции сопутствующей лекарственной терапии;
- стабильное сохранение результата после завершения курса приема;
- возможность самостоятельного применения и относительно невысокую цену.
БАД активно рекламируются, однако эффективность немногих из них оценена в клинических исследованиях.
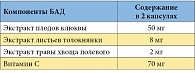
Рассмотрим один из новых фитопродуктов – Уропрофит® – биологически активную добавку к пище, изготовленную на производстве ООО «В-Мин+» по заказу и под контролем компании «Экомир», Россия. В его состав входят (табл.):
- экстракт плодов клюквы (Vaccinium oxycoccos), стандартизованный по органическим кислотам: бензойной, яблочной, Лекции для врачей 26 лимонной, обладающий противовоспалительным, диуретическим, противомикробным и общеукрепляющим действием;
- экстракт листьев толокнянки (Arctostaphylos uva-ursi), стандартизованный по 10% содержанию арбутина, обладающий противовоспалительным, противомикробным и диуретическим действием;
- экстракт хвоща полевого (Equisetum arvense), стандартизованный по 7% содержанию кремния, обладающий мягким спазмолитическим, противомикробным действием, способствующий восстановлению слизистой мочевых путей;
- витамин С (Ac. аscorbinicum) – антиоксидант, повышающий устойчивость тканей к ишемии, увеличивающий диурез.
Экстракты этих растений и витамин С, обладающие выраженными мочегонным и антимикробным свойствами, доказали свою эффективность при многолетнем опыте применения.
Исследования, проводимые в последние годы на основе принципов доказательной медицины, достоверно подтвердили значение экстракта плодов клюквы для профилактики рецидивирования инфекции мочевых путей. Получены новые объективные доказательства того, что применение экстракта плодов клюквы (Vaccinium macrocarpon) в дозиров- ке 36–72 мг/сут эффективно уменьшает частоту рецидивов инфекции нижних мочевых путей у женщин. Установлен доказанный механизм действия экстракта плодов клюквы, который состоит в эффективном блокировании проантоцианидинами (действующим веществом экстракта плодов клюквы) бактериальной адгезии E. coli к клеткам уротелия. Применение экстракта плодов клюквы в дозировке 36–72 мг/сут рекомендуется Европейской ассоциацией урологов (European Association of Urology, EAU) для профилактики инфекции нижних мочевых путей у женщин (Рекомендации EAU, 2011). Экстракт плодов клюквы (Vaccinium oxycoccos) содержит органические кислоты, аскорбиновую кислоту, витамины группы B, флавоновые кислоты, дубильные вещества, тритерпеноиды (урсоловая и олеаноловая кислоты), лейкоантоцианы, филлохинон (витамин K), гликозиды, микроэлементы (железо, марганец, медь, калий, кальций, фосфаты).
Гиппуровая кислота – активный метаболит экстракта ягод клюквы – образуется в печени и в неизмененном виде выделяется почками, оказывая антибактериальный эффект [2]. Исследования, проведенные в эксперименте и в клинике у больных с инфекционно-воспалительными заболеваниями мочевых путей, показали, что гиппуровая кислота в моче пациентов, принимающих экстракт клюквы, достоверно снижает адгезивные свойства патогенной кишечной палочки и ее способность к формированию биопленок на уротелии мочевых путей [4, 5]. Пилотное двойное слепое плацебоконтролируемое исследование антиоксидантного статуса после приема клюквенного сока у здоровых лиц показало достоверное снижение продукции оксидантных протеинов [4]. Именно поэтому ягоды клюквы эффективны при лечении и профилактике мочевой инфекции, а также для предупреждения развития окислительного стресса при агрессивных методах лечения, к которым, в частности, относится литотрипсия. Именно содержанием экстракта плодов клюквы объясняется противовос палительное, мочегонное, противомикробное и общеукрепляющее действие БАД Уропрофит®.
Основными действующими веществами экстракта листьев толокнянки (Arctostaphylos uva-ursi, медвежье ушко) являются фенольные гликозиды, флавоноиды и дубильные вещества, которые обладают противомикробным действием благодаря наличию в экстракте арбутина и метиларбутина. Флавоноиды, содержащиеся в толокнянке, повышают диурез с одновременным выведением из организма ионов натрия и хлора. Активные метаболиты экстракта медвежьего ушка тормозят реабсорбцию мочевой кислоты в почечных канальцах и увеличивают ее растворимость, снижая возможность образования мочевых конкрементов [7]. Гидрохинон – метаболит листьев толокнянки, образующийся в моче при гидролизе арбутина, – обусловливает антибактериальный эффект [8]. Экстракт листьев толокнянки (медвежьего ушка), наряду с экстрактом ягод клюквы, обусловливает противовоспалительное действие БАД Уропрофит®.
Экстракт хвоща полевого (Equisetum arvense) содержит флавоноиды, органические кислоты, магний, кальций, хром, железо, калий, большое количество солей кремниевой кислоты, которые способствуют защите эпителия при воспалении, обеспечивают удаление токсинов из организма, обладают мягким спазмолитическим эффектом, кровоостанавливающим и антисептическим действием [9]. Установлено, что хвощ полевой усиливает и увеличивает диурез у экспериментальных животных [10]. Сравнительные исследования мочегонных средств показало, что он обладает более выраженными диуретическими свойствами, чем диуретин и почечный чай. Исследования, проведенные в I ММИ им. И.М. Сеченова и ГКБ им. С.П. Боткина еще в 1970-е гг., показали увеличение диуреза на 200–500 мл у больных с заболеваниями сердца и почек, принимавших экстракт полевого хвоща [9].
Аскорбиновая кислота (витамин С) – общеизвестный водорастворимый антиоксидант, иммуномодулятор, необходимый для обеспечения неспецифической иммунной защиты и подавления патогенной микрофлоры [10]. Образование свободных радикалов вследствие ишемических/реперфузионных повреждений паренхимы почек во время сеанса ДЛТ ведет к снижению диуреза и окислительному стрессу. Результаты рандомизированного клинического исследования показали, что прием витаминов Е (токоферол) и С в качестве антиоксидантов перед и после сеансов литотрипсии не только значительно снижает повреждение почечной ткани за счет сохранения микроциркуляции, но и уменьшает отек тканей почки и образование медиаторов воспаления. Назначение токоферола и аскорбиновой кислоты до и после ДЛТ повышает устойчивость тканей к ишемии и сохраняет высокий диурез, что стимулирует элиминацию образовавшегося песка и фрагментов конкремента [11–13]. Можно полагать, что комбинация свойств каждого из компонентов комбинированного фитопрепарата Уропрофит® в уменьшенной экстрактивной дозировке позволит получить более высокий терапевтический эффект.
Исследователями ФГБУ «НИИ урологии» Минздравсоцразвития России (В.А. Максимов, Л.А. Ходырева, А.А. Дударева, А.А.Сердюк, 2011) был проведен клинический анализ историй болезни 60 пациентов с МКБ и хроническим пиелонефритом, перенесших ДЛТ, 30 из которых (возраст от 27 до 65 лет) получали в составе противовоспалительной терапии БАД Уропрофит® по 1 капсуле 2 раза в день в течение 30 дней. Группу сравнения составили 30 пациентов 23–67 лет, у которых комплексная терапия данный препарат не включала. В основной группе конкременты (5–12 мм) располагались в почке и лоханочно-мочеточниковом сегменте у 2 больных (6,7%), в верхней трети мочеточника – у 6 (20%), в средней трети – у 4 (13,3%) и нижней трети – у 18 (60%). В группе сравнения ДЛТ проведена больным с размерами конкрементов от 5 до 11 мм, расположенных в почке и лоханочно-мочеточниковом сегменте (у 1 пациента, 3,3%), в верхней (у 7 пациентов, 23,3%), средней (у 6 пациентов, 20%) и нижней (у 16 пациентов, 53,3%) третях мочеточника. Лейкоцитурия до ДЛТ была выявлена у 20 (66,7%) пациентов основной группы и у 18 (60%) больных группы сравнения. Результаты общего анализа мочи у пациентов после 30-дневного приема препарата показали достоверное уменьшение частоты лейкоцитурии у больных, принимавших БАД Уропрофит®, в 1,5 раза – у 11 больных (36,6%), в группе сравнения – у 16 пациентов (53,3%). Применение Уропрофита позволило добиться достоверно более выраженного повышения суточного диуреза у пациентов основной группы.
Кристаллурия была выявлена у 18 (60%) пациентов основной группы до ДЛТ, а после приема Уропрофит® в течение месяца ее частота достоверно снизилась – у 6 пациентов (19,8%). Через 1 месяц после завершения приема препарата частота выявления кристаллурии возросла: кристаллурия определялась у 11 больных (36,7%). У пациентов группы сравнения на протяжении всего периода наблюдения частота кристаллурии сохранялась на уровне 56,6–43,3%. Результаты, полученные авторами, показали исчезновение кристаллурии у пациентов, получавших Уропрофит®, достоверно чаще, чем в группе сравнения. Проведенный авторами анализ результатов клинических и биохимических исследований крови не выявил различий в обеих группах на протяжении 30 дней приема препарата и 1 месяца последующего наблюдения. Ни один из пациентов, принимавших Уропрофит®, не отметил аллергических реакций и побочных эффектов. Полученные данные позволили авторам считать, что комплекс биологически активных веществ, входящих в состав БАД Уропрофит®, оказывает противовоспалительное, диуретическое и литокинетическое действие, и это средство может использоваться как один из компонентов терапии и профилактики инфекционно-воспалительных процессов в мочевых путях у больных МКБ. Уропрофит® хорошо переносится пациентами и поэтому может применяться длительно.
Примером успешного применения БАД Уропрофит® у больных МКБ после ДЛТ могут служить исследования, проведенные в ГБОУ ВПО «Рязанский государственный медицинский университет им. академика И.П. Павлова» под руководством профессора Б.Н. Жиборева (2011). Были обследованы и пролечены 38 больных МКБ в возрасте 20–60 лет. Основную группу составили 20 пациентов (12 мужчин и 8 женщин), им была выполнена ДЛТ, после которой в состав комплексной терапии был включен Уропрофит® по 1 капсуле 2 р/сут в течение 30 дней. Группу сравнения составили 18 пациентов (11 мужчин и 7 женщин), которым после ДЛТ назначали комплексную терапию с добавлением почечного чая. У всех пациентов конкременты (5–20 мм) располагались в чашечно-лоханочной системе. До начала лечения лейкоцитурия более 10 в поле зрения была выявлена в основной группе у 14 (70%) пациентов, в группе сравнения – у 11 (61,1%) больных. Через 5 дней от начала приема Уропрофита в основной группе ее частота снизилась до 8 (40%) больных против 9 (50%) в группе сравнения. Через 30 дней приема Уропрофита она достоверно уменьшилась до 4 (20%) пациентов в основной группе и 6 (33%) в группе сравнения. Таким образом, исследование продемонстрировало достоверное и быстрое уменьшение количество лейкоцитов в моче у пациентов, принимавших Уропрофит®.
В основной группе авторами установлено умеренное повышение рН мочи с 6,025 ± 0,71 до 6,425 ± 0,56 (6,23%). В группе сравнения увеличение рН было менее значимо: с 5,94 ± 0,70 до 6,03 ± 0,62 (1,49%). Зафиксированный на 5-й день приема Уропрофита подщелачивающий эффект стойко сохранялся на протяжении всего периода приема, что, по-видимому, может играть важную роль в профилактике рецидива конкрементов. Кроме того, на протяжении приема Уропрофита установлено более значительное увеличение суточного диуреза у пациентов основной группы в среднем на 312 мл (с 1190 до 1502 мл/сут), в группе сравнения увеличение составило в среднем всего 91 мл (с 1165 до 1256 мл/сут). Увеличение суточного диуреза и рН мочи, как известно, является важным условием уменьшения кристаллизации литогенных веществ, таких как мочевая кислота, ураты и оксалаты. До начала приема Уропрофита кристаллурия была зафиксирована у 20 пациентов (11 больных в основной группе и 9 – в группе сравнения). В основной группе число пациентов с кристаллурией через 5 дней уменьшилось до 8, а через 30 дней – до 4 (55, 40 и 20% соответственно), тогда как в группе сравнения число таких пациентов снизилось незначительно: с 9 до 7 – через 5 дней и через 30 дней увеличилось до 8 (50; 38,9 и 44,5% соответственно). Ни у кого из 20 пациентов на протяжении всего периода приема Уропрофита не было зафиксировано ни одного нежелательного побочного эффекта и аллергической реакции.
Ученые из ГБОУ ВПО «Башкирский государственный медицинский университет» Минздрав-соцразвития РФ (2011) провели обследование с использованием клинических, инструментальных и лабораторных методов 52 пациентов с МКБ до и после КЛТ. 28 пациентов, составивших основную группу, в течение 3 недель до операции принимали Уропрофит® по 1 капсуле 2 р/сут. 24 пациента были включены в группу сравнения. Целью исследования было изучение влияния БАД Уропрофит® на показатели водно-электролитного и азотистого обмена пациентов с уретеролитиазом после контактной литотрипсии. Как известно, после КЛТ увеличивается экскреция электролитов и продуктов азотистого обмена, возрастает способность канальцев разводить и концентрировать мочу. Эти изменения, вероятнее всего, обусловлены только внутрипочечными механизмами, поскольку основные гормональные системы, регулирующие водно-электролитный обмен, существенно не меняют параметры своего функционирования. При использовании в качестве предоперационной подготовки БАД Уропрофит® суточная экскреция осмотически активных веществ снижается в меньшей степени, что свидетельствует об уменьшении канальцевой дисфункции в результате окклюзии мочеточника конкрементом. После операции рост маркеров канальцевого повреждения незначителен, возможно, в результате уменьшения дооперационного негативного влияния мочевой гипертензии на паренхиму почки. Полученные данные позволяют авторам рекомендовать в течение 3 недель перед контактной уретеролитотрипсией прием БАД Уропрофит® с целью снижения дисбаланса экскреторных функций нефрона и снижения повреждения почечной ткани во время операции.
По данным проведенных исследований, критериями эффективности БАД Уропрофит® у пациентов с МКБ можно считать уменьшение выраженности лейкоцитурии и кристаллурии, увеличение суточного диуреза, что говорит о положительном влиянии фитопрепарата на течение воспалительного процесса в мочевых путях и отхождение осколков раздробленных конкрементов. Комплекс биологически активных веществ, входящих в состав БАД Уропрофит®, оказывает противовоспалительное, диуретическое, легкое ощелачивающее, литокинетическое действие, уменьшает кристаллообразование при урати оксалурии, что может быть одной из мер профилактики МКБ и ее инфекционно-воспалительных осложнений. Уропрофит® обладает хорошей переносимостью и может применяться длительно. Природные вещества растительного происхождения, как правило,отличаются широким спектром терапевтического действия и малой токсичностью, что обусловливает возможность их длительного применения. Отечественное лекарственное производство сегодня оснащено современным оборудованием, позволяющим выпускать качественные растительные препараты, проходящие тщательный многократный контроль. Появление комбинированных фитопрепаратов в удобной форме для приема внутрь способствует рациональному использованию растительного сырья, позволяет осуществлять стандартизацию средств как на стадии изготовления, так и получения конечного продукта, что существенно повышает точность дозирования и практического применения. Кроме того, выбор фитопрепаратов отечественных производителей позволит снизить зависимость России от импортных лекарственных препаратов, а российским компаниям, используя полученную прибыль, разрабатывать новые, инновационные лекарства.
1. Борисов В.В., Дзеранов Н.К. Мочекаменная болезнь. Терапия больных камнями почек и мочеточников. М., 2011. 87 с.
2. Дзеранов Н.К., Константинова О.В., Москаленко С.А., Бешлиев Д.А. Роль фитотерапии в пред- и послеоперационном периоде у больных уролитиазом // Урология. 2005. № 2. С. 18–20.
3. Маркарян А.А. Теоретическое и экспериментальное обоснование разработки профилактических средств, рекомендуемых при заболеваниях мочеполовой системы, и их стандартизация: дис. … д-ра фарм. наук. М., 2005. 344 с.
4. Valentova K., Stejskal D., Bednar P. et al. Biosafety, antioxidant status, and metabolites in urine after consumption of dried cranberry juice in healthy women: a pilot double-blind placebo-controlled trial // J. Agric. Food Chem. 2007. Vol. 55. № 8. P. 3217–3224.
5. Risco E., Miguélez C., Sánchez de Badajoz E., Rouseaud A. Effect of american cranberry (Cysticlean) on Escherichia coli adherence to bladder epithelial cells. In vitro and in vivo study // Arch. Esp. Urol. 2010. Vol. 63. № 6. P. 422–430.
6. Башмурин А.Ф. Фармакологическое исследование галеновых и новогаленовых препаратов толокнянки // Сборник научных трудов Ленинградского института усовершенствования врачей. Л., 1951. С. 174–177.
7. Турова А.Д. Лекарственные растения СССР и их применение. М.: Медицина, 1974. 218 с.
8. Сырчина А.И., Воронков М.Г., Тюкавкина Н.А. Апигенин – гликозид из Equisetum arvense // Химия природн. соедин. 1974. № 5. С. 666.
9. Основина-Ломовицкая А.Д. К испытанию мочегонного действия хвоща полевого Equisetum arvense и зимолюбки Chimofilla umbellata // Сборник научно-исследовательских работ по новым лекарственным растениям Сибири. Вып. 2. Томск, 1946. С. 118– 120.
10. Al-Awadi K.A., Kehinde E.O., Loutfi I. et al. Treatment of renal calculi by lithotripsy: minimizing short-term shock wave induced renal damage by using antioxidants // Urol. Res. 2008. Vol. 36. № 1. P. 51–60.
11. Печерский А.В., Александров В.П., Гулямов С.М. Способ профилактики осложнений дистанционной ударно-волновой литотрипсии. Патент 2179438. Санкт-Петербургская медицинская академия последипломного образования. 20.02.2002.
12. Biri H., Oztürk H.S., Büyükkoçak S. et al. Antioxidant defense potential of rabbit renal tissues after ESWL: protective effects of antioxidant vitamins // Nephron. 1998. Vol. 79. № 2. P. 181–185.
13. Борисов В.В. Оригинальные лекарственные препараты и их дженерики // Материалы I Конгресса урологов Сибири. Кемерово, 2012. С. 37.
Новости на тему
17.02.2023
08.12.2022
12.09.2022 01:00:00
СТАТЬИ по теме
07.07.2023
19.10.2022
Отправить статью по электронной почте
Ваш адрес электронной почты:
В статье обсуждается место фитотерапии в лечении больных с камнями почек и мочеточников, в том числе при проведении дистанционной литотрипсии. На примере БАД Уропрофит® (производство компании «Экомир») подтверждена эффективность включения препаратов растительного происхождения в комплексную терапию мочекаменной болезни, а также их использования для профилактики мочекаменной болезни и ее инфекционно-воспалительных осложнений.
Комплекс биологически активных веществ, входящих в состав БАД Уропрофит®, обусловливает его противовоспалительное, диуретическое, легкое ощелачивающее, литокинетическое действие. Эффективность применения БАД Уропрофит® подтверждена успешными клиническими исследованиями, проведенными отечественными учеными.
По данным результатов исследований, прием БАД Уропрофит® способствует уменьшению лейкоцитурии и кристаллурии, увеличению суточного диуреза, что положительно влияет на течение воспалительного процесса в мочевых путях и отхождение осколков раздробленных конкрементов. Уропрофит® обладает хорошей переносимостью и может применяться длительно.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.