количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Теория
Дефицит железа у подростков и его коррекция препаратами железа
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Педиатрия" №1 (3)
- Аннотация
- Статья
- Ссылки
- English
Диагностика и коррекция железодефицитных состояний остаются актуальной проблемой практической педиатрии. В статье представлены данные о распространенности и особенностях клинических проявлений, диагностики и лечения дефицита железа у подростков. Отмечено особое значение диеты и важность правильного выбора железосодержащего препарата для коррекции дефицита железа у подростков.
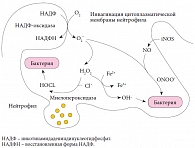
Рис. 1. Участие железа в работе иммунных клеток
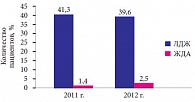
Рис. 2. Частота анемии и латентного дефицита железа среди воспитанниц Пансиона Министерства обороны РФ по итогам диспансеризации за два года
![Рис. 3. Механизм действия железа (III) гидроксид-полимальтозного комплекса [адаптировано из: «Монография по препарату Мальтофер», Vifor International]](/upload/resize_cache/iblock/3e7/195_350_1/3e739753189f9dd3bd90d76f498784b2.jpg)
Рис. 3. Механизм действия железа (III) гидроксид-полимальтозного комплекса [адаптировано из: «Монография по препарату Мальтофер», Vifor International]
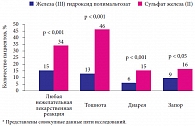
Рис. 4. Частота нежелательных явлений у пациентов при приеме препарата железа (III) гидроксида полимальтозата в сравнении с сульфатом железа (II)
![Рис. 5. Влияние терапии железа (III) гидроксидом полимальтозатом и поливитаминами в течение 4–6 месяцев на средние баллы коэффициента интеллекта (IQ) у 30 детей в возрасте от 6 до 12 лет с ЖДА [28]](/upload/resize_cache/iblock/5a6/195_350_1/5a66a2407466bde95ddc226c27f550fd.jpg)
Рис. 5. Влияние терапии железа (III) гидроксидом полимальтозатом и поливитаминами в течение 4–6 месяцев на средние баллы коэффициента интеллекта (IQ) у 30 детей в возрасте от 6 до 12 лет с ЖДА [28]
![Рис. 6. Среднее изменение баллов тестов для оценки памяти у 120 подростков в возрасте от 15 до 18 лет через 8 месяцев терапии [29]](/upload/resize_cache/iblock/1b6/195_350_1/1b6418478156d32a4d3f12ddf3a3c283.jpg)
Рис. 6. Среднее изменение баллов тестов для оценки памяти у 120 подростков в возрасте от 15 до 18 лет через 8 месяцев терапии [29]
![Рис. 7. Среднее изменение баллов тестов для оценки интеллекта и успеваемости у 120 подростков в возрасте от 15 до 18 лет через 8 месяцев терапии [29]](/upload/resize_cache/iblock/e88/195_350_1/e880feafde6ada0241ebc03b66385ed9.jpg)
Рис. 7. Среднее изменение баллов тестов для оценки интеллекта и успеваемости у 120 подростков в возрасте от 15 до 18 лет через 8 месяцев терапии [29]
![Таблица 1. Биохимические критерии диагностики железодефицитных состояний у подростков [17]](/upload/resize_cache/iblock/d73/195_350_1/d733742c76315ab234fd9ef89a384a3f.jpg)
Таблица 1. Биохимические критерии диагностики железодефицитных состояний у подростков [17]
![Таблица 2. Суточная потребность в железе для детей и подростков в РФ [23]](/upload/resize_cache/iblock/ccb/195_350_1/ccbf42283f26e805fcf7b26feefaade5.jpg)
Таблица 2. Суточная потребность в железе для детей и подростков в РФ [23]
![Таблица 3. Форма выпуска и содержание элементарного железа в препарате железа (III) гидроксида полимальтозата (Мальтофер) [31]](/upload/resize_cache/iblock/7ad/195_350_1/7ade17bce4f412c767caa792bad2e317.jpg)
Таблица 3. Форма выпуска и содержание элементарного железа в препарате железа (III) гидроксида полимальтозата (Мальтофер) [31]
Во-вторых, у подростков имеются повышенные потребности в железе ввиду ускоренных темпов роста (пубертатный «скачок» роста). В-третьих, для этой возрастной группы характерны различные заболевания, сопровождающиеся повышенными потерями железа, – глистные и паразитарные инвазии, эрозивно-язвенные заболевания желудка и двенадцатиперстной кишки, частые носовые кровотечения, травмы, хирургические вмешательства, обильные менструации и т.д. [11]. Дефицит железа, как явный, так и скрытый, имеет негативные последствия для здоровья ребенка. Железо входит в состав не только гема, но и многих ферментных систем организма (ферменты системного и клеточного аэробного метаболизма, окислительно-восстановительного гомеостаза) (рис. 1). Уменьшение количества железа в организме (в тканевых депо, сыворотке крови, костном мозге) приводит к нарушению образования гемоглобина и развитию гипохромной анемии, а также возникновению трофических расстройств в различных тканях [12, 13].
Дефицит железа у ребенка способствует задержке физического, нервно-психического, полового развития, возникновению когнитивных нарушений, провоцирует формирование синдрома хронической усталости, иммунологической недостаточности, нарушает работу желез внутренней секреции, увеличивает всасывание тяжелых металлов, особенно свинца [14, 15]. Несмотря на то что подростки входят в группу риска по развитию дефицита железа, ЖДА у них диагностируется нечасто, что связано, в первую очередь, с неспецифическим характером клинических проявлений дефицита железа. К клиническим проявлениям дефицита железа относятся бледность кожных покровов и слизистых оболочек, трофические нарушения волос и ногтей, ангулярный стоматит, извращение вкуса, пристрастия к необычным запахам, мышечная слабость, астено-вегетативные проявления, повышенная заболеваемость вирусными инфекциями [11]. Обнаружение у подростка подобных симптомов должно вызвать у врача подозрение на дефицит железа, для подтверждения которого необходимо провести ряд лабораторных исследований.
Классическим лабораторным признаком анемии является снижение концентрации гемоглобина, затем – числа эритроцитов и величины гематокрита. Согласно рекомендациям ВОЗ (2001), нижняя граница нормы для гемоглобина венозной крови составляет 115 г/л у детей 6–11 лет и 120 г/л у детей старше 12 лет [16]. Для подтверждения железодефицитного характера выявленной анемии необходимо определить показатели транспортного фонда железа: уровень сывороточного железа, общую железосвязывающую способность сыворотки, коэффициент насыщения трансферрина, а также уровень сывороточного ферритина. Определение этих показателей также необходимо в случае подозрения на наличие ЛДЖ. ВОЗ рекомендует использовать биохимические критерии диагностики ЛДЖ и ЖДА [17] (табл. 1). Определение уровня ферритина сыворотки крови является одним из оптимальных методов оценки содержания запасов железа.
Независимо от возраста, критерием истощения тканевых запасов железа считается уровень сывороточного ферритина ниже 10–12 мкг/л [18]. Для диагностики железодефицитных состояний широко используют и другие лабораторные показатели: цветовой показатель, гематокрит, среднее содержание гемоглобина в эритроците, среднюю концентрацию гемоглобина в эритроците, средний объем эритроцитов, показатель анизоцитоза, протопорфирин цинка, ретикулоцитарные индексы, латентную железосвязывающую способность сыворотки [19]. В настоящее время для скрининга железодефицитных состояний у подростков педиатры чаще всего используют оценку клинического анализа крови (уровня гемоглобина, эритроцитов, эритроцитарных индексов и цветового показателя), поскольку биохимические анализы крови достаточно дороги. С целью определения распространенности железодефицитных состояний среди подростков мы провели анализ результатов диспансеризации детей учебного учреждения с круглосуточным пребыванием детей – ФГКОУ «Московский кадетский корпус “Пансион воспитанниц Министерства обороны Российской Федерации”» (далее – Пансион).
Контингент учащихся Пансиона составляют более 700 девочек в возрасте 10–18 лет. Для скрининга железодефицитных состояний среди воспитанниц Пансиона в ходе ежегодной диспансеризации проводится клинический анализ крови. За анемию принимается уровень гемоглобина ниже 120 г/л, косвенным признаком латентного дефицита железа служит сочетание сниженных эритроцитарных индексов (MCV, mean corpuscular volume – средний объем эритроцита, MCH, mean corpuscular hemoglobin – среднее содержание гемоглобина в эритроцитах) и цветового показателя (ниже 0,85) при нормальном уровне гемоглобина. Данные по распространенности ЖДА и ЛДЖ среди учащихся Пансиона представлены на рис. 2. Всем воспитанницам, у которых в ходе диспансеризации были выявлены признаки железодефицитного состояния, было рекомендовано проведение дополнительных лабораторных исследований – проведение биохимического анализа крови с целью определения уровня сывороточного железа, железосвязывающей способности сыворотки крови, уровня ферритина, после чего назначалась терапия препаратами железа.
В дальнейшем проводилось динамическое наблюдение за состоянием здоровья детей, переносимостью препаратов, а также лабораторные исследования по оценке эффективности терапии. Важность активного выявления железодефицитных состояний среди воспитанниц Пансиона связана с несколькими аспектами. Учащиеся Пансиона относятся к группе риска по развитию дефицита железа по многим критериям (подростковый возраст, интенсивный рост, становление менструальной функции, наличие частых дисфункциональных маточных кровотечений). При лечении железодефицитных состояний необходимо придерживаться двух основных направлений: воздействие на причину, которая привела к развитию данной патологии, и восполнение дефицита железа лекарственными железосодержащими препаратами [20]. Для устранения причины дефицита железа необходимо лечить фоновые заболевания (устранять источники кровопотери, расстройства пищеварения, глистные инвазии и т.д.). Поскольку одной из основных причин развития дефицита железа у подростков является алиментарный фактор (недостаточное поступление железа с пищей), необходимо принять меры по коррекции диеты пациента (увеличить потребление мяса как основного продукта питания, содержащего железо).
Основное количество железа (~90%) всасывается в двенадцатиперстной кишке, остальное – в верхних отделах тощей кишки. Количество железа, поступающего в течение суток с пищей, равно примерно 10–12 мг (гемовое в сочетании с негемовым), но лишь десятая его часть (1–1,2 мг) всасывается в кишечнике здорового человека. При железодефицитном состоянии всасывающая поверхность тонкой кишки увеличивается. Установлено, что биодоступность гемового железа в пищевых продуктах более высокая, чем негемовых соединений, и составляет 25–30%. Источниками гемового железа являются гемоглобин и миоглобин в составе продуктов животного происхождения (мясо животных и птицы). В продуктах растительного происхождения (овощи, фрукты, злаки), а также в молоке и рыбе содержится железо в негемовой форме [21, 22]. Рекомендуемые нормы потребления железа (табл. 2) [23] учитывают физиологическую потребность организма и среднюю биодоступность железа из обычного пищевого рациона, которая не превышает 10%.
Диетические рекомендации являются важным дополнением к медикаментозной коррекции сидеропении. Правильный выбор препарата железа, его дозы и длительности лечения для коррекции железодефицитных состояний у подростков – залог эффективности лечения. Важно не только правильно подобрать препарат, определить длительность его приема, но и учесть все возможные побочные эффекты [19]. Важнейшими требованиями к препаратам железа для приема внутрь, применяемым в детской практике, являются хорошая биодоступность, высокая безопасность, наличие различных лекарственных форм, удобных для пациентов всех возрастов, а также характеристики, обеспечивающие хорошую приверженность лечению. Многочисленные исследования, проведенные в нашей стране и за рубежом, показывают, что этим требованиям в наибольшей степени отвечает препарат железа (III) гидроксид-полимальтозный комплекс (Мальтофер) [25, 26, 27]. Благодаря оптимальному соединению железа с полимальтозой механизм действия препарата таков, что практически невозможна передозировка и развитие связанного с ней окислительного стресса [30] (рис. 3).
По данным метаанализа 6 рандомизированных контролируемых исследований [27], железа (III) гидроксид полимальтозат переносится лучше солевых препаратов железа и вызывает меньше нежелательных явлений, чем сульфат железа (II) (рис. 4). Подтверждена высокая эффективность терапии препаратами железа (III) гидроксид-полимальтозного комплекса, в частности, ее влияние на когнитивную функцию у школьников, страдающих ЖДА (рис. 5) [28]. В исследованиях P.B. Devaki и соавт. (2009) показано влияние терапии железа (III) гидроксидом полимальтозатом на показатели памяти (рис. 6) и интеллекта (рис. 7) у подростков с ЖДА [29]. Помимо доказанной эффективности и хорошей переносимости железа (III) гидроксид полимальтозат отличается удобством применения для пациентов, что особенно важно для подростков, так как повышает приверженность терапии, а следовательно, ее эффективность. Препараты железа (III) гидроксида полимальтозата выпускаются в различных лекарственных формах для разных возрастных групп (табл. 3) [31].
Лечебная доза препаратов железа (III) гидроксид-полимальтозного комплекса составляет 5 мг/кг в сутки. Суточная доза может делиться на один или два приема. Длительность курса лечения железодефицитной анемии препаратами железа составляет от 2 до 5 месяцев в зависимости от степени тяжести анемии: при анемии легкой степени – 2 месяца; при анемии средней степени – 3–4 месяца; при анемии тяжелой степени – 4–5 месяцев [31]. Для коррекции латентного дефицита препарат железа назначают в половинной дозе 2,5 мг/кг в сутки, при этом продолжительность курса профилактики составляет 8 недель (или в полной лечебной дозе 5 мг/кг массы тела в сутки – 4 недели). Таким образом, диагностика, лечение и профилактика дефицита железа у подростков имеют особенности, которые необходимо учитывать практикующим педиатрам. Кроме того, подростки входят в группу риска по развитию железодефицитных состояний по целому ряду причин, в связи с чем актуальной задачей является разработка новых программ скрининга железодефицитных состояний у подростков с целью своевременной диагностики и лечения.
1. Feeding and nutrition of infants young children. Guidelines for the WHO European Region, with emphasis on the former Soviet countries. WHO Regional Publications, European Series, #87. WHO. 2000. Updated reprint 2003.
2. Baker R.D., Greer F.R.; Committee on Nutrition American Academy of Pediatrics. Diagnosis and prevention of iron deficiency and iron-deficiency anemia in infants and young children (0-3 years of age) // Pediatrics. 2010. Vol. 126. № 5. P. 1040–1050.
3. Zhu Y.P., Liao Q.K.; Collaborative Study Group for “The Epidemiological Survey of Iron Deficiency in Children in China”. Prevalence of iron deficiency in children aged 7 months to 7 years in China // Zhonghua Er Ke Za Zhi. 2004. Vol. 42. № 12. P. 886–891.
4. Corapci F., Calatroni A., Kaciroti N. et al. Longitudinal evaluation of externalizing and internalizing behavior problems following iron deficiency in infancy // J. Pediatr. Psychol. 2010. Vol. 35. № 3. P. 296–305.
5. Zhu A., Kaneshiro M., Kaunitz J.D. Evaluation and treatment of iron deficiency anemia: a gastroenterological perspective // Dig. Dis. Sci. 2010. Vol. 55. № 3. P. 548–559.
6. Angulo-Barroso R.M., Schapiro L., Liang W. et al. Motor development in 9-month-old infants in relation to cultural differences and iron status // Dev. Psychobiol. 2011. Vol. 53. № 2. P. 196–210.
7. Cotta R.M., Oliveira Fde C., Magalhães K.A. et al. Social and biological determinants of iron deficiency anemia // Cad. Saude Publica. 2011. Vol. 27. Suppl. 2. P. S309–S320.
8. Hay G., Sandstad B., Whitelaw A., Borch-Iohnsen B. Iron status in a group of Norwegian children aged 6–24 months // Acta Paediatr. 2004. Vol. 93. № 5. P. 592–598.
9. Worldwide prevalence of anaemia, 1993–2005: WHO global database on anaemia / Ed. by B. Benoist, E. McLean, I. Egli, M. Cogswell. Geneva: WHO, 2008.
10. Buchanan G.R. Screening for iron deficiency during early infancy: is it feasible and is it necessary? // Am. J. Clin. Nutr. 2009. Vol. 89. № 2. P. 473–474.
11. Коровина Н.А., Заплатников А.Л., Захарова И.Н. Железодефицитные анемии у детей. М., 1999. 56 с.
12. Павлов А.Д., Морщакова Е.Ф., Румянцев А.Г. Эритропоэз, эритропоэтин, железо. М.: ГЭОТАР-Медиа, 2011. 304 с.
13. Анемии у детей: диагностика, дифференциальная диагностика, лечение / Под ред. А.Г. Румянцева и Ю.Н. Токарева. 2-е изд., доп. и перераб. М.: МАКС Пресс, 2004. 216 с.
14. Красильникова М.В. Железодефицитные состояния у подростков: частотные характеристики, структура и вторичная профилактика: дис. ... канд. мед. наук. М., 2006. 92 с.
15. Коровина Н.А., Захарова И.Н., Свинцицкая В.И. Дефицит железа и когнитивные расстройства у детей // Лечащий врач. 2006. № 5. С. 69–71.
16. WHO / NHD. Iron deficiency anaemia. Assessment, prevention and control: a guide for programme managers. Geneva: WHO, 2001.
17. The World Health Report. 22. Screening for Iron Deficiency Anemia – Including Iron Prophilaxis. Recommendation. Geneva: WHO, 1998.
18. DeMaeyer E.M., Dallman P., Gurney J.M. et al. The prevalence of anaemia in the world. Preventing and controlling iron deficiency anaemia through primary health care: a guide for health administrators and programme managers: 5-58.1989. Geneva: WHO, 1989.
19. Тарасова И.С., Чернов В.М. Новые направления в диагностике, лечении и профилактике железодефицитных состояний // Современная педиатрия. 2012. № 2. С. 18–24.
20. Казюкова Т.В., Самсыгина Г.А., Левина А.Л. Проблемы терапии железодефицитной анемии у детей // Педиатрия. 2002. № 6. С. 4–10.
21. Захарова И.Н., Дмитриева Ю.А. Коррекция сидеропении у детей // Вопросы практической педиатрии. 2011. Т. 6. № 2. С. 36–40.
22. Коровина Н.А., Захарова И.Н., Заплатников А.Л., Малова Н.Е. Профилактика и лечение железодефицитных состояний у детей // Педиатрия. 2008. № 1. С. 101.
23. Нормы физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации // Методические рекомендации МР 2.3.1.2432 -08 (от 18 декабря 2008 года). 41 с.
24. Идельсон Л.И. Гипохромные анемии. М.: Медицина, 1981. 190 с.
25. Erichsen K., Ulvik R.J., Grimstad T. et al. Effects of ferrous sulphate and non-ionic iron-polymaltose complex on markers of oxidative tissue damage in patients with inflammatory bowel disease // Aliment. Pharmacol. Ther. 2005. Vol. 22. № 9. P. 831–838.
26. Захарова И.Н., Заплатников А.Л., Малова Н.Е. Выбор препаратов железа для ферротерапии железодефицитной анемии у детей // Русский медицинский журнал. 2003. Т. 11. № 1. С. 38–41.
27. Toblli J.E., Brignoli R. Iron(III)-hydroxide polymaltose complex in iron deficiency anemia / review and meta-analysis // Arzneimittelforschung. 2007. Vol. 57. № 6A. P. 431–438.
28. Agaoglu L., Torun O., Unuvar E. et al. Effects of iron deficiency anemia on cognitive function in children // Arzneimittelforschung. 2007. Vol. 57. № 6A. P. 426–430.
29. Devaki P.B., Chandra R.K., Geisser P. Effects of oral iron(III) hydroxide polymaltose complex supplementation on hemoglobin increase, cognitive function, affective behavior and scholastic performance of adolescents with varying iron status: a single centre prospective placebo controlled study // Arzneimittelforschung. 2009. Vol. 59. № 6. P. 303–310.
30. Geisser P., Müller A. Pharmacokinetics of iron salts and ferric hydroxide-carbohydrate complexes // Arzneimittelforschung. 1987. Vol. 37. № 1A. P. 100–104.
31. Инструкция по медицинскому применению препарата Мальтофер.
Iron deficiency and its treatment with iron preparations in adolescents
I.N. Zakharova,
I.N. Zakharova,
Ye.B. Machneva
State Budgetary Educational Institution for Continuing Professional Education ‘Russian Medical Academy of Postgraduate Education’ of the Ministry of Health of Russia
Contact person: Irina Nikolayevna Zakharova, zakharova-rmapo@yandex.ru
Diagnosis and management of iron deficiency is still a major problem of modern pediatry. The article discusses the data on epidemiology, clinical manifestations, diagnosis and treatment of iron deficiency in adolescents. The authors emphasize the importance of dietary measures and proper choice of iron preparation for the correction of iron deficiency in adolescents.
Key words: adolescents, iron deficiency, iron deficiency anemia, latent iron deficiency, ferritin, erythrocyte indexes, blood color index, iron (III) hydroxide polymaltose complex, therapy
State Budgetary Educational Institution for Continuing Professional Education ‘Russian Medical Academy of Postgraduate Education’ of the Ministry of Health of Russia
Contact person: Irina Nikolayevna Zakharova, zakharova-rmapo@yandex.ru
Diagnosis and management of iron deficiency is still a major problem of modern pediatry. The article discusses the data on epidemiology, clinical manifestations, diagnosis and treatment of iron deficiency in adolescents. The authors emphasize the importance of dietary measures and proper choice of iron preparation for the correction of iron deficiency in adolescents.
Key words: adolescents, iron deficiency, iron deficiency anemia, latent iron deficiency, ferritin, erythrocyte indexes, blood color index, iron (III) hydroxide polymaltose complex, therapy
Новости на тему
СТАТЬИ по теме
05.04.2023
СТАТЬИ этих авторов
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
