Диабетическая полиневропатия: оптимальная фармакотерапия и междисциплинарный подход
- Аннотация
- Статья
- Ссылки
- English
Согласно результатам инструментальных исследований до 95% пациентов с сахарным диабетом (СД) имеют поражение периферической нервной системы [1, 2]. Невропатии, развивающиеся вследствие СД, различаются клинической картиной и патогенезом [1]. В связи с этим выделяют генерализованные, фокальные и мультифокальные формы диабетической невропатии [1, 3]. В свою очередь первую форму принято подразделять на типичную и атипичную диабетическую полиневропатию (ДПН) [4]. К типичной ДПН относится диабетическая дистальная симметричная сенсорномоторная полиневропатия (ДСПН). На ее долю приходится приблизительно 50% случаев ДПН [4, 5]. Основу патогенеза ДСПН составляют нарушения метаболизма и микроциркуляции. Атипичные ДПН – острая болевая невропатия Элленберга, острая болевая невропатия, связанная с нормализацией углеводного обмена [4]. Предполагают, что в основе ее развития лежат другие, в том числе дизиммунные, патогенетические механизмы [6].
В статье рассматриваются диагностика и лечение самой распространенной и наиболее изученной формы ДПН – диабетической дистальной симметричной сенсорномоторной полиневропатии.
Диагностика
Скринингововое обследование на наличие ДСПН рекомендуется проводить всем пациентам с СД: сразу после постановки диагноза СД 2 типа, через пять лет после постановки диагноза СД 1 типа, далее – ежегодно [5]. Оно предполагает проведение тестов, оценивающих поверхностную и глубокую чувствительность: исследование болевой чувствительности (с помощью неврологической иглы), температурной (с помощью тиотерма или пробирок с холодной и теплой водой), вибрационной (с помощью камертона в 128 Гц), тактильной (используются 10 г монофиламента), коленных и ахилловых рефлексов [3].
Выявление симметричных чувствительных нарушений в ногах по результатам более чем одного теста у пациента с длительно текущим СД в 87% случаев свидетельствует о наличии ДСПН [3, 5].
Определение клинического фенотипа полиневропатии – основополагающий этап диагностики. Для ДСПН характерны симметричные нарушения поверхностной чувствительности в ногах, начинающиеся со стоп: онемение, парестезии, боль, жжение. При прогрессировании ДСПН может отмечаться нарушение чувствительности в кистях. Вследствие повреждения волокон глубокой чувствительности снижаются или исчезают ахилловы, при прогрессировании процесса – и коленные рефлексы [5]. Нарушение проприоцептивной чувствительности в ногах может приводить к ощущению неустойчивости при ходьбе, что также рассматривается как признак ДСПН [5, 7]. Мышечная слабость и гипотрофия мышц при ДСПН минимальны или отсутствуют.
По клиническим симптомам, наблюдаемым при осмотре пациентов, может быть рассчитан невропатический индекс [8]. В практической деятельности и клинических исследованиях для определения данного индекса наиболее часто применяются шкалы TSS (Total Symptom Score – Общая оценка симптомов), NSS (Neuropathy Symptom Score – Оценка симптомов невропатии), NISS-LL (Neuropathy Impairment Score Low Limb – Оценка невропатии в нижних конечностях) [5, 7]. Невропатический индекс позволяет оценить тяжесть ДПН и динамику симптомов на фоне проводимого лечения. В практической деятельности оценочные шкалы помогают объективизировать результаты осмотра пациентов. Однако все они основаны на субъективной оценке ощущений пациентами и могут быть малочувствительны для оценки минимальных изменений на фоне проводимого лечения.
Диагноз ДСПН может быть поставлен только по результатам электронейромиографии (ЭНМГ), подтверждающим повреждение чувствительных и в меньшей степени двигательных волокон в дистальных сегментах нервов конечностей [8].
ДПН может дебютировать с поражения тонких волокон, которое не выявляется при ЭНМГ. В этом случае рекомендуется проведение ортостатической пробы или количественного вегетативного тестирования (исследования функции вегетативных волокон), а также количественного сенсорного тестирования (исследование тонких волокон, проводящих болевую и температурную чувствительность) [8].
К информативным методам диагностики повреждения и утраты нервных волокон периферическими нервами относятся исследование плотности интрадермальных нервных волокон, корнеальная конфокальная микроскопия [8, 9]. Первый метод – минимально инвазивная процедура, позволяющая количественно и качественно оценить состояние нервных волокон в эпидермисе. Установлено, что изменение интрадермальных нервных волокон коррелирует со структурной патологией аксонов периферических нервов [8]. Корнеальная конфокальная микроскопия позволяет визуализировать нервы роговицы, поврежденные вследствие СД. Степень повреждения и восстановления нервов роговицы коррелирует со степенью повреждения и восстановления периферических нервов [9]. На это указывают результаты клинического исследования, в котором продемонстрировано значимое уменьшение размера волокон роговичного нерва у пациентов с ДСПН по сравнению с пациентами с СД, но без ДСПН, и здоровыми лицами [10].
Показано также, что в 10% случаев у пациентов с СД наблюдаются полиневропатии недиабетической природы – воспалительные, дизиммунные, дистиреоидные, В12-дефицитные, наследственные [11].
Диагноз ДПН может быть поставлен после исключения других причин поражения периферических нервов.
Лечение
В соответствии с современными представлениями о патогенезе и факторах риска развития ДСПН лечение пациентов должно быть комплексным: сочетать лекарственные и нелекарственные методы. Достижение нормогликемии; образовательные программы; изменение образа жизни, направленное на снижение массы тела и повышение активности пациентов (диета, лечебная гимнастика, повседневная активность), – основополагающие принципы терапии пациентов с СД и ДСПН [3, 5, 12]. В симптоматической фармакотерапии невропатической боли при ДПН достигнуты значительные успехи, однако данная терапия не замедляет процесс повреждения периферических нервов [8, 12]. Патогенетическая фармакотерапия ДСПН на сегодняшний день одна из самых дискутабельных тем неврологической практики. В России среди препаратов, направленных на изменение течения ДСПН, наиболее широко применяются препараты альфа-липоевой кислоты (АЛК), витаминов группы В, комплексы витаминов и метаболически активных веществ [13, 14].
При психологических проблемах, связанных с трудностями принятия пациентом диагноза СД, развитии психических расстройств (депрессии, тревожного расстройства), нарушений сна и наличии невропатической боли при болевой форме ДСПН целесообразно назначение когнитивно-поведенческой терапии (КПТ).
Оптимальный контроль уровня глюкозы в крови
Основополагающая задача в лечении пациентов с ДПН – достижение показателей гликемии, близких к норме. В настоящее время установлено, что нормализация уровня HbA1c должна предшествовать медикаментозной терапии ДПН [5].
Доказано, что поддержание нормального уровня глюкозы в крови у пациентов с СД 1 типа предупреждает развитие как невропатии, так и других микрососудистых осложнений – ретинопатии и нефропатии [15]. В отношении пациентов с СД 2 типа и риска развития ДПН выводы неоднозначны [3, 5, 12]. Результаты одних исследований подтверждают гипотезу о том, что контроль гликемии предупреждает развитие ДСПН, других (их большинство) – ее несостоятельность. Однако, по мнению D. Ziegler и соавт., отрицательные результаты исследований связаны с погрешностями их дизайна [16]. Так, в отличие от крупного исследования по контролю СД 1 типа и его осложнений (DCCT) [17] в шести рандомизированных контролируемых исследованиях по контролю СД 2 типа, включенных в последний метаанализ [18], отмечается более ограниченная оценка ДСПН, при этом в дизайне ни одного из них не была поставлена задача оценить влияние жесткого контроля гликемии на риск развития ДСПН [16]. Превосходство жесткого контроля гликемии над обычным было выявлено в проспективном исследовании UKPDS, однако достоверные положительные результаты отмечались только через 15 лет от начала наблюдения за пациентами с СД 2 типа [19].
Недостаточный гликемический контроль, гипергликемия – предикторы возникновения невропатической боли [20]. В то же время для предупреждения развития и прогрессирования ДСПН только контроля гликемии недостаточно [21].
Изменение образа жизни
Соблюдение диеты, поддержание или достижение нормальной массы тела, лечебная гимнастика, повседневная активность – основные методы нелекарственного лечения СД, предупреждения развития и прогрессирования его осложнений, в частности ДСПН [12]. Данные ряда исследований свидетельствуют о том, что для предупреждения развития осложнений СД целесообразны контроль липидного профиля, массы тела, значений артериального давления, отказ от курения и употребления алкоголя [12].
Фармакотерапия боли
Для симптоматической терапии невропатической боли при болевой форме ДПН применяют ряд препаратов, доказавших свою эффективность в многоцентровых рандомизированных плацебоконтролируемых исследованиях и рекомендованных европейскими и американскими клиническими руководствами [3, 22]:
- антиконвульсанты: прегабалин, габапентин, вальпроат. Роль топирамата продолжает обсуждаться, так как недостаточно данных, подтверждающих его эффективность;
- антидепрессанты: трициклический антидепрессант – амитриптилин, ингибиторы обратного захвата серотонина и норадреналина – венлафаксин и дулоксетин. Применение амитриптилина может быть ограничено в связи с риском развития побочных эффектов, поэтому рекомендуется проводить постепенную титрацию дозы препарата для снижения такового. Эффективность селективных ингибиторов обратного захвата серотонина обсуждается. Согласно результатам ряда исследований пароксетин и циталопрам могут быть эффективны в снижении боли. Флуоксетин не продемонстрировал эффективности в лечении болевой ДПН;
- опиоиды – трамадол;
- крем с капсаицином.
Патогенетическая терапия
Доказано, что одним из ключевых патогенетических механизмов ДПН является оксидативный стресс, приводящий к повреждению эндотелия сосудов и нервных волокон [23]. На сегодняшний день среди всех лекарственных средств, позиционируемых как антиоксиданты, только препараты АЛК имеют доказательную базу клинической эффективности при ДПН [24].
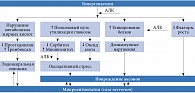
АЛК – липофильный антиоксидант, при введении в организм восстанавливающийся до дигидролипоевой кислоты, которая, в частности, нейтрализует свободные радикалы, супероксиды (рисунок) [6, 25].
Результаты метаанализа клинических исследований подтвердили эффективность АЛК при ДПН в дозе 600 мг/сут в форме внутривенных инфузий в течение трех недель [28]. По итогам совещания экспертов в области лечения ДПН в Торонто в 2009 г., АЛК признана единственным препаратом, который можно отнести к патогенетическим при ДПН [6, 12]. Поэтому обсуждается вопрос внесения АЛК в клинические рекомендации по ведению пациентов с ДПН [26].
Изучение эффективности и безопасности альфа-липоевой кислоты в виде внутривенных инфузий
ALADIN – первое рандомизированное двойное слепое плацебоконтролируемое исследование эффективности АЛК в лечении ДПН при внутривенном введении, проведенное в Германии. Результаты исследования позволили сделать следующий вывод: АЛК – эффективное и безопасное средство для лечения ДПН. Оптимальная терапевтическая доза АЛК – 600 мг/сут, так как доза 1200 мг/сут не повышает эффективность лечения, однако увеличивает риск развития побочных эффектов (головная боль, тошнота, рвота). Шкала TSS является основным инструментом для оценки эффективности лечения препаратами АЛК [27].
ALADIN III – второе исследование эффективности внутривенного введения АЛК при ДПН, проведенное также в Германии. В ходе него установлено, что через три недели лечения статистически значимо снижаются баллы по шкале NIS-LL, выраженность позитивной невропатической симптоматики (боль, жжение, парестезии) и неврологический дефицит [28].
SYDNEY I – рандомизированное двойное слепое плацебоконтролируемое исследование, проведенное в России. Его результаты показали, что на четвертой неделе лечения статистически значимо уменьшается выраженность симптомов ДПН по шкалам TSS и NIS-LL относительно исходных значений.
M.A. Fitzcharles и соавт. подтвердили эффективность трехнедельного курса внутривенного введения АЛК в дозе 600 мг/сут [29].
NATHAN 2 – крупное рандомизированное плацебоконтролируемое исследование, проведенное на базе 33 диабетологических центров США, Канады и Европы. Результаты исследования также продемонстрировали эффективность трехнедельного курса внутривенного введения АЛК [23].
На сегодняшний день остается нерешенным вопрос о длительности эффекта терапии и оптимальной длительности курса внутривенных инфузий препарата [30]. И.А. Строковым и соавт. установлено, что дальнейшее улучшение состояния пациентов наблюдается в течение первого месяца после окончания трехнедельной терапии АЛК, эффект лечения существенно снижается через шесть месяцев [31].
Изучение эффективности альфа-липоевой кислоты в форме таблеток
Внутривенное введение препаратов АЛК возможно не у всех пациентов с СД, например из-за плохого состояния вен, местных кожных реакций или отсутствия у пациентов возможности проводить амбулаторный или стационарный курс инфузий. Поэтому особую актуальность приобретают изучение эффективности таблетированной формы АЛК и оценка целесообразности длительной терапии препаратами АЛК с целью профилактики и прогрессирования ДПН.
Согласно результатам исследований ALADIN II, SYDNEY II, NATHAN 1, применение АЛК в форме таблеток ассоциировалось со статистически значимым уменьшением выраженности симптомов ДПН [31]. Оптимальная доза АЛК – 600 мг/сут.
По данным рандомизированного двойного слепого плацебоконтролируемого исследования NATHAN 1, терапия АЛК в дозе 600 мг/сут в течение четырех лет предупреждает прогрессирование ДПН и развитие синдрома диабетической стопы [32].
В исследовании DEKAN отмечено положительное влияние АЛК на функцию вегетативных волокон, обеспечивающих иннервацию сердца [28].
Эффективность рассматриваемой формы АЛК доказана в ряде зарубежных и российских исследований, однако продолжительность терапевтического эффекта и необходимость длительного приема препарата продолжают обсуждаться [8, 25, 30, 33, 34]. Отмечается необходимость проведения новых рандомизированных плацебоконтролируемых исследований эффективности таблетированных форм АЛК при ДПН с длительным периодом наблюдения за пациентами [33].
Берлитион – препарат альфа-липоевой кислоты: эффективность в лечении диабетической полиневропатии
Берлитион выпускается в форме концентрата для приготовления раствора для инфузий (300 или 600 мг) и таблеток (300 мг). Терапия Берлитионом приводит к значительному снижению выраженности позитивных (боль, жжение, парестезии) и негативных (онемение, гипестезия) симптомов ДПН. Об этом свидетельствуют результаты открытого исследования, включавшего 24 пациента с ДПН [35]. Все пациенты получали терапию препаратом АЛК по следующей схеме: в течение трех недель – 600 мг/сут внутривенно капельно, далее в течение месяца – 600 мг/сут перорально. По окончании лечения достоверная клиническая эффективность (по результатам шкалы TSS) отмечалась у 95,5% участников исследования. Наблюдалась тенденция к улучшению вибрационной чувствительности. Побочные эффекты отмечались у одной пациентки – аллергическая кожная сыпь. При сравнении полученных данных с результатами предыдущих исследований авторы сделали вывод, что более длительный курс (до 20 дней) Берлитиона в виде внутривенных капельных инфузий эффективнее короткого курса инфузий (10 дней). Терапия Берлитионом способствует не только уменьшению невропатических симптомов, но и улучшению показателей функции проведения нервных волокон (по результатам стимуляционной ЭНМГ) [36]. Так, в исследовании, включавшем 27 пациентов с ДПН, наряду с улучшением показателей по шкалам TSS и NIS-LL у 17 (63%) пациентов наблюдалось повышение скорости проведения по чувствительным и двигательным волокнам, у 6 (22%) – нормализация скорости проведения.
При отсутствии изменений в базисной сахароснижающей терапии через 74 дня от начала применения Берлитиона отмечено улучшение биохимических показателей крови – глюкозы, гликированного гемоглобина, общего холестерина.
Улучшение проведения по чувствительным и двигательным волокнам нервов ног на фоне терапии Берлитионом подтверждено и результатами другого отечественного исследования [37].
Оптимальной терапевтической дозой Берлитиона признана доза 600 мг/сут [38]. Рекомендуемая схема лечения Берлитиона: 600 мг/сут внутривенно капельно в течение двух-трех недель, в дальнейшем – 600 мг/сут перорально в течение двух – четырех месяцев [39].
Когнитивно-поведенческая терапия у пациентов с сахарным диабетом 2 типа и его осложнениями
Когнитивно-поведенческая терапия – самый изученный вид психотерапии, который имеет большую доказательную базу эффективности в лечении ряда психических, неврологических, терапевтических заболеваний и широко применяется в клинической практике [40]. Опубликованы результаты свыше 300 контролируемых исследований эффективности КПТ распространенных психических, неврологических и терапевтических расстройств [41].
КПТ рекомендуется для лечения депрессии (уровень рекомендаций А) [42, 43], тревожных расстройств (уровень рекомендаций А) [43], обсессивно-компульсивного расстройства (уровень рекомендаций А) [44], хронического посттравматического стрессового расстройства (уровень рекомендаций А) [45], фибромиалгии (уровень рекомендаций А) [46, 47], хронической неспецифической боли в нижней части спины (уровень рекомендаций А) [48], мигрени (уровень рекомендаций А) [49], головной боли напряжения (уровень рекомендаций С) [21], инсомнии (уровень рекомендаций В) [50, 51] и других заболеваний. В соответствии с результатами крупного статистического исследования, проведенного на базе междисциплинарной клиники лечения болевой ДПН, у двух третей пациентов диагностируются тревожные и/или депрессивные расстройства, 95% пациентов страдают нарушениями сна [12]. Указанные коморбидные расстройства ухудшают течение болевой ДПН, снижают функциональную активность пациентов. Поэтому очевидна практическая значимость применения КПТ у пациентов с болевой ДПН и коморбидными расстройствами.
В соответствии с последними рекомендациями национального руководства США по лечению СД когнитивно-поведенческая терапия считается эффективным поведенческим методом лечения таких пациентов. Она помогает принять болезнь без развития психологических и психических нарушений и следовать рекомендациям врача в отношении изменения образа жизни (уровень рекомендаций А) [52]. С помощью КПТ врач мотивирует пациентов на лечение и поддержание повседневной активности, что улучшает течение заболевания.
Обсуждается эффективность КПТ в лечении невропатической боли при ДСПН. Недавно опубликованы результаты американского пилотного рандомизированного контролируемого исследования, проведенного J.D. Otis и соавт. [53]. В исследование были включены 20 пациентов с болевой ДСПН. Их разделили на две группы: стандартной терапии ДСПН и комбинированной терапии (стандартная терапия ДСПН и КПТ). Период наблюдения за пациентами составил четыре месяца. По результатам работы авторы сделали вывод о том, что добавление КПТ к стандартной терапии ДСПН повышает эффективность проводимого лечения. Так, у пациентов, получавших комбинированное лечение, в достоверно большей степени уменьшались интенсивность боли и ее влияние на повседневную активность.
В мировой практике разработаны и эффективно применяются междисциплинарные программы лечения пациентов с СД, ДПН, сочетанными болевыми синдромами и эмоциональными расстройствами [3, 4]. Междисциплинарный подход предполагает назначение фармакотерапии (СД, невропатической боли, сочетанных расстройств), организацию образовательных программ, проведение КПТ, физиотерапии (лечебной гимнастики).
Заключение
Диагностика ДСПН основывается на клиническом фенотипе полиневропатии, результатах неврологического осмотра и данных ЭНМГ. Количественное сенсорное и вегетативное тестирование – чувствительные методы диагностики повреждения тонких чувствительных и вегетативных волокон периферических нервов. Конфокальная микроскопия – специальный чувствительный метод исследования, который позволяет оценивать состояние нервных волокон роговицы и косвенно нервных волокон периферических нервов.
Оптимальная программа лечения пациентов с СД и ДСПН включает образовательные программы, контроль гликемии, изменение образа жизни, диету, достижение и поддержание нормальной массы тела, поддержание физической активности, отказ от курения, назначение фармакотерапии.
При наличии психологических проблем, связанных с постановкой диагноза СД, и возникновении трудностей с соблюдением рекомендаций по изменению образа жизни показана КПТ.
Добавление КПТ к стандартной терапии болевой ДСПН повышает эффективность патогенетического лечения.
Для симптоматической фармакотерапии невропатической боли при ДСПН применяются антидепрессанты, антиконвульсанты, крем с капсаицином и опиоиды. Однако данные препараты не замедляют процесс повреждения периферических волокон. В России в качестве патогенетической терапии широко применяются препараты АЛК. К данным препаратам относится Берлитион. Эффективность и безопасность терапии АЛК, в частности Берлитионом, основана на результатах большого количества клинических исследований.
V.A. Golovachyova, V.A. Parfyonov
I.M. Sechenov First Moscow State Medical University
Contact person: Veronika Aleksandrovna Golovachyova, xoxo.veronicka@gmail.com
Diabetic distal symmetrical sensorimotor polyneuropathy (DSPN) is the most common complication of peripheral nervous system in diabetes mellitus (DM) impaired metabolism and microcirculation underlie its development. Early diagnostics and proper treatment program for DSPN allow to decrease disability rate, improve patients’ quality of life and increase life expectancy. The major principles of successful management of patients with DM and diabetic polyneuropathy (DPN) rely on reaching optimal blood glucose level, conducting educational programs, changing life style (diet, maintenance or achievement of normal body weight, therapeutic exercises, supporting activities of daily living), administration of therapy for DPN (both pathogenetic and symptomatic therapy) as well as cognitive-behavioral therapy if indicated. Pronounced success was reached in symptomatic treatment of neuropathic pain during DPN, but it does not retard damage of peripheral nerves. A search for pathogenetic pharmacotherapy is continued to efficiently influence on neuropathic symptoms. Drugs containing alpha-lipoic acid are used in Germany and Russia for pathogenetic therapy of DPN, which efficacy and safety was confirmed in a number of clinical studies.