Эффективное лечение диабетической нейропатии комплексным препаратом Кокарнит
- Аннотация
- Статья
- Ссылки
- English


Распространенность сахарного диабета (СД) приобретает угрожающие масштабы. Особую тревогу вызывают осложнения заболевания, приводящие к ранней инвалидизации и смерти пациентов. При СД типа 2 риск развития сердечно-сосудистых осложнений настолько высок, что в настоящее время заболевание относится к группе сердечно-сосудистых [1, 2].
Главная причина развития осложнений – хроническая гипергликемия. Метаболизм глюкозы у больных СД нарушается в результате дефицита инсулина или инсулинорезистентности периферических тканей.
Утилизация глюкозы в инсулинзависимых тканях – печени, жировой ткани, мышцах осуществляется при участии инсулина [3]. Связываясь со специфическим рецептором на поверхности клеточной мембраны, инсулин способствует экспрессии глюкозного транспортера 4 в мышечной и жировой тканях и поступлению глюкозы внутрь клетки.
Инсулиннезависимые ткани (эндотелий, нервная ткань, хрусталик) также используют глюкозу в качестве энергетического материала. Глюкоза в эти ткани поступает беспрепятственно, в частности в нервную ткань – путем диффузии.
Помимо глюкозы нервной клетке необходим кислород [4].
В клетке глюкоза расщепляется до пирувата, который при прохождении цикла Кребса окисляется с образованием аденозинтрифосфата (АТФ). Собственные запасы глюкозы и кислорода в нервной клетке крайне малы, и для ее удовлетворительного функционирования необходимо их постоянное поступление [5].
Метаболизм глюкозы осуществляется и в теле нейрона, и в его отростках, шванновских клетках (миелиновой оболочке). Следовательно, все структуры нервной ткани способны синтезировать АТФ.
Функция нервной клетки заключается в проведении нервного импульса, который зависит от градиента концентрации ионов K+ и Nа+ внутри и вне клетки. АТФ необходима для поддержания активности Nа+/K+-АТФазы – фермента, участвующего в генерации нервного импульса и транспорте ионов против градиента концентрации [6].
Диабетическая нейропатия
Диабетическая нейропатия (ДН) – наиболее частое осложнение СД.
Первая монография, посвященная неврологическим осложнениям СД, вышла в 1864 г. (автор Ш.-Я. Маршал де Кальви) [7], однако клинические описания пациентов с СД и болевым синдромом и парестезиями в нижних конечностях появились уже в 1798 г. [8].
Впервые клиническую классификацию ДН предложил В.М. Прихожан (1981 г.). Он описал центральную и периферическую ДН, острые и хронические нарушения со стороны центральной и периферической нервной системы [9]. В 1998 г. была принята классификация, подразделяющая ДН на доклиническую и клиническую [10].
У пациентов с СД типа 1 клинические проявления диабетической полинейропатии (ДПН) обычно выявляются через пять лет после манифестации заболевания [11, 12]. У больных СД типа 2 – одновременно с диагностированием заболевания. Необходимо отметить, что симптомы периферической ДН наблюдаются у 50–70% пациентов. Однако результаты электромиографического исследования свидетельствуют о наличии заболевания у всех страдающих СД.
Признаками периферической ДН являются жалобы на онемение, боль в ногах, мышечную слабость, зябкость конечностей, парестезии. Симметрично нарушается температурная, тактильная и болевая чувствительность, развивается гипо- и арефлексия. Кроме того, отмечаются трофические нарушения вплоть до язвенных дефектов тканей, нарушение потоотделения, изменение цвета кожных покровов [13].
Большой проблемой для врача и пациента является автономная (висцеральная) ДН [14].
В 1986 г. D.J. Ewing выделил две группы расстройств вегетативной регуляции у больных СД: клинически явные и бессимптомные. Он также показал зависимость продолжительности жизни больных от наличия или отсутствия автономной ДН [15]. Клинические проявления заболевания настолько разнообразны, что часто маскируют истинную причину плохого самочувствия больного.
Наиболее опасная форма автономной ДН – кардиоваскулярная. Для нее характерна синусовая тахикардия, ригидный сердечный ритм, ортостатическая гипотония, безболевые стенокардия и инфаркт миокарда, изменения на электрокардиограмме: депрессия ST, удлинение интервала QT, инверсия зубца Т.
Поздняя диагностика и отсутствие терапии на ранних стадиях становятся причиной инвалидизации и высокой смертности больных СД [16]. Автономная ДН характеризуется множественными дисфункциями желудочно-кишечного тракта: рефлюкс-эзофагитами, дисфагиями, тошнотой, рвотой, атонией желудка и гастропарезом, энтеропатией с усилением моторики кишечника с профузными поносами или стойкими, не поддающимися терапии запорами.
К нарушениям мочеполовой системы при автономной ДН относятся эректильная дисфункция, мочевой рефлюкс, атония мочевого пузыря.
У больных с длительным течением СД на фоне автономной ДН нарушается адреналин-опосредованная клиника гипогликемического состояния: внезапное развитием эпизодов тяжелой гипогликемии [17].
Патогенез
Морфологические изменения нервной ткани у больных СД достаточно специфичны и отмечаются во всех отделах центральной, периферической и вегетативной нервной системы. Они характеризуются уменьшением числа аксонов в нервных стволах. Сначала поражаются более тонкие, безмиелиновые волокна, в дальнейшем происходят истончение и демиелинизация нервных волокон, повреждение шванновских клеток вплоть до полной их дегенерации. Все это приводит к денервации тканей. При этом дегенеративные изменения происходят и в нервных ганглиях, в результате чего уменьшается число клеточных структур [18].
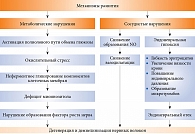
Для адекватного терапевтического воздействия необходимо учитывать механизмы, лежащие в основе указанных изменений. Наиболее доказанными на сегодняшний день являются метаболический и сосудистый (см. рисунок).
В условиях относительного или абсолютного дефицита инсулина и, как следствие, гипергликемии происходит активация полиолового пути – пути утилизации глюкозы в инсулиннезависимых тканях, в том числе нервной. В условиях нормогликемии посредством него утилизируется около 1% глюкозы. При хронической гипергликемии вследствие активации полиолового пути происходит частичное истощение ферментных систем (альдозоредуктазы и сорбитолдегидрогеназы). В результате в нервных клетках накапливается сорбитол, а также происходит каскад метаболических изменений: истощение эндогенного антиоксиданта таурина, усиление аутоокисления глюкозы и накопление кислородосодержащих свободных радикалов.
Нарушение утилизации глюкозы через полиоловый путь, снижение образования АТФ и активности Nа+/K+-АТФазы приводят к накоплению внутриклеточного Nа+ и структурным изменениям нейронов, снижению скорости проведения импульса по миелиновым волокнам.
Вследствие накопления сорбитола снижается поступление миоинозитола в клетку, из которого синтезируется фосфоинозитол – основной регулятор Nа+/K+-АТФазы [19].
Еще одно метаболическое нарушение в условиях гипергликемии –гликирование белков, в частности белковых структур нервного волокна. Гликирование – процесс соединения альдегидной группы углеводной молекулы (глюкозы, фруктозы) и аминогруппы белковой молекулы без участия ферментов.
Гликирование миелина приводит к нарушению проводимости нервного волокна. Гликирование ферментов (альдозоредуктазы, сорбитолдегидрогеназы) – к увеличению энергетического дефицита в нервной клетке.
Помимо метаболических нарушений на развитие нейропатии влияют и изменения эндоневральных капилляров – vasa nervorum. Гипергликемия вызывает эндотелиальную дисфункцию. Механизм – избыточная продукция вазоконстрикторных факторов (эндотелина 1, ангиотензина), подавление синтеза простациклина, оксида азота (NО) – сосудорасширяющих и антиагрегантных факторов.
Роль NО не ограничивается расширением локального участка сосудистого русла. Это вещество способно подавлять пролиферативный ответ гладкомышечных клеток сосудистой стенки, блокировать агрегацию тромбоцитов, окисление липопротеинов низкой плотности, адгезию молекул воспаления на эндотелиальных клетках, продукцию эндотелина и др.
У больных СД отмечается эндотелиальная дисфункция с отложением фибрина, утолщением и фиброзом медии, избыточной продукцией коллагена, фибронектина, ламенина. Указанные изменения приводят к развитию ишемической гипоксии нервов, усилению анаэробного гликолиза с избыточным образованием лактата и сниженным синтезом АТФ.
Современная фундаментальная наука ключевую роль в инициации повреждения эндоневрального кровотока отводит окислительному стрессу. Причинами избыточного образования свободных радикалов считаются гипоксия, снижение антиоксидантной защиты, аутоокисление глюкозы, активация полиолового пути.
Избыточная продукция кислородосодержащих свободных радикалов способствует окислению мембранных липидов в нервных клетках. Мишенью свободных радикалов является и молекула NО, при окислении которой образуется высокотоксичное вещество пироксинитрит (ONOO). Деградация NO усиливается и вследствие повышенного образования супероксидного аниона – продукта окислительного стресса.
При активации полиолового пути у больных СД резко снижается функция эндотелиальной NO-синтазы – фермента, ответственного за синтез NO из L-аргинина.
У здорового человека активность окислительного стресса ограничивается супероксиддисмутазой, каталазой, глутатионпероксидазой, витаминами Е, С, А и восстановленным глутатионом. При гипергликемии снижается активность гликированных ферментов, поэтому превалируют прооксидантные факторы.
В экспериментальной эндокринологии доказана возможность влияния изосорбита нитрата (источник NO) на скорость проведения возбуждения по нервному волокну и улучшение эндоневрального кровотока [5, 20].
Терапия
Результаты исследований UKPDS и DCCT доказали зависимость развития осложнений СД от длительности заболевания и компенсации углеводного обмена [21, 22]. Так, в исследовании DCCT благодаря поддержанию адекватного контроля гликемии прогрессирование ретинопатии снизилось на 54%, риск развития ретинопатии – на 76%, микроальбуминурии – на 39%, нейропатии – на 60%. В исследовании UKPDS снижение гликированного гемоглобина на 1% способствовало уменьшению смертности от СД на 21%, частоты острого коронарного синдрома – на 14%, риска развития микроангиопатии – на 37%, нарушения периферического кровообращения – на 43%. Следовательно, основным условием профилактики и лечения осложнений СД является стойкая компенсация углеводного обмена. Однако при ДПН этого бывает недостаточно.
В терапии ДПН выделяют два направления:
патогенетическое – для восстановления пораженных нервов и улучшения проведения возбуждения в нервных клетках;
симптоматическое – для уменьшения боли.
Кокарнит
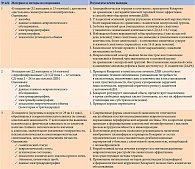
Принимая во внимание четыре составляющих успешной терапии – эффективность, безопасность, комплаентность и удобство в применении, разрабатываются и модернизируются лекарственные препараты, в состав которых входит несколько компонентов. К таким препаратам относится Кокарнит компании World Medcine (ЛП 002839 от 23.01.2015) (табл. 1).
Согласно исследованиям, проведенным в Германии (2015 г.), плазменная концентрация пиридоксальфосфата (активная форма витамина В6) у пациентов с СД достоверно ниже по сравнению с пациентами контрольной группы. При наличии микроальбуминурии этот показатель снижается еще более выраженно.
Дефицит витамина В12 по результатам измерения концентрации голотранскобаламина и метилмалоновой кислоты в плазме крови отмечался реже, чем дефицит витаминов В1 и В6. Он выявлялся у 6,8% пациентов с СД, при наличии микроальбуминурии – у 8,7%.
По данным других исследований (2000, 2003, 2007 гг.), распространенность дефицита витамина В12 среди лиц пожилого возраста составляет от 5 до 40%. У пациентов с СД, особенно пожилого возраста, отмечается высокая частота атрофического гастрита и ассоциированной с ним мальабсорбции кобаламина. Высокий уровень гомоцистеина, обусловленный дефицитом витамина В12, приводит к прогрессированию атеросклероза. В то же время низкий уровень цианокобаламина в сыворотке крови связан с повышением риска когнитивного дефицита в два – четыре раза, особенно у пациентов с частыми гипогликемическими состояниями и неудовлетворительной компенсацией СД.
Согласно результатам многоцентрового рандомизированного плацебоконтролируемого исследования (2012), длительное лечение СД типа 2 метформином ведет к дефициту витамина В12. При этом снижение уровня витамина В12 носит прогрессирующий характер.
Установлено также снижение фолиевой кислоты у пациентов, длительно получавших метформин.
В ряде исследований доказано, что аспирин может уменьшить всасывание витамина В12 в желудочно-кишечном тракте на 55%. Получены данные о развитии мегалобластной анемии на фоне приема ацетилсалициловой кислоты. Именно поэтому уровень витамина В12 необходимо контролировать у всех больных, получающих аспирин более месяца [23].
Таким образом, применение препаратов, содержащих витамины В6 и В12, является обоснованным и целесообразным у пациентов с СД.
В табл. 2 перечислены эффекты компонентов препарата Кокарнит.
Боль является частой жалобой при полинейропатии. Она может быть жгучей или ноющей, хронической или развиться стремительно в течение нескольких недель и даже дней (острая форма). Лидокаин, входящий в состав Кокарнита, помогает купировать болевой синдром.
Эффективность и безопасность Кокарнита доказаны во многих клинических исследованиях, результаты трех из них представлены в табл. 3 [24, 25].
Важно отметить, что при применении препарата Кокарнит не наблюдается покраснения кожных покровов и чувства жара, тахикардии, головокружения, выраженного снижения артериального давления.
Заключение
Лечение ДПН должно быть комплексным. Пациентам показаны сахароснижающие препараты для оптимального контроля гликемии, а также препараты, в состав которых входят компоненты, действующие на разные мишени метаболизма. Речь, в частности, идет о кокарбоксилазе, которая улучшает усвоение глюкозы, трофику нервной ткани, способствует нормализации функции сердечно-сосудистой системы; никотинамиде, который участвует в метаболизме жиров, протеинов, аминокислот, пуринов, тканевом дыхании, гликогенолизе и в отличие от никотиновой кислоты не оказывает выраженного сосудорасширяющего действия, препятствует демиелинизации нерва; цианокобаламине; АТФ, который регулирует энергетический обмен. Все указанные вещества содержатся в препарате Кокарнит.
A.M. Mkrtumyan, S.V. Podachina, Ye.V. Doskina, K.N. Ablina
Moscow State University of Medicine and Dentistry named after A.I. Evdokimov
Russian Medical Academy of Postgraduate Education
Contact person: Ashot Musayelovich Mkrtumyan, vagrashot@mail.ru
It has been proven that as a rule, neuropathy is not an independent disease but is a symptom or manifestation of somatic diseases. Diabetic polyneuropathy (DPN) is the most frequent complication in patients with diabetes mellitus, and the aim of the clinician is the earliest diagnostics of diabetic polyneuropathy, as well as due and early prevention and treatment of DPN. Therapy with combination drug Cocarnit is one of contemporary methods for DPN management.
