Эффективность дазатиниба в качестве второй линии терапии хронического миелолейкоза
- Аннотация
- Статья
- Ссылки
Большая часть событий констатирована в период от 0 до 36 месяцев, в период интенсификации дозы иматиниба. 40% больных ХМЛ остаются резистентными к лечению иматинибом, несмотря на увеличение дозы. Данной группе больных показано назначение ингибиторов тирозинкиназ второго поколения (ИТК-II). Анализ эффективности дазатиниба в качестве второй линии терапии при первичной и вторичной резистентности к иматинибу показал высокий уровень эффективности с наилучшими результатами у больных с ранней сменой ИТК.
Большая часть событий констатирована в период от 0 до 36 месяцев, в период интенсификации дозы иматиниба. 40% больных ХМЛ остаются резистентными к лечению иматинибом, несмотря на увеличение дозы. Данной группе больных показано назначение ингибиторов тирозинкиназ второго поколения (ИТК-II). Анализ эффективности дазатиниба в качестве второй линии терапии при первичной и вторичной резистентности к иматинибу показал высокий уровень эффективности с наилучшими результатами у больных с ранней сменой ИТК.
За последнее десятилетие в связи с широким внедрением таргетной терапии выживаемость больных хроническим миелолейкозом (ХМЛ) значительно увеличилась [1]. В то же время от 31 до 43% больных ХМЛ в хронической фазе, получающих иматиниб, к 12 месяцам лечения не достигают полного цитогенетического ответа (ПЦО) [2, 3]. Резистентность к иматинибу обусловлена многими причинами, ведущими из которых являются мутации гена BCR-Abl, хромосомные аберрации [4, 5]. Исход ХМЛ при резистентности к иматинибу во многом зависит от раннего перевода больных на ингибиторы тирозинкиназ второго поколения (ИТК-II) [6, 7]. В связи с этим актуальным представляется изучение эффективности терапии ИТК-II в широкой клинической практике.
Материалы и методы исследования
Был проведен анализ результатов проспективного наблюдения за лечением 141 больного ХМЛ (хроническая фаза) в Астраханской и Волгоградской областях. Мониторинг и оценка эффективности терапии иматинибом проводились согласно рекомендациям экспертов Европейской сети по борьбе с лейкозом (European Leukemia Net, ELN) 2006 и 2009 гг. Окончательные расчеты проведены с учетом рекомендаций ELN–2009 [7]. Период наблюдения за больными ХМЛ составил 10 лет. Расчет кумулятивной общей беспрогрессивной и бессобытийной выживаемости проведен по методу Каплана – Майера.
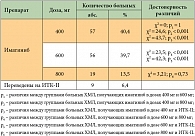
На момент диагностики ХМЛ в хронической фазе заболевания (согласно рекомендациям ELN) назначался иматиниб в дозе 400 мг. При развитии первичной или вторичной резистентности к лечению доза иматиниба была увеличена до 600 мг, а затем до 800 мг. При отсутствии эффекта от максимально допустимой дозы иматиниба (800 мг) назначались ИТК-II (нилотиниб, дазатиниб). На момент окончания исследования дозу 400 мг и 600 мг иматиниба получало почти равное количество больных – 57 (40,4%) и 56 (39,7%) соответственно (р1 > 0,05). Достоверно большее количество больных ХМЛ получали иматиниб в дозе 400 мг – 57 (40,4%) – и 600 мг – 56 (39,7%) – по сравнению с дозой 800 мг – 19 (13,5%) пациентов (р2 < 0,001 и р4 < 0,001 соответственно). Девять (6,4%) больных ХМЛ были переведены на ИТК-II (табл. 1).
Результаты исследования
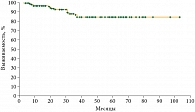
Общая восьмилетняя выживаемость больных ХМЛ в хронической фазе составила 84% (умерло 11,3% больных, 16 из 141). Медиана не достигается. Обращает на себя внимание выход кривой выживаемости на плато после трехлетнего периода (рис. 1).
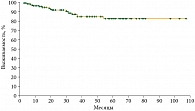
Восьмилетняя выживаемость без прогрессии у больных ХМЛ в хронической фазе равна 83%. Медиана не достигается, прогрессия зафиксирована у 12,1% (17 из 141) больных. Прогрессией считался факт трансформации хронической фазы в фазу акселерации или в бластный криз, смерть больного. Все случаи прогрессирования ХМЛ сосредоточены в период 1–4 года от момента начала терапии иматинибом (рис. 2).
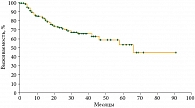
Бессобытийная семилетняя выживаемость у больных ХМЛ составила 45% (события констатированы у 30,5% больных, у 43 из 141). Медиана равна 66 месяцам, 95% доверительный интервал (ДИ) [38; 94]. Событием в настоящем исследовании считались потеря полного гематологического ответа, потеря полного цитогенетического ответа, потеря большого молекулярного ответа (БМО), смерть больного (рис. 3).
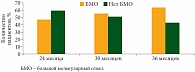
Как видно из рис. 3, большая часть событий зарегистрирована в период от 0 до 36 месяцев. Именно в этот период проходила интенсификация дозы иматиниба (через 36 месяцев только 40% больных ХМЛ получали иматиниб в дозе 400 мг). Это улучшило результаты лечения за счет увеличения глубины ответов – количество пациентов с наличием БМО возросло до 61%. Однако, несмотря на увеличение дозы иматиниба, около 40% больных (39,44%) остаются резистентными к лечению (рис. 4).
Больным ХМЛ, не ответившим на лечение иматинибом, целесообразно как можно раньше (оценивая ответ на терапию по критериям ELN-2009) назначать ИТК-II. В нашем исследовании из 40% больных ХМЛ, нуждающихся в смене терапии, ИТК-II были назначены только 6,4%. В большинстве случаев ИТК-II назначались в качестве «терапии спасения» у больных с прогрессией заболевания, после повышения доз иматиниба до 600 мг и 800 мг. Результаты лечения дазатинибом представлены в табл. 2.
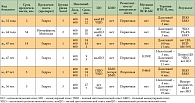
Как следует из анализа данных, представленных в табл. 2, среди больных ХМЛ, переведенных на терапию дазатинибом, преобладали женщины, диагноз ХМЛ которым установлен в возрасте от 32 до 47 лет. Большее количество больных начали лечение иматинибом в первые полгода от диагностики ХМЛ, срок предлеченности у одной больной составил 54 месяца. Срок лечения иматинибом в повышенной дозировке составлял от 37 до 68 месяцев и только у одной больной не превышал 12 месяцев. Преобладали больные с первичной резистентностью к иматинибу. У 2 из 6 больных были обнаружены мутации гена BCR-Abl (подробный клинический анализ больных ХМЛ с обнаруженными мутациями опубликован нами ранее) [8].
Все больные получали дазатиниб в дозе 100 мг. У 2 больных положительный эффект от дазатиниба достигнут через 3 месяца терапии (ПЦО и БМО, ЧЦО и БМО соответственно), у одного больного – через 6 месяцев (ПЦО и БМО). У одной больной ПЦО констатирован через 19 месяцев лечения дазатинибом. У одной пациентки отмечена потеря достигнутого ответа на фоне терапии дазатинибом (ЧЦО). Особо стоит отметить больную с длительной неэффективной терапией иматинибом в течение 69 месяцев и, как возможное следствие этого, отсутствие ответа на терапию дазатинибом (цитогенетическая и молекулярная резистентность).
Выводы
Бессобытийная семилетняя выживаемость у больных ХМЛ в хронической фазе, получавших лечение иматинибом, составила 45%. Большая часть событий констатирована в период от 0 до 36 месяцев, в период интенсификации дозы иматиниба.
40% больных ХМЛ остаются резистентными к лечению иматинибом, несмотря на увеличение дозы. Данной группе больных показано назначение ИТК-II.
Анализ эффективности дазатиниба в качестве второй линии терапии при первичной и вторичной резистентности к иматинибу показал высокий уровень эффективности с наилучшими результатами у больных с ранней сменой ИТК.
