Эффективность препарата Целлекс при использовании с системным тромболизисом при ишемическом инсульте
- Аннотация
- Статья
- Ссылки
- English

Острые нарушения мозгового кровообращения продолжают оставаться одними из наиболее распространенных и тяжелых поражений головного мозга [1–4]. За период 2008–2016 гг. показатель первичной заболеваемости инсультом в России вырос на 24,8%, составив 355,6 случаев на 100 тыс. населения. Вместе с тем благодаря активным мероприятиям по борьбе с сердечно-сосудистой патологией заболеваемость повторным инсультом в нашей стране уменьшилась с 1,09 в 2009 г. до 0,79 новых случаев на 1000 населения в 2014 г. [2]. Общая смертность от цереброваскулярных заболеваний в период с 2003 по 2014 г. снизилась на 39,7% [1, 5], а в период с 2008 по 2016 г. – на 45%, составив 123,0 на 100 тыс. населения.
В России, как и в большинстве стран мира, в структуре острых нарушений мозгового кровообращения преобладает ишемический инсульт (ИИ) [2, 6]. В качестве основных модифицируемых факторов риска ИИ на основании многочисленных проспективных и ретроспективных исследований в настоящее время рассматриваются артериальная гипертензия, гиперлипидемия, атеросклероз, гиперкоагуляция, васкулиты и др. [1, 7]. Знание этиопатогенетических аспектов инсульта, внедрение новых прогрессивных методов лечения заболевания позволяют достичь определенных успехов в решении проблемы острых нарушений мозгового кровообращения.
В ряду наиболее эффективных методов лечения достойное место занимает тромболитическая терапия. Системный тромболизис проводится в первые четыре с половиной часа после развития ИИ путем внутривенного введения тканевого активатора плазминогена (rt-PA, алтеплаза), который на сегодняшний день имеет самый высокий уровень доказательности (класс I, уровень А). Указания на применение метода есть во всех международных и российских клинических рекомендациях по ведению пациентов с ИИ [6, 8–10].
Внедрение тромболитической терапии в практику первичных сосудистых отделений и региональных сосудистых центров основано на данных о механизмах гибели нейронов при острой ишемии. Было показано, что при окклюзии церебральной артерии гибель нейронов происходит катастрофически быстро [11]. Тезис «Time is brain» («Время – мозг») стал своеобразным лозунгом в области тромболитической терапии ИИ [11, 12].
Формирование ядерной зоны ишемии с необратимыми изменениями как результат сложного каскада патобиохимических реакций завершается в течение нескольких минут с момента острого нарушения мозгового кровообращения. Данная область мозга окружена потенциально жизнеспособной зоной ишемической полутени, в которой снижен уровень кровотока, но в целом сохранен энергетический метаболизм и присутствуют только функциональные, но не структурные изменения. В последующие 6–12 часов в зоне ишемической полутени может происходить отсроченная гибель нейронов. Очевидно, что восстановление циркуляции путем реканализации окклюзированной интракраниальной артерии способствует сохранению обратимо поврежденной ткани мозга в зоне пенумбры. Это позволяет уменьшить размеры инфаркта и выраженность неврологического дефицита [6, 11, 12].
Необходимо помнить, что, несмотря на высокую эффективность, тромболитическая терапия может сопровождаться развитием осложнений. Одно из наиболее тяжелых – геморрагическая трансформация инфаркта мозга, которая связана с достижением реканализации и обусловлена развитием острой эндотелиальной дисфункции, реперфузионным повреждением мозга [10, 12].
Логично предположить, что применение алтеплазы в комбинации с тем или иным нейропротектором будет способствовать сохранению жизнеспособности нейронов в пенумбре, позволит расширить диапазон «терапевтического окна» и снизить частоту геморрагических осложнений [13]. Нейропротективная и нейрометаболическая терапия направлена на уменьшение повреждения, которое вызвано патологическими процессами, протекающими в веществе мозга при его ишемическом поражении, а также на активацию процессов нейропластичности и нейрорепарации [1, 14–16].
Именно такими свойствами обладает современный отечественный препарат Целлекс, тканеспецифичный высокомолекулярный белково-полипептидный комплекс с массой протеинов 10–250 кДа, полученный из эмбриональной мозговой ткани поросят. Он содержит более 1200 сигнальных белков и полипептидов, в том числе факторы роста и дифференцировки нервных клеток и сосудов. Препарат обладает как первичным нейропротективным действием, снижая избыток возбуждающих аминокислот, так и вторичным нейропротективным действием, подтвержденным клиническими и экспериментальными исследованиями [17–21]. Активация препаратом вторичной нейропротекции в виде стимуляции редупликации ДНК и деления клеток (нейроны, глия), запуска синаптогенеза, торможения апоптоза путем восстановления сигналов аутофагии, улучшения тканевой иммунорегуляции с торможением иммуногенной цитотоксичности макрофагов, регуляции нейромедиации с торможением спиловера нейротрансмиттеров объясняет его эффективность при ИИ [19].
Для подтверждения вышеизложенной гипотезы было проведено российское проспективное наблюдательное сравнительное исследование в параллельных группах (IV фаза), в котором приняли участие три исследовательских центра (первичные сосудистые отделения и региональный сосудистый центр).
Цель исследования
Определение влияния препарата Целлекс на динамику и сроки восстановления утраченных функций у пациентов с острым ИИ на фоне базисной и тромболитической терапии.
Материал и методы
В исследование включено 60 пациентов с установленным в соответствии с критериями Международной классификации болезней 10-го пересмотра и данными нейровизуализации диагнозом ИИ в системе внутренней сонной артерии и вертебрально-базилярном бассейне независимо от патогенетического подтипа в возрасте от 35 лет (мужчины) и 45 лет (женщины) с гемипарезом/монопарезом или афатическими нарушениями в структуре неврологических нарушений, а также их сочетанием, суммарным баллом по Шкале тяжести инсульта Национального института здоровья США (National Institutes of Health Stroke Scale – NIHSS) не менее 4.
Пациенты разделены на две группы, сопоставимые по возрасту, тяжести инсульта, сосудистому бассейну, в котором произошло нарушение кровообращения, времени с момента развития ИИ, клиническим проявлениям по NIHSS, шкале Глазго, индексу Бартел. Группы различались только по полу: в основной группе было 11 (36,7%) мужчин и 19 (63,3%) женщин, в контрольной – 20 (66,7%) мужчин и 10 (33,3%) женщин (р = 0,038).
Основная группа (n = 30) на фоне стандартизированной базисной терапии получала Целлекс, стерильный раствор для подкожного введения по 0,1 мг один раз в сутки в течение десяти дней. Первая инъекция препарата Целлекс выполнялась перед проведением процедуры тромболизиса.
Контрольная группа (n = 30) получала стандартизированную базисную терапию, согласно действующему федеральному стандарту оказания медицинской помощи для данной группы пациентов.
Всем пациентам основной и контрольной групп проводилась процедура тромболизиса в соответствии с инструкцией по медицинскому применению препарата Актилизе (алтеплаза): внутривенное введение в дозе 0,9 мг/кг, максимально – 90 мг (10% дозы болюсно, последующая инфузия в течение 60 минут).
Для определения эффективности препарата на четырех визитах: визит 0 (в течение «терапевтического окна», до проведения тромболитической терапии), визит 1 (первые сутки от начала заболевания), визит 2 (пятые сутки от начала заболевания) и визит 3 (19-е сутки от начала заболевания) – анализировались следующие показатели:
- частота возникновения геморрагической трансформации (с помощью рентгеновской компьютерной томографии головного мозга до проведения тромболизиса, через 24 часа и на пятые сутки);
- динамика степени выраженности неврологических нарушений по NIHSS;
- динамика степени выраженности нарушений жизнедеятельности по индексу Бартел;
- динамика степени выраженности нарушений жизнедеятельности по модифицированной шкале Рэнкина.
В исследование были включены пациенты преимущественно с ИИ в системе внутренней сонной артерии (n = 46, 76,7%), число пациентов с ИИ в системе вертебрально-базилярного бассейна было значительно меньше – 14 (23,3%). Все пациенты основной и контрольной групп были госпитализированы в стационар в среднем через 1 час 36 минут ± 36 минут (р = 0,210) от появления первых симптомов заболевания. Всем пациентам обеих групп был выполнен системный тромболизис в течение 2 часов 34 минут ± 40 минут от начала инсульта (р = 0,052). Таким образом, группы были сопоставимы по основным показателям. Завершили исследование 57 человек: три пациента из контрольной группы умерли, случаев смерти пациентов в основной группе не было. Вероятно, относить снижение частоты смертельных исходов при ИИ у пациентов, получавших тромболитическую терапию в сочетании с Целлексом, на счет Целлекса было бы преждевременно, для этого необходимы дальнейшие наблюдения.
Статистическая обработка выполнялась при помощи пакета для статистического анализа Statistica. Все непрерывные данные представлены при помощи описательной статистики в виде среднего значения, стандартного отклонения максимальных и минимальных значений, медианы, интерквартильного интервала. Все категориальные конечные данные обобщены с указанием частот и процентных соотношений, использованием критерия Манна – Уитни, рангового дисперсионного анализа Фридмана, критерия хи-квадрат, двустороннего критерия Фишера.
Результаты исследования и их обсуждение
Наиболее частым и грозным осложнением тромболитической терапии является геморрагическая трансформация ИИ [22, 23], поэтому прежде всего была сопоставлена частота этого осложнения в сравниваемых группах, в том числе по данным рентгеновской компьютерной томографии головного мозга перед тромболитической терапией, через 24 часа и на пятые сутки. В основной группе в ходе исследования было зарегистрировано три (10,0%) случая развития асимптомного внутримозгового кровоизлияния, в контрольной – пять (16,7%) (два – асимптомного внутримозгового кровоизлияния, три – симптомного). В целом, частота симптомных геморрагических трансформаций составила 5%, что сопоставимо с данными литературы [22, 23]. Несмотря на то что межгрупповые различия частоты геморрагической трансформации ИИ не достигли степени статистической достоверности (р = 0,707), имеющаяся тенденция может свидетельствовать о пользе нейропротективного эффекта Целлекса при тромболитической терапии. Оценка геморрагической трансформации проводилась в соответствии с критериями ECASS (European Australasian Cooperative Acute Stroke Study). Асимптомные геморрагические инфаркты развивались по типу петехиального пропитывания зоны ишемического повреждения без объемного эффекта, симптомные в одном случае – сливающиеся петехиальные кровоизлияния, в двух – паренхиматозные гематомы < 30% объема ишемии с масс-эффектом.
Безусловный интерес представляет динамика состояния больных ИИ в ходе проводимой терапии. Результаты анализа данных NIHSS, проводимого с помощью рангового дисперсионного анализа Фридмана, свидетельствуют о том, что комплексная терапия приводила к статистически значимому уменьшению тяжести неврологической симптоматики в остром периоде ИИ как в основной, так и в контрольной группе (р = 0,000).
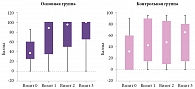
Сравнение групп по данным NIHSS на визитах 1–3 с помощью критерия Манна – Уитни продемонстрировало более выраженную динамику в основной группе. Уже через сутки (на визите 1) среднее значение балла по NIHSS составило в основной группе 1,2 против 4,2 в контрольной группе (р = 0,014). Результаты представлены на рис. 1. Вместе с тем снижение суммарного балла NIHSS в контрольной группе продолжалось и достигло 2,4 балла (среднее значение) к пятым суткам и 2,0 балла (среднее значение) к 19-м суткам, что привело к нивелированию статистических различий между основной и контрольной группами на визитах 2 и 3 (р = 0,083 и р = 0,198 соответственно).
Для оценки степени выраженности нарушений повседневной жизнедеятельности использовали индекс Бартел. В начале исследования статистически значимых различий по индексу Бартел между основной и контрольной группами не наблюдалось (р = 0,099). В ходе комбинированной терапии так же, как и при анализе предыдущих данных, происходило уменьшение степени выраженности нарушений жизнедеятельности у пациентов обеих групп (р = 0,000). Однако уже через сутки от начала заболевания у больных, получавших Целлекс, динамика улучшения состояния была более выраженной, сохраняясь таковой и при последующих обследованиях на 5-е и 19-е сутки от начала заболевания (р = 0,029, р = 0,000 и р = 0,000 соответственно) (рис. 2).
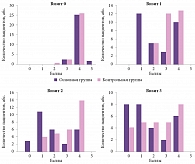
Первоначально в обеих группах у пациентов отмечалась средняя, среднетяжелая и тяжелая степень нарушения дееспособности по модифицированной шкале Рэнкина, статистически значимых межгрупповых различий не наблюдалось (р > 0,05). В ходе исследования степень выраженности нарушений жизнедеятельности по модифицированной шкале Рэнкина снижалась как в основной, так и в контрольной группе. Однако в группе, получавшей Целлекс, наблюдалась более значительная динамика снижения степени выраженности нарушений жизнедеятельности, что способствовало переходу подавляющего числа пациентов из категории «тяжелых» (с выраженным нарушением жизнедеятельности, неспособностью ходить, справляться с физическими потребностями без посторонней помощи, либо прикованных к постели) в категорию «легких» (с отсутствием существенных нарушений жизнедеятельности, несмотря на некоторые симптомы болезни, не мешающие выполнять повседневные обязанности) или регрессу неврологической симптоматики. Статистически значимыми были различия между основной и контрольной группами на визите 1 (по градациям «1 балл» и «3 балла», р = 0,0001 и р = 0,015 соответственно), на визите 2 (по градации «4 балла», р = 0,029) (рис. 3).
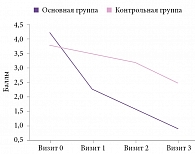
Таким образом, за время наблюдения у больных, получавших Целлекс, процесс восстановления утраченных функций происходил гораздо успешнее по сравнению с группой контроля. Рисунок 4 наглядно иллюстрирует существенную роль Целлекса в регрессе неврологического дефицита: к 19-м суткам от начала заболевания разница в сумме баллов по модифицированной шкале Рэнкина между основной и контрольной группами достигла 1,5 балла (р < 0,05).
Важно отметить, что, по мнению как врачей, так и пациентов, значительный терапевтический эффект Целлекса сочетался с его хорошей переносимостью. Серьезных нежелательных явлений и побочных эффектов, связанных с приемом препарата, в ходе исследования зарегистрировано не было, что свидетельствует о безопасности его применения.
Заключение
Необходимо выделить как минимум два аспекта использования Целлекса при ИИ. Во-первых, в данном исследовании, как и в предыдущих экспериментальных и клинических работах, подтвердилась эффективность препарата, который способствовал регрессу неврологического дефицита, расширению возможности реабилитации пациентов. Во-вторых, выявленная тенденция по уменьшению числа случаев геморрагической трансформации инфаркта мозга на фоне тромболитической терапии может свидетельствовать о нейропротективном влиянии препарата на зону пенумбры путем снижения степени реперфузионного повреждения мозга при реканализации артерии.
Основными выводами исследования стали доказанные преимущества добавления Целлекса к стандартной схеме лечения больных ИИ, получавших тромболитическую терапию. Применение Целлекса позволило достичь более выраженного регресса неврологического дефицита и повысить уровень повседневной активности пациентов. Целлекс продемонстрировал хорошую переносимость, что открывает перспективы его применения в ургентной ангионеврологии.
G.N. Belskaya, M.A. Sokolov, I.A. Izmaylov, S.V. Vlasenko, N.V. Larina
South-Urals State Medical University, Chelyabinsk
Pharm-Sintez, Moscow
Research Institute of Сhildren's Health Resort, Physiotherapy and Rehabilitation, Yevpatoriya
V.I. Vernadsky Crimean Federal University, Simferopol
Contact person: Galina Nikolayevna Belskaya, belskayag74@yandex.ru
Provided the results of prospective observational comparative study in parallel groups (phase IV) aimed at determination of the effect of the drug Cellex on the dynamics and recovery time of lost functions in patients with acute ischemic stroke on the background of baseline and thrombolytic therapy. For 60 patients with ischemic stroke the procedure of systemic thrombolysis was made. The control group (n = 30) underwent standardized basic therapy. Patients of the main group (n = 30) additionally received the drug Cellex (0.1 mg 1 times daily by s.c. injection for ten days). The use of the drug Cellex as a part of complex therapy for ischemic stroke with thrombolysis allowed to achieve more pronounced improvement in the neurological status (on the National Institutes of Health Stroke Scale) and everyday activities (according to Bartel Index and Rankin Scale) of patients compared to standard therapy for acute cerebral circulation disorders.
