Фармакотерапия сахарного диабета 2 типа: последние достижения и пути их внедрения в клиническую практику. VII Всероссийский конгресс эндокринологов. Сателлитный симпозиум компании Takeda
- Аннотация
- Статья
- Ссылки




Что мы знаем о безопасности ПССП с точки зрения сердечно-сосудистых рисков? Как результаты последних исследований отразятся на выборе терапии?
Известно, что сосудистые осложнения обусловливают тяжесть заболевания и преждевременную смерть пациентов. Эпидемиологические данные и метаанализы многочисленных исследований доказывают существование прямой зависимости между уровнем гликированного гемоглобина (HbA1c) и риском развития ССЗ. Результаты исследований демонстрируют, что снижение уровня HbA1c на 1% приводит к снижению риска развития ССЗ на 18%, ишемической болезни сердца (ИБС) – на 13%, инсульта – на 17%1. В то же время данные о влиянии интенсивного гликемического контроля на риск развития макроангиопатии противоречивы. Результаты десятилетнего исследования UKPDS с последующим десятилетним наблюдением свидетельствуют о том, что жесткий гликемический контроль на ранних стадиях СД 2 типа может оказать благоприятный эффект в отношении ССЗ2.
Однако результаты исследований ACCORD, ADVANCE, VADT не подтвердили способность интенсивного контроля уровня глюкозы крови снижать риск развития ССЗ. Например, в исследовании ACCORD зафиксировано увеличение летальных исходов от ССЗ. Проведенный впоследствии метаанализ, включавший большее количество исследований, показал, что в целом есть положительный эффект интенсивного контроля в отношении снижения риска развития ССЗ, но не в отношении общей смертности.
Во всех трех исследованиях (ACCORD, ADVANCE, VADT) именно тяжелая гипогликемия стала прогностическим фактором летального исхода как в группе строгого контроля гликемии, так и в группе стандартного контроля3–5. В дальнейшем эти данные были подтверждены рядом исследований. Сделан вывод: положительный эффект интенсивного контроля гликемии на снижение риска развития ССЗ при СД 2 типа нивелируется негативным влиянием гипогликемий. Следовательно, необходимы более тщательный мониторинг уровня глюкозы в крови и использование терапевтического подхода, направленного на снижение риска гипогликемий.
Установлено, что гипогликемия индуцируется инсулином и препаратами сульфонилмочевины. Сократить риск развития гипогликемии позволяют ингибиторы дипептидилпептидазы 4 (ДПП-4), агонисты глюкагоноподобного пептида 1 (ГПП-1), тиазолидиндионы (ТЗД), ингибиторы натрий-глюкозного котранспортера 2 типа (SGLT-2), добавленные к метформину.
Поскольку риск заболеваний сердца и сосудов при СД в несколько раз выше, чем в популяции без СД, в исследованиях оценивались не только эффективность ПССП в отношении нормализации уровня HbA1c, но и их влияние на сердечно-сосудистые риски. Метаанализ рандомизированных исследований показал, что препараты сульфонилмочевины не оказывают влияния на риск развития ССЗ, однако при их применении увеличивается частота летальных исходов.
В ряде исследований (PROactive, CHICAGO, PERISCOPE) было продемонстрировано благоприятное влияние пиоглитазона на события, связанные с поражением крупных сосудов6–8.
Новые требования Управления по контролю за качеством пищевых продуктов и лекарственных препаратов (Food and Drug Administration – FDA) за 2008 г. существенно ужесточили критерии одобрения сахароснижающих средств. Согласно им препараты должны не только контролировать гликемию, но и обладать безопасным кардиологическим профилем. В руководстве FDA рекомендовано проводить оценку сердечно-сосудистой безопасности зарегистрированных и разрабатываемых препаратов в широкомасштабных исследованиях фаз II и III с учетом верхней границы двухстороннего 95%-ного доверительного интервала (ДИ) для расчета относительного риска (ОР). Достижение верхней границы < 1,3 показывает достаточное для одобрения препарата соотношение риска и пользы.
Обнадеживающие результаты получены в ходе исследования EMPA-REG9, продемонстрировавшего способность ингибитора SGLT-2 эмпаглифлозина снижать основные сердечно-сосудистые исходы у больных СД 2 типа. Уже опубликованы данные исследования ELIXA10 о нейтральном воздействии агониста ГПП-1 ликсисенатида на риск развития ССЗ.
В настоящее время завершен ряд исследований по изучению кардиологической безопасности ингибиторов ДПП-411. В исследовании SAVOR-TIMI12 по оценке влияния саксаглиптина на сердечно-сосудистые риски у больных СД 2 типа в возрасте 40 лет и старше, имеющих ССЗ в анамнезе, отмечено сопоставимое нейтральное влияние саксаглиптина и плацебо на частоту крупных сердечно-сосудистых событий. В исследовании TECOS13 по оценке сердечно-сосудистой безопасности ситаглиптина показано, что группы ситаглиптина и плацебо были сопоставимы по частоте достижения первичных и вторичных конечных точек.
В 2013 г. завершено рандомизированное двойное слепое плацебоконтролируемое исследование EXAMINE14 по оценке влияния алоглиптина на сердечно-сосудистые исходы у больных СД 2 типа старше 18 лет, перенесших острый инфаркт миокарда или госпитализированных по причине нестабильной стенокардии в течение 15–90 дней до рандомизации. Пациенты были рандомизированы в группу терапии алоглиптином (n = 2701) и группу плацебо (n = 2679). Препараты добавлялись к стандартной терапии.
Длительность лечения составила 40 месяцев (медиана 18 месяцев). Первичная конечная точка представляла собой комбинацию крупных сердечно-сосудистых событий (МАСЕ), нефатального инфаркта миокарда и нефатального инсульта.
Цель исследования – показать, что риск наступления сердечно-сосудистых событий у пациентов на фоне стандартной терапии и приема алоглиптина не хуже, чем у пациентов, получавших только стандартную терапию.
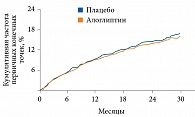
Результаты исследования показали, что у лиц с очень высоким риском развития ССЗ частота событий первичной конечной точки при применении алоглиптина была аналогичной частоте таковых при применении плацебо. Так, частота наступления МАСЕ в группе алоглиптина составила 11,3% (305 пациентов) против 11,8% (316 пациентов) в группе плацебо (рис. 1).
ОР составило 0,96 с верхней границей 95% ДИ 1,16, что соответствовало установленной границе < 1,3.
Результаты субанализа с точки зрения частоты сердечно-сосудистой смерти показали, что алоглиптин более эффективно защищает от сердечно-сосудистой смерти женщин (ОР 60 (95% ДИ 0,40–0,91)), пациентов со скоростью клубочковой фильтрации (СКФ) ≥ 60 мл/мин/1,73 м2 (ОР 67 (95% ДИ 0,46–0,96)) и больных с длительностью диабета < 5 лет (ОР 61 (95% ДИ 0, 37–1,0)). При этом не было различий в частоте сердечно-сосудистой смерти в группах алоглиптина и плацебо у мужчин, пациентов с пониженной СКФ или больных с более длительным течением диабета.
Таким образом, результаты исследования EXAMINE показали, что применение алоглиптина в дополнение к стандартной терапии не увеличивает риск крупных сердечно-сосудистых событий или экстренной реваскуляризации по поводу нестабильной стенокардии по сравнению с применением плацебо.
Совсем недавно опубликованы данные исследования SPEAD-A15 по оценке профилактического воздействия алоглиптина на атеросклероз у больных СД 2 типа. В этом многоцентровом рандомизированном открытом исследовании продолжительностью 24 месяца оценивалось влияние препарата на толщину комплекса «интима – медиа» у пациентов без ССЗ. Результаты исследований позволили сделать следующий вывод: терапия алоглиптином способствует уменьшению плотности сонной артерии, как следствие, замедляется прогрессирование атеросклероза. Это дает основание для проведения проспективных крупномасштабных исследований с целью подтверждения целесообразности применения алоглиптина для первичной профилактики ССЗ у больных СД 2 типа.
Завершая выступление, профессор Э. Боси подчеркнул, что снижение риска сердечно-сосудистых заболеваний у пациентов с СД 2 типа остается одной из ключевых медицинских проблем. На сегодняшний день доказано, что такие препараты, как пиоглитазон, ингибиторы ДПП-4, агонисты ГПП-1, ингибиторы SGLT-2, обладают как минимум нейтральным эффектом в отношении сердечно-сосудистых рисков у данной категории больных. Кроме того, получены данные о противоатеросклеротическом эффекте алоглиптина, которые требуют подтверждения (результаты исследования SPEAD-A).
Управление сердечно-сосудистыми рисками у пациентов с сахарным диабетом 2 типа: взгляд кардиолога
Специалистам следует учитывать, что течение сердечно-сосудистой патологии у больных СД имеет свои особенности. В чем заключается, например, особенность течения ИБС? Прежде всего у таких пациентов ИБС более выражена – чаще выявляется многососудистое поражение, дистальное поражение, что определяет сложность реваскуляризации. У больных диабетом нередко отмечаются немая ишемия и безболевой инфаркт миокарда. Они, как правило, моложе и имеют худшие результаты реваскуляризации (аортокоронарное шунтирование и стентирование коронарных артерий), чем пациенты без диабета. Среди таких пациентов высока распространенность субклинических форм атеросклероза и наблюдается более тяжелое поражение коронарных артерий17, 18. Диабет ассоциируется с повышением риска развития острого коронарного синдрома (ОКС), высоким риском повторного инфаркта миокарда после ОКС и смерти. Установлено, что 20–30% пациентов с инфарктом миокарда страдают СД19.
Гипергликемия при ОКС – отрицательный прогностический признак20. Она часто фиксируется у пациентов без установленного диагноза «сахарный диабет», госпитализированных по поводу ОКС. Доказано, что примерно у 65% пациентов с ОКС при проведении глюкозотолерантного теста выявляется нарушение углеводного обмена. К сожалению, этот фактор риска недооценивается и не корректируется с помощью сахароснижающей терапии, между тем сохраняющаяся гипергликемия становится предиктором госпитальной смерти в случае инфаркта миокарда.
Терапевтическая стратегия при ОКС предусматривает проведение двойной антитромбоцитарной терапии, ранней инвазивной стратегии и реваскуляризации, высокоинтенсивной терапии статинами, бета-блокаторами и блокаду системы «ренин – ангиотензин – альдостерон».
Примерно 25% реваскуляризированных пациентов страдают СД, что создает значительные проблемы в виде диффузного атеросклероза и предполагает худшие результаты при проведении стентирования, а зачастую и просто техническую невозможность стентирования коронарных артерий, либо риск повторного рестеноза после чрескожного коронарного вмешательства.
Эффективность реваскуляризации и медикаментозной терапии у пациентов с СД 2 типа при стабильной ИБС на сегодняшний день неравнозначна. Реваскуляризация с помощью имплантации стента не способствует улучшению прогноза и снижению частоты инфаркта миокарда, а лишь влияет на качество жизни пациента. Оптимальная медикаментозная терапия с использованием всего арсенала имеющихся средств предпочтительна в тех случаях, когда нет обширных зон ишемии и стеноза ствола левой коронарной артерии или проксимального стеноза передней желудочковой артерии.
Контроль артериального давления (АД) играет важную роль в снижении сердечно-сосудистого риска, особенно у больных диабетом. Примерно у 60% больных СД отмечается артериальная гипертония. Комбинация этих двух заболеваний значительно повышает риск сердечно-сосудистых событий. Одной из значимых особенностей профиля АД у пациентов с диабетом является недостаточное его снижение или повышение во время ночного сна. В настоящее время целью лечения артериальной гипертонии считается снижение показателей систолического и диастолического АД < 140 и 85 мм рт. ст., у пациентов с нефропатией и выраженной протеинурией – < 130 и 85 мм рт. ст. соответственно.
Согласно принципам гипотензивной терапии бета-блокаторы не являются препаратами выбора в отсутствие показаний со стороны сердечно-сосудистой системы, поэтому в этом случае больным метаболическим синдромом следует избегать комбинации бета-блокатора с диуретиком. Однако если пациент страдает сердечной недостаточностью, ИБС или перенес инфаркт миокарда, нормализация АД оказывается намного важнее, чем незначительный метаболический эффект бета-адреноблокаторов. Рациональной комбинацией в данной ситуации будет та, которая усиливает гипотензивное действие при нейтральном воздействии на частоту побочных эффектов.
Особенностями липидного обмена при СД считаются низкий уровень холестерина липопротеинов высокой плотности (ХС-ЛПВП), высокий уровень триглицеридов (ТГ) и нормальный или относительно невысокий уровень холестерина липопротеинов низкой плотности (ХС-ЛПНП). В качестве гиполипидемической терапии зачастую используются статины. Эндокринологам следует учитывать, что статины при длительном применении способны повысить риск развития СД21.
Однако метаанализ 14 исследований продемонстрировал способность статинов снижать риск сердечно-сосудистых событий как у пациентов без диабета, так и у больных СД. Доказанный сердечно-сосудистый эффект липидоснижающей терапии статинами дает основание применять их у больных СД с очень высоким и высоким сердечно-сосудистым риском22. Согласно европейским рекомендациям терапия статинами у больных СД 1 и 2 типа с очень высоким сердечно-сосудистым риском проводится с целью снижения уровня ЛПНП < 1,8 ммоль/л, у больных СД 2 типа с высоким сердечно-сосудистым риском < 2,5 ммоль/л.
Безусловно, первичную профилактику ССЗ у пациентов с СД следует проводить с учетом оценки соотношения «польза/риск». Так, до настоящего времени не получены достоверные данные об эффективности применения аспирина для первичной профилактики ССЗ. В ряде исследований показано незначительное снижение риска инсульта и инфаркта миокарда у пациентов с СД 2 типа на фоне приема аспирина. Однако продемонстрировано существенное повышение риска развития язвы желудка и двенадцатиперстной кишки. Поэтому аспирин в низких дозах рекомендован для лечения острых ишемических синдромов и вторичной профилактики ССЗ.
Отсутствуют также данные о том, что какой-либо из блокаторов рецепторов P2Y12 более эффективен у больных СД, чем у пациентов без диабета.
По мнению М.Ю. Гилярова, только достижение целевых уровней HbA1c, ЛПНП, ТГ, систолического АД и C-реактивного белка способствует снижению сердечно-сосудистых рисков. Это подтверждают результаты исследования Y. Katacka и соавт. Так, достижение целевых значений HbA1c < 7%, ЛПНП < 2,5 ммоль/л, ТГ < 1,7 ммоль/л, систолического АД < 130 мм рт. ст., C-реактивного белка < 2,0 мг/л у пациентов с СД 2 типа и ИБС способствовало уменьшению объема атеромы23. «Это та путеводная звезда, к которой мы должны стремиться, и бороться с врагом на всех фронтах», – констатировал докладчик.
Сердечная недостаточность у больных сахарным диабетом 2 типа: влияние антидиабетической терапии
Общепризнано, что чем хуже контроль гликемии, тем выше риск развития ССЗ, в том числе сердечной недостаточности. Снижение HbA1c на 1% уменьшает риск развития последней на 16%. Важно и то, что при СД 2 типа высокий (> 10%) и низкий (< 6%) уровни HbA1c ассоциируются с риском развития сердечной недостаточности. Результаты рандомизированных клинических исследований показали, что от начала сахароснижающей терапии ОР ее развития претерпевает изменение. В течение первого года ОР составляет 4,75, второго – 1,21, через два года – 0,89.
Профессор Г.Р. Галстян проанализировал влияние разных классов антидиабетических препаратов (глитазоны, препараты сульфонилмочевины, инсулин, ингибиторы ДПП-4, агонисты ГПП-1, ингибиторы SGLT-2) на риск развития сердечной недостаточности. Результаты рандомизированных исследований (DREAM25, ProACTIVE) показали, что применение тиазолидиндионов в высоких дозах на 20% повышает риск развития таковой. Это может быть связано с формированием отеков на фоне их применения.
Согласно данным наблюдательных исследований по сердечно-сосудистым исходам у пациентов с диабетом, принимавших препараты сульфонилмочевины, их прием в высоких дозах сопровождается увеличением риска развития сердечной недостаточности на 38% по сравнению с приемом меньших доз26. При сравнении препаратов сульфонилмочевины, глитазонов и метформина показано, что риск развития сердечной недостаточности минимален у пациентов, получавших монотерапию метформином, и сопоставимо выше у пациентов, получавших препараты сульфонилмочевины и глитазоны.
Результаты исследований по оценке частоты развития сердечной недостаточности на фоне инсулина у больных СД 2 типа демонстрируют, что такая терапия сопровождается повышением частоты развития сердечной недостаточности и худшим ее прогнозом. Инсулинотерапия может приводить к задержке жидкости. Наибольшая задержка жидкости и формирование отеков наблюдаются при комбинации инсулина с тиазолидиндионами27.
На сегодняшний день завершено пять исследований по влиянию новых классов сахароснижающих препаратов на сердечно-сосудистые риски, в трех из них – EXAMINE, SAVOR-TIMI и TECOS – оценивалось влияние ингибиторов ДПП-4 на сердечно-сосудистые исходы. Исследования различались по продолжительности, количеству пациентов, степени сердечно-сосудистых рисков. «Если расположить все пять исследований по степени выраженности сердечно-сосудистых заболеваний и степени риска развития новых событий, можно с уверенностью сказать, что исследование EXAMINE (влияние алоглиптина) и исследование ELIXA (влияние агонистов ГПП-1) были самыми экстремальными с точки зрения их участников», – уточнил профессор Г.Р. Галстян.
Наиболее высокий риск развития ССЗ отмечался у участников исследования EXAMINE, у которых ОКС произошел в течение 15–90 дней до включения в исследование. По данному параметру промежуточное положение занимало исследование TECOS, а наименее обремененными сопутствующими ССЗ, но имеющими высокий сердечно-сосудистый риск были участники исследования SAVOR-TIMI. Результаты исследований показали равнозначные результаты по количеству сердечно-сосудистых событий, что позволило сделать вывод о том, что ингибиторы ДПП-4 являются безопасными у пациентов, имеющих высокие и очень высокие сердечно-сосудистые риски.
Во всех трех исследованиях (EXAMINE, SAVOR-TIMI и TECOS) было отмечено улучшение гликемического контроля, особенно на ранних этапах наблюдения. Гипогликемические эпизоды имели место в группе саксаглиптина и группе получавших саксаглиптин в комбинации с препаратами сульфонилмочевины (SAVOR-TIMI 53). В исследованиях EXAMINE, SAVOR-TIMI и TECOS регистрировалось снижение потребности в инсулине или назначении инсулинотерапии. Частота развития панкреатита и рака поджелудочной железы за весь период наблюдения была сопоставимой, хотя в группе ситаглиптина несколько превышала таковую в группе плацебо (TECOS).
В исследовании SAVOR-TIMI 53 получены результаты о достоверном (р = 0,007) увеличении частоты госпитализаций в связи с сердечной недостаточностью – на 27% в группе саксаглиптина по сравнению с группой плацебо. Недостоверные данные о повышении частоты госпитализаций на 19% получены в группе алоглиптина по сравнению с группой плацебо. Принимая во внимание эти данные, в исследовании EXAMINE был проведен анализ post hoc в зависимости от наличия сердечной недостаточности в анамнезе до рандомизации и после и ее влияния на первичные и вторичные конечные точки (сердечно-сосудистая смерть, нефатальный инсульт/инфаркт миокарда, экстренная реваскуляризация в результате нестабильной стенокардии)28.
Больные с сердечной недостаточностью и больные без сердечной недостаточности в группе алоглиптина и группе плацебо по исходым характеристикам не различались. Результаты анализа показали, что у больных СД 2 типа комбинированная конечная точка по госпитализации вследствие сердечной недостаточности и сердечно-сосудистой смерти была сходной между группами, как у больных с отягощенным анамнезом по сердечной недостаточности, так и у больных без сердечной недостаточности в анамнезе (рис. 2).
В исследовании EXAMINE также проведен субанализ в отношении сердечной недостаточности в зависимости от уровня N-терминального фрагмента мозгового натрийуретического пептида (NT-proBNP), который является маркером тяжести заболевания. В группе алоглиптина и группе плацебо зарегистрировано снижение уровня NT-proBNP, однако оно было более значимым в первой группе. Согласно данным анализа post hoc, алоглиптин не оказывал влияния на частоту сердечно-сосудистой смерти и госпитализаций по поводу сердечной недостаточности.
Исследование EXAMINE показало, что у больных СД 2 типа, недавно перенесших ОКС, применение ингибитора ДПП-4 алоглиптина не приводит к развитию сердечной недостаточности или ухудшению ее течения. Полученные результаты позволили сделать вывод: применение алоглиптина безопасно у пациентов с СД 2 типа и высоким сердечно-сосудистым риском, включая пациентов с сердечной недостаточностью в анамнезе. Частота достижения комбинированной конечной точки – госпитализации по поводу сердечной недостаточности и сердечно-сосудистой смерти – была аналогичной в обеих группах: 7,4% на фоне терапии алоглиптином и 7,5% – плацебо (ОР 1,00 (95% ДИ 0,82–1,21)).
Результаты рандомизированных исследований, продемонстрировавших способность инкретиннаправленной терапии не ухудшать прогноз в отношении сердечной недостаточности у больных СД с отягощенным сердечно-сосудистым анамнезом, подтверждены рядом масштабных наблюдательных исследований.
В исследовании, опубликованном в европейском кардиологическом журнале, были проанализированы данные 128 000 пациентов с СД 2 типа, из них 14% получали ингибиторы ДПП-4, 72% – препараты сульфонилмочевины, 13% – тиазолидиндионы, порядка 70% пациентов находились на комбинированной терапии теми или иными препаратами с метформином. Ингибиторы ДПП-4 на 25% снижали риск развития сердечной недостаточности по сравнению с препаратами сульфонилмочевины и ассоциировались с уменьшением риска госпитализаций по поводу сердечной недостаточности.
В другое популяционное исследование29 по оценке влияния препаратов инкретинового ряда на риск развития сердечной недостаточности было включено около 58 000 пациентов с СД 2 типа. Срок наблюдения в среднем составил два с половиной года. За указанный период выявлено 1,118 нового случая госпитализаций по поводу сердечной недостаточности. Таким образом, препараты инкретинового ряда вне зависимости от длительности их применения не влияют на развитие сердечной недостаточности.
Завершая выступление, профессор Г.Р. Галстян сформулировал следующие выводы:
- исследования EXAMINE, SAVOR-TIMI и TЕCOS показали отсутствие различий по частоте достижения МАСЕ в группе ингибиторов ДПП-4 по сравнению с группой плацебо у пациентов с высоким риском развития ССЗ;
- анализ post hoc исследования EXAMINE продемонстрировал отсутствие различий по частоте достижения комбинированной конечной точки у пациентов, получавших как алоглиптин, так и плацебо, а также снижение уровня NT-proBNP по сравнению с исходным;
- в настоящее время оснований для ограничения применения ингибиторов ДПП-4 у больных СД 2 типа и ССЗ не существует, однако следует более внимательно относиться к своевременной диагностике сердечной недостаточности и оптимизации терапии.
Заключение
Поскольку СД 2 типа связан с высоким риском макрососудистых осложнений, сахароснижающие препараты должны не только эффективно снижать уровень гликемии, но и обладать безопасным кардиологическим профилем. На сегодняшний день доказано, что ингибиторы ДПП-4, агонисты ГПП-1, ингибиторы SGLT-2 отличаются как минимум нейтральным влиянием на риск развития ССЗ. В наибольшей степени требованиям эффективности и сердечно-сосудистой безопасности отвечает алоглиптин – современный представитель ингибиторов ДПП-4, широко вошедший в диабетологическую практику. Доказано, что у пациентов с СД 2 типа и очень высоким сердечно-сосудистым риском применение алоглиптина не сопряжено с повышением риска сердечно-сосудистых событий, в том числе у пациентов с сердечной недостаточностью.
