«Флорентийская перспектива»: механизмы формирования
- Аннотация
- Статья
- Ссылки

Комбинированная терапия в лечении сахарного диабета (СД) 2 типа – общепризнанный факт мировой клинической практики. Последние годы были богаты на предложения различных алгоритмов подобного лечения. Один из последних, рекомендованный 19 апреля 2012 г. Американской диабетический ассоциацией (American Diabetes Association, ADA) и Европейской ассоциацией по изучению диабета (European Association for the Study of Diabetes, EASD), уже достаточно хорошо известен в нашей стране (рис. 1) [1].
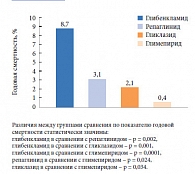
Препараты сульфонилмочевины по-прежнему находятся в первых рядах в лечении СД 2 типа. По вполне понятным причинам их комбинация с метформином оказывается наиболее применяемым сочетанием сахароснижающих препаратов у пациентов с СД. Поcле Флорентийского исследования, показавшего различия в уровне сердечно-сосудистой безопасности комбинаций метформина с разными препаратами сульфонилмочевины и другими секретагогами инсулина (рис. 2) [2], вопрос о причинах этих различий приобрел особую клиническую актуальность.
При обсуждении сердечно-сосудистой безопасности комбинаций сахароснижающих средств, включающих в себя препараты сульфонилмочевины, в первую очередь традиционно анализируется влияние этих препаратов на естественные механизмы защиты миокарда от ишемии, на так называемые процессы прекондиционирования, или предишемической подготовки миокарда.
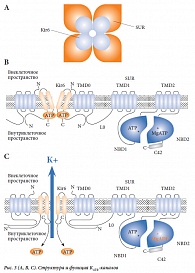
Как давно известно, препараты сульфонилмочевины способны изменять естественное течение этих защитных процессов, воздействуя на аденозинтрифосфат(АТФ)-зависимые калиевые каналы миокардиальных клеток (КАТФ-каналы). КАТФ-каналы широко распространены во всех тканях высших организмов и играют важную роль в регуляции многих физиологических процессов. КАТФ-канал представляет собой гетерооктамер, состоящий из 4 Kir-субъединиц и 4 SUR-субъединиц. Четыре центрально расположенные Kir-субъединицы образуют пору, в то время как расположенные на периферии 4 SUR-субъединицы играют роль регуляторов состояния канала (рис. 3А) [3].
Препараты сульфонилмочевины обладают способностью связываться с субъединицами SUR. Именно поэтому эти единицы и получили свое название SUR – sulphonyl urea receptor – рецептор сульфонилмочевины. SUR является атипичным ABC-белком-транспортером, который, воздействуя на субъединицу Kir, определяет функциональное состояние КАТФ-канала [4]. Интересно, что ABC-транспортеры локализованы как в плазменных мембранах, так и в мембранах внутриклеточных органелл, таких как пероксисомы, лизосомы, вакуоли, эндосомы, в мембранах аппарата Гольджи, эндоплазматическом ретикулуме и митохондриях [5].
Митохондриальные ABC-транспортеры, обладающие КАТФ-активностью, являются компонентами структуры митохондрий и обеспечивают цитопротекторную защиту при окислительном стрессе в процессе развития кардиомиопатий [6, 7]. Обнаружено, что сердце содержит много ABC-транспортеров, играющих большую роль в физиологии и патологии сердечной деятельности.
Существуют две изоформы SUR: SUR1 и SUR2, последняя имеет 2 типа – SUR2A и SUR2B [3, 8]. Субъединица SUR2A наиболее распространена в кардиомиоцитах, в то время как SUR2B чаще всего обнаруживается в гладкомышечных клетках [9]. Субъединица SUR1 чаще всего встречается в поджелудочной железе и мозговой ткани [9]. Сложно устроенная субъединица SUR воздействует на состояние субъединицы Kir через трансмембранный домен (transmembrane domain, TMD) TMD0 и компоновочный участок L0, которые расположены на N-конце субъединицы SUR (рис. 3В).
Субъединица SUR содержит еще 2 трансмембранных домена – TMD1 и TMD2, а также 2 нуклеотидсвязывающих домена (nucleotide-binding domain, NBD). NBD1 расположен на цитоплазматической поверхности SUR между TMD1 и TMD2. NBD2 расположен в цитоплазме около С-конца SUR. Клеточная аденозинтрифосфорная кислота может связываться с обоими нуклеотидсвязывающими доменами (как с NBD1, так и с NBD2), которые определяют активность ее гидролиза. Образование С42, расположенное на NBD2, является еще одним регулятором активности гидролиза АТФ. С42 одинаково у SUR1 и SUR2А, что обусловливает функциональное сходство этих каналов.
В результате гидролиза АТФ трансмембранный домен NBD2 приобретает способность связываться с комплексом Mg-аденозиндифосфат (Mg-АДФ). Это вызывает конформационные изменения TMD0/L0 области SUR, передающиеся на порообразующую субъединицу Kir и приводящие к открытию канала (рис. 3С). Таким образом, состояние сложно устроенной субъединицы SUR в значительной мере регулируется уровнем клеточной АТФ, что, в свою очередь, определяет состояние субъединицы Kir и открытое или блокированное состояние канала для калия.
Субъединица Kir регулирует транспорт калия. Связывание АТФ непосредственно с Kir вызывает закрытие канала, а гидролиз АТФ после присоединения ее к субъединице SUR способствует его открытию [10]. Таким образом, субъединица SUR играет регуляторную роль, модулируя состояние канала в зависимости от клеточного уровня АТФ. КАТФ-каналы играют важную физиологическую роль во многих метаболически активных тканях, включая поджелудочную железу, мозг и мышцы. Лучше всего изучена их определяющая роль в секреции инсулина из бета-клеток поджелудочной железы [10, 11].
В панкреатической бета-клетке высокий уровень АТФ, связанный с увеличением глюкозы плазмы крови, приводит к закрытию КАТФ-каналов. В результате происходит деполяризация клеточной мембраны и поступление в клетку Са2+ с последующей секрецией инсулина из бета-клетки поджелудочной железы. Секретагоги инсулина, связывающиеся с SUR-субъединицами КАТФ-каналов в поджелудочной железе, вызывают закрытие этих каналов, вследствие чего выделение инсулина из поджелудочной железы усиливается [12].
В сердечной мышце КАТФ-каналы кардиомиоцитов играют важнейшую роль в активизации защитных антиишемических механизмов. Как уже отмечалось, в миокарде преимущественно экспрессируются КАТФ-каналы, содержащие SUR2A-субъединицы [13]. Их состояние, в первую очередь, регулируется сдвигами во внутриклеточной концентрации аденозинмонофосфата(АМФ)/АТФ. При снижении внутриклеточного уровня АТФ количество открытых миокардиальных КАТФ-каналов увеличивается.
Открытые КАТФ-каналы миокарда регулируют ответ сердечной мышцы на стресс и играют важную роль в развитии физиологической защиты миокарда от ишемии (ишемическое прекондиционирование). Ранее считалось, что сарколеммальные КАТФ-каналы являются единственными калиевыми каналами, влияющими на ишемическое прекондиционирование миокарда. В настоящее время взгляды изменились. Сейчас общепринятым считается, что не сарколеммальные, а митохондриальные КАТФ-каналы миокарда (митКАТФ-каналы) играют ведущую роль в регуляции ишемического прекондиционирования.
При этом их воздействие на ишемическое прекондиционирование не зависит от функционирования сарколеммальных КАТФ-каналов [14]. Недавно было показано, что SUR2A входит в состав как сарколеммальных, так и внутренней части митохондриальных мембран. Это еще раз подтвердило то, что КАТФ-каналы митохондрий миокарда являются АТФ-зависимыми элементами защитной системы ишемического прекондиционирования сердечной мышцы.
Секретагоги инсулина, которые блокируют как сарколеммальные, так и митохондриальные КАТФ-каналы, оказывают негативное воздействие на процессы защиты от ишемии миокарда. Среди препаратов группы секретагогов, не относящихся к производным сульфонилмочевины, существуют препараты, связывающиеся только с SUR1-рецепторами бета-клеток поджелудочной железы: например, натеглинид и митиглинид (класс глинидов).
Доказано, что высокоселективный в отношении SUR1-рецепторов бета-клеток поджелудочной железы митиглинид влияния на выраженность ишемического прекондиционирования не оказывает [15]. Напротив, также относящийся к глинидам репаглинид в одинаковой мере связывается и с SUR1-рецепторами бета-клеток поджелудочной железы, и с SUR2А-рецепторами миокарда [16]. В результате препарат оказывает неблагоприятное влияние на прекондиционирование миокарда, что и указывается в инструкции по медицинскому применению препарата.
Сахароснижающие препараты группы сульфонилмочевины являются наиболее известными лекарственными веществами, влияющими на функциональное состояние КАТФ-каналов миокарда [12]. Такие препараты, как глибенкламид и глимепирид, преимущественно связываются с SUR1-рецепторами бета-клеток поджелудочной железы, но, кроме того, они обладают определенной способностью связываться и с SUR2А-рецепторами миокарда.
Вызывая закрытие КАТФ-каналов миокарда, препараты сульфонилмочевины способны существенно снижать эффективность функциональной защиты миокарда от транзиторной ишемии, уменьшая активность процессов ишемического прекондиционирования. Однако отдельные препараты этого класса лекарственных средств, обладая общей способностью связываться с SUR1-рецепторами поджелудочной железы, демонстрируют различную связывающую способность с SUR2А-рецепторами миокарда.
Именно на подобного типа различиях и базируются специфические кардиальные свойства препаратов сульфонилмочевины. Необходимо подчеркнуть, однако, что кардиальные свойства препаратов сульфонилмочевины определяются не только их степенью сродства к SUR2А-рецепторам миокарда, но и тем, в каких структурах миокарда расположены эти рецепторы. Оказалось, что по данному признаку препараты сульфонилмочевины также различаются между собой.
К настоящему времени известно, что глибенкламид взаимодействует как с сарколеммальными, так и с митохондриальными SUR2А-рецепторами миокарда, блокируя КАТФ-каналы этих структур. В отличие от него глимепирид, блокируя сарколеммальные КАТФ-каналы, оставляет открытыми их митохондриальные аналоги. Существуют и препараты (например, производное сульфонилмочевины 1-го поколения толбутамид), которые, наоборот, оставляют открытыми сарколеммальные КАТФ-каналы миокарда, блокируя каналы в митохондриях.
Учитывая различный спектр действия препаратов сульфонилмочевины в отношении SUR2А-субъединиц, вполне естественно ожидать, что они по-разному воздействуют на процессы защиты миокарда от ишемии. В отношении глибенкламида, который блокирует и сарколеммальные, и митохондриальные каналы миокарда, существуют данные о подавлении им процессов ишемического прекондиционирования миокарда. О некоторых препаратах известно, что отрицательный эффект в отношении ишемического прекондиционирования у них выявляется только при нарастании используемой дозы. К таким препаратам можно отнести гликлазид.
Говоря о глимепириде, необходимо подчеркнуть, что этот препарат, взаимодействуя с SUR2А-рецепторами, блокирует сарколеммальные КАТФ-каналы миокарда, но оставляет открытыми аналогичные митКАТФ-каналы. В результате ишемическое прекондиционирование не нарушается [17, 18]. Именно поэтому глимепирид можно рассматривать как наиболее безопасный вариант препарата сульфонилмочевины, который может использоваться в качестве сахароснижающей терапии у больных СД 2 типа, страдающих ишемической болезнью сердца.
Как оказалось, схожий спектр сердечно-сосудистой безопасности сохраняется и при использовании комбинации препаратов сульфонилмочевины с метформином (рис. 2) [2]. Более того, присоединение к терапии метформином препаратов сульфонилмочевины делает эти различия в показателях сердечно-сосудистой безопасности еще более контрастными. Развитие подобного феномена можно объяснить следующим образом. В 2001 г. группа исследователей G. Zhou и соавт. [19] обнаружили, что метформин способен активизировать миокардиальный внутриклеточный фермент, носящий название АМФ-активируемая протеинкиназа (АМПК), который сам по себе является ключевым элементом клеточного метаболического статуса [20].
AMПK представляет собой гетеротримерный энзим, состоящий из каталитической альфа-субъединицы и регуляторных бета- и гамма-субъединиц. AMПK находится во всех тканях млекопитающих, в различных тканях он представляет собой различную смесь изоформ и обладает специфическими функциями. Убедительно доказана центральная роль AMПK в регуляции углеводного и липидного обменов. Активация или угнетение активности АМПК сопровождается изменением внутриклеточной концентрации АМФ/АТФ.
Недавние исследования показали, что задействованность и активность миокардиальных КАТФ-каналов находятся под воздействием АМПК [20]. При активации АМПК увеличивается внутриклеточное соотношение АМФ/АТФ и, как показывают исследования, увеличивается количество и активность открытых миокардиальных КАТФ-каналов, что ведет к усилению процесса ишемической преадаптации миокарда [20, 21]. Метформин, активизируя АМПК, приводит к изменению внутриклеточного соотношения АМФ/АТФ и таким образом увеличивает количество и активность открытых миокардиальных КАТФ-каналов, что, в свою очередь, усиливает процессы, ведущие к ишемической защите миокарда [22].
По-видимому, это усиление ишемического прекондиционирования с помощью метформина возможно только тогда, когда миокардиальные КАТФ-каналы не блокированы препаратами сульфонилмочевины. Действительно, результаты Флорентийского регистра указывают на то, что, когда метформин применяется одновременно с глимепиридом, оставляющим открытыми митКАТФ-каналы, отмечается наиболее безопасный сердечно-сосудистый эффект подобной комбинации в отношении смертности пациентов.
Несколько хуже результаты были получены при сочетании метформина с препаратом, оставляющим открытыми сарколеммальные КАТФ-каналы (гликлазид). В то же время при сочетании метформина с препаратами, блокирующими как сарколеммальные, так и митохондриальные КАТФ-каналы миокарда (в первую очередь, глибенкламидом), отмечается существенное увеличение риска смерти.
Таким образом, двойное положительно направленное воздействие на ишемическое прекондиционирование, в максимальной степени свойственное комбинации глимепирида и метформина, приносит свои удивительные клинические плоды. Используя подобную комбинацию у больных СД 2 типа, можно не только эффективно достигнуть целевых показателей углеводного обмена, но и сделать это максимально безопасно с точки зрения развития тяжелых сердечно-сосудистых осложнений.
