Использование препарата Лонгидаза® при повторных трансуретральных операциях на нижних мочевых путях
- Аннотация
- Статья
- Ссылки
- English






Введение
С одной стороны, развитие и широкое внедрение современных эндоурологических и лапароскопических операций, требующих трансуретрального дренирования, позволили уменьшить сроки госпитализации и социальной реабилитации пациентов. С другой стороны, использование мочеиспускательного канала в качестве доступа для проведения операции или дренирования почки, а также извлечения дренажа привело к росту частоты рубцовых осложнений. Примерно у 10–15% пациентов после первичных трансуретральных операций возникают рубцовые осложнения со стороны мочеиспускательного канала и шейки мочевого пузыря [1–4]. При повторных операциях вероятность наступления рецидива рубцового процесса возрастает.
Больные с рецидивирующими рубцовыми сужениями в области шейки мочевого пузыря относятся к тяжелой категории пациентов, так как они вынуждены повторно оперироваться по поводу обтурации шейки мочевого пузыря. Процесс лечения усложняет присоединение вторичной гипотонии детрузора, что может привести к неадекватным результатам терапии. Актуальными остаются не только проблемы хирургического вмешательства (метод лечения, выбор источника энергии, срок послеоперационного дренирования), но и вопросы профилактики рубцового процесса после выполнения трансуретральных операций.
Второе урологическое отделение городской клинической больницы им. Д.Д. Плетнева ориентировано на помощь пациентам, перенесшим первичные, а нередко и повторные трансуретральные операции по поводу рубцовых осложнений в области шейки мочевого пузыря и мочеиспускательного канала в других клиниках. Накопленный в отделении опыт лечения данной категории пациентов, эндоскопическое оборудование экспертного класса и современные урологические лазеры позволяют проводить малоинвазивные операции на качественно ином уровне.
Лонгидаза® – инновационный препарат, с доказанной эффективностью применяется для профилактики и комплексного лечения заболеваний, сопровождающихся гиперплазией соединительной ткани: хронического простатита, интерстициального цистита, стриктур уретры и мочеточников, начальных стадий доброкачественной гиперплазии предстательной железы [5]. Перспективы применения препарата у пациентов с рецидивами склероза шейки мочевого пузыря до настоящего времени не оценивались. В связи с вышеизложенными данными нами проведено ретроспективное исследование, отражающее опыт лечения больных с рецидивами склероза шейки мочевого пузыря.
Цель исследования
Проанализировать возможности использования препарата Лонгидаза® в лечении пациентов со склерозом шейки мочевого пузыря.
Материал и методы
Исследование продолжалось с января по сентябрь 2016 г. На амбулаторном этапе были установлены критерии включения и исключения из исследования, определены показания к операции, изучены режимы и сроки проведения терапии препаратом Лонгидаза® (рис. 1).
В исследование набирались пациенты со склерозом мочевого пузыря, перенесшие в разное время после основной операции от одной до трех трансуретральных резекций шейки мочевого пузыря в различных клиниках. Потенциальные участники исследования прошли комплексное амбулаторное обследование.
Критерии включения в исследование:
- самостоятельное мочеиспускание;
- сумма баллов по Международной шкале суммарной оценки симптомов при заболеваниях простаты (International Prostate Symptom Score – IPSS) более 18;
- сумма баллов по шкале качества жизни (Quality of Life – QoL) более 3;
- объем остаточной мочи до 200 мл;
- максимальная скорость мочеиспускания менее 10 мл/с;
- отсутствие недержания мочи;
- подписанное информированное согласие.
Из исследования были исключены 27 пациентов по причине онкологического заболевания в области малого таза в анамнезе (n = 12), остаточной мочи более 200 мл (n = 6), поражения наружного сфинктера (n = 4), низкой комплаентности (n = 3), заболевания прямой кишки в стадии обострения (n = 2).
Критериям включения соответствовали 87 пациентов с рецидивами склероза шейки мочевого пузыря (табл. 1). После амбулаторного дообследования всем пациентам была выполнена эндоскопическая коррекция шейки мочевого пузыря. В послеоперационном периоде всем пациентам помимо стандартной противовоспалительной терапии проводилась противофиброзная терапия препаратом Лонгидаза®. Спустя три месяца пациенты прошли контрольное клинико-лабораторное обследование, включающее в себя сбор жалоб, оценку качества жизни путем анкетирования по IPSS, оценку уродинамических показателей при помощи урофлоуметрии, ультразвуковое исследование на предмет остаточной мочи, оценку лабораторных данных при помощи общего анализа мочи и микробиологического исследования мочи при уровне лейкоцитов более 5 в поле зрения.
Удовлетворительным результат лечения признавали при следующих условиях: самостоятельное мочеиспускание, снижение выраженности симптомов нижних мочевых путей более чем на 50% по шкале IPSS, улучшение качества жизни более чем на 1 балл, количество остаточной мочи менее 50 мл, максимальная объемная скорость мочеиспускания более 15 мл/с при отсутствии недержания мочи. Отрицательным результат лечения считался при наступлении рецидива склероза шейки мочевого пузыря, что выявлялось на основании совокупности субъективных жалоб и объективных параметров по данным урофлоуметрии и ультразвукового исследования. Необходимость выполнения диагностической уретроцистоскопии, бужирования или повторного оперативного лечения по поводу рецидива склероза шейки мочевого пузыря также расценивалась как неудовлетворительный результат.
Техника операции
Операции проводились в условиях эндоскопической операционной под спинальной анестезией с применением цистоскопа № 22F или уретротома № 21F. Сначала выполнялась уретроскопия, во время которой производился осмотр мочеиспускательного канала. Прежде всего оценивалось состояние наружного сфинктера (сохранность элементов, тонус) и простатического отдела уретры (протяженность, наличие резидуальных аденоматозных тканей). Далее осматривался суженный участок шейки мочевого пузыря, особое внимание уделялось протяженности обструкции (только зона шейки протяженностью менее 5 мм, шейка и простатический отдел уретры протяженностью более 5 мм).
После лазерной коррекции шейки мочевого пузыря инструмент проводился в мочевой пузырь. Уточнялись признаки гипотонии детрузора (дивертикулы, эндоскопическая емкость мочевого пузыря), оценивалось состояние устьев мочеточников (локализация по отношению к шейке мочевого пузыря, тонус). При осмотре задней уретры использовалась узкоспектровая эндоскопия или компьютерная хромоэндоскопия. Определялись участки с сохраненным кровотоком в области суженного участка слизистой. Сохранение питающих сосудов подслизистого слоя важно для поддержания адекватного кровоснабжения данной зоны и предотвращения гиперплазии рубцовой ткани. После того как инструмент проводился в мочевой пузырь и появлялась возможность для ретроградного осмотра зоны шейки мочевого пузыря, дополнительно осматривалась зона операции: уточнялось направление разрезов, определялись их количество и глубина.
Зоны для рассечения слизистой при рецидивном стенозе выбирались так, чтобы максимально сохранить кровообращение, а также поддержать широкий просвет шейки мочевого пузыря и простатического отдела уретры, сохранить наружный сфинктер.
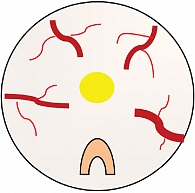
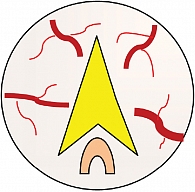
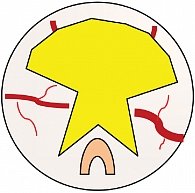
Схема этапов операции представлена на рис. 2–5 (сосуды изображены в режиме узкоспектральной эндоскопии (Narrow Band Imaging – NBI)). В случае протяженного стеноза (более 5 мм) направление разрезов было не прямым, а спиралевидным.
При необходимости взятия материала для морфологического исследования (n = 5) или возникновении сомнений в возможности образования клапана задней уретры после операции (n = 23) проводилась лазерная резекция данного участка шейки. На рис. 6 представлена схема операции после удаления двух клапанов по верхней полуокружности условного циферблата.
Все операции выполнены с использованием гольмиевого лазера Auriga 30W и 50W (Starmedtec, Германия) в режиме аблации мягких тканей с максимальной энергией и частотой для увеличения скорости удаления тканей. После операции инструмент удалялся и устанавливался двухходовой силиконовый уретральный катетер № 16.
Послеоперационный период
Наименьшее время дренирования мочевого пузыря составило двое суток, что было обусловлено не сроками купирования гематурии, а необходимостью не допустить химического повреждения свежей раневой поверхности мочой при чрезмерно раннем удалении катетера на первые сутки.
В послеоперационном периоде назначались антимикробные препараты согласно предоперационному посеву мочи. При стерильном посеве проводилась только антибактериальная премедикация антибиотиком широкого спектра действия (цефтриаксон 1 г в/м, ципрофлоксацин 200 мг/сут в/в).
Еще одна важная задача послеоперационного периода – предупредить возникновение послеоперационного простатита. Известно, что воспаление в области шейки мочевого пузыря в течение первого месяца после операции может привести к рецидиву склероза шейки мочевого пузыря. В этой связи в некоторых случаях антибактериальная терапия продолжалась дольше рекомендованных сроков (три – пять дней), достигая 21 дня.
Дополнительно проводилась терапия суппозиториями, содержащими нестероидные противовоспалительные препараты (индометацин 50 мг, вольтарен 100 мг) в течение первой недели после операции. Для профилактики сужения зоны шейки мочевого пузыря в течение первого месяца пациенты применяли альфа-адреноблокаторы (тамсулозин 0,4 мг/сут).
Главную роль в профилактике сужения шейки мочевого пузыря после операции играла противофиброзная терапия с использованием ферментного препарата гиалуронидазы 3000 ЕД (Лонгидаза®). В течение первой недели препарат вводился внутримышечно один раз в три дня, после выписки из стационара внутримышечная форма была заменена на форму в виде суппозиториев. В течение трех месяцев после операции 79% пациентов прошли повторный курс терапии препаратом Лонгидаза® в форме суппозиториев.
Результаты
Результаты оперативного лечения были проанализированы спустя три месяца. Положительные результаты были достигнуты у 71 (81,6%) пациента. 16 пациентов отметили ослабление струи мочи, что было подтверждено данными урофлоуметрии. Эти пациенты были отнесены к категории больных с риском рецидива склероза шейки мочевого пузыря. Трем пациентам в срок три месяца от момента первой операции были выполнены повторные уретроскопии. В первом случае был диагностирован клапан задней уретры, была проведена лазерная резекция последнего. Во втором случае выявлен невыраженный склероз шейки мочевого пузыря, выполнена повторная лазерная инцизия данной зоны. В третьем случае шейка мочевого пузыря была проходима, диагностирована гипотония детрузора, была назначена соответствующая консервативная терапия.
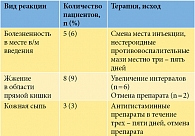
Данные об интра- и послеоперационном периоде, консервативной терапии до и после операции, нежелательных явлениях, отмеченных на фоне применения препарата Лонгидаза®, приведены в табл. 2–4.
Все зарегистрированные нежелательные явления были несерьезными. С одной стороны, небольшой объем выборки не позволяет судить о профиле безопасности препарата, с другой – незначительное число нежелательных явлений, их обратимость свидетельствуют о том, что препарат Лонгидаза® характеризуется благоприятным соотношением «польза – риск».
Обсуждение результатов
Вторичный склероз шейки мочевого пузыря – серьезное осложнение операций на предстательной железе. Инфравезикальная обструкция, вызываемая данным заболеванием, приводит к резкому возрастанию внутрипузырного давления во время мочеиспускания. В зависимости от характера первичного заболевания и вида первичной операции частота развития данного осложнения варьирует от 0,14 до 20% [1–4]. По данным, которые приводятся в рекомендациях Европейской ассоциации урологов, частота развития обструкции шейки мочевого пузыря после трансуретральной резекции простаты составляет примерно 4,7% [1], после открытой аденомэктомии – около 6% [2]. Широко используемая радикальная простатэктомия приводит к обтурации уретроцистоанастомоза у 0,5–14,6% пациентов [6].
Для лечения склероза шейки мочевого пузыря традиционно применяются монополярная трансуретральная инцизия и резекция шейки мочевого пузыря, а также плазменная инцизия, резекция и вапоризация шейки мочевого пузыря. Использование лазерной энергии (Но:YAG, Th:YAG) позволило повысить безопасность данных операций [7, 8]. Однако вне зависимости от характера энергии, применяемой для рассечения или удаления рубцовых тканей, основным осложнением трансуретральных операций остается риск наступления рецидива. К рецидиву могут привести избыточная резекция в области шейки мочевого пузыря, выполнение операции на фоне имеющегося воспаления (острая задержка мочеиспускания, простатит, в том числе и после биопсии простаты), а также рецидивирующего воспаления в области послеоперационной раны [4]. После открытой, лапароскопической и роботизированной аденомэктомии помимо воспаления осложнить состояние пациентов могут ишемические нарушения в области шейки мочевого пузыря (избыточное наложение швов, длительное натяжение уретрального катетера), прорезывание шовного материала с формированием камней и аллергической реакции на шовный материал [6, 9].
Трансуретральная монополярная или холодная инцизия шейки мочевого пузыря до сих пор остается эффективным методом лечения в большинстве случаев, но некоторые больные нуждаются в повторной операции [10]. У пациентов с рецидивами заболевания после радикальной простатэктомии частота рецидивов после трансуретральной инцизии варьирует от 9 до 38% [9, 12]. Проведению полноценных доказательных исследований в этой области препятствует выраженная гетерогенность групп больных, которая не позволяет набрать две сравнимые группы больных.
Вопрос о сравнительной эффективности инцизии и резекции у больных со склерозом шейки мочевого пузыря, особенно с рецидивирующим, до конца не изучен [11]. Есть данные о том, что трансуретральная инцизия позволяет достичь лучших результатов по сравнению с резекцией рубцовых тканей [13]. Однако в урологической практике чаще проводится радикальное удаление рубцовых тканей. Частота рецидивов после резекции ниже, чем после инцизии – 22,5 против 38,5% [13, 14].
Ряд авторов отмечают, что рецидивный рубцовый процесс – относительное противопоказание к повторной расширенной резекции в данной зоне [13]. Оптимистичные результаты были показаны при инъекциях митомицина в сочетании с инцизией шейки мочевого пузыря (частота успеха 72% после первой операции и 89% после повторной) [13].
Биполярная вапоризация также применяется в лечении пациентов со склерозом шейки мочевого пузыря. К преимуществам метода относится отсутствие прохождения тока через организм пациента. Это позволяет удалять рубцовые ткани без риска повреждения подлежащих структур (устья мочеточника, наружного сфинктера, сосудисто-нервных пучков), а значит, достигать лучших функциональных результатов, если не в отношении развития повторного рецидива, то по крайней мере в отношении удержания мочи и сохранения эректильной функции [14, 15]. B. Geavlete и соавт. сравнили эффективность инцизии холодным ножом, резекции и биполярной вапоризации у пациентов со склерозом шейки мочевого пузыря. Частота рецидивов составила 18,7, 12,8 и 5,4% соответственно [11].
Следует отметить работу B. Lagerveld и соавт., в которой были проанализированы результаты применения гольмиевого лазера. Впервые авторы указали на необходимость сохранения сосудов при удалении рубцовых тканей, и это позволило улучшить результаты лечения данной категории пациентов. При использовании гольмиевой энергии повреждающее действие минимально и не приводит к выраженному повреждению сосудов в зоне удаленных тканей, что создает условия для лучшего заживления послеоперационной раны [7]. Позднее сходные данные были показаны и для тулиевого лазера, за тем исключением, что у последнего выше скорость удаления рубцовых тканей, что, однако, не принципиально, так как общая продолжительность операции не превышает одного часа [8].
Важное преимущество лазерной энергии – безопасность ввиду предсказуемой глубины проникновения (0,4 мм), отсутствия риска стимуляции запирательного нерва и перфорации капсулы. Операции с лазерной энергией можно проводить пациентам, принимающим антикоагулянты, не переводя их на низкомолекулярные гепарины. Развитие кровотечения в послеоперационном периоде, требующее усиления гемостатической терапии, повторной цистоскопии, с отмыванием сгустков, электрокоагуляции кровоточащих сосудов, повторной катетеризации, считается одним из факторов риска, приводящих к рецидиву фиброза в зоне операции [14].
Наш опыт проведения подобных операций позволил разработать собственную методику, которая не описана в доступной нам литературе. Места для проведения разрезов определяются на основании изучения ангиоархитектоники в области шейки мочевого пузыря при проведении узкоспектровой фиброскопии или компьютерной хромоэндоскопии. Улучшают результаты оперативного лечения такие факторы, как ликвидация инфекции до операции, пролонгированный курс антибактериальной терапии после операции, прием альфа-адреноблокаторов на период заживления послеоперационной раны, отсроченное удаление уретрального катетера для профилактики острой задержки мочеиспускания и повторных катетеризаций мочевого пузыря, связанных с сопутствующей гипотонией детрузора.
Принципиальное значение для получения положительных результатов в данном исследовании имела профилактика повторного рецидива препаратом Лонгидаза®. Лонгидаза® – полифункциональный ферментный препарат, который используется для терапии заболеваний с преобладанием пролиферативной стадии воспаления. Наш опыт свидетельствует о необходимости применения препарата Лонгидаза® с раннего послеоперационного периода и на протяжении всего срока заживления послеоперационной раны. Главное преимущество препарата Лонгидаза® заключается в нормализации соединительнотканных процессов в области послеоперационной раны.
Лонгидаза® по механизму действия существенно отличается от всех препаратов, имеющих в своей основе гиалуронидазу. Благодаря уникальной технологии конъюгации фермента в препарате Лонгидаза® значительно увеличивается устойчивость гиалуронидазы к инактивирующим воздействиям (действию ингибиторов гепарина, двухвалентного железа и т.д.), достигается пролонгированное действие препарата (режим введения один раз в три – десять дней), уменьшается число побочных реакций. Препарат оказывает двойное действие: подавляет гиперплазию соединительной ткани и ингибирует воспалительный процесс – причину гиперплазии.
К основным терапевтическим эффектам препарата относятся подавление способности гликозаминогликанов связывать воду, уменьшение вязкости экстрацеллюлярного матрикса соединительной ткани. Как следствие снижается отечность, улучшается микроциркуляция, усиливается обмен веществ в тканях, облегчается движение жидкости в межклеточном пространстве, рассасываются воспалительные экссудаты, гематомы, инфильтраты. Кроме того, применение препарата Лонгидаза® повышает эффективность противовоспалительной терапии, способствуя элиминации возбудителей из очага воспаления за счет увеличения биодоступности антибиотиков и других лекарственных средств.
Благодаря нескольким формам выпуска можно последовательно назначить препарат Лонгидаза® сначала внутримышечно, а потом ректально, а также рекомендовать пациенту провести амбулаторно повторный курс лечения ректальными суппозиториями.
Терапия препаратом Лонгидаза® позволяет снизить риск наступления рецидива даже у пациентов с рецидивами после предыдущих операций.
Заключение
Использование лазерной энергии на основании изучения строения сосудов подслизистого слоя в зоне шейки мочевого пузыря для определения направления разрезов в сочетании с терапией препаратом Лонгидаза® позволяет улучшить результаты лечения больных с рецидивами склероза шейки мочевого пузыря.
A.G. Martov, D.V. Yergakov
FSBI ‘State Research Center – Burnasyan Federal Medical Biophysical Center’
City Clinical Hospital named after D.D. Pletnev
Contact person: Aleksey Georgiyevich Martov, martovalex@mail.ru
After performing primary transurethral operations, it was found that cicatrical complications in urethra and bladder neck emerged in 10–15% patients. Here, an experience of using Holmium laser bladder neck incision vs. resection in 87 patients with recurrent bladder neck sclerosis is discussed. Special attention was paid to using Longidaza® as intramuscular injections and rectal suppositories to prevent development of cicatricial process in post-surgery period.
