Клиническая эффективность антигипертензивной терапии у беременных с артериальной гипертензией и различной прибавкой массы тела за период беременности
- Аннотация
- Статья
- Ссылки
- English

В последнее время отмечается повышение распространенности артериальной гипертензии среди беременных [1, 2]. С одной стороны, это обусловлено планированием беременности в более позднем возрасте, с другой – общемировой тенденцией увеличения числа беременных с избыточной массой тела, ожирением и другими метаболическими нарушениями. Так, по данным проспективного когортного исследования в отношении 245 526 практически здоровых беременных, избыточная масса тела (индекс массы тела (ИМТ) ≥ 25 кг/м2) выявлена у 32,8% из них [3].
Ожирение у матери, так же как и патологическая прибавка массы тела за период беременности, может стать причиной неблагоприятных исходов для женщины и плода. Ретроспективный анализ 2098 беременностей показал, что патологическая прибавка массы тела в первом и втором триместрах ассоциируется с высокой частотой преждевременных родов и оперативного родоразрешения, а также с недоношенностью и незрелостью новорожденного [4]. В другом масштабном ретроспективном исследовании, включавшем пациенток с многоплодной беременностью, выявлена связь патологической прибавки массы тела с высоким риском развития гестационной артериальной гипертензии и преэклампсии [5].
У пациенток с артериальной гипертензией, так же как и у плода, повышается риск тяжелых осложнений. Кроме того, артериальная гипертензия по-прежнему остается ведущей причиной материнской, фетальной и неонатальной смерти. Именно поэтому поиск оптимальных методов ведения таких пациенток является приоритетным и требует междисциплинарного подхода.
Анализ эффективности антигипертензивной терапии у беременных с легкой и умеренной артериальной гипертензией (46 и 28 исследований с участием 4282 и 3200 пациенток соответственно) показал, что назначение одного препарата или более снижает в два раза риск развития тяжелой артериальной гипертензии (19 исследований (n = 2409)). Относительный риск (ОР) составил 0,50 при 95%-ном доверительном интервале (ДИ) 0,41–0,61. Различия рисков – -0,10 (-0,12–-0,07) [6].
Необходимо констатировать, что на сегодняшний день арсенал антигипертензивных препаратов, которые можно применять во время беременности, достаточно ограничен. Любое воздействие, в том числе медикаментозное, может отрицательно повлиять на плод, при положительном влиянии препарата на плод влияние на организм матери может оказаться субоптимальным.
Кроме того, по этическим причинам рандомизированные клинические исследования препаратов во время беременности практически не проводятся, поэтому сведений об эффективности и безопасности новых препаратов для лечения артериальной гипертензии у данной категории пациенток крайне мало.
Согласно рекомендациям Российского кардиологического общества (2013) и экспертов Европейского общества гипертонии/Европейского общества кардиологов (2014) в настоящее время для лечения беременных можно использовать четыре группы антигипертензивных препаратов [7, 8]:
- препараты центрального действия (метилдопа);
- антагонисты кальция дигидропиридинового ряда (нифедипин длительного действия);
- кардиоселективные бета-адреноблокаторы (метопролол, бисопролол);
- альфа- и бета-адреноблокаторы (лабеталол).
Комбинированная терапия показана в случае неэффективности монотерапии в максимальных дозах. Рациональной комбинацией считается «нифедипин длительного действия + бета-адреноблокатор». При ее неэффективности возможно добавление хлортиазида (Гипотиазид) в малых дозах (6,25–12,5 мг в сутки).
Таким образом, артериальная гипертензия и патологическая прибавка массы тела во время беременности являются факторами, оказывающими неблагоприятное влияние на течение беременности и перинатальные исходы. Однако в доступной нам литературе работы, в которых рассматривается эффективность антигипертензивной терапии у беременных при сочетании этих двух патологических состояний, не найдены. Это и стало целью настоящего исследования.
Материал и методы исследования
В исследование было включено 60 пациенток во втором триместре беременности, подписавших информированное согласие на участие. Длительность наблюдения – период беременности.
Обследование участниц осуществлялось по стандартной методике: сбор анамнеза, физикальное обследование, в том числе расчет ИМТ по формуле Кетле, офисное измерение артериального давления (АД) на обеих руках. Контроль АД и самочувствия проводился еженедельно, все лабораторные и инструментальные исследования – исходно и в течение периода наблюдения.
Для суточного мониторирования АД использовали аппарат CardioTens (Meditech Ltd, Венгрия). АД регистрировалось с интервалом 15 минут в период бодрствования (с 07.00 до 23.00) и 30 минут в период сна (с 23.00 до 07.00). Анализировали среднее значение систолического и диастолического АД в дневные (ср. САД дн., ср. ДАД дн.) и ночные (ср. САД н., ср. ДАД н.) часы, максимальное САД дн. и ДАД дн., временной гипертонический индекс (ГИ) САД и ДАД, суточный индекс (СИ) САД и ДАД, среднюю частоту сердечных сокращений (ЧСС).
Микроальбуминурию (МАУ) определяли с помощью аппарата HemoCue Albumin 201 методом иммунохимической реакции. В качестве анализируемого образца использовали первую утреннюю мочу. МАУ измерялась исходно и три раза во время лечения. В качестве статистических значений брали средний результат. Нормой считалась МАУ < 20 мг/л.
Допустимую физиологическую прибавку массы тела в период беременности рассчитывали с учетом ИМТ до беременности согласно рекомендациям Института медицины и Национального исследовательского совета по увеличению массы тела во время беременности в контексте эпидемии ожирения (2010) [9] (табл. 1).
У всех пациенток была диагностирована гипертоническая болезнь первой-второй стадии первой и второй степени [10]. Примерно треть из них знала о заболевании и эпизодически принимала антигипертензивные препараты. После наступления беременности 85% пациенток применяли метилдопу (средняя доза 1500 мг в сутки), оставшаяся часть – на момент включения в исследование никаких препаратов не получала.
При стойком повышении АД со второго триместра 47 (78%) пациенткам в связи с неэффективностью метилдопы назначили бисопролол (препарат Конкор, компания «Такеда») в дозе 2,5–5,0 мг в сутки, через восемь недель из-за отсутствия должного гипотензивного эффекта 9 (19%) из них в схему лечения был добавлен нифедипин SR/GITS (препарат Нифекард ХЛ, компания «Сандоз») в дозе 30 мг в сутки. 13 (22%) пациенток с начала наблюдения получали комбинацию бисопролола 5,0–10,0 мг и нифедипина SR/GITS 30 мг в сутки. Таким образом, через 14 недель 38 (63%) беременных получали монотерапию бисопрололом и 22 (37%) – терапию бисопрололом и нифедипином SR/GITS. Данные антигипертензивные средства отнесены к категории С по классификации Управления по контролю за качеством пищевых продуктов и лекарственных средств США и могут быть использованы у беременных [11].
Если при сроке беременности 20 недель и более обнаруживали ≥ 300 мг белка в 24-часовом образце мочи и фиксировали повышение АД, ставили диагноз «преэклампсия».
Статистическую обработку результатов осуществляли с помощью пакета прикладных программ Statistica 6.0 (StatSoft Inc., США). При непараметрическом распределении данных рассчитывали медиану (Ме) и интерквартильный размах (25-й квартиль; 75-й квартиль). Сравнение двух независимых групп проводили с использованием непараметрического критерия Манна – Уитни. Оценку межгрупповых различий по качественным порядковым и бинарным признакам выполняли с использованием критерия Пирсона (критерия χ2). Использовали также многофакторный анализ с расчетом ОР и 95% ДИ. Различие считали достоверным при p < 0,05.
Результаты
Ретроспективно в зависимости от прибавки массы тела за время беременности все пациентки были разделены на две группы. В первой группе (n = 43) увеличение массы тела было в пределах физиологической нормы (Ме 12,9 кг [11,8; 16,1]). Во второй (n = 17) – указанный показатель превышал допустимые референсные значения (Ме 15,3 кг [11,4; 17,6]).
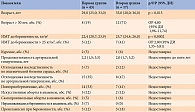
Анализ полученных данных продемонстрировал, что риск патологической прибавки массы тела у беременных с артериальной гипертензией в возрасте 30 лет и старше увеличивается в 4,8 раза. Неблагоприятное прогностическое значение имеет ИМТ, превышающий 25 кг/м2 (ОР 2,80 (95% ДИ 1,35–5,81)) (табл. 2).
Другие факторы не оказывали существенного влияния на динамику данного показателя.
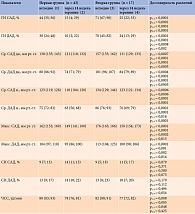
Результаты суточного мониторирования АД через 14 недель лечения в обеих группах свидетельствовали о достоверном снижении всех основных показателей (табл. 3).
Следует отметить, что исходно значения суточного мониторирования АД были выше во второй группе. Около 85% пациенток этой группы имели артериальную гипертензию второй степени. У пациенток первой группы чаще отмечалась первая степень.
Несмотря на достоверное снижение всех показателей АД, через 14 недель от начала терапии целевых значений достигли только 97% беременных первой группы и 82% – второй, что потребовало дальнейшей коррекции антигипертензивной терапии.
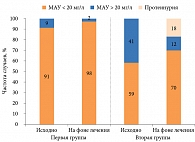
Отмечено также положительное влияние антигипертензивной терапии на уровень МАУ и частоту ее выявления. Так, во втором триместре беременности МАУ установлена у 11 пациенток: 4 (9%) из первой группы и 7 (41%) из второй. Через 14 недель лечения число пациенток с МАУ значительно сократилось в обеих группах: в первой – одна больная (2%), во второй – две (11%). Однако у трех пациенток была выявлена протеинурия. Наличие протеинурии в сочетании с артериальной гипертензией дало основание поставить диагноз «преэклампсия» (см. рисунок).
Полученные данные свидетельствуют о том, что адекватная антигипертензивная терапия способствует оптимизации АД, оказывает нефропротективный эффект, улучшает функцию сосудистого эндотелия, одним из ранних маркеров повреждения которого является МАУ.
Обсуждение результатов
Чрезмерная прибавка массы тела во время беременности – прогностически неблагоприятный фактор. Установлено, что у женщин с нормальной массой тела до беременности и патологической ее прибавкой в течение беременности вероятность развития сердечно-сосудистых событий, ожирения и дислипидемии в отсроченном послеродовом периоде значительно возрастает [12]. У женщин с избыточной массой тела или ожирением до беременности чрезмерное увеличение массы тела в ряде случаев способствует развитию гестационного сахарного диабета [13]. Наше исследование продемонстрировало, что к факторам, способным повлиять на чрезмерную прибавку массы тела у беременных, относятся возраст старше 30 лет и ИМТ более 25 кг/м2 до беременности – повышение указанного риска в 4,8 и 2,8 раза соответственно. Кроме того, пациенткам с патологической прибавкой массы тела для коррекции АД требовалась комбинированная терапия. При этом положительного ответа через 14 недель лечения достигло меньшее количество больных.
Следует подчеркнуть, что антигипертензивная терапия проводилась современными препаратами, способными оказать органопротективный эффект. Так, дигидропиридиновые антагонисты кальция, к которым относится нифедипин SR/GITS, за счет блокады медленных потенциалзависимых кальциевых каналов L-типа, уменьшения внутриклеточной концентрации Са2+, а также стимуляции синтеза эндотелием NO и брадикинина вызывают периферическую вазодилатацию и, как следствие, снижение АД [14, 15]. Компенсаторной реакцией организма на системную вазодилатацию является активация симпатико-адреналовой системы. Однако в ряде исследований показано, что не все препараты данной группы обладают подобным эффектом. Как правило, к симпатической активации с развитием тахикардии приводит применение нифедипина короткого действия, такого эффекта не наблюдается при применении нифедипина пролонгированного действия [16, 17]. Результаты многоцентрового рандомизированного исследования свидетельствуют, что рутинное назначение нифедипина пролонгированного действия при легкой и среднетяжелой артериальной гипертензии во втором триместре беременности не оказывает положительного влияния на исходы беременности, но и не сопряжено с повышенным риском отрицательного воздействия на плод [18–20]. Исследователи отмечают, что нифедипин не приводил к повышению частоты врожденных аномалий у 57 детей, матери которых применяли препарат с первого триместра беременности [21]. Вместе с тем, по данным баз Medline (1996–2005), EMBASE (1996–2003), BIOSIS (1993–2003), Current contents (1995–2003), DERWENT DRUGFILE (1983–2003) и COCHRANE LIBRARY (2005) – 269 докладов, у 5607 пациенток, получавших нифедипин в дозе более 60 мг в сутки, а также у их плода зарегистрированы неблагоприятные побочные эффекты (отношение шансов (ОШ) 3,78 (95% ДИ 1,27–11,2, р = 0,017)). ОШ в исследованиях с небольшим количеством пациенток по сравнению с контролируемыми исследованиями составило 2,45 (95% ДИ 1,17–5,15), р = 0,018 [22].
Бисопролол, используемый в исследовании как в монотерапии, так и в комбинированной терапии с нифедипином медленного действия, представляет собой высокоселективный бета-адреноблокатор. Согласно классификации Управления по контролю за качеством пищевых продуктов и лекарственных средств США препарат относится к категории С. Механизм его действия заключается в ослаблении или устранении эффектов, связанных с возбуждением катехоламинами бета-1-адренорецепторов, которые вызывают учащение сердечного ритма, повышение автоматизма атриовентрикулярного узла и возбудимости миокарда, скорости проведения импульсов, усиление сократительной способности миокарда, уменьшение рефрактерного периода, активации липолиза. Возбуждение катехоламинами бета-2-адренорецепторов приводит к расширению артериол, снижению тонуса гладкой мускулатуры бронхов, мочевого пузыря, тонуса матки при беременности, тремору скелетной мускулатуры, ингибированию высвобождения гистамина, лейкотриенов в тучных клетках при аллергических реакциях первого типа, гипокалиемии, усилению печеночного гликогенолиза. Бета-адреноблокаторы могут вызвать задержку внутриутробного развития плода вследствие снижения маточно-плацентарного и фетоплацентарного кровотока, преждевременную родовую деятельность. Это касается в основном низкоселективного атенолола, который входит в категорию D по классификации Управления по контролю за качеством пищевых продуктов и лекарственных средств США и который не рекомендуют назначать при беременности. При применении препаратов этой группы у плода могут наблюдаться брадикардия, гипогликемия, апноэ, метаболические расстройства. Однако частота указанных неблагоприятных явлений достаточно низкая и при необходимости назначения бета-адреноблокаторов рассматривается соотношение «риск – польза». В 2003 г. L.A. Magee и соавт. обобщили опыт применения бета-адреноблокаторов при легкой и умеренной артериальной гипертензии у беременных. Для анализа использованы данные Кокрановских обзоров и других регистров [23]. Авторы изучили результаты 29 клинических исследований (примерно 2500 пациенток), в которых сравнивались эффективность и безопасность бета-адреноблокаторов с плацебо, отсутствием терапии или другими антигипертензивными препаратами. Показано, что пероральный прием бета-адреноблокаторов снижает риск развития тяжелой гипертензии (ОР 0,37 (95% ДИ 0,26–0,53) по 11 клиническим исследованиям, n = 1128) и необходимость назначения дополнительной антигипертензивной терапии (ОР 0,44 (95% ДИ 0,31–0,62) по семи клиническим исследованиям, n = 856). Авторы сделали вывод, что бета-адреноблокаторы не влияют на показатели смертности и преждевременных родов. Однако они отметили, что применение препаратов ассоциировалось с увеличением числа новорожденных с малым гестационным возрастом (ОР 1,36 (95% ДИ 1,02–1,82) по 12 клиническим исследованиям, n = 1346), увеличением неонатальной брадикардии и снижением респираторного дистресс-синдрома у новорожденных. Указанные конечные точки анализировались в небольшом количестве исследований. Таким образом, улучшение контроля АД с помощью бета-адреноблокаторов у беременных с артериальной гипертензией может быть показано только при условии существенной пользы для матери и/или ребенка.
Органопротективный эффект антигипертензивной терапии, отмеченный другими авторами [24–26], продемонстрирован и в нашем исследовании: уменьшилось количество пациенток с МАУ, кроме того, снизились ее средние значения. На фоне лечения увеличилось количество пациенток с нормальной МАУ (< 20 мг/л). Если исходно в первой и второй группах таковых было 91 и 59%, на фоне антигипертензивной терапии их доля составила 98 и 70% соответственно.
Однако у пациенток с патологической прибавкой массы тела во время беременности и изначально высокими значениями МАУ (более 100 мг/л) нефропротективный эффект проявился слабее и чаще диагностировалась преэклампсия.
Следует отметить, что полученные данные согласуются с данными исследований, показавших важность динамического контроля уровня МАУ, который рассматривается как один из ранних маркеров преэклампсии [27].
Вывод
Результаты проведенного исследования показали, что у женщин старше 30 лет с исходно повышенным ИМТ достоверно чаще наблюдаются чрезмерная прибавка массы тела во время беременности и более высокие значения АД, соответствующие второй степени по классификации Всемирной организации здравоохранения/Российского медицинского общества по артериальной гипертонии. Применение высокоселективного бета-адреноблокатора бисопролола и нифедипина медленного действия как в виде моно-, так и комбинированной терапии способствует нормализации АД и снижению скорости экскреции альбумина с мочой, частоты выявления МАУ.
R.I. Stryuk, Ya.V. Brytkova
Moscow State University of Medicine and Dentistry named after A.I. Еvdokimov
Contact person: Raisa Ivanovna Stryuk, rstryuk@list.ru
Here we present study results on efficacy of antihypertensive therapy in pregnant women with hypertension and varying weight gain during the pregnancy. It was shown that women over 30 having initially increased Body Mass Index were found to have significantly more frequent body gain during pregnancy and higher magnitude of arterial blood pressure, which correspond to stage II. Use of highly selective beta-blocker bisoprolol and slow-release nifedipine both as monotherapy and in a combination therapy results in normalized arterial blood pressure and decreased albumin excretion rate and frequency of microalbuminuria.
