количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Клинические случаи
Клинический опыт применения оригинального метаболического препарата Элтацин у больных с хронической сердечной недостаточностью
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Кардиология и Ангиология" №5
- Аннотация
- Статья
- Ссылки
В статье представлены результаты клинического изучения метаболического препарата Элтацин (разработан в ООО «МНПК “БИОТИКИ”»), фиксированной комбинации трех заменимых аминокислот: глицина, L-глутаминовой кислоты и L-цистина (по 70 мг каждой).
В четырех лечебных учреждениях г. Москвы обследованы 156 больных с хронической сердечной недостаточностью (ХСН) по протоколу двойного слепого плацебоконтролируемого исследования. В дополнение к стандартной терапии (ингибиторы АПФ, бета-адреноблокаторы, нитраты, антиагреганты и/или диуретики) 104 пациента получали препарат Элтацин по 1 таблетке сублингвально три раза в день в течение трех недель, 52 пациента – плацебо.
Анализ сравнительной оценки результатов лечения показал: включение Элтацина в стандартную терапию (СТ) больных ХСН положительно влияет на динамику клинических симптомов: стойкий клинический эффект в группе Элтацина отмечен на 3,8-е сутки, в группе плацебо – на 5,8-е сутки; снижение ФК ХСН составило 33% и 19%, повышение толерантности к физической нагрузке – 60% и 38%, улучшение показателя 6-минутного теста ходьбой – 30% и 22% соответственно (различия достоверны). Включение Элтацина в СТ приводит к значительному улучшению систолической функции левого желудочка, способствует повышению сократительной способности миокарда, в значительной степени нормализует диастолическую функцию левого желудочка, оказывает нормализующее влияние на баланс в системе «оксиданты/антиоксиданты». На основании полученных данных рекомендовано применять Элтацин в составе комплексной терапии больных хроническими заболеваниями сердца.
В статье представлены результаты клинического изучения метаболического препарата Элтацин (разработан в ООО «МНПК “БИОТИКИ”»), фиксированной комбинации трех заменимых аминокислот: глицина, L-глутаминовой кислоты и L-цистина (по 70 мг каждой).
В четырех лечебных учреждениях г. Москвы обследованы 156 больных с хронической сердечной недостаточностью (ХСН) по протоколу двойного слепого плацебоконтролируемого исследования. В дополнение к стандартной терапии (ингибиторы АПФ, бета-адреноблокаторы, нитраты, антиагреганты и/или диуретики) 104 пациента получали препарат Элтацин по 1 таблетке сублингвально три раза в день в течение трех недель, 52 пациента – плацебо.
Анализ сравнительной оценки результатов лечения показал: включение Элтацина в стандартную терапию (СТ) больных ХСН положительно влияет на динамику клинических симптомов: стойкий клинический эффект в группе Элтацина отмечен на 3,8-е сутки, в группе плацебо – на 5,8-е сутки; снижение ФК ХСН составило 33% и 19%, повышение толерантности к физической нагрузке – 60% и 38%, улучшение показателя 6-минутного теста ходьбой – 30% и 22% соответственно (различия достоверны). Включение Элтацина в СТ приводит к значительному улучшению систолической функции левого желудочка, способствует повышению сократительной способности миокарда, в значительной степени нормализует диастолическую функцию левого желудочка, оказывает нормализующее влияние на баланс в системе «оксиданты/антиоксиданты». На основании полученных данных рекомендовано применять Элтацин в составе комплексной терапии больных хроническими заболеваниями сердца.
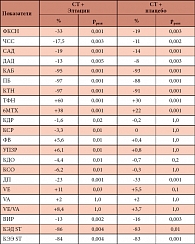
Таблица 1. Динамика основных исследуемых параметров (%) в группах больных, получавших на фоне традиционной терапии Элтацин сублингвально и
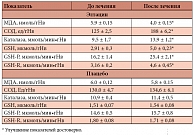
Таблица 2. Влияние Элтацина и плацебо на системы ПОЛ и АОЗ
Хроническая сердечная недостаточность (ХСН) является одним из тяжелых и прогностически неблагоприятных осложнений таких сердечно-сосудистых заболеваний, как ишемическая болезнь сердца (ИБС), артериальная гипертония, кардиомиопатии, пороки сердца и др. [1, 2].
Среди пациентов с ХСН I–IV ФК средняя годовая смертность достигает 12% даже в условиях лечения в специализированных стационарах, то есть за один год в РФ умирают более 600 тыс. больных ХСН [3, 4, 5].
Исходя из ключевой роли атеросклероза в патогенезе большинства сердечно-сосудистых заболеваний, следует отметить, что наиболее радикальным способом помощи больным является восстановление нарушенного кровообращения. Однако хирургическое воздействие на сосуды не всегда возможно из-за общего тяжелого состояния пациента, сопутствующих заболеваний и т.д. С другой стороны, применение традиционной терапии (блокаторы нейрогуморальных систем, диуретики, сердечные гликозиды) часто сопровождается нежелательными явлениями и имеет свои пределы. Все это определяет необходимость разработки новых лекарственных препаратов, которые по механизму действия отличаются от блокаторов нейрогуморальных систем и могут дополнить комбинированную терапию ХСН [14].
В последние годы широкое применение получили принципиально новые подходы к лечению ИБС, основанные на использовании препаратов, влияющих на метаболизм клетки [8, 9, 10, 12]. Основой кардиопротективного действия метаболитных препаратов, в первую очередь, является их способность к стимуляции энергообразующей и энергосберегающей функции клеток [7].
При ИБС, особенно с явлениями недостаточности кровообращения, происходит как нарастание окислительного стресса, так и снижение активности защитных систем, в частности глутатион-пероксидазной системы, осуществляющей в конечном итоге детоксикацию перекисей. Такие метаболические нарушения сопровождаются увеличением активных форм кислорода и истощением, угнетением системы антиоксидантной защиты организма (АОЗ) [7, 9]. Для профилактики указанных метаболических сдвигов особое значение приобретают щадящие способы коррекции, основанные на исправлении нарушенного баланса и восстановлении пула ключевых метаболитов, к которым относится, в частности, глутатион. Особая роль глутатиона, как кофактора целого ряда окислительно-восстановительных ферментов, регулятора содержания SH-групп, активного компонента глутатион-конъюгирующей системы, участвующей в детоксикации ксенобиотиков и инактивации свободнорадикальных продуктов, позволяет рассматривать препараты, повышающие уровень глутатиона в клетке, как истинные антиоксиданты [11]. И если такие препараты полностью безопасны, их применение в клинике приобретает особенно актуальное значение. В этой связи создание нового лекарственного препарата, содержащего оригинальную композицию аминокислот, оказывающего эффективное индуцирующее действие на внутриклеточный пул глутатиона, активирующего глутатион-зависимые и антиоксидантные ферменты, представляет значительный практический интерес как для клинической, так и для профилактической медицины.
Примером такого класса препаратов является новый метаболитный препарат Элтацин, разработанный в ООО «МНПК “БИОТИКИ”». Элтацин – композиция из трех заменимых аминокислот: глицина, L-глутаминовой кислоты и L-цистина, по 70 мг каждой. Все вышеназванные аминокислоты являются естественными метаболитами.
Доклинические исследования показали, что фармакологическое действие препарата связано с избирательной индукцией синтеза глутатиона (GSH) – одного из основных эндогенных антиоксидантов и кофакторов окислительно-восстановительных ферментов. Элтацин – многоплановый препарат и обладает способностью увеличивать энергетику клетки, связывать свободные радикалы, уменьшать процессы перекисного окисления, повышать эффективность использования кислорода. А снижение уровня GSH и антиоксидантных ферментов является одним из ведущих факторов в развитии процессов старения, ИБС и таких осложнений, как сердечная недостаточность.
Экспериментально было доказано, что Элтацин повышает внутриклеточный уровень глутатиона и глутатион-зависимых ферментов, активность окислительно-восстановительных ферментов и синтез АТФ, уменьшает процессы перекисного окисления, то есть проявляет свойства прямого и непрямого антиоксиданта и антигипоксанта. Токсикологические исследования препарата показали, что препарат безопасен.
Материалы и методы
Клиническое изучение Элтацина проведено в четырех лечебных учреждениях г. Москвы у 156 больных с ХСН по протоколу двойного слепого плацебоконтролируемого исследования.
Обследовано 156 больных (64 мужчины и 92 женщины) в возрасте от 59 до 83 лет с ишемической болезнью сердца, стабильной стенокардией (СС), перенесших инфаркт миокарда и страдающих хронической сердечной недостаточностью II–III ФК по классификации NYHA. У 54 больных была диагностирована гипертоническая болезнь (ГБ) III ст., у 25 больных – сахарный диабет (СД) 2 типа, 4 пациента перенесли острое нарушение мозгового кровообращения (ОНМК) в анамнезе. Тяжелые соматические больные, с высокими цифрами АД (САД выше 220 мм рт. ст. и ДАД более 120 мм рт. ст.), больные с фракцией выброса менее 35%, с постоянной формой мерцательной аритмии, с психическими отклонениями в исследование не включались.
Все обследуемые получали стандартную терапию (СТ): ингибиторы АПФ, бета-адреноблокаторы, нитраты, антиагреганты и/или диуретики. Кроме того, 104 пациента получали в дополнение к стандартной терапии препарат Элтацин по 1 таблетке сублингвально три раза в день в течение трех недель, 52 пациента – плацебо (внешне плацебо представляло собой такую же таблетку, как и Элтацин, не различались таблетки и по вкусу, но Элтацин был в розовом блистере, а плацебо – в синем).
Лабораторные анализы включали: общий анализ крови, общий анализ мочи, определение содержания в крови холестерина, триглицеридов, билирубина, показателей коагулограммы, общего белка, мочевины, креатинина, остаточного азота, глюкозы, ферментов (аланиновая и аспарагиновая трансаминазы, лактатдегидрогеназы и креатинфосфокиназы). Данные ЭКГ-исследования помогали подтвердить диагноз перенесенного ИМ в анамнезе и выявить локализацию рубцовых зон, а также нарушения коронарного кровообращения при обострении заболевания в виде участков ишемии, нарушения сердечного ритма и проводимости. При рентгенологическом исследовании интерес представляло наличие застойных явлений в легких и расширение левых границ сердца, почти у всех больных выявлялось уплотнение аорты и расширение левых границ сердца. Для измерения артериального давления использовали метод Н.С. Короткова.
Изучение клинических симптомов включало: количество ангинозных болей в сутки (КАБ), продолжительность ангинозных болей (ПБ), количество таблеток нитроглицерина в сутки (КТН), толерантность к физической нагрузке (ТФН), тест с 6-минутной ходьбой (6МТХ).
Для удобства оценки клинического состояния пациент ежедневно вел дневник, в котором фиксировались КАБ, ПБ, КТН и ТФН. Показатели центральной гемодинамики (ПЦГ) оценивали с помощью ЭхоКГ.
Степень окислительного стресса определяли по уровню продуктов перекисного окисления липидов (ПОЛ) и антиоксидантной защиты (АОЗ) до лечения и после: уровень малонового диальдегида (МДА), содержание глутатиона (GSH), глутатион-зависимых ферментов: глутатион-пероксидазы и глутатион-редуктазы (GSH-P, GSH-R), а также каталазы и супероксиддисмутазы (СОД) в эритроцитах.
Полученные результаты проанализированы методом вариационной статистики, включая разностный метод, с помощью t-критерия Стьюдента. Различия считали достоверными при р < 0,05.
Результаты и обсуждение
В обеих группах больные отметили улучшение общего самочувствия, повышение настроения, выраженное снижение количества ангинозных болей в течение суток, их продолжительности и потребности в нитроглицерине для купирования болей. Больные отмечали постепенное уменьшение одышки и, как следствие этого, повышение толерантности к физической нагрузке. День наступления стойкого клинического эффекта в первой группе (Элтацин) отмечается раньше (на 3,8 ± 0,2 сутки), чем в группе плацебо (на 5,8 ± 0,5 сутки).
Анализ сравнительной оценки результатов лечения в основной группе и контрольной (больные на фоне СТ получали плацебо) свидетельствует, что включение Элтацина в стандартную терапию оказывает наиболее благоприятное воздействие по сравнению с контрольной группой, то есть при сочетании СТ с плацебо.
Снижение ФК ХСН было достоверным в обеих группах, однако в большей степени оно отмечалось в первой группе – на 33%, в контрольной – на 19%.
Кроме этого, включение в СТ Элтацина приводит к достоверному снижению уровней ХС и ТГ в основной группе. Динамика этих показателей в контрольной группе была недостоверной. В то же время динамика таких клинических показателей, как количество ангинозных болей (КАБ), продолжительность боли (ПБ) и количество таблеток нитроглицерина (КТН), была достоверной в обеих группах. В первой группе КАБ, ПБ и КТН уменьшились на 95%, 97% и 97%, в контрольной – на 93%, 88% и 91% соответственно, то есть по динамике этих показателей группы не отличались. Это можно объяснить тем, что, безусловно, нитраты действуют в любой группе одинаково и быстро.
Положительная динамика клинической симптоматики проявлялась достоверным повышением толерантности к физической нагрузке (ТФН) и 6-минутного теста ходьбой (6МТХ) в обеих группах. Более выраженное увеличение этих параметров отмечается в основной группе: в первой группе ТФН и 6МТХ возросли на 60% и 38%, в контрольной группе – на 30% и 22% соответственно.
Анализ сравнительной оценки параметров гемодинамики в исследуемых группах показал, что изменение данных показателей в основной группе было достоверным, а в контрольной группе динамика только уровня ДАД была значимой. Снижение ЧСС и уровня САД и ДАД в первой группе составило 11%, 14% и 8%, в контрольной группе – 17,5%, 19% и 13% соответственно, то есть было сопоставимо. Сравнительный анализ морфофункциональных параметров свидетельствует, что достоверное изменение размеров и объемов левого желудочка, а также ФВ, УПЗР, УО и размера ЛП отмечается только в первой (основной) группе. Динамика указанных параметров у пациентов контрольной группы была недостоверна. Изложенное свидетельствует, что включение в СТ Элтацина приводит к значительному улучшению систолической функции левого желудочка (СФ ЛЖ) и способствует повышению сократительной способности миокарда, чего не наблюдается в группе больных, получавших на фоне СТ плацебо.
С помощью допплер-ЭхоКГ во всех группах до начала лечения была выявлена нарушенная модель диастолической функции левого желудочка (ДФ ЛЖ). Это проявилось тем, что значения величин VE, VА, VE/VA и ВИР более приблизились к нарушенной модели замедленного расслабления (или аномальной релаксации). Курс проведенного лечения в основной группе в большей степени оказывал нормализующее влияние на диастолическую дисфункцию. Это проявилось в первой подгруппе достоверным повышением величины VE на 11% и снижением ВИР на 13%. В контрольной группе достоверным было лишь уменьшение значения ВИР на 16%.
Таким образом, включение в СТ Элтацина в значительной степени нормализует ДФЛЖ по сравнению с контрольной группой.
Влияние Элтацина и плацебо на перекисное окисление липидов и антиоксидантную защиту представлено в таблице 2.
Легко видеть, что курс проведенного лечения Элтацином способствовал благоприятной динамике параметров антиоксидантного статуса. Это выражалось в достоверном увеличении всех исследуемых показателей АОЗ: СОД, каталазы, GSH, GSH-P, GSH-R. В группе плацебо подобных изменений в антиоксидантной системе выявлено не было.
Изложенное свидетельствует о том, что проведенная стандартная терапия в сочетании с Элтацином оказывает нормализующее влияние на баланс в системе «оксиданты/антиоксиданты», уменьшая при этом уровень ПОЛ и увеличивая АОЗ организма.
Таким образом, исследование влияния препарата Элтацин на параметры клеточного редокс-статуса позволило установить его сбалансированное действие на внутриклеточный уровень антиоксидантной системы. В то же время традиционная терапия практически не оказывала влияния на уровень перекисного окисления липидов.
Элтацин хорошо переносится, ни у одного пациента на протяжении лечения Элтацином не было выявлено ни одного нежелательного явления.
Выводы
Среди пациентов с ХСН I–IV ФК средняя годовая смертность достигает 12% даже в условиях лечения в специализированных стационарах, то есть за один год в РФ умирают более 600 тыс. больных ХСН [3, 4, 5].
Исходя из ключевой роли атеросклероза в патогенезе большинства сердечно-сосудистых заболеваний, следует отметить, что наиболее радикальным способом помощи больным является восстановление нарушенного кровообращения. Однако хирургическое воздействие на сосуды не всегда возможно из-за общего тяжелого состояния пациента, сопутствующих заболеваний и т.д. С другой стороны, применение традиционной терапии (блокаторы нейрогуморальных систем, диуретики, сердечные гликозиды) часто сопровождается нежелательными явлениями и имеет свои пределы. Все это определяет необходимость разработки новых лекарственных препаратов, которые по механизму действия отличаются от блокаторов нейрогуморальных систем и могут дополнить комбинированную терапию ХСН [14].
В последние годы широкое применение получили принципиально новые подходы к лечению ИБС, основанные на использовании препаратов, влияющих на метаболизм клетки [8, 9, 10, 12]. Основой кардиопротективного действия метаболитных препаратов, в первую очередь, является их способность к стимуляции энергообразующей и энергосберегающей функции клеток [7].
При ИБС, особенно с явлениями недостаточности кровообращения, происходит как нарастание окислительного стресса, так и снижение активности защитных систем, в частности глутатион-пероксидазной системы, осуществляющей в конечном итоге детоксикацию перекисей. Такие метаболические нарушения сопровождаются увеличением активных форм кислорода и истощением, угнетением системы антиоксидантной защиты организма (АОЗ) [7, 9]. Для профилактики указанных метаболических сдвигов особое значение приобретают щадящие способы коррекции, основанные на исправлении нарушенного баланса и восстановлении пула ключевых метаболитов, к которым относится, в частности, глутатион. Особая роль глутатиона, как кофактора целого ряда окислительно-восстановительных ферментов, регулятора содержания SH-групп, активного компонента глутатион-конъюгирующей системы, участвующей в детоксикации ксенобиотиков и инактивации свободнорадикальных продуктов, позволяет рассматривать препараты, повышающие уровень глутатиона в клетке, как истинные антиоксиданты [11]. И если такие препараты полностью безопасны, их применение в клинике приобретает особенно актуальное значение. В этой связи создание нового лекарственного препарата, содержащего оригинальную композицию аминокислот, оказывающего эффективное индуцирующее действие на внутриклеточный пул глутатиона, активирующего глутатион-зависимые и антиоксидантные ферменты, представляет значительный практический интерес как для клинической, так и для профилактической медицины.
Примером такого класса препаратов является новый метаболитный препарат Элтацин, разработанный в ООО «МНПК “БИОТИКИ”». Элтацин – композиция из трех заменимых аминокислот: глицина, L-глутаминовой кислоты и L-цистина, по 70 мг каждой. Все вышеназванные аминокислоты являются естественными метаболитами.
Доклинические исследования показали, что фармакологическое действие препарата связано с избирательной индукцией синтеза глутатиона (GSH) – одного из основных эндогенных антиоксидантов и кофакторов окислительно-восстановительных ферментов. Элтацин – многоплановый препарат и обладает способностью увеличивать энергетику клетки, связывать свободные радикалы, уменьшать процессы перекисного окисления, повышать эффективность использования кислорода. А снижение уровня GSH и антиоксидантных ферментов является одним из ведущих факторов в развитии процессов старения, ИБС и таких осложнений, как сердечная недостаточность.
Экспериментально было доказано, что Элтацин повышает внутриклеточный уровень глутатиона и глутатион-зависимых ферментов, активность окислительно-восстановительных ферментов и синтез АТФ, уменьшает процессы перекисного окисления, то есть проявляет свойства прямого и непрямого антиоксиданта и антигипоксанта. Токсикологические исследования препарата показали, что препарат безопасен.
Материалы и методы
Клиническое изучение Элтацина проведено в четырех лечебных учреждениях г. Москвы у 156 больных с ХСН по протоколу двойного слепого плацебоконтролируемого исследования.
Обследовано 156 больных (64 мужчины и 92 женщины) в возрасте от 59 до 83 лет с ишемической болезнью сердца, стабильной стенокардией (СС), перенесших инфаркт миокарда и страдающих хронической сердечной недостаточностью II–III ФК по классификации NYHA. У 54 больных была диагностирована гипертоническая болезнь (ГБ) III ст., у 25 больных – сахарный диабет (СД) 2 типа, 4 пациента перенесли острое нарушение мозгового кровообращения (ОНМК) в анамнезе. Тяжелые соматические больные, с высокими цифрами АД (САД выше 220 мм рт. ст. и ДАД более 120 мм рт. ст.), больные с фракцией выброса менее 35%, с постоянной формой мерцательной аритмии, с психическими отклонениями в исследование не включались.
Все обследуемые получали стандартную терапию (СТ): ингибиторы АПФ, бета-адреноблокаторы, нитраты, антиагреганты и/или диуретики. Кроме того, 104 пациента получали в дополнение к стандартной терапии препарат Элтацин по 1 таблетке сублингвально три раза в день в течение трех недель, 52 пациента – плацебо (внешне плацебо представляло собой такую же таблетку, как и Элтацин, не различались таблетки и по вкусу, но Элтацин был в розовом блистере, а плацебо – в синем).
Лабораторные анализы включали: общий анализ крови, общий анализ мочи, определение содержания в крови холестерина, триглицеридов, билирубина, показателей коагулограммы, общего белка, мочевины, креатинина, остаточного азота, глюкозы, ферментов (аланиновая и аспарагиновая трансаминазы, лактатдегидрогеназы и креатинфосфокиназы). Данные ЭКГ-исследования помогали подтвердить диагноз перенесенного ИМ в анамнезе и выявить локализацию рубцовых зон, а также нарушения коронарного кровообращения при обострении заболевания в виде участков ишемии, нарушения сердечного ритма и проводимости. При рентгенологическом исследовании интерес представляло наличие застойных явлений в легких и расширение левых границ сердца, почти у всех больных выявлялось уплотнение аорты и расширение левых границ сердца. Для измерения артериального давления использовали метод Н.С. Короткова.
Изучение клинических симптомов включало: количество ангинозных болей в сутки (КАБ), продолжительность ангинозных болей (ПБ), количество таблеток нитроглицерина в сутки (КТН), толерантность к физической нагрузке (ТФН), тест с 6-минутной ходьбой (6МТХ).
Для удобства оценки клинического состояния пациент ежедневно вел дневник, в котором фиксировались КАБ, ПБ, КТН и ТФН. Показатели центральной гемодинамики (ПЦГ) оценивали с помощью ЭхоКГ.
Степень окислительного стресса определяли по уровню продуктов перекисного окисления липидов (ПОЛ) и антиоксидантной защиты (АОЗ) до лечения и после: уровень малонового диальдегида (МДА), содержание глутатиона (GSH), глутатион-зависимых ферментов: глутатион-пероксидазы и глутатион-редуктазы (GSH-P, GSH-R), а также каталазы и супероксиддисмутазы (СОД) в эритроцитах.
Полученные результаты проанализированы методом вариационной статистики, включая разностный метод, с помощью t-критерия Стьюдента. Различия считали достоверными при р < 0,05.
Результаты и обсуждение
В обеих группах больные отметили улучшение общего самочувствия, повышение настроения, выраженное снижение количества ангинозных болей в течение суток, их продолжительности и потребности в нитроглицерине для купирования болей. Больные отмечали постепенное уменьшение одышки и, как следствие этого, повышение толерантности к физической нагрузке. День наступления стойкого клинического эффекта в первой группе (Элтацин) отмечается раньше (на 3,8 ± 0,2 сутки), чем в группе плацебо (на 5,8 ± 0,5 сутки).
Анализ сравнительной оценки результатов лечения в основной группе и контрольной (больные на фоне СТ получали плацебо) свидетельствует, что включение Элтацина в стандартную терапию оказывает наиболее благоприятное воздействие по сравнению с контрольной группой, то есть при сочетании СТ с плацебо.
Снижение ФК ХСН было достоверным в обеих группах, однако в большей степени оно отмечалось в первой группе – на 33%, в контрольной – на 19%.
Кроме этого, включение в СТ Элтацина приводит к достоверному снижению уровней ХС и ТГ в основной группе. Динамика этих показателей в контрольной группе была недостоверной. В то же время динамика таких клинических показателей, как количество ангинозных болей (КАБ), продолжительность боли (ПБ) и количество таблеток нитроглицерина (КТН), была достоверной в обеих группах. В первой группе КАБ, ПБ и КТН уменьшились на 95%, 97% и 97%, в контрольной – на 93%, 88% и 91% соответственно, то есть по динамике этих показателей группы не отличались. Это можно объяснить тем, что, безусловно, нитраты действуют в любой группе одинаково и быстро.
Положительная динамика клинической симптоматики проявлялась достоверным повышением толерантности к физической нагрузке (ТФН) и 6-минутного теста ходьбой (6МТХ) в обеих группах. Более выраженное увеличение этих параметров отмечается в основной группе: в первой группе ТФН и 6МТХ возросли на 60% и 38%, в контрольной группе – на 30% и 22% соответственно.
Анализ сравнительной оценки параметров гемодинамики в исследуемых группах показал, что изменение данных показателей в основной группе было достоверным, а в контрольной группе динамика только уровня ДАД была значимой. Снижение ЧСС и уровня САД и ДАД в первой группе составило 11%, 14% и 8%, в контрольной группе – 17,5%, 19% и 13% соответственно, то есть было сопоставимо. Сравнительный анализ морфофункциональных параметров свидетельствует, что достоверное изменение размеров и объемов левого желудочка, а также ФВ, УПЗР, УО и размера ЛП отмечается только в первой (основной) группе. Динамика указанных параметров у пациентов контрольной группы была недостоверна. Изложенное свидетельствует, что включение в СТ Элтацина приводит к значительному улучшению систолической функции левого желудочка (СФ ЛЖ) и способствует повышению сократительной способности миокарда, чего не наблюдается в группе больных, получавших на фоне СТ плацебо.
С помощью допплер-ЭхоКГ во всех группах до начала лечения была выявлена нарушенная модель диастолической функции левого желудочка (ДФ ЛЖ). Это проявилось тем, что значения величин VE, VА, VE/VA и ВИР более приблизились к нарушенной модели замедленного расслабления (или аномальной релаксации). Курс проведенного лечения в основной группе в большей степени оказывал нормализующее влияние на диастолическую дисфункцию. Это проявилось в первой подгруппе достоверным повышением величины VE на 11% и снижением ВИР на 13%. В контрольной группе достоверным было лишь уменьшение значения ВИР на 16%.
Таким образом, включение в СТ Элтацина в значительной степени нормализует ДФЛЖ по сравнению с контрольной группой.
Влияние Элтацина и плацебо на перекисное окисление липидов и антиоксидантную защиту представлено в таблице 2.
Легко видеть, что курс проведенного лечения Элтацином способствовал благоприятной динамике параметров антиоксидантного статуса. Это выражалось в достоверном увеличении всех исследуемых показателей АОЗ: СОД, каталазы, GSH, GSH-P, GSH-R. В группе плацебо подобных изменений в антиоксидантной системе выявлено не было.
Изложенное свидетельствует о том, что проведенная стандартная терапия в сочетании с Элтацином оказывает нормализующее влияние на баланс в системе «оксиданты/антиоксиданты», уменьшая при этом уровень ПОЛ и увеличивая АОЗ организма.
Таким образом, исследование влияния препарата Элтацин на параметры клеточного редокс-статуса позволило установить его сбалансированное действие на внутриклеточный уровень антиоксидантной системы. В то же время традиционная терапия практически не оказывала влияния на уровень перекисного окисления липидов.
Элтацин хорошо переносится, ни у одного пациента на протяжении лечения Элтацином не было выявлено ни одного нежелательного явления.
Выводы
- Новый отечественный метаболитный препарат Элтацин, разработанный ООО «МНПК “БИОТИКИ”», обладая кардиопротекторными и антиоксидантными свойствами, показан в комплексной терапии хронической сердечной недостаточности. Учитывая его положительное влияние на сократительную функцию миокарда, рекомендуется включать Элтацин в комплексную терапию как можно раньше.
- Элтацин – безопасный препарат.
- Принимают Элтацин по 1 таблетке 3 раза в день не менее 1 месяца, а далее – по усмотрению врача, в зависимости от тяжести состояния больного.
- Включение отечественного метаболитного препарата Элтацин в стандартную терапию больных хроническими заболеваниями сердца является патогенетически обоснованным и перспективным.
1. Национальные рекомендации по диагностике и лечению хронической сердечной недостаточности (третий пересмотр) // Сердечная недостаточность. 2010. Т. 11. № 1.
2. Согласованное мнение экспертов о роли этиловых эфиров ω-3 полиненасыщенных жирных кислот 90% для лечения и профилактики хронической сердечной недостаточности (заключение совещания экспертов, июнь 2011 года) // Рациональная фармакотерапия в кардиологии. 2011. Т. 7. № 4. С. 507–509.
3. Фомин И.В. Артериальная гипертония в Российской Федерации последние 10 лет. Что дальше // Сердце. 2007. Т. 6. № 3. С. 120–123.
4. Фомин И.В. Эпидемиология хронической сердечной недостаточности в Российской Федерации // Агеев Ф.Т., Арутюнов Г.П., Беленков Ю.Н. и др. Хроническая сердечная недостаточность. М.: Гэотар-Медиа, 2010. С. 7–77.
5. Бадин Ю.В., Фомин И.В. Выживаемость больных ХСН в когортной выборке Нижегородской области (данные 1998–2002 годов). Всероссийская конференция ОССН «Сердечная недостаточность, 2005 год». М., 2005. С. 31–32.
6. Даниелян М.О. Прогноз и лечение хронической сердечной недостаточности (данные 20-летнего наблюдения): Автореф. дисс. … канд. мед. наук. М., 2001.
7. Ревенко М.В., Лупанов В.Т., Ланкин В.З. и др. Изменение активности антиоксидантных ферментов и уровня липидов крови у больных коронарным атеросклерозом при лечении пробуколом // Кардиология. 1991. Т. 31. № 10. С. 41–44.
8. Benzi G., Moretti A. Age- and peroxidative stress-related modifications of the cerebral enzymatic activities linked to mitochondria and the glutathione system // Free Radic. Biol. Med. 1995. Vol. 19. № 1. P. 77–101.
9. Закирова А.Н. Использование антиоксидантов при ишемической болезни сердца: Дисс. … докт. мед. наук. М., 1995.
10. Кратнов А.Е. Атеросклероз и ишемическая болезнь сердца: роль окислительного стресса. Ярославль: изд-во ЯГТУ, 2003.
11. Неверов И.В. Место антиоксидантов в комплексной терапии пожилых больных ишемической болезнью сердца // РМЖ. 2001. Т. 9. № 18. C. 767–769.
12. Калинина Е.В., Комиссарова И.А., Заславская Р.М., Новичкова М.Д., Келимбердиева Э.С. Влияние метаболической терапии на внутриклеточный уровень антиоксидантной системы больных ишемической болезнью сердца пожилого возраста // Клиническая медицина. 2000. Т. 78. № 1. С. 40–43.
13. Лилица Г.В., Заславская Р.М., Калинина Е.В. Эффективность метаболических препаратов в комплексном лечении пожилых больных постинфарктным кардиосклерозом и недостаточностью кровообращения // Клиническая медицина. 2005. № 3. С. 54–57.
14. Лаврентьева О.В., Воронина Л.П., Татжикова К.А. Медикаментозная коррекция нарушений в системе «свободнорадикальное окисление – антиоксидантная защита» у больных бронхиальной астмой // Сибирский медицинский журнал. 2009. № 1. С. 51–53.
Новости на тему
05.02.2024
02.02.2024
СТАТЬИ по теме
Отправить статью по электронной почте
Ваш адрес электронной почты:
В статье представлены результаты клинического изучения метаболического препарата Элтацин (разработан в ООО «МНПК “БИОТИКИ”»), фиксированной комбинации трех заменимых аминокислот: глицина, L-глутаминовой кислоты и L-цистина (по 70 мг каждой).
В четырех лечебных учреждениях г. Москвы обследованы 156 больных с хронической сердечной недостаточностью (ХСН) по протоколу двойного слепого плацебоконтролируемого исследования. В дополнение к стандартной терапии (ингибиторы АПФ, бета-адреноблокаторы, нитраты, антиагреганты и/или диуретики) 104 пациента получали препарат Элтацин по 1 таблетке сублингвально три раза в день в течение трех недель, 52 пациента – плацебо.
Анализ сравнительной оценки результатов лечения показал: включение Элтацина в стандартную терапию (СТ) больных ХСН положительно влияет на динамику клинических симптомов: стойкий клинический эффект в группе Элтацина отмечен на 3,8-е сутки,
в группе плацебо – на 5,8-е сутки; снижение ФК ХСН составило 33% и 19%, повышение толерантности к физической нагрузке – 60% и 38%, улучшение показателя 6-минутного теста ходьбой – 30% и 22% соответственно (различия достоверны). Включение Элтацина в СТ приводит к значительному улучшению систолической функции левого желудочка, способствует повышению сократительной способности миокарда, в значительной степени нормализует диастолическую функцию левого желудочка, оказывает нормализующее влияние на баланс в системе «оксиданты/антиоксиданты». На основании полученных данных рекомендовано применять Элтацин в составе комплексной терапии больных хроническими заболеваниями сердца.
в группе плацебо – на 5,8-е сутки; снижение ФК ХСН составило 33% и 19%, повышение толерантности к физической нагрузке – 60% и 38%, улучшение показателя 6-минутного теста ходьбой – 30% и 22% соответственно (различия достоверны). Включение Элтацина в СТ приводит к значительному улучшению систолической функции левого желудочка, способствует повышению сократительной способности миокарда, в значительной степени нормализует диастолическую функцию левого желудочка, оказывает нормализующее влияние на баланс в системе «оксиданты/антиоксиданты». На основании полученных данных рекомендовано применять Элтацин в составе комплексной терапии больных хроническими заболеваниями сердца.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
