количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Комплекс из натуральных волокон снижает вес при избыточной массе тела и ожирении: двойное слепое, рандомизированное, плацебоконтролируемое исследование*
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Эндокринология" №1 (9)
- Аннотация
- Статья
- Ссылки
- English
В доклинических исследованиях и в исследованиях с участием людей было показано, что патентованный комплекс из натуральных волокон (литрамин IQP G-002AS), полученный из опунции индийской (Opuntia ficus-indica) и стандартизованный в отношении липофильной активности, уменьшает всасывание жира, содержащегося в пище, посредством связывания жиров в желудочно-кишечном тракте. В настоящей работе мы изучали эффективность и безопасность применения IQP G-002AS для уменьшения массы тела. В исследовании участвовали 125 взрослых пациентов с избыточным весом и ожирением. Участники исследования получили рекомендации по физической нагрузке и диетотерапии, включая планы гипокалорийной диеты (30% калорий из жиров и дефицит в 500 ккал/день). По окончании двухнедельной вводной фазы приема плацебо участники исследования были случайным образом распределены по группам лечения и получали IQP G-002AS (далее IQ) или плацебо по 3 г/день. Первичным ожидаемым результатом было изменение массы тела по сравнению с исходным значением; вторичные ожидаемые результаты включали дополнительные показатели ожирения и параметры безопасности. Фазу лечения продолжительностью 12 недель завершили 123 участника (популяция «все пациенты, начавшие получать лечение» (ITT): 30 мужчин и 93 женщины; средний индекс массы тела (ИМТ) – 29,6 ± 2,8 кг/м², средний возраст – 45,4 ± 11,3 лет). Среднее изменение массы тела относительно исходного значения составило 3,8 ± 1,8 кг в группе пациентов, принимавших IQ, в сравнении с 1,4 ± 2,6 кг в группе плацебо-контроля (p < 0,001). На фоне приема IQ большее количество пациентов достигло 5%-ного уменьшения массы тела относительно исходных показателей по сравнению с пациентами, получавшими плацебо (p = 0,027). Кроме того, в сравнении с группой плацебо в группе приема IQ наблюдалось значимо более выраженное уменьшение ИМТ, содержания жира в организме и окружности талии. Комплекс IQ хорошо переносился, его прием не сопровождался нежелательными побочными реакциями. Полученные результаты позволяют заключить, что комплекс из натуральных волокон литрамин IQP G-002AS эффективно стимулирует снижение массы тела.
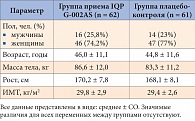
Таблица 1. Исходные характеристики всех пациентов, начавших получать лечение (n = 123)
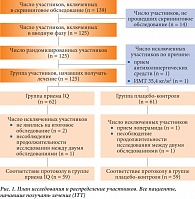
Рис. 1. План исследования и распределение участников. Все пациенты, начавшие получать лечение (ITT)

Таблица 2. Среднее (± СО) уменьшение массы тела на 12-й неделе по сравнению с исходным значением
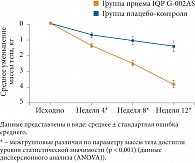
Рис. 2. Динамика массы тела в группах приема IQP G-002AS и плацебо-контроля
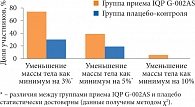
Рис. 3. Доля участников, достигших по меньшей мере 3, 5 и 10%-ного уменьшения массы тела по сравнению с исходным значением

Таблица 3. Статистический анализ вторичных параметров эффективности
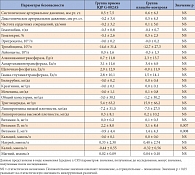
Таблица 4. Статистический анализ параметров безопасности
Введение
Ожирение – это избыточное накопление жира, связанное с хроническими заболеваниями и уменьшающее ожидаемую продолжительность жизни. Ожирение занимает пятое место в мире среди рисков смерти [1]. Заболевание развивается вследствие избыточного уровня потребления калорий, превышающего расход энергии. Ожирение и избыточный вес отмечаются у 44% больных сахарным диабетом, у 23% пациентов с ишемической болезнью сердца и у 7–41% пациентов со злокачественными новообразованиями, такими как рак толстой кишки и рак молочной железы [1]. Ожирение признано глобальной проблемой здравоохранения, приобретшей масштаб эпидемии. Это заболевание не зависит от пола, этнической принадлежности и возраста и поражает одного из десяти взрослых во всем мире [2].
В настоящее время в США насчитывается 100 млн человек (взрослых) с избыточным весом или ожирением, а по оценкам, произведенным в рамках проекта Всемирной организации здравоохранения (ВОЗ) MONICA (Multinational monitoring of trends and determinants in cardiovascular disease – Международный мониторинг в области сердечно-сосудистых заболеваний и факторов риска их развития), в странах Европы ожирением страдают по меньшей мере 15% мужчин и 22% женщин. Аналогичные данные получены во многих развивающихся странах (включая Китай, Малайзию и часть Северной Америки). В отличие от развитых стран, где ожирение ассоциируется с низким социальным статусом, в развивающихся странах оно считается показателем благосостояния и рост частоты этого заболевания положительно коррелирует с улучшением социально-экономической ситуации в целом [3].
Широкое распространение и увеличение частоты случаев ожирения, наблюдаемые в последние два десятилетия, отрицательно влияют на экономику многих стран мира [4]. Установлена прямая связь между ожирением и депрессией [5–7], причиной которой может быть низкая оценка своего внешнего вида и отрицательная эмоциональная реакция на соблюдение диеты [8]. В Соединенных Штатах Америки общие прямые и косвенные годовые затраты, связанные с ожирением, составили не менее 215 млрд долларов США (по данным на 2010 г.) [9], а в 15 странах Европейского Союза – около 32,8 млрд евро (по данным на 2002 г.) [10].
Вместе с тем уменьшение общего потребления калорий может предотвратить появление избыточного веса и развитие ожирения. Ранее проведенные исследования показали, что высокое содержание в рационе питания жиров, как и углеводов (при недостаточной физической активности), играет большую роль в развитии ожирения [11]. Таким образом, использование средств, уменьшающих усвоение в кишечнике содержащихся в пище жиров, является эффективным подходом к регулированию массы тела.
Тем не менее выбор эффективных и безопасных средств для уменьшения всасывания жиров, содержащихся в пище, весьма ограничен. Ингибиторы липазы, как правило, регистрируются органами здравоохранения как средства, способствующие снижению веса, уменьшая всасывание жиров, содержащихся в пище, путем ингибирования панкреатической липазы [12–15]. Однако при этом виде фармакотерапии отмечаются побочные эффекты со стороны желудочно-кишечного тракта (ЖКТ), такие как недержание кала, метеоризм, сопровождающийся диареей, маслянистые выделения из прямой кишки [13, 16, 17], а также поражение печени [18]. Между тем интерес к нефармакологическим средствам, включая прием пищевых волокон, продолжает расти, несмотря на то что ненадлежащее определение характеристик продуктов и недостаток данных клинических исследований ставят под вопрос эффективность пищевых продуктов для уменьшения массы тела.
Литрамин IQP G-002AS представляет собой комплекс из натуральных волокон, полученный из опунции индийской (Opuntia ficus-indica), обогащенный растворимыми волокнами акации (Acacia spp.) Установлено, что комплекс IQP G-002AS, стандартизованный по параметру липофильной активности, понижает всасывание жира, содержащегося в пище, посредством связывания жиров в ЖКТ. Липофильный комплекс IQP G-002AS связывается с жирами пищи, образуя комплексы «жир – волокно», которые не всасываются в кишечнике и поэтому выводятся из организма [19].
Ранее в экпериментальных работах на in vitro моделях ЖКТ, в исследованиях с участием животных и людей была показана эффективность IQP G-002AS в отношении связывания с жирами, при этом уменьшение всасывания жиров, содержащихся в пище, после приема IQP G-002AS составляло до 27% [19].
В настоящей работе мы изучали эффективность и безопасность IQP G-002AS в рамках рандомизированного контролируемого исследования, проведенного с целью проверки гипотезы, согласно которой прием IQP G-002AS способствует более выраженному снижению массы тела в сравнении с плацебо у людей с избыточной массой тела и умеренным ожирением.
Материалы и методы
Участники исследования
Участников исследования набирали через объявления в местной прессе. К числу подходящих участников относились мужчины и женщины с ожирением и избыточным весом (25 ≤ ИМТ ≤ 35) в возрасте от 18 до 60 лет. Женщин детородного возраста включали в исследование только после согласия использовать одобренные методы контрацепции на протяжении всего исследования. Участники с известной чувствительностью к ингредиентам исследуемых средств были исключены из исследования. Другими критериями исключения являлись наличие любого заболевания ЖКТ, расстройство питания в анамнезе, прием препаратов против ожирения, применение препаратов, оказывающих влияние на функцию ЖКТ, злоупотребление алкоголем, отказ от курения в течение предыдущих 6 месяцев, заболевания сердца в анамнезе, заболевания почек в анамнезе, участие в аналогичных исследованиях или программах снижения веса в течение 6 месяцев до начала настоящего исследования, а также беременность и грудное вскармливание.
Все участники добровольно подписали форму информированного согласия. Клиническое исследование было одобрено комитетом по этике Университетского медицинского комплекса «Шарите» в Берлине и проводилось в соответствии с европейской нормой Международной организации по стандартизации (ИСО) EN ISO 14155, Хельсинкской декларацией (Сомерсет, 1996) Всемирной медицинской ассоциации (World Medical Association – WMA) и Руководством по надлежащей клинической практике (Guideline for Good Clinical Practice, CPMP/ICH/135/95).
Дизайн исследования
Данное двойное слепое, рандомизированное, плацебоконтролируемое клиническое исследование проводилось в двух исследовательских центрах Германии с августа по декабрь 2010 г. Германия является одной из европейских стран, значительная часть населения которой имеет избыточный вес или страдает ожирением: ИМТ ≥ 25 кг/м² отмечен у 61,7% мужчин и 45,2% женщин [20].
Исследование включало вводную фазу приема плацебо продолжительностью 2 недели и фазу лечения продолжительностью 12 недель. Предполагалось, что вводная фаза поможет оценить уровень соблюдения участником исследования режима приема препарата (на основании совокупного приема таблеток плацебо) и режима питания. По завершении двухнедельной вводной фазы участники, соблюдавшие инструкции по меньшей мере на 80% и достигшие уменьшения массы тела на фоне диетотерапии, а также участники, суточный прием калорий у которых отклонялся менее чем на 20% от предписанного, были случайным образом в соотношении 1:1 распределены по группам приема IQP G-002AS (IQ) или плацебо. Рандомизация производилась независимым биостатистиком с использованием блоков (размер блока – 4 участника) в соответствии со схемой BIAS для Windows, версия 9.2 (http://www.bias-online.de).
Во время двенадцатинедельного периода лечения участники получали две таблетки IQ по 500 мг или такие же таблетки плацебо три раза в день (во время завтрака, обеда и ужина). Таблетка плацебо, внешне идентичная таблетке IQ, содержала 500 мг микрокристаллической целлюлозы вместо активных ингредиентов. Таблетки были упакованы во флаконы и промаркированы независимым фармацевтом для каждого участника в соответствии со схемой рандомизации. Все участники и занятый в исследовании персонал не были информированы относительно распределения по группам.
Участников просили соблюдать сбалансированную и умеренную гипокалорийную диету на протяжении двухнедельной вводной фазы и двенадцатинедельной фазы лечения. В соответствии с планом умеренной гипокалорийной диеты, разработанным Германским институтом сердца в Берлине, 30% калорий поступали с жирами, 55% – с углеводами и 15% – с белками. Суточная норма калорий (для каждого участника) рассчитывалась при помощи уравнения Института медицины (Institute of Medicine – IOM) Национальной академии наук США с учетом возраста, пола, массы тела и интенсивности физической нагрузки [21]. Количество калорий, содержащихся в умеренной гипокалорийной диете, равнялось оцененной суточной потребности минус 500 ккал. Участникам также рекомендовали постепенно повышать физическую нагрузку (30 минут физической нагрузки умеренной интенсивности, такой как ходьба или поездки на велосипеде). Перед началом исследования всем участникам были розданы планы диеты, которые корректировались каждые 4 недели в течение двенадцатинедельного периода лечения. Перед началом исследования, а также по истечении 4 и 8 недель исследования участники получали дневники самоконтроля, которые оценивались во время каждого визита (за исключением нулевого).
Скрининг
На скрининговом визите осуществлялся сбор анамнеза, проводилось общее физикальное обследование и измерение артериального давления, частоты сердечных сокращений, массы тела, роста, окружности талии и содержания жира в организме. Производился забор крови для биохимического анализа, общего анализа крови, определения липидного профиля и теста на беременность. Анализ образцов крови производился централизованно (Институт медицинской диагностики в Берлине, Германия).
Параметры эффективности
Первичным параметром эффективности являлось изменение массы тела (кг) через 12 недель в сравнении с исходным значением. Масса тела измерялась перед началом фазы лечения и каждые 4 недели в течение двенадцатинедельного периода с использованием калиброванных весов (Tanita BC-420 SMA; «Танита», Токио, Япония), при этом участники исследования были в нижнем белье и без обуви.
К вторичным параметрам эффективности относили долю участников, достигших не менее 5 и 10%-ного снижения исходного уровня массы тела; уменьшение среднего ИМТ; уменьшение средней окружности талии (измеряли на уровне середины расстояния между боковой нижней границей ребер и гребнем подвздошной кости); изменение содержания жира в организме (в кг и %) (содержание жира оценивали методом анализа биоэлектрического сопротивления с применением валидизированных электронных весов Tanita BC-420 SMA). Указанные параметры определяли исходно и каждые 4 недели в течение двенадцатинедельного периода лечения.
Параметры безопасности
Оценку безопасности производили на основании показателей жизненно важных функций (частота сердечных сокращений и артериальное давление в состоянии покоя) и показателей крови – биохимических (электролиты, содержание жирорастворимых витаминов, функция печени и почек и пуриновый метаболизм), гематологических и липидных (общий холестерин, триглицериды, липопротеины низкой и высокой плотности). Частоту сердечных сокращений и артериальное давление в состоянии покоя измеряли во время каждого визита с помощью стандартных средств. Параметры крови оценивали два раза – во время скринингового обследования и по завершении двенадцатинедельного исследования. В конце исследования участники оценивали переносимость исследуемого препарата. Регистрировались все нежелательные явления вне зависимости от их причинно-следственной связи с лечением.
Статистический анализ
Оценка эффективности комплекса IQ производилась с использованием нулевой гипотезы, согласно которой различия между IQ и плацебо в отношении среднего уменьшения массы тела отсутствуют.
Объем выборки рассчитывался на основании первичного ожидаемого результата – изменения массы тела в сравнении с исходным значением. Минимальный объем выборки, который составил 125 участников (с учетом поправки на 30%-ное выбывание), обеспечивает 80%-ную мощность исследования, позволяющую выявлять различия между группами по уменьшению массы тела в 1,78 кг при уровне статистической значимости 0,045. Поскольку пилотное исследование с применением комплекса IQ не проводилось, оценка объема выборки производилась на основании ограниченных данных, опубликованных в литературных источниках [22, 23]. В связи с этим была признана необходимость проведения промежуточного анализа без раскрытия рандомизационного кода. С помощью метода Виттес – Бриттан уровень значимости был скорректирован до 4,5% (двусторонний критерий), что удовлетворяло критерию номинального уровня значимости О’Брайена-Флеминга. Промежуточный анализ (проведенный после того, как половина пациентов завершили участие в двенадцатинедельном исследовании) показал, что коррекции объема выборки не требуется.
В начале исследования демографические характеристики и исходные параметры эффективности и безопасности оценивали методами описательной статистики. Все первичные и вторичные параметры эффективности, а также показатели безопасности, полученные в ходе исследования, оценивали как относительные изменения в каждой группе исследования. Для определения различий между группами использовался параметрический анализ (независимый критерий (t-критерий) Стьюдента). Дисперсионный анализ повторных измерений ANOVA проводился для оценки всех показателей эффективности в рамках модели повторных измерений. Разница между группами в категориальных переменных была проанализирована методом χ2. Дополнительно были выделены две подгруппы – с избыточным весом (ИМТ < 30 кг/м²) и с ожирением (ИМТ ≥ 30 кг/м²) – и определена эффективность комплекса IQ только у пациентов с ожирением и только у пациентов с избыточным весом.
Для целей анализа статистическая значимость (двусторонний критерий) была установлена на уровне p < 0,05. Все значения, если не указано иное, представлены в виде: среднее ± стандартное отклонение (СО). Показатели эффективности и безопасности анализировались для популяции пациентов, начавших получать лечение (intention-to-treat – ITT), которые определялись как участники, в отношении которых была произведена по меньшей мере одна оценка эффективности. Все данные обрабатывали с использованием программного обеспечения SPSS, версия 19.0 (SPSS, Чикаго, штат Иллинойс).
Результаты
В скрининговом обследовании приняли участие 139 пациентов, из них в исследование было включено 125. Все 125 пациентов в течение вводной фазы исследования надлежащим образом соблюдали режим приема препарата и рекомендации по диетотерапии и были случайным образом распределены по группам лечения. Группа пациентов, начавших получать лечение, состояла из 123 человек: 62 участника входили в группу приема IQ и 61 участник составлял группу плацебо-контроля. Один участник выбыл из исследования после приема антихолинергического препарата, еще один участник был исключен по причине несоответствия критериям – его ИМТ составил 35,4 кг/м². Демографические характеристики группы пациентов, начавших получать лечение, приводятся в табл. 1. Исходные характеристики пациентов в группах приема IQ и плацебо были одинаковыми; значимые различия между группами в отношении пола, возраста, роста, веса и ИМТ отсутствовали. В процессе анализа, проведенного в соответствии с протоколом, были исключены еще 5 участников (причины указаны на рис. 1), таким образом, в группах приема IQ и плацебо осталось по 59 человек.
Эффективность
Вес тела. За 2 недели вводной фазы среднее уменьшение массы тела по сравнению с исходным значением составило 1,6%. В конце исследования (12-я неделя) в группе приема IQ было достигнуто значимо большее уменьшение массы тела, чем в группе плацебо-контроля (4,5% (3,8 кг) и 1,8% (1,4 кг) соответственно; разница составила 2,4 кг (p < 0,001)) (табл. 2). Статистически достоверная разница в изменении массы тела в группах приема IQ и плацебо наблюдалась уже на 4-й неделе (p < 0,001)
(рис. 2).
Всего 75,8% пациентов в группе приема IQ потеряли по меньшей мере 3% от своей исходной массы тела в сравнении с 27,9% пациентов в группе плацебо. Указанное различие между двумя группами было статистически значимым (p < 0,001). Кроме того, статистически значимо различались доли пациентов, достигших как минимум 5%-ного уменьшения массы тела (35,4% на фоне приема IQ и 16,4% на фоне приема плацебо; p = 0,027) (рис. 3).
Проведенный в соответствии с протоколом анализ показал, что в среднем потеря веса составила 3,9 ± 1,8 кг в группе участников, получавших комплекс IQ, и 1,4 ± 2,6 кг в группе участников, получавших плацебо. Данное различие между исследуемыми группами (2,5 кг) не было достоверным (p < 0,001) (табл. 2).
Был произведен подгрупповой анализ данных по уменьшению массы тела у 81 участника с избыточным весом и у 42 участников с ожирением. У пациентов с избыточным весом прием комплекса IQ привел к уменьшению массы тела, более чем в три раза превышающему таковое у пациентов, принимавших плацебо (3,6 ± 1,8 кг и 0,9 ± 2,3 кг соответственно; разница составила
2,7 кг (p < 0,001)). У пациентов с ожирением среднее уменьшение массы тела в группе приема IQ примерно в 1,8 раза превышало тот же параметр в группе плацебо (4,3 ± 1,9 кг и 2,4 ± 2,9 кг соответственно; разница составила 1,9 кг (p = 0,007)).
ИМТ. В конце исследования в группе приема IQ отмечено уменьшение среднего ИМТ, значимо превышающее уменьшение среднего ИМТ в группе плацебо-контроля (1,3 кг/м² в сравнении с 0,5 кг/м² (p < 0,001)) (табл. 3).
Окружность талии. В конце исследования в группе приема IQ окружность талии уменьшилась значимо более выраженно, чем в группе плацебо (разница составила 1,7 см; p < 0,001) (табл. 3).
Содержание жира в организме. Среднее уменьшение содержания жира в организме оказалось более выраженным в группе приема IQ в сравнении с плацебо-контролем. По окончании 12 недель исследования различие в массе жира в группах получения IQ и плацебо составило 1,4 кг (p < 0,001) или 0,8% (p = 0,005) (табл. 3).
Безопасность и переносимость
Значимых изменений средних показателей частоты сердечных сокращений и артериального давления, измеренных исходно и через 12 недель, не отмечено. Кроме того, в обеих группах лечения не наблюдалось клинически значимых изменений параметров крови (табл. 4).
В конце исследования 98,4% пациентов из группы приема IQ оценивали переносимость комплекса IQP G-002AS как «хорошую» или «очень хорошую», что совпадало с соответствующими оценками плацебо.
За время исследования было зарегистрировано 26 нежелательных явлений (НЯ) у 24 участников. К числу НЯ относились инфекции верхних дыхательных путей и другие типичные симптомы простуды. Ни одно из зарегистрированных НЯ не было тяжелым и не было связано с приемом исследуемого продукта.
Обсуждение
Влияние IQP G-002AS на уменьшение массы тела (первичная цель)
Первичной целью исследования являлась демонстрация способности IQP G-002AS эффективно уменьшать массу тела в течение 12 недель у пациентов с избыточным весом и ожирением. В настоящем исследовании у пациентов, принимавших комплекс IQ, наблюдалось значимо большее снижение веса, чем у пациентов, принимавших плацебо; при этом среднее различие между группами составило 2,4 кг; у 35,4% пациентов, принимавших комплекс IQ, уменьшение массы тела составляло по меньшей мере 5% от исходного значения. Данный эффект может быть клинически значимым [24, 25], поскольку 5%-ное или более снижение исходного веса уменьшает риск развития метаболического синдрома (в соответствии с критериями третьей Национальной образовательной программы по холестерину США, для лечения взрослых (National Cholesterol Education Program’s Adult Treatment Panel III)) на 59% [26].
Сравнение комплекса IQ и других снижающих вес средств, таких как хитозан (пищевые волокна с похожим механизмом действия) и орлистат (медикаментозное средство для лечения ожирения), по причине методологических трудностей, обусловленных отсутствием соответствующих прямых сравнительных исследований, затруднено. A.B. Jull и соавт. сообщали, что применение хитозана приводит лишь к ограниченному уменьшению веса (0,9 кг) [27]. Лекарственный препарат орлистат в дозировке 60 мг на один прием пищи (три раза в день) и 120 мг на один прием пищи (три раза в день) приводил к среднему снижению веса на 1,86 и 2,55 кг соответственно после 24 недель приема [28].
ИМТ, содержание жира в организме и окружность талии
Другой результат нашего исследования состоит в том, что прием IQP G-002AS в течение 12 недель приводил к значимому уменьшению ИМТ, содержания жира в организме и окружности талии. ИМТ используется ВОЗ в качестве стандарта для диагностики ожирения, однако точность этого метода ограничена, поскольку не учитываются индивидуальные особенности физической конституции, особенно мышечная и костная масса [29]. Более того, значимое уменьшение окружности талии у пациентов, принимавших IQ, указывает на уменьшение именно центрального ожирения, что понижает риск развития сахарного диабета, ишемической болезни сердца и артериальной гипертонии. Полученный результат очень важен, поскольку окружность талии признается более точным показателем содержания абдоминального жира, чем отношение «окружность талии / окружность бедер» [25].
Ограничения исследования
Последующего наблюдения после завершения настоящего клинического исследования не проводилось. В более продолжительном исследовании можно ожидать повторного набора массы тела, как это было зарегистрировано в других ранее проведенных исследованиях [12, 13]. Таким образом, целью дальнейших клинических исследований может стать изучение устойчивого продолжительного эффекта снижения веса после приема IQP G-002AS.
Еще одним ограничением настоящего исследования является измерение содержания жира в организме методом анализа биоэлектрического сопротивления. Содержание воды в организме может повлиять на точность анализа биоэлектрического сопротивления. Двухэнергетическая рентгеновская абсорбциометрия является более точным методом, но при этом сопряжена с повышенным риском облучения участников исследования. Таким образом, метод анализа биоэлектрического сопротивления использовался как разумный компромисс между точностью и безопасностью.
Эффекты литрамина IQP G-002AS, связанные с уменьшением факторов риска развития заболеваний, связанных с ожирением, в настоящем исследовании не оценивались, поскольку протокол исследования и критерии включения в него разрабатывались исключительно для определения эффекта IQP G-002AS в отношении уменьшения массы тела. Кроме того, продолжительность исследования в 3 месяца является сравнительно короткой для точного определения возможного положительного влияния на факторы риска развития таких заболеваний на фоне приема IQP G-002AS. Тем не менее представляется целесообразным провести исследование, чтобы оценить, как продолжительное употребление IQP G-002AS в сочетании с умеренным снижением веса изменяет связанный с ожирением профиль риска развития сопутствующего заболевания.
Прекращение участия в исследовании / соблюдение инструкций по приему исследуемого препарата и безопасность пациентов
Применение средств против ожирения часто сопровождается неприятными ощущениями в области живота и связано с нарушением функции печени и психиатрическими побочными эффектами [16–18]. В большинстве клинических исследований препаратов против ожирения это повышало уровень выбывания из исследования и понижало степень соблюдения инструкций по приему препарата (примерно 75%). В нашей работе исследование завершили 95,2% пациентов, получавших комплекс IQ, что подтверждает безопасность и хорошую переносимость IQP G-002AS. Кроме того, побочных эффектов со стороны ЖКТ, таких как маслянистые выделения из прямой кишки, боль в животе, метеоризм и запор, у участников, получавших IQP G-002AS, не отмечено. Это может быть обусловлено составом IQP G-002AS (комплекс из натуральных волокон, полученных из опунции индийской (Opuntia ficus-indica), обогащенный растворимыми волокнами акации (Acacia spp.)), который связывается с жирами, поступающими вместе с пищей. Образование комплексов «натуральные волокна IQP G-002AS – жир» уменьшает выраженность симптомов, связанных с нарушением всасывания жира. Эффективность пищевых волокон в отношении уменьшения числа и понижения степени тяжести побочных реакций со стороны ЖКТ была продемонстрирована в исследовании ингибиторов панкреатической липазы. На основании этого исследования был сделан вывод о том, что слизистое вещество пищевых волокон предупреждает развитие побочных эффектов со стороны ЖКТ, вероятнее всего, путем всасывания свободного жира (масла) [30].
Эффективность применения IQP G-002AS в условиях реальной жизни
В настоящей работе благодаря очень низкой частоте выбывания участников из исследования результаты, полученные для популяции пациентов, начавших получать лечение, и популяции пациентов, завершивших исследование в соответствии с протоколом, совпадали. Высокий уровень соблюдения инструкций в соответствии с протоколом позволяет утверждать, что применявшаяся нами схема (IQP G-002AS в сочетании с гипокалорийной диетой и умеренной физической нагрузкой) может эффективно применяться в условиях реальной жизни.
Таким образом, представленные результаты подтверждают, что комплекс натуральных волокон литрамин IQP G-002AS для приема внутрь является эффективным нефармакологическим средством уменьшения массы тела. В настоящее время проводится дополнительное исследование, направленное на изучение поддержания достигнутого на фоне приема IQ снижения веса. Следует отметить, что благоприятное действие комплекса IQ достигалось без каких-либо побочных эффектов.
Авторы выражают благодарность Норману Биттерлиху и Регине Буш за помощь в проведении исследования. Настоящее исследование зарегистрировано под номером: NCT01233349. Исследование финансировалось «ИнКьюФарм Юроп Лтд.».
1. Stevens G., Mascarenhas M., Mathers C. Global health risks: progress and challenges // Bull. World Health Organ. 2009. Vol. 87. № 9. P. 646.
2. Finucane M.M., Stevens G.A., Cowan M.J. et al. National, regional, and global trends in body-mass index since 1980: systematic analysis of health examination surveys and epidemiological studies with 960 country-years and 9,1 million participants // Lancet. 2011. Vol. 377. № 9765. P. 557–567.
3. Uwaifo A.G.I., Editor C., Griffing G.T. Obesity. Medscape Reference. 2011 // www.emedicine.medscape.com/article/123702-overview.
4. Wellman N.S., Friedberg B. Causes and consequences of adult obesity: health, social and economic impacts in the United States // Asia Pac. J. Clin. Nutr. 2002. Vol. 11. Suppl. 8. P. S705–S709.
5. De Wit L., Luppino F., van Straten A. et al. Depression and obesity: a meta-analysis of community-based studies // Psychiatry Res. 2010. Vol. 178. № 2. P. 230–235.
6. Simon G.E., Ludman E.J., Linde J.A. et al. Association between obesity and depression in middle-aged women // Gen. Hosp. Psychiatry. 2008. Vol. 30. № 1. P. 32–39.
7. Simon G.E., Von Korff M., Saunders K. et al. Association between obesity and psychiatric disorders in the US adult population // Arch. Gen. Psychiatry. 2006. Vol. 63. № 7. P. 824–830.
8. Wadden T.A., Stunkard A.J. Social and psychological consequences of obesity // Ann. Intern. Med. 1985. Vol. 103. № 6. Pt 2. P. 1062–1067.
9. Hammond R.A., Levine R. The economic impact of obesity in the United States // Diabetes Metab. Syndr. Obes. 2010. Vol. 3. P. 285–295.
10. Fry J., Finley W. The prevalence and costs of obesity in the EU // Proc. Nutr. Soc. 2005. Vol. 64. № 3. P. 359–362.
11. Bray G.A., Paeratakul S., Popkin B.M. Dietary fat and obesity: a review of animal, clinical and epidemiological studies // Physiol. Behav. 2004. Vol. 83. № 4. P. 549–555.
12. Sjöström L., Rissanen A., Andersen T. et al. Randomised placebo-controlled trial of orlistat for weight loss and prevention of weight regain in obese patients. European Multicentre Orlistat Study Group // Lancet. 1998. Vol. 352. № 9123. P. 167–172.
13. Davidson M.H., Hauptman J., DiGirolamo M. et al. Weight control and risk factor reduction in obese subjects treated for 2 years with orlistat: a randomized controlled trial // JAMA. 1999. Vol. 281. № 3. P. 235–242.
14. Rössner S., Sjöström L., Noack R. et al. Weight loss, weight maintenance, and improved cardiovascular risk factors after 2 years treatment with orlistat for obesity. European Orlistat Obesity Study Group // Obes. Res. 2000. Vol. 8. № 1. P. 49–61.
15. Hauptman J., Lucas C., Boldrin M.N. et al. Orlistat in the long-term treatment of obesity in primary care settings // Arch. Fam. Med. 2000. Vol. 9. № 2. P. 160–167.
16. Collazo-Clavell M.L. Safe and effective management of the obese patient // Mayo Clin. Proc. 1999. Vol. 74. № 12. P. 1255–1259.
17. Johansson K., Neovius K., DeSantis S.M. et al. Discontinuation due to adverse events in randomized trials of orlistat, sibutramine and rimonabant: a meta-analysis // Obes. Rev. 2009. Vol. 10. № 5. P. 564–575.
18. US Food and Drug Administration. Safety orlistat (marketed as Alli and Xenical): early communication about an ongoing safety review. 2009. 180057–180057.
19. Bachmann C. Ein Fasernkomplex zur Gewichts – reduktion und kontrolle // Ars. Medici. Thema. Phytotherapie. 2010. P. 25–27.
20. International Association for the Study of Obesity. Overweight and Obesity in the EU27. International Association for the Study of Obesity: London, 2008.
21. Trumbo P., Schlicker S., Yates A.A. et al. Dietary reference intakes for energy, carbohydrate, fiber, fat, fatty acids, cholesterol, protein and amino acids // J. Am. Diet. Assoc. 2002. Vol. 102. № 11. P. 1621–1630.
22. Drent M.L., van der Veen E.A. Lipase inhibition: a novel concept in the treatment of obesity // Int. J. Obes. Relat. Metab. Disord. 1993. Vol. 17. № 4. P. 241–244.
23. Drent M.L., Larsson I., William-Olsson T. et al. Orlistat (Ro 18-0647), a lipase inhibitor, in the treatment of human obesity: a multiple dose study // Int. J. Obes. Relat. Metab. Disord. 1995. Vol. 19. № 4. P. 221–226.
24. US Food and Drug Administration. Guidance for industry: developing products for weight management. 2007.
25. National Institutes of Health (NIH), National Heart, Lung, and Blood Institute (NHLBI), North American Association for the Study of Obesity (NAASO). The practical guide: identification, evaluation and treatment of overweight and obesity in adults. 2000.
26. Phelan S., Wadden T.A., Berkowitz R.I. et al. Impact of weight loss on the metabolic syndrome // Int. J. Obes. (Lond.). 2007. Vol. 31. № 9. P. 1442–1448.
27. Jull A.B., Rodgers A., Walker N. Honey as a topical treatment for wounds // Cochrane Database Syst. Rev. 2008. № 4. CD005083.
28. Van Gaal L.F., Broom J.I., Enzi G., Toplak H. Efficacy and tolerability of orlistat in the treatment of obesity: a 6-month dose-ranging study. Orlistat Dose-Ranging Study Group // Eur. J. Clin. Pharmacol. 1998. Vol. 54. № 2. P. 125–132.
29. Romero-Corral A., Somers V.K., Sierra-Johnson J. et al. Accuracy of body mass index in diagnosing obesity in the adult general population // Int. J. Obes. (Lond.). 2008. Vol. 32. № 6. P. 959–966.
30. Cavaliere H., Floriano I., Medeiros-Neto G. Gastrointestinal side effects of orlistat may be prevented by concomitant prescription of natural fibers (psyllium mucilloid) // Int. J. Obes. Relat. Metab. Disord. 2001. Vol. 25. № 7. P. 1095–1099.
A natural fiber complex reduces body weight in the overweight and obese: a double-blind, randomized, placebo-controlled study
B. Grube
Practice for General Medicine, Berlin, Germany
P.W. Chong, K.Zh. Lau
Research and Development Department, InQpharm Europe Ltd., London, UK
H.D. Orzechowski
Practice for General Medicine, Berlin, Germany
P.W. Chong, K.Zh. Lau
Research and Development Department, InQpharm Europe Ltd., London, UK
H.D. Orzechowski
Institute of Clinical Pharmacology and Toxicology, Charité Universitaetsmedizin, Berlin, Germany
Contact person: Pee-Win Chong, pwchong@inqpharm.com
A proprietary natural fiber complex (Litramine IQP G-002AS) derived from Opuntia ficus-indica, and standardized on lipophilic activity, was previously shown in preclinical and human studies to reduce dietary fat absorption through gastrointestinal (GI) fat binding. Here, we investigated the efficacy and safety of IQP G-002AS in body weight reduction. One hundred twenty-five overweight and obese adults participated in the study. Subjects were advised on physical activity, and received nutritional counseling, including hypocaloric diet plans (30% energy from fat and 500 kcal deficit/day). After a 2-week placebo run-in phase, subjects were randomized to receive either 3 g/day of IQP G-002AS (IQ) or a placebo. The primary endpoint was change in body weight from baseline; secondary endpoints included additional obesity measures and safety parameters. One hundred twenty-three subjects completed the 12-week treatment phase (intention-to-treat (ITT) population: 30 male and 93 female; mean BMI: 29.6 ± 2.8 kg/m2 and age: 45.4 ± 11.3 years). The mean body weight change from baseline was 3.8 ± 1.8 kg in IQ vs. 1.4 ± 2.6 kg in placebo (p < 0.001). More IQ subjects lost at least 5% of their initial body weight compared to placebo (p = 0.027). Compared with placebo, IQ also showed significantly greater reduction in BMI, body fat composition, and waist circumference. IQ was well tolerated with no adverse reactions reported. These results suggest that the natural fiber complex Litramine IQP G-002AS is effective in promoting weight loss.
Новости на тему
04.07.2022 13:00:00
29.06.2022 17:00:00
12.04.2022 09:00:00
31.03.2022 12:00:00
СТАТЬИ по теме
09.04.2024
27.12.2023
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
