Кожная токсичность блокаторов EGFR (по данным клинических исследований цетуксимаба)
- Аннотация
- Статья
- Ссылки


Одно из важнейших современных направлений таргетной терапии злокачественных опухолей – блокада рецепторов эпидермального фактора роста (EGFR), которые играют ключевую роль в передаче сигнала и стимуляции пролиферации клеток опухоли. Несколько препаратов этого класса зарегистрировано для клинического применения: моноклональные антитела (МКА) к экстрацеллюлярному домену EGFR цетуксимаб (Эрбитукс) и панитумумаб (Вектибикс) и малые молекулы – ингибиторы тирозинкиназы во внутриклеточном домене рецептора эрлотиниб (Тарцева) и гефитиниб (Иресса). Самыми частыми побочными эффектами анти-EGFR-препаратов являются специфические реакции со стороны кожных покровов.
Наиболее часто встречается кожная сыпь, которая больше выражена при применении МКА по сравнению с ингибиторами тирозинкиназы. Кожные токсические реакции очень редко являются жизнеугрожающими состояниями, однако они могут представлять собой серьезную проблему для пациента и вызывать тяжелые эмоциональные расстройства. Знание таких особенностей позволяет своевременно начать симптоматическую терапию и значительно снизить степень выраженности нежелательных явлений.
Цетуксимаб в терапии злокачественных опухолей
Цетуксимаб (Эрбитукс, компания «Мерк Сероно», Германия) является наиболее широко изученным препаратом из группы блокаторов EGFR. Он эффективен при колоректальном раке, опухолях головы и шеи. Проводятся исследования эффективности цетуксимаба при немелкоклеточном раке легкого, раке пищевода, желудка, поджелудочной железы, шейки матки, трижды негативном раке молочной железы и др. Препарат представляет собой химерные МКА IgG1, которые специфично связываются с экстрацеллюлярным доменом рецептора эпидермального фактора роста (EGFR или HER1/ErbB1). Цетуксимаб обладает примерно в 10 раз большей аффинностью, чем естественные лиганды EGFR (EGF и TGF-α).
Препарат конкурентно ингибирует рецептор и предотвращает индуцированное лигандами фосфорилирование в тирозинкиназном домене рецептора, блокируя последующую активацию сигнального каскада, что приводит к подавлению пролиферации, инвазии и метастазирования с одновременной стимуляцией апоптоза и повышением чувствительности к химио- и лучевой терапии [1]. Кроме того, комплекс «антитело – рецептор» подвергается эндоцитозу и внутриклеточной деградации, в результате чего плотность EGFR на поверхности клеток снижается. Еще одним важным механизмом действия цетуксимаба является индукция противоопухолевого эффекта посредством антителозависимой клеточно-опосредованной цитотоксичности [2]. Помимо реализации иммунных механизмов, значимым аспектом применения цетуксимаба является тот факт, что сигнальный каскад EGFR тесно связан с VEGF и процессами ангиогенеза посредством фосфатидилинозитол-3-киназы (PI3-K), протеин-серин/треонин-киназы Akt и молекулярной мишени рапамицина у млекопитающих (mTOR). Таким образом, один из важнейших противоопухолевых эффектов цетуксимаба заключается в подавлении избыточной продукции VEGF опухолевыми клетками, а значит, и неоангиогенеза [3].
Лечение колоректального рака
Мутации гена KRAS в 12–13 кодонах определяются примерно в 40% случаев метастатического рака толстой кишки [4]. При наличии такой мутации KRAS-протеин (р21ras) активен независимо от EGFR [5] и блокада EGFR с помощью МКА (панитумумаб или цетуксимаб) не приводит к блокаде нижележащих сигнальных путей. Клинические исследования подтвердили значение мутации гена KRAS как предиктора резистентности к цетуксимабу и панитумумабу. Данные препараты должны использоваться только у больных без мутации KRAS в опухоли (так называемый «дикий» тип по результатам молекулярно-генетического анализа).
В первой линии терапии мКРР цетуксимаб изучен в комбинации с иринотекансодержащим режимом в исследовании CRYSTAL (Cetuximab Combined With Irinotecan in First-Line Therapy for Metastatic Colorectal Cancer). Исходно (при включении больных, n = 1198) оценка статуса KRAS не проводилась, позднее статус KRAS был оценен у 89% пациентов, мутации обнаружены в 37% случаев. Показано, что в подгруппе с «диким» типом KRAS (n = 666) добавление цетуксимаба к химиотерапии по схеме FOLFIRI приводило к достоверному улучшению всех основных оцениваемых результатов лечения [6–8]:
- увеличение общей выживаемости (ОВ) на 3,5 мес. (медиана ОВ в группе цетуксимаба составила 23,5 мес., в группе терапии только FOLFIRI – 20,0 мес., коэффициент риска смерти HR = 0,796; p = 0,0093);
- снижение риска прогрессирования болезни на 30,4% (медиана выживаемости без прогрессирования (ВБП) составила 9,9 мес. против 8,4 мес., HR = 0,696; p = 0,0012);
- увеличение объективного ответа опухоли с 39,7% до 57,3% (отношение шансов ОR = 2,069; р < 0,001).
Необходимо отметить, что цетуксимаб является единственным на сегодняшний день таргетным препаратом, который, при добавлении его к современным режимам химиотерапии первой линии, включающим инфузию 5-фторурацила, достоверно увеличивает общую выживаемость больных мКРР (в подгруппе без мутации KRAS).
Очень важной особенностью цетуксимаба является высокая непосредственная эффективность, которая оценивается по частоте полных и частичных регрессий, что очень важно в отношении больных с потенциально резектабельными метастазами в печень. Так, по данным исследования CRYSTAL, у пациентов с изолированным поражением печени и «диким» типом KRAS эффективность режима «цетуксимаб + FOLFIRI» достигает 77%. Аналогичные результаты получены в исследовании CELIM, в котором 109 пациентов с метастазами рака толстой кишки в печень получали неоадъювантную химиотерапию по схеме «цетуксимаб + FOLFOX6» или «цетуксимаб + FOLFIRI». В группе без мутации KRAS зарегистрировано 70% полных и частичных регрессий, а уровень R0 резекций у больных с исходно нерезектабельными метастазами достиг 34% [9].
В исследовании OPUS оценили эффективность режимов «FOLFOX4 +/- цетуксимаб» также в первой линии терапии мКРР. Показано, что у больных без мутации KRAS применение цетуксимаба сопровождалось достоверным снижением риска прогрессирования болезни (HR = 0,57; р = 0,0163) и увеличением общей эффективности лечения (частота регрессий составила 61% против 37%; OR = 2,54; p = 0,011) по сравнению с химиотерапией только FOLFOX4 [10]. У интенсивно-предлеченных пациентов без мутации KRAS монотерапия цетуксимабом, по сравнению с наилучшей поддерживающей терапией, достоверно увеличивала общую выживаемость (медиана ОВ составила 9,5 мес. против 4,8 мес., HR = 0,55; 95% доверительный интервал (ДИ) 0,41–0,74; р < 0,001) и выживаемость без прогрессирования болезни (медиана ВБП 3,7 мес. и 1,9 мес., HR = 0,40; 95% ДИ 0,30–0,54; p < 0,001) [11].
Интересные данные по эффективности цетуксимаба в зависимости от типа мутации KRAS были представлены на ежегодном конгрессе ASCO 2011. Впервые показано, что у пациентов с мутацией KRAS G13D анти-EGFR-терапия также может быть эффективной [12], однако этот факт нуждается в дополнительном анализе и обсуждении.
Терапия плоскоклеточного рака головы и шеи
На сегодняшний день цетуксимаб является единственным таргетным препаратом, который одобрен для лечения плоскоклеточного рака головы и шеи. Результаты многоцентрового клинического исследования III фазы, сообщенные J.A. Bonner и соавт., показали, что добавление цетуксимаба к лучевой терапии при лечении местнораспространенного рака ротоглотки, гортаноглотки и гортани значительно улучшает локорегиональный контроль заболевания, выживаемость без прогрессирования и общую выживаемость больных по сравнению с проведением только лучевой терапии [13]. Длительное наблюдение подтвердило долгосрочный эффект препарата: 5-летняя общая выживаемость составила 45,6% в группе «цетуксимаб + лучевая терапия» по сравнению с 36,4% в группе только лучевой терапии, медиана ОВ – 49,0 мес. против 29,3 мес. (HR = 0,73; 95% ДИ 0,56–0,95; p = 0,018) [14].
Эффективность цетуксимаба в комбинации с платиносодержащей химиотерапией в первой линии лечения рецидивного и метастатического рака головы и шеи изучена J.B. Vermorken и соавт. [15]. Пациенты контрольной группы (n = 220) получали цисплатин 100 мг/м2 (или карбоплатин AUC5) в 1-й день плюс 5-фторурацил по 1000 мг/м2 в 1–4-й дни каждые 3 недели, максимальное количество циклов – 6, в экспериментальной группе дополнительно применяли цетуксимаб: первая доза – 400 мг/м2, затем – по 250 мг/м2 1 раз в неделю, максимальное количество циклов – 6. Показано, что добавление цетуксимаба достоверно увеличивает медиану общей выживаемости с 7,4 до 10,1 мес. (HR = 0,8; 95% ДИ 0,64–0,99; р = 0,04) и медиану выживаемости без прогрессирования с 3,3 до 5,6 мес. (HR = 0,54; р = 0,001), а также частоту объективных ответов с 20% до 36% (р < 0,001). Кроме того, цетуксимаб оказался эффективен при платино-резистентных рецидивах плоскоклеточного рака головы и шеи [16–18].
Кожные токсические эффекты цетуксимаба
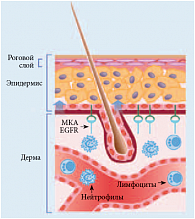
Специфическим побочным эффектом всех ингибиторов EGFR является кожная токсичность, причем при использовании МКА частота ее выше и достигает 90% по сравнению c лечением ингибиторами тирозинкиназ (около 60%) [19, 20]. Патогенез развития кожной токсичности хорошо изучен и связан с высокой экспрессией EGFR на нормальных клетках эпидермиса и фолликулярных кератиноцитах, а также на клетках эпителия сальных и эккриновых желез, антиген-презентирующих дендритных клетках и различных клетках соединительной ткани [21]. EGFR играет важную роль в нормальном развитии и физиологии клеток эпидермиса и верхних слоев волосяного фолликула, а его ингибирование приводит к подавлению роста и преждевременному созреванию базальных кератиноцитов, лейкоцитарной инфильтрации, апоптозу и гибели клеток и сопровождается уменьшением толщины эпидермиса (рис. 1) [22–25]. Необходимо отметить, что патогенез истинной угревой и связанной с анти-EGFR-терапией сыпи различен, поэтому большинство исследователей при описании последней советуют использовать термин не «угревая», а «угреподобная» [26]. В целом описывают несколько групп дерматологических реакций, связанных с ингибированием EGFR [21, 27, 28]:
- кожа: угреподобная сыпь, сухость, трещины, экзема, кожный зуд, фотосенсибилизация, гиперпигментация;
- слизистые оболочки: сухость во рту и мукозит;
- ногти: паронихии;
- волосы: трихомегалия и гипертрихоз.
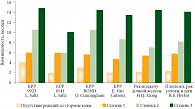
Показано, что степень выраженности побочных эффектов со стороны наружных покровов в процессе проведения терапии МКА к EGFR меняется (рис. 2).
Клинические проявления и способы борьбы с кожными токсическими эффектами терапии Акнеформный дерматит и угреподобная сыпь
Кожная сыпь является наиболее частым нежелательным явлением, которое вызвано цетуксимабом. Так, при мКРР сыпь любой степени наблюдалась у 81% пациентов, получавших цетуксимаб в сочетании с иринотеканом, и у 83% пациентов, получавших монотерапию цетуксимабом. При этом 3–4-я степень тяжести зарегистрирована у 13% и 9% пациентов соответственно [29]. При плоскоклеточном раке головы и шеи кожные реакции 3-й степени наблюдались у 9% больных, получавших цетуксимаб в комбинации с производными платины и 5-фтор-урацилом [30].
В метаанализ, в котором оценивалась частота кожных токсических эффектов в процессе терапии цетуксимабом, было включено 16 клинических исследований с участием 2037 пациентов [52]. Различные виды кожной токсичности всех степеней зарегистрированы в 88,2% случаев (95% ДИ 84,8–91,0%), высокой степени – в 11,3% (95% ДИ 8,8–14,3). Кожная сыпь всех степеней выраженности отмечалась у 81,6% больных (95% ДИ 75,4–86,6%), тяжелой степени – у 6,5% (95% ДИ 4,1–10,0%). Интересно, что при колоректальном раке выраженные проявления кожной сыпи наблюдались значительно чаще, чем при опухолях других локализаций (12,6% против 6,6%; HR = 1,9; 95% ДИ 1,0–3,6; p = 0,049).
Кожная сыпь появляется уже в начале терапии, на 2–4-й неделе [31], и состоит из множественных макул, папул или пустул без комедонов, которые чаще всего локализуются на лице, верхней половине туловища и спине, иногда распространяясь на конечности [21, 29, 49–51]. В ряде случаев сыпь регистрируется сразу же после введения первой дозы и часто служит необоснованной причиной отсрочки очередного введения препарата или полного отказа от лечения. Важно, что со временем у большинства пациентов кожные реакции ослабевают, после пропуска введения препарата или снижения его дозы значительно уменьшаются, а после отмены цетуксимаба, как правило, исчезают полностью без каких-либо последствий (рис. 2).
При 1–2-й степени кожной токсичности анти-EGFR-терапии рекомендуется продолжение терапии в стандартном режиме, в дальнейшем выраженность угреподобной сыпи, как правило, уменьшается. В случае развития нежелательных явлений 3-й степени (поражение более 50% поверхности тела) лечение прерывается и возобновляется без снижения дозы препарата при уменьшении токсичности до 1–2-й степени. При возникновении второго эпизода кожной токсичности 3-й степени лечение вновь приостанавливается, последующая доза препарата редуцируется (табл. 1).
До начала терапии важно предупредить больного о простых мерах профилактики: избегать травм, перед выходом на улицу наносить солнцезащитный крем со степенью защиты не менее 30, избегать инсоляции, по возможности исключить макияж, использовать мягкие моющие средства и увлажнители. Необходимо также отметить, что динамика проявлений сыпи зависит от лекарственного препарата и его дозы, однако отмечается существенная вариабельность между пациентами. После прекращения терапии сыпь исчезает, и это может происходить в течение месяца. При появлении сыпи в качестве местного лечения рекомендуются:
- местные антибиотики (эритромицин, клиндамицин, гентамицин гель, крем или лосьон, метронидазол гель или крем 2 раза в день);
- мазь с карбамидом (мочевиной), например Кератолан;
- местные кортикостероиды (гидрокортизон, триамцинолон и др.), как правило, в комплексе с местными антибиотиками, обычно кратковременно, с целью устранения кожного зуда (при длительном применении кортикостероиды могут усиливать сухость кожи).
Кроме того, проявления кожной токсичности можно уменьшить с помощью кремов, содержащих витамин К1 [34, 35], солевых компрессов (в течение 15 минут 2–3 раза в день), которые способствуют быстрому подавлению воспалительного процесса; симптоматическое действие оказывают кремы с ментолом.
Недавно появились публикации о возможной эффективности дерматотропного препарата пимекролимус, который используется для лечения атопического дерматита [36], однако рандомизированное исследование показало, что в отношении сыпи, вызванной цетуксимабом, препарат неэффективен [37]. Препараты, применяемые для лечения обыкновенных или розовых угрей (ретиноиды, бензоилпероксид и др.), не рекомендованы при ассоциированной с анти-EGFR-терапией сыпи [21], хотя у некоторых больных они были эффективны. Использование спиртосодержащих лосьонов нежелательно, так как они могут подсушивать кожу. Необходимо тщательно наблюдать за пациентом, чтобы не допустить ухудшения течения ксероза. Системное лечение:
- антибиотики (как правило, пероральные тетрациклины: доксициклин 100 мг 1–2 раза в сутки, миноциклин 100 мг 1 раз в сутки длительно, при развитии токсичности 3-й степени дозу антибиотика на короткое время увеличивают; реже используют цефалексин 250–500 мг 4 раза в сутки или эритромицин 250–500 мг 4 раза в сутки);
- антигистаминные препараты – для снятия кожного зуда;
- анальгетики – при 3–4-й степени токсичности, например прегабалин (Лирика);
- системные кортикостероиды назначаются, как правило, при 4-й степени (при 3-й степени – редко), поскольку они могут вызывать появление стероидных угрей.
При подтверждении суперинфекции S. aureus немедленно должна быть назначена терапия цефуроксимом или флуклоксациллином.
Прурит (кожный зуд), ксероз и экземоподобные изменения
При кожном зуде и сухости кожи ограничиваются водные процедуры (не более одного короткого теплого душа в день), исключается мыло, используются смягчающие средства, жирные кремы, рекомендовано системное использование антигистаминных препаратов, местно назначаются мази с карбамидом (мочевина). Эритема и десквамация, которые могут перейти в экземоподобные изменения, требуют назначения топических кортикостероидов, при 3-й степени рекомендовано кратковременное системное применение пероральных стероидов.
Изменения ногтей
Еще одним часто встречающимся побочным эффектом цетуксимаба являются изменения ногтей. В исследованиях эти побочные эффекты наблюдались у 44 (12%) больных с распространенным КРР, получавших препарат в комбинации с иринотеканом, и у 46 (16%) пациентов, получавших монотерапию цетуксимабом. Изменения ногтей проявлялись в виде воспаления паронихия с сопутствующим отеком латеральных ногтевых складок на пальцах ног и рук. Чаще поражались большие пальцы конечностей [29], степень тяжести большинства подобных явлений была легкой или умеренной (1-я или 2-я).
Основную роль в предотвращении развития паронихия играют простые меры профилактики: больные должны быть предупреждены о необходимости избегать травм кутикулы, исключить обрезной маникюр и искусственные ногти, носить свободную удобную обувь, избегать воздействия раздражителей и химических веществ, не парить ноги и руки в воде, пользоваться хлопчатобумажными перчатками, увлажняющими кремами и антисептическими растворами. Целесообразно применять подсушивающие пасты, содержащие антисептики (например, хлоргексидин), противогрибковые препараты (например, нистатин) и/или местные кортикостероиды; в случае пиогенной гранулемы – нитрат серебра.
При паронихии 2-й степени (отек ногтевого валика или эритема с болью; ассоциируется с расслоением и отслойкой ногтевой пластины) показано проведение местной терапии, кроме того, может быть рекомендовано назначение пероральных лекарственных препаратов (антибиотики и противогрибковые препараты). При паронихии 3-й степени показано хирургическое вмешательство и/или назначение антибиотиков внутривенно.
A. Scope и соавт. [37] оценили возможность профилактики кожной токсичности в процессе проведения терапии цетуксимабом. В рандомизированном исследовании принимали участие 48 больных: 24 пациента профилактически получали миноциклин и 24 – плацебо, местно всем больным на правую или левую половину лица был назначен ретиноид тазаротен. Профилактическая терапия миноциклином начиналась в день первого введения цетуксимаба и продолжалась в течение 8 недель. К четвертой неделе кожная токсичность 2-й и выше степени была зарегистрирована у 20% больных профилактической и у 50% больных контрольной группы (р = 0,05), к 8-й неделе различия несколько уменьшились. Из-за сыпи 3-й степени тяжести лечение было прервано у 4 больных контрольной группы, всем пациентам, получавшим миноциклин, полностью проведены запланированные введения. Клинического улучшения от аппликаций тазаротена не зарегистрировано (на сегодняшний день применение ретиноидов для борьбы с сыпью в процессе анти-EGFR-терапии не рекомендовано).
Связь кожной токсичности с эффективностью анти-EGFR-терапии
Как уже говорилось ранее, угреподобная сыпь рассматривается как специфический побочный эффект цетуксимаба, который встречается у 50–100% больных (3-я степень – у 5–9%) [20]. При этом практически во всех клинических исследованиях показана достоверная взаимосвязь между кожной сыпью, степенью ее выраженности и эффективностью препарата [20, 39]. В группе больных, у которых в течение первых 28 дней лечения возникла сыпь 2-й и выше степени, отмечено двукратное увеличение медианы общей выживаемости (HR = 0,58; 95% ДИ 0,38–0,87; p = 0,002) [40].
Таким образом, возникновение и степень выраженности кожной сыпи являются своеобразным фармакодинамическим маркером адекватности применяемой дозы и эффективности лечения ингибиторами EGFR, о чем свидетельствуют данные о корреляции кожной сыпи с эффективностью анти-EGFR-терапии. Аналогичные дозозависимые побочные эффекты отмечаются у всех ингибиторов EGFR (HER1/ErbB1), включая ErbB1-специфичные МКА цетуксимаб (Эрбитукс®) и панитумумаб (Вектибикс®), ErbB1-специфичные ингибиторы тирозинкиназы гефитиниб (Иресса®) и эрлотиниб (Тарцева®), а также ErbB1/ErbB2-ингибитор лапатиниб (Тукерб®) и ErbB1/ErbB2 + VEGFR ингибитор вандетаниб (Зактима®). Не отмечено подобного эффекта у ингибитора ErbB2 трастузумаба (Герцептин®).
В заключение следует отметить, что в целом таргетная терапия имеет значительно более благоприятный профиль безопасности по сравнению с лечением традиционными цитостатиками, однако использование новых лекарств сопряжено с появлением неизвестных ранее побочных эффектов. Специфическим и наиболее частым нежелательным явлением при применении блокаторов EGFR является кожная токсичность. Показано, что кожная сыпь 2-й и выше степени ассоциирована с увеличением выживаемости больных и может служить своеобразным предиктивным фармакодинамическим маркером эффективности, однако ухудшает качество жизни пациентов. Своевременная и адекватная симптоматическая терапия токсических реакций является ключевым фактором, улучшающим переносимость противоопухолевого лечения.
