Кожный зуд: о чем следует задуматься
- Аннотация
- Статья
- Ссылки
- English
Кожа составляет около 15% от общей массы тела человека и является самым большим органом. Наиболее важная ее функция – защитная.
Состояние кожного покрова оказывает существенное влияние на самооценку человека и формирование межличностных отношений.
Кожный зуд – неприятное субъективное ощущение, которое вызывает желание почесаться. Этот симптом в подавляющем большинстве случаев вызывает дискомфорт, психоэмоциональное напряжение и истощение. Кроме того, в результате расчесывания нарушается целостность кожного покрова.
Следует отметить, что, несмотря на высокую распространенность симптома, он недостаточно изучен в связи с трудностями его адекватной оценки и отсутствием моделей для исследования.
Соматические триггеры зуда
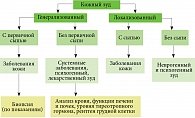
Генерализованный зуд, возникающий без сопутствующих проявлений на коже, может быть обусловлен разными причинами – от ксероза кожи до эндокринологических патологий или карциномы. Именно поэтому в клинической практике не следует пренебрегать оценкой этого важного прогностического симптома.
К относительно доброкачественным этиологическим факторам относятся лекарственные аллергические реакции, сухость кожи, чесотка и первичные дерматологические заболевания. Чаще всего кожный зуд наблюдается при сухой коже. У пациентов старшего возраста он отмечается в 10–50% случаев [1]. Генерализованный зуд встречается у 13% пациентов с хронической почечной недостаточностью и у 70–90% находящихся на гемодиализе [2]. Заболевания печени, сопровождающиеся холестазом (первичный билиарный цирроз печени, холестаз, вызванный приемом пероральных контрацептивов, внутрипеченочный холестаз при беременности и др.), также часто становятся причиной кожного зуда [2].
Среди гематологических заболеваний, вызывающих зуд, можно назвать полицитемию, железодефицитные анемии, эндокринных – тиреотоксикоз и сахарный диабет [3].
Кожный зуд – частое клиническое проявление СПИДа и связанных с ним саркомы Капоши, оппортунистических инфекций. Так, зуд с высыпаниями на коже или без таковых наблюдается у 84% больных СПИДом, у 35,5% пациентов с саркомой Капоши, развившейся на фоне СПИДа. Ассоциированные со СПИДом оппортунистические инфекции сопровождаются зудом в 100% случаев [4].
Установлено, что кожный зуд может появиться при злокачественных заболеваниях. Например, при ходжкинской лимфоме зуд отмечается у 10–25% больных, характеризуется большой интенсивностью и ограниченной локализацией, чаще в нижней части ног. В некоторых случаях указанный симптом предшествует диагностике лимфомы и может служить показателем менее благоприятного прогноза заболевания, чем лихорадка или снижение массы тела [4]. Аденокарциномы и плоскоклеточный рак различных органов (желудка, поджелудочной железы, легких, толстой кишки, головного мозга, молочной железы, простаты) сопровождаются зудом на более обширных участках кожного покрова: на ногах, верхней части туловища и разгибательных поверхностях рук. При этом наблюдается прямая зависимость между наличием зуда и активностью/рецидивом онкологического заболевания [4].
Вторичный зуд кожи, как правило, связан с приемом лекарственных препаратов, таких как производные опия (кокаин, морфин, буторфанол), фенотиазины, толбутамид, эритромицин, анаболические гормоны, эстрогены, прогестины, тестостерон, аспирин, хинидин и другие противомалярийные препараты, биопрепараты (моноклональные антитела), витамин B. Кроме того, известно, что зуд может быть субклиническим проявлением гиперчувствительности к любому лекарственному средству [5].
Поскольку зуд наблюдается не только при дерматологических патологиях, целесообразно проводить тщательное обследование пациентов (рис. 1) и лечить их с учетом выявленной патологии.
Механизмы развития и купирования зуда
Гипотезы механизмов развития зуда были сформулированы на основании исследования патофизиологии боли, поскольку боль и зуд объединяют общие молекулярные и нейрофизиологические механизмы.
Ощущение зуда и боли является результатом активации сети свободных нервных окончаний в дермально-эпидермальной зоне. Пусковой механизм – влияние внутренних или внешних термических, механических, химических раздражителей или электростимуляция. Раздражение кожного нерва может быть опосредовано несколькими биологическими агентами, включая гистамин, вазоактивные пептиды, энкефалины, субстанцию Р, простагландины.
Считается, что иные, неанатомические факторы, такие как психоэмоциональный стресс, индивидуальное субъективное восприятие, наличие и интенсивность других ощущений и/или отвлекающих факторов, оказывают существенное влияние на степень чувствительности зуда на различных участках кожи.
Нервный импульс, который вызывает появление ощущения зуда, возникшего под воздействием какого-либо из перечисленных факторов, передается по той же нейронной связи, что и болевые импульсы: от периферических нервных окончаний в дорсальные рога спинного мозга, через переднюю комиссуру, по спиноталамическому тракту к контралатеральному ламинарному ядру таламуса. Предполагают, что таламокортикальный тракт третичных нейронов выступает в качестве «реле» для передачи импульса посредством интеграции ретикулярной активирующей системы таламуса в нескольких областях головного мозга. В ответ возникает желание расчесывать кожу, которое формируется в кортикоталамическом центре и реализуется в виде спинномозгового рефлекса. После почесывания кожный зуд вновь возникает спустя 15–25 минут. Однако в ряде случаев, особенно у пациентов с хроническими дерматозами, ощущение зуда после расчесывания не прекращается, что приводит к экскориации.
Несмотря на то что в настоящее время известно много этиологических и патогенетических факторов, способствующих возникновению зуда, их изучение продолжается и открываются все новые механизмы.
Механизм, посредством которого зуд купируетcя при расчесывании, достоверно не установлен. Возможно, во время расчесывания формируются сенсорные импульсы, прерывающие нервную дугу, ответственную за возникновение ощущения.
Кроме расчесывания уменьшить зуд помогают вибрации, уколы в зудящую область, воздействие тепла, холода, ультрафиолетового излучения [3].
Лечение
Терапевтические методы должны быть направлены прежде всего на устранение патогенетических факторов.
Пациентам показаны седативные препараты (особенно при интенсивном хроническом зуде), эмоленты (для уменьшения сухости кожи, являющейся как причиной, так и следствием зуда), топические отвлекающие средства (холодные примочки, ментол-содержащие средства и проч.), антигистаминные препараты, которые в подавляющем большинстве случаев являются препаратами первой линии.
Существуют два поколения антигистаминных препаратов: седативные (Супрастин, Тавегил, Диазолин, Димедрол, Фенкарол, Фенистил) и неседативные/слабо седативные (цетиризин, левоцетиризин, лоратадин, дезлоратадин, фексофенадин, эбастин, рупатадин).
Важно отметить, что, несмотря на необходимость приема седативных препаратов, антигистаминные препараты первого поколения (обладающие помимо антигистаминного седативным эффектом) лучше не использовать. Во-первых, сон при их применении нефизиологичный (препараты угнетают фазу быстрого сна). Во-вторых, множественные побочные эффекты, характерные для этой группы лекарственных средств, ограничивают возможность их применения у пациентов с сопутствующими заболеваниями.
Поэтому в качестве седативных препаратов лучше использовать транквилизаторы, а при выборе антигистаминных препаратов предпочтение следует отдавать блокаторам второго поколения.
Особое место среди них занимает цетиризин.
Цетиризин
Цетиризин тормозит гистамин-опосредованную раннюю фазу аллергической реакции, предотвращает различные физиологические и патофизиологические эффекты гистамина, такие как расширение и повышенная проницаемость капилляров (развитие отека, крапивницы, покраснение), стимулирование чувствительных нервных окончаний (зуд, боль) и сокращение гладких мышц органов дыхания и желудочно-кишечного тракта.
На поздней стадии аллергической реакции цетиризин не только ингибирует выделение гистамина, но и миграцию эозинофилов и других клеток, ослабляя таким образом позднюю аллергическую реакцию. Снижает экспрессию молекул адгезии, таких как молекула межклеточной адгезии 1-го типа (Intercellular Adhesion Molecule 1 – ICAM-1) и молекула адгезии сосудистого эндотелия 1-го типа (Vascular Cellular Adhesion Molecule 1 – VCAM-1), которые являются маркерами аллергического воспаления.
Кроме того, в отличие от других препаратов, применяемых при кожных проявлениях аллергии, цетиризин не только блокирует H1-гистаминовые рецепторы, но и подавляет кожный ответ на тромбоцит-активирующий фактор [6, 7]. Это подтверждено результатами многочисленных клинических сравнительных исследований: благодаря способности кумулироваться в кожных покровах препарат купирует зуд и гиперемию эффективнее, чем такие средства, как эбастин, эпинастин, терфенадин, фексофенадин и лоратадин [8–10].
По сравнению с другими антигистаминными препаратами для цетиризина характерен низкий объем распределения – 0,5 л/кг. Это обеспечивает более высокие концентрации вещества во внеклеточном пространстве, где и находятся H1-гистаминовые рецепторы. Таким образом обеспечиваются их полная занятость и наивысший противогистаминный эффект [11]. Еще одной особенностью препарата является высокая способность проникать в кожу. Через 24 часа после приема однократной дозы цетиризина концентрация в коже равна или даже несколько превышает концентрацию в крови. Преимуществом цетиризина является стероид-спаринговый эффект: при одновременном назначении цетиризина и ингаляционных глюкокортикостероидов у больных бронхиальной астмой доза последних может быть снижена или не повышаться, несмотря на контакт с аллергеном.
Среди цетиризинов особое место занимает Цетрин. В исследовании Е.Е. Некрасовой и соавт. у пациентов с хронической крапивницей Цетрин показал наиболее высокую эффективность среди других дженериков цетиризина и лучшие результаты с точки зрения фармакоэкономики [12].
Опыт применения
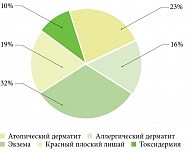
Под нашим наблюдением находилось 75 пациентов в возрасте от 18 до 76 лет (34 мужчины и 41 женщина) с диагнозами «атопический дерматит», «аллергический дерматит», «хроническая экзема в стадии обострения», «красный плоский лишай», «токсидермия» (рис. 2).
Все больные получали топическую и системную терапию, включавшую антигистаминный препарат Цетрин (цетиризин) в дозе 10 мг один раз в сутки на ночь. Длительность терапии – от 14 до 21 дня в зависимости от диагноза.
Эффективность купирования зуда пациенты оценивали по балльной системе: 0 баллов – отсутствие зуда, 1 балл – слабый зуд (присутствует, но не беспокоит), 2 балла – умеренный (беспокоит, но не мешает ежедневной активности и/или сну), 3 балла – тяжелый/интенсивный зуд (беспокоит и мешает ежедневной активности и/или сну).
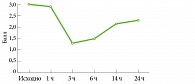
Максимальное снижение интенсивности зуда наблюдалось уже через три часа от приема препарата в первые пять суток (рис. 3).
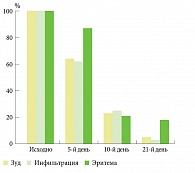
В дальнейшем уменьшение зуда или его отсутствие отмечалось к десятому дню терапии с одновременным уменьшением клинических проявлений заболеваний (рис. 4).
Полученные результаты демонстрируют высокую эффективность Цетрина (цетиризина) в терапии хронических и острых дерматозов. Цетрин (цетиризин) отличается выраженным противозудным эффектом, а также уменьшает другие клинические проявления аллергодерматозов (инфильтрацию, эритему). Кроме того, в качестве симптоматической терапии препарат может применяться и при соматических заболеваниях.
I.M. Korsunskaya, Ye.V. Dvoryankova, K.T. Pliyeva, O.O. Melnichenko, S.V. Panyukova
Center for Theoretical Problems of Physicochemical Pharmacology
Moscow Scientific and Practical Center of Dermatology and Cosmetology
Contact person: Irina Markovna Korsunskaya, marykor@bk.ru
Here we discuss aspects of pathogenesis underlying skin itching as well as potential psycho-emotional problems and somatic triggers of itching. Benefits of the second-generation antihistamines, particularly cetirizine are described: along with blockade of H1-histamine receptors, it also migration of eosinophils into the site of inflammation and suppresses cutaneous response to the platelet activating factor. The results of personal studies presented in the paper demonstrated that cetirizine was efficient in dermatological diseases: it extensively reduced intensity of skin itching as early as 3 hours after administering the drug within the first five days of the therapy
