Не спорим, а ведем диалог! Медикаментозная терапия в урологии. XVI конгресс Российского общества урологов. Сателлитный симпозиум компании «Астеллас»
- Аннотация
- Статья
- Ссылки






Перспективы применения тамсулозина у пациентов с СНМП/ДГПЖ
В последнее время набирает популярность тенденция консервативного лечения симптомов нижних мочевыводящих путей (СНМП), возникающих на фоне доброкачественной гиперплазии предстательной железы (ДГПЖ). Успешное медикаментозное лечение стало возможным с появлением селективных альфа-1-адреноблокаторов, наиболее известным из которых является тамсулозин. Профессор О.Б. ЛОРАН представил участникам симпозиума результаты российской многоцентровой наблюдательной программы НЕОС, которая проводилась под его руководством. В рамках программы оценивались эффективность и безопасность тамсулозина (препарат Омник ОКАС®) у пациентов с СНМП/ДГПЖ в рутинной клинической практике на территории РФ. По дизайну программа НЕОС представляла собой многоцентровое проспективное наблюдательное исследование. Перед исследователями стояло несколько задач.
- Проанализировать выраженность симптомов по Международной шкале оценки симптомов при заболеваниях предстательной железы (International Prostate Symptom Score – IPSS) через шесть месяцев лечения препаратом Омник ОКАС® у пациентов с СНМП/ДГПЖ.
- Оценить изменение симптомов, связанных с нарушением функции накопления и опорожнения мочевого пузыря (по шкале IPSS).
- Проанализировать изменение качества жизни пациентов с СНМП/ДГПЖ, получающих терапию препаратом Омник ОКАС®.
- Провести анализ изменения качества жизни и уменьшения симптомов в подгруппах пациентов в зависимости от возраста, исходного уровня простатспецифического антигена (ПСА) и размера предстательной железы.
В исследование были включены 7 тыс. пациентов с СНМП/ДГПЖ, получавших лечение препаратом Омник ОКАС® в условиях стандартной клинической практики в различных российских регионах. Общая характеристика участников на момент включения в исследование была такова:
- средний возраст – 63,9 ± 9,6 года;
- средний суммарный балл по шкале IPSS – 18 ± 6,4;
- средний балл IPSS по симптомам наполнения – 7,7 ± 3;
- средний балл IPSS по симптомам опорожнения – 10,1 ± 4,3;
- средний балл качества жизни (Quality of Life – QoL) – 3,9 ± 1,1;
- средний объем предстательной железы – 46,4 ± 11,7 мл;
- средний уровень ПСА – 2,32 ± 1,56 нг/мл.
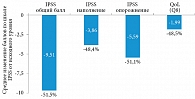
Оценка клинической эффективности и безопасности терапии препаратом Омник ОКАС® проводилась во время второго (через три месяца от начала лечения) и третьего (через шесть месяцев от начала лечения) визитов. Полученные результаты продемонстрировали высокую эффективность препарата Омник ОКАС® по таким показателям, как снижение симптомов нарушенного мочеиспускания и улучшение качества жизни пациентов с СНМП/ДГПЖ. Средний суммарный балл по шкале IPSS снизился на 51,5% (-9,51 балла), средний балл IPSS по симптомам наполнения – на 48,4% (-3,86 балла), средний балл IPSS по симптомам опорожнения – на 51,1% (-5,59 балла), при этом качество жизни улучшилось на 48,5% (рисунок).
Оценка изменений показателей качества жизни с помощью опросника EQ-5D-5L также показала позитивную динамику в улучшении основных показателей (боль/дискомфорт, тревога/депрессия, подвижность, уход за собой, повседневная активность).
Препарат Омник ОКАС® продемонстрировал хорошую переносимость и безопасность. Зарегистрирована крайне низкая частота нежелательных явлений (0,51% – у 36 из 7 тыс. участников), причем только семь случаев нежелательных явлений были классифицированы как серьезные.
Следует отметить, что анализ динамики симптомов и показателей качества жизни также проводился в подгруппах пациентов, которые формировались в соответствии с возрастом, объемом предстательной железы и уровнем ПСА. Наиболее выраженное уменьшение симптомов по шкале IPSS и улучшение показателей качества жизни отмечалось у более молодых пациентов, пациентов с объемом предстательной железы менее 30 мл, а также в подгруппе с низким уровнем ПСА (< 1,5 нг/мл). «Эти данные в очередной раз демонстрируют, что назначение альфа-блокаторов при правильно выбранных показаниях оказывается наиболее эффективным», – констатировал профессор О.Б. Лоран.
Оригинальные и дженерические препараты: есть ли отличие?
За последние годы в арсенале врача-уролога появилось немало дженерических препаратов. Соответствуют ли дженерические препараты оригинальным по биоэквивалентности, биодоступности, уроселективности и могут ли отличия по данным параметрам отразиться на качестве проводимой терапии? По словам заместителя руководителя Федерального центра мониторинга безопасности лекарственных средств Росздравнадзора, профессора кафедры общей и клинической фармакологии РУДН, д.м.н. Елены Андреевны УШКАЛОВОЙ, основное преимущество препаратов-дженериков заключается в низкой стоимости. Согласно концепции ВОЗ, появление на фармрынке более дешевых дженерических препаратов при условии их терапевтической эквивалентности оригинальным препаратам должно было привести к снижению затрат системы здравоохранения. Однако стоимость лечения может снизиться лишь в том случае, если эффективность и безопасность дженерика соответствуют таковым оригинального препарата. К сожалению, часто это не так.
Регистрация дженерических препаратов, как правило, проводится на основании данных биоэквивалентности. При этом в соответствии с российскими и международными требованиями основные фармакокинетические параметры могут отличаться от параметров оригинального лекарственного средства на ±20–25%. Это особенно опасно для препаратов с узким терапевтическим индексом (антиаритмических препаратов, сердечных гликозидов, антикоагулянтов, противоэпилептических лекарственных средств), а также для препаратов, назначаемых для лечения тяжелых угрожающих жизни состояний. В случае антимикробных препаратов это чревато риском возникновения и распространения резистентности. Кроме того, при проведении теста на биоэквивалентность дженерик оценивается на здоровых добровольцах и при однократном введении. В реальной практике фармакокинетика дженерического препарата может меняться при наличии у пациента коморбидных заболеваний и повторных приемах. Кроме того, различные модификации систем доставки у некоторых дженерических аналогов могут повысить уровень максимальной концентрации вещества.
Уроселективность является еще одним критерием, который определяет эффективность и безопасность альфа-адреноблокатора. В исследовании Д.Ю. Пушкаря и соавт. по оценке уроселективности оригинального препарата тамсулозина (Омник®) и его дженерических аналогов оценивались параметры специфического связывания лигандов альфа-адренорецепторов биоптатов простаты пациентов с ДГПЖ1. Согласно результатам исследования, максимальная связывающая способность была продемонстрирована у препарата Омник®.
Продолжая тему, доцент кафедры урологии МГМСУ им. А.И. Евдокимова, д.м.н. Павел Ильич РАСНЕР предложил при выборе дженерического препарата пользоваться выпускаемой Управлением по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration – FDA) Оранжевой книгой (Orange Book) соответствия дженерических препаратов оригинальным. С 2015 г. запущена мобильная версия книги – Orange Book Express. В книге дженерические препараты классифицируются по трем кодам:
- А – дженерический препарат рекомендуется как возможная замена оригинальному;
- АВ – дженерический препарат применяется с осторожностью в ургентных состояниях и ситуациях резистентности оригинальному;
- В – препарат может использоваться, но терапевтическая эквивалентность его не подтверждена.
Он также отметил, что в уставе Европейской ассоциации производителей дженериков и биоподобных лекарственных средств (European Generic and Biosimilar Medicines Association) указано, что использование в описании свойств дженерика любых данных доклинических и клинических исследований оригинального препарата считается нарушением этики и противоречит международной конвенции.
В настоящее время в разных странах соотношение рынка оригинальных и дженерических препаратов сильно различается. В Японии, например, 90% фармрынка занимают оригинальные препараты и только 10% – дженерические, а в России наблюдается обратная тенденция – 20 и 80% соответственно.
Профессор Д.Ю. ПУШКАРЬ отметил, что к выбору дженерика следует подходить ответственно, с учетом его соответствия оригинальному лекарственному средству по эффективности и безопасности.
Актуальность применения препаратов с контролируемым высвобождением
Лекарственные препараты с контролируемым высвобождением действующего вещества способны не только продемонстрировать высокую эффективность, но и обеспечить благоприятный профиль безопасности при лечении пациентов с СНМП при ДГПЖ2. За счет чего достигается данный эффект, профессор Е.А. Ушкалова продемонстрировала на примере препарата Омник ОКАС®.
Как известно, альфа-адреноблокаторы – самая часто применяемая группа препаратов у пациентов с СНМП/ДГПЖ. Однако все они, за исключением одной лекарственной формы, имеют общий недостаток – зависимость от приема пищи и невозможность постоянного высвобождения действующего вещества в толстом кишечнике из-за недостаточного содержания в нем воды. Безусловно, это приводит к уменьшению продолжительности действия препаратов и снижению их эффективности.
Как поддержать постоянный уровень тамсулозина в крови? Эту проблему удалось решить с помощью пероральной системы контролируемого всасывания ОКАС® (Oral Controlled Absorption System). Уникальная технология доставки лекарственного препарата позволяет создать непрерывное высвобождение активного вещества на протяжении всего желудочно-кишечного тракта. Система ОКАС® устраняет влияние пищи на всасывание тамсулозина, контролирует его высвобождение, препятствуя как повышенному всасыванию тамсулозина, так и замедленному из-за недостатка воды. Доказано, что прием препарата Омник ОКАС® один раз в день обеспечивает стабильную концентрацию тамсулозина в крови независимо от приема пищи2.
Препарат Омник ОКАС® с контролируемым высвобождением действующего вещества в течение суток имеет более благоприятный профиль безопасности, чем традиционный тамсулозин, поскольку исключает вероятность гиперконцентрации вещества в плазме крови, снижая риск нежелательных явлений, в том числе сердечно-сосудистых событий, что важно для пожилых пациентов. M.C. Michel и соавт. оценивали сердечно-сосудистый риск на фоне применения препарата Омник ОКАС® в дозе 0,4 г и традиционного тамсулозина в капсулах по 0,4 г у пожилых здоровых пациентов. Омник ОКАС® оказывал достоверно (р < 0,05) менее выраженное действие на сердечно-сосудистую систему.
П.И. Раснер вновь акцентировал внимание участников симпозиума на проблеме выбора альфа-адреноблокатора для лечения симптомов нарушенного мочеиспускания при ДГПЖ. Он привел данные независимого рандомизированного исследования по оценке безопасности терапии тамсулозином и силодозином у пациентов с ДГПЖ и их предпочтений в отношении приема этих альфа-адреноблокаторов3. Две группы пациентов с ДГПЖ получали лечение в течение восьми недель. Первая группа – тамсулозином, затем силодозином, вторая группа – силодозином, затем тамсулозином. 70% пациентов предпочли использовать тамсулозин и только 22% – силодозин. Во главу угла они поставили профиль безопасности препаратов, который был выше у тамсулозина: общая частота нежелательных явлений на фоне тамсулозина составила 3,3%, а на фоне силодозина – 28,4%3.
По словам профессора Е.А. Ушкаловой, гериатрия – это один из параметров, на который надо ориентироваться. У пожилых пациентов повышена чувствительность ко всем побочным эффектам, для них чреваты падения артериального давления ортостатического характера. Кроме того, для них особое значение имеет режим приема препарата. Если препарат предназначен для двукратного или большего количества приемов в сутки, то такой режим терапии соблюдают не более 50% пациентов, а при однократном приеме приверженность лечению демонстрируют более 80% больных. Благодаря однократному режиму приема препарат Омник ОКАС® с фиксированным высвобождением тамсулозина и постоянной ровной концентрацией в организме будет способствовать повышению комплаентности терапии.
Преимущества фиксированной комбинации солифенацина и тамсулозина ОКАС®
П.И. Раснер отметил, что среди симптомов нарушения функции нижних мочевых путей наибольшее беспокойство у пациентов вызывает фаза накопления (51,3%), или гиперактивный мочевой пузырь. В настоящее время в ряде исследований показано, что добавление М-холиноблокатора к альфа-адреноблокатору всегда положительно сказывается на самочувствии пациентов, уменьшая выраженность симптомов.
В урологии при лечении пациентов с СНМП/ДГПЖ с преобладанием симптомов наполнения все чаще используют комбинированные препараты. Профессор Е.А. Ушкалова рассмотрела основные преимущества препарата Везомни®, который представляет собой фиксированную комбинацию солифенацина (6 мг) и тамсулозина с системой ОКАС® (0,4 мг). Везомни® – первый комбинированный препарат, который содержит М-холинолитик, одобренный к применению у пациентов с симптомами нарушения функции нижних мочевых путей, обусловленных ДГПЖ.
По мнению профессора Е.А. Ушкаловой, сочетание селективного М-холиноблокатора (солифенацина) и альфа-адреноблокатора (тамсулозина) обосновано с физиологической точки зрения. Солифенацин преимущественно воздействует на симптомы со стороны мочевого пузыря, включая ургентные позывы к мочеиспусканию и учащенное мочеиспускание, а тамсулозин – на симптомы со стороны предстательной железы, включая затрудненное начало мочеиспускания, слабую струю мочи и капельное выделение мочи в конце мочеиспускания4–7.
Двухслойная таблетка Везомни® обеспечивает быстрый эффект за счет немедленного высвобождения солифенацина и одновременно равномерный длительный эффект благодаря пролонгированному высвобождению тамсулозина.
В исследовании II фазы SATURN комбинация солифенацина с тамсулозином ОКАС® характеризовалась большей эффективностью по сравнению с монотерапией тамсулозином ОКАС® и обладала хорошей переносимостью в подгруппе мужчин с СНМП, связанных с накоплением мочи и опорожнением мочевого пузыря5.
В III фазе исследования NEPTUNE определяли наличие дополнительной пользы при применении в течение 12 недель комбинированного препарата солифенацина и тамсулозина по сравнению с монотерапией тамсулозином и плацебо6. В исследовании приняли участие мужчины с умеренными и тяжелыми симптомами, связанными с накоплением мочи и опорожнением. Было продемонстрировано преимущество комбинированной терапии перед монотерапией и плацебо в отношении уменьшения ургентности и частоты мочеиспусканий, купирования симптомов наполнения и улучшения качества жизни7.
М-холинолитик или бета-3-агонист: как сделать правильный выбор
Влияют ли особенности фармакокинетики и фармакодинамики М-холинолитиков на клинические результаты? По мнению профессора Е.А. Ушкаловой, в основе эффективности и переносимости М-холинолитиков – селективность. В исследованиях показано, что солифенацин (Везикар®) более селективен в отношении рецепторов мочевого пузыря, чем толтеродин, оксибутинин и дарифенацин8. Солифенацин (Везикар®) обладает оптимальным профилем переносимости, не влияет на когнитивные функции, поэтому его можно назначать пожилым пациентам. Кроме того, он отличается удобной схемой приема (один раз в сутки). Солифенацин (Везикар®) является препаратом первого ряда терапии гиперактивного мочевого пузыря. Тем не менее терапевтический эффект при применении антимускариновых препаратов может быть недостаточным. В большинстве случаев именно отсутствие ожидаемого эффекта является основной причиной прекращения приема М-холиноблокаторов при гиперактивном мочевом пузыре9. Выходом из ситуации может стать назначение селективного агониста бета-3-адренорецепторов мирабегрона (Бетмига®) .
Как известно, бета-3-адренорецепторы регулируют наполнение мочевого пузыря, вызывая расслабление детрузора. Активация бета-3-адренорецепторов с помощью мирабегрона стимулирует расслабление детрузора и способствует удержанию мочи, приводя к увеличению накопительной емкости мочевого пузыря и интервала между мочеиспусканиями10. Мирабегрон не оказывает влияния на парасимпатическую стимуляцию сокращения детрузора и поэтому не повышает риск острой задержки мочи.
Мирабегрон назначается пожилым пациентам с высокой антихолинергической нагрузкой, а также при недостаточной эффективности М-холиноблокатора, наличии противопоказаний к М-холиноблокаторам (гиперчувствительность, глаукома), плохой переносимости и риске лекарственных взаимодействий, поскольку сам мирабегрон (Бетмига®) отличается крайне низким риском лекарственных взаимодействий.
Как отметил профессор кафедры урологии РНИМУ им. Н.И. Пирогова, д.м.н. Григорий Георгиевич КРИВОБОРОДОВ, эффективность мирабегрона в лечении гиперактивного мочевого пузыря как у пациентов, ранее не принимавших антимускариновые препараты, так и у прервавших ранее проводимую терапию, доказана результатами 12-недельных исследований III фазы11, 12. Согласно полученным данным, мирабегрон снижал частоту недержаний на 34,5%, частоту мочеиспусканий на 44%10. При этом препарат отличался хорошей переносимостью. Частота жалоб на сухость во рту была сопоставима с таковой при применении плацебо и значительно ниже, чем при применении толтеродина в дозе 4 мг. Профессор Г.Г. Кривобородов отметил, что большое значение в лечении гиперактивного мочевого пузыря имеют длительность и непрерывность терапии. Необходимо настраивать пациента на долгое, а возможно, и пожизненное лечение, так как все препараты, применяемые на сегодняшний день в терапии гиперактивного мочевого пузыря, являются симптоматическими. В этой связи важную роль играют переносимость назначаемой терапии и приверженность к ней. Из М-холиноблокаторов следует отметить солифенацин (Везикар®), который благодаря своей селективности демонстрирует хорошую переносимость и высокую комплаентность13. Мирабегрон (Бетмига®) по данным показателям превосходит всю группу М-холиноблокаторов. В рамках проведенных исследований его адренергические побочные эффекты были выражены слабо и не имели клинического значения14.
Рациональная терапия инфекций мочевых путей
Известно, что чувствительность уропатогенов к антибактериальным препаратам in vitro отличается от клинической и микробиологической эффективности in vivo. Почему резистентность in vitro является плохим предиктором клинического исхода? Как отметила профессор кафедры урологии и хирургической андрологии РМАПО, д.м.н. Любовь Александровна СИНЯКОВА, эффективность антибактериальной терапии зависит не только от чувствительности патогена к антибиотику, но и от состояния иммунорегуляторных механизмов организма, гетерогенности микробной популяции, наличия микробных ассоциаций в виде биопленок, факторов риска. Установлено, что инфекция, вызванная чувствительным штаммом, в 90% случаев отвечает на антибактериальную терапию, при резистентности штамма к антибиотику – в 60% случаев15.
Профессор Г.Г. Кривобородов напомнил о существующей нелинейной зависимости между микро- и макроорганизмом: в процессе развития инфекции меняются свойства и того и другого. В результате эффективность многих антибактериальных препаратов снижается, приходится менять режим приема, поскольку стандартный уже не работает.
Как подобрать оптимальное лечение пациенту с инфекцией мочевых путей, принимая во внимание, что неправильное применение антибиотиков приводит к развитию резистентности, росту частоты рецидивов и наносит экономический ущерб? В клинической практике следует ориентироваться на международные и отечественные рекомендации. Рекомендации Европейской ассоциации урологов основываются на данных о частоте возбудителей и их чувствительности к антибактериальным препаратам16. Для инициальной эмпирической терапии неосложненных инфекций нижних мочевых путей эксперты рекомендуют использовать:
- триметоприм-сульфаметоксазол (только в регионах, где резистентность < 20% для Escherichia coli);
- нитрофурантоин (макрокристаллический);
- фосфомицина трометамол;
- цефалоспорины (альтернативно) при известной чувствительности;
- фторхинолоны (альтернативно). Избегать назначения при неосложненном цистите всякий раз, когда возможно.
В федеральных клинических рекомендациях по лечению острого неосложненного бактериального цистита17 препаратами выбора называются:
- фосфомицина трометамол (3 г однократно);
- фуразидина калиевая соль с магния карбонатом основным (100 мг три раза в течение пяти дней);
- нитрофурантоин 100 мг три-четыре раза в сутки в течение пяти дней.
Альтернативная терапия:
- офлоксацин внутрь 200 мг два раза в сутки – три дня;
- левофлоксацин внутрь 500 мг один раз в сутки – три дня;
- ципрофлоксацин внутрь 500 мг два раза в сутки – три дня;
- цефтибутен внутрь 400 мг один раз в сутки – пять дней;
- цефиксим внутрь 400 мг один раз в сутки – пять дней.
Необходимо учесть, что широкое применение фосфомицина (рост потребления на 56,6%) привело к распространению среди БЛРС-продуцентов резистентной к фосфомицину Escherichia coli с 2,2 до 21,7%18. В этой связи следует избегать назначения фосфомицина и нитрофуранов, если невозможно исключить пиелонефрит.
Благодаря хорошей способности цефалоспоринов и фторхинолонов проникать в ткани и органы эти препараты рекомендуют также использовать для лечения более серьезных инфекций мочевых путей (например, пиелонефрита). По словам профессора Л.А. Синяковой, до недавнего времени в клинической практике с целью профилактики и лечения инфекций мочевыводящих путей весьма успешно применялись низкие дозы фторхинолонов. В настоящее время установлено, что фторхинолоны в низких дозах малоэффективны. Кроме того, летом текущего года FDA опубликовало данные о новых тяжелых побочных эффектах фторхинолонов относительно поражения периферической и центральной нервной системы и ограничило их применение при неосложненных циститах, бронхитах и синуситах. FDA постановило, что фторхинолоны следует использовать только в тех случаях, когда у пациентов не остается других альтернатив антибактериальной терапии при остром бактериальном синусите, обострении хронического бронхита, неосложненных урологических инфекциях, поскольку риск серьезных побочных эффектов может перевесить потенциальную пользу для этих пациентов.
Чем еще помимо клинических рекомендаций и уровня резистентности возбудителей урологических инфекций в регионе следует руководствоваться при выборе антимикробного препарата? «Следует отдавать предпочтение оригинальным препаратам или качественным дженерикам. Применение некачественных препаратов может послужить причиной рецидива заболевания или привести к дополнительным экономическим расходам, связанным со стоимостью альтернативных препаратов», – уточнила профессор Л.А. Синякова. Например, в настоящее время в аптеках продаются два препарата цефиксима – Супракс® Солютаб® и Панцеф®. Для того чтобы ответить на вопрос, эквивалентны ли они, профессор Е.А. Ушкалова привела данные исследования сравнительной кинетики растворения этих препаратов19. При исследовании кинетики растворения препарата Панцеф® количество растворенного цефиксима через час было на 20–30% меньше, чем у препарата Супракс® Солютаб®. Несоответствие кинетики растворения может быть прогностическим признаком недостаточной биодоступности дженерика и, как следствие, недостаточной клинической эффективности препарата.
По мнению профессора Л.А. Синяковой, антибактериальные препараты следует использовать рационально. Уменьшить потребность в антибиотиках позволяют альтернативные методы лечения, например использование иммуностимулятора Уро-Ваксом® для профилактики рецидивирующих ИМП. Это подтверждают результаты многоцентровой наблюдательной программы FLORA, в ходе которой оценивалась эффективность терапии рецидивирующих ИМП препаратами Супракс® Солютаб® и Уро-Ваксом®20. Длительное наблюдение за пациентками с рецидивирующим циститом, получавшими лечение препаратами Супракс® Солютаб® и Уро-Ваксом®, показало высокую эффективность такого терапевтического подхода, приведшего к статистически значимому (р < 0,001) снижению числа и продолжительности рецидивов (на 93 и 94% соответственно), а также к уменьшению средней продолжительности антибиотикотерапии (на 90%).
Подводя итог, профессор Г.Г. Кривобородов подчеркнул необходимость персонифицированного подхода к лечению пациентов с инфекциями мочевыводящих путей: «Недаром выдающийся древнегреческий врач Гиппократ в свое время сказал, что нужно лечить больного, а не болезнь».
Заключение
В ходе проведенной дискуссии специалисты пришли к выводу о необходимости рационального подхода к лечению СНМП при ДГПЖ и гиперактивного мочевого пузыря, а также инфекций мочевых путей с использованием современных оригинальных препаратов или качественных дженериков. Приведенные данные показывают, что линейка препаратов компании «Астеллас», включающая Омник®, Омник ОКАС®, Везомни®, Везикар®, Бетмига®, Супракс® Солютаб® и Уро-Ваксом®, в полной мере соответствует всем требованиям, предоставляя практикующим врачам широкий выбор лекарственных средств с доказанной эффективностью и безопасностью.
