Современные подходы к терапии НИМП
Неосложненные инфекции нижних мочевых путей. Новые данные по резистентности возбудителей. Новые подходы к терапии
- Аннотация
- Статья
- Ссылки






Симпозиум открыл доклад д.м.н., профессора, зав. отделом воспалительных заболеваний с группами клинической фармакологии и эфферентных методов лечения ФГБУ «НИИ урологии» Минздравсоцразвития России Т.С. ПЕРЕПАНОВОЙ. Неосложненные инфекции мочевых путей (НИМП) характеризуются отсутствием обструктивных уропатий и структурных изменений в почках и мочевыводящих путях. К неосложненным инфекциям мочевых путей относятся острый цистит и острый восходящий пиелонефрит, которые могут наблюдаться у относительно здоровых женщин. НИМП широко распространены в мире.
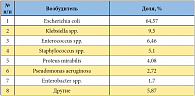
В России ежегодно регистрируется около 26–36 млн случаев острого цистита среди женщин. Высок уровень рецидивов, которые наблюдаются у 30–40% женщин, перенесших НИМП. При этом у 20–30% женщин рецидив случается в течение 4 месяцев после острого эпизода. Нередко развивается хроническая инфекция, устойчивая к лечению антибиотиками. Последствия рецидивирующей и хронической инфекции бывают тяжелыми. «Женщинам даже приходится бросать работу, отказываться от половых контактов, соответственно, рушатся семьи и прочее», – подчеркнула социальную значимость болезни доктор Т.С. Перепанова. Острый неосложненный бактериальный цистит в 80% случаев вызывается E. coli и в 15% – другими возбудителями: St. saprophyticus, Klebsiella spp., Proteus spp. 98% штаммов, обнаруженных в моче больных острым циститом, присутствуют в кале.
Существует ряд факторов, предрасполагающих к развитию инфекции нижних мочевых путей у женщин. К их числу относятся анатомо-физиологические особенности женского организма (короткая и широкая уретра, близость уретры к естественным резервуарам инфекции – анусу, влагалищу, «вагинализация» уретры); органические или функциональные нарушения уродинамики нижних мочевых путей (НМП) и различные гинекологические заболевания (вагиниты, вагинозы, вульвиты, гормональные нарушения). Существует и генетическая предрасположенность к инфекциям мочевых путей: наличие специфических E.-coli-связывающих рецепторов, именуемых Toll-like receptors (TLRs). Наконец, развитию болезни может способствовать неадекватная реакция слизистой оболочки мочевого пузыря.
Факторами риска развития ИМП являются сексуальная активность, использование спермицидов, появление ИМП в раннем возрасте, наличие ИМП у матери, рецидивы ИМП, а в постменопаузе – атрофия слизистой, сахарный диабет и недержание мочи. К факторам, способствующим развитию ИМП, следует также отнести снижение скорости потока и кислотности мочи, концентрации в ней мочевины. Имеет значение снижение антиадгезивных свойств и увеличение проницаемости уротелия вследствие несостоятельности гликозаминогликанового слоя слизистой мочевого пузыря.
Характерные симптомы цистита – резкое начало, дизурия, частые императивные позывы к мочеиспусканию, боли внизу живота, напряжение мышц над лоном. Клиническая картина уретрита и вагинита несколько иная. Так, уретрит характеризуется постепенным началом, неяркой симптоматикой, наличием выделений из влагалища, болей внизу живота, развитием цервицита, вульвовагинита. При вагините наблюдаются выделения из влагалища, неприятный запах, зуд, дизурия, нечастое мочеиспускание (нет императивных позывов), вульвовагинит.
Диагноз неосложненной инфекции НМП ставят при наличии таких ирритативных симптомов, как дизурия, частые и неотложные позывы к мочеиспусканию и ургентность, при отсутствии отделяемого из влагалища и раздражения влагалища, а также при отсутствии факторов риска развития осложненной ИМП. Большое диагностическое значение имеет анализ мочи. Однако процент ошибок при этом анализе довольно велик. «Почему-то в России до сих пор не применяются тест-полоски, которые широко используются во всем мире,» – заметила профессор Т.С. Перепанова. Применение тест-полосок – очень информативный метод, и, кроме того, он существенно удешевляет диагностику.
Важнейшим свойством микроорганизмов – возбудителей НИМП является способность к адгезии – прикреплению при помощи ворсинок к клеткам эпителия, что позволяет бактериям противостоять току мочи и обеспечивает их способность к колонизации. Кроме того, патогенные микроорганизмы обладают свойствами репликации, репродукции в зонтичных клетках эпителия мочевых путей, инвазии в глубокие слои уротелия и образования биопленок.
Более точные сведения о структуре возбудителей внебольничной ИМП содержат результаты исследования ДАРМИС (2011), проведенного в лечебных учреждениях 20 городов России, Беларуси и Казахстана, в ходе которого были изучены 987 штаммов возбудителей ИМП (табл. 1). Подходы к лечению острого и рецидивирующего цистита несколько различаются. Лечение острого цистита направлено на полную эрадикацию возбудителей, что позволит предотвратить развитие рецидивов в дальнейшем. Цель лечения рецидивирующего цистита – улучшение качества жизни (увеличение безрецидивного периода).
При выборе антибиотиков для лечения неосложненной ИНМП необходимо учитывать целый ряд факторов. К ним относятся спектр и чувствительность уропатогенов, эффективность антибиотиков в клинических исследованиях, переносимость препаратов, побочные эффекты, стоимость и доступность препарата. Антибиотики должны создавать высокую концентрацию в моче и в то же время оказывать минимальное побочное действие на микрофлору кишечника и влагалища. Следует избегать назначения антибиотиков, характеризующихся плохим всасыванием из кишечника.
Хорошо известно, что побочным следствием широкого применения антимикробных препаратов стала селекция резистентных возбудителей. Это относится и к части уропатогенных штаммов E. coli, которые синтезируют бета-лактамазы расширенного спектра, что делает их устойчивыми к цефалоспоринам всех 4 поколений, бисептолу, тетрациклинам и некоторым другим препаратам. «Возникает вопрос – чем лечить? При наличии возбудителя, синтезирующего бета-лактамазы расширенного спектра, сразу несколько групп препаратов будут неэффективны», – с сожалением констатировала Т.С. Перепанова.
Одна из главных проблем в лечении НИМП заключается в использовании антибиотиков системного действия. Это способствует росту резистентности штаммов ведущих возбудителей и значительно ограничивает эффективность любого вида антибактериальной терапии. Чувствительность штаммов E. coli к антибиотикам изучалась в ходе исследования ARESC (2006), проводившегося в 10 странах. Установлено, что чувствительность E. coli к фосфомицину составляла более 98% во всех исследуемых регионах. Чувствительность к нитрофурантоину превышала 95% в 6 из 10 стран. Чувствительность к мециллинаму (этот препарат не зарегистрирован в России) превосходила 95% в 5 из 10 стран. Чувствительность к ципрофлоксацину составила более 95% в 3 из 10 стран.
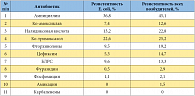
В России, по данным за 2004–2005 гг., резистентность E. coli, выделенной у пациенток с неосложненной амбулаторной ИМП, к нитрофурантоину была равна нулю и в Москве, и в Петербурге, и в Новосибирске. Резистентность к фторхинолонам в Петербурге и Новосибирске также оказалась нулевой, но в Москве составляла 6,3%. Довольно высокой оказалась резистентность к ко-тримоксазолу (25% в Новосибирске, 18,8% в Москве и 16,7% в Петербурге) и особенно к ампициллину (43,7% в Москве, 25% в Новосибирске и 22% в Петербурге). Более поздние данные, полученные в 2010–2011 гг. в России, Беларуси и Казахстане, продемонстрировали рост резистентности E. coli к антибиотикам (табл. 2).
Рекомендации по лечению острого неосложненного цистита Европейской ассоциации урологии от 2006 и 2011 гг. сильно отличаются, что обусловлено быстрым ростом резистентности бактерий-возбудителей к антибиотикам. Так, в рекомендации 2006 г. были включены такие антибиотики, как ТМП/СМХ (курс – 3 дня), фторхинолоны (1–3 дня), фосфомицин (1 день), пивмециллинам (3–7 дней) и нитрофурантоин (5–7 дней). Список препаратов, включенный в последние рекомендации, изменился (табл. 3). В качестве альтернативных препаратов в рекомендациях указаны ципрофлоксацин, левофлоксацин, норфлоксацин, офлоксацин и цефлодоксима проксетил. Таким образом, препаратами первого выбора при лечении НИМП являются фосфомицина трометамол (Монурал, 3 г) и нитрофураны. Это отнюдь не новые препараты. Нитрофураны применяются уже около полувека, а Монурал – в течение 30 лет. Чувствительность к ним E. coli сохраняется на протяжении многих десятилетий, а воздействие этих антибиотиков на нормальную фекальную флору минимально.
Фосфомицина трометамол – производное фосфоновой кислоты, ингибитор синтеза пептидогликана клеточной стенки бактерий. Оказывает исключительно сильное бактерицидное действие благодаря очень высокой концентрации в моче. Именно по этой причине достаточно принять одну дозу Монурала. 99,5% препарата выделяется с мочой в неизменном виде. Диагноз «асимптоматическая бактериурия/кандидурия» ставится в тех случаях, когда в 2 культуральных исследованиях с промежутком в 24 часа и более количество бактерий в средней порции мочи составляет более 100 000 КОЕ/мл (при отсутствии катетера, по крайней мере, в течение 7 дней перед исследованиями). Но в России, как уже отмечала докладчица, бессимптомная бактериурия расценивается как хронический пиелонефрит, что является ошибкой. Лечение асимптоматической бактериурии показано при беременности, перед проведением урологических инвазивных манипуляций, а также пациентам с трансплантированной почкой. Следует учесть, что все это – относительные показания. При сахарном диабете, наличии различных катетеров или протезов лечение бактериурии не проводится.
Эпидемиологические данные свидетельствуют, что бессимптомная бактериурия наблюдается примерно у 6% беременных, гораздо чаще, чем острый цистит (1–2%) или острый пиелонефрит (1–2,5%). При этом многие лекарственные препараты не показаны беременным. К их числу относятся сульфаниламиды, триметоприм, аминогликозиды, хинолоны и фторхинолоны, нитроксолин. В III триместре беременности исключаются нитрофураны. Для лечения инфекции нижних отделов мочевыводящих путей у беременных рекомендованы только пенициллины, цефалоспорины и фосфомицина трометамол. Рекомендуемые схемы антибактериальной терапии инфекций нижних отделов мочевыводящих путей у беременных:
- амоксициллин/клавуланат 375–625 мг 2–3 раза в сутки;
- цефуроксим аксетил 250–500 мг 2–3 раза в сутки или цефтибутен 400 мг 1 раз в сутки;
- фосфомицина трометамол 3 г однократно.
Ведение беременных с инфекцией нижних отделов НМП, будь то бессимптомная бактериурия или острый цистит, начинается с 7-дневного курса терапии или одной дозы фосфомицина. Через 7–14 дней проводят культуральное исследование мочи. Если возбудители не выявлены, лечение считается успешно завершенным. При обнаружении возбудителей назначается повторный курс терапии с бактериологическим контролем, который проводится ежемесячно до наступления родов даже при отсутствии возбудителей в моче. При наличии патогенных микроорганизмов после повторного курса терапии назначают супрессивную терапию за 2 недели до родов и в течение 2 недель после с ежемесячным бактериологическим контролем.
Профессор Т.С. Перепанова высказалась против чрезмерного применения антибиотиков при хронической инфекции нижних отделов мочевыводящих путей (МВП) у беременных. По ее мнению, лучше назначать курс лечения антибиотиками только в период обострения, в противном случае это способствует естественному отбору возбудителей на резистентность. По имеющимся данным, в России при лечении антибиотиками инфекций нижних отделов МВП у беременных назначают преимущественно фосфомицин (41,8%), поскольку данный препарат безопасен. Прием 1 дозы Монурала1 раз в 10 дней в течение 3 месяцев является наилучшим вариантом терапии. В то же время довольно часто беременным назначают препараты, которые им абсолютно не показаны (нитроксолин, нитрофураны, фторхинолоны), и этот факт не может не беспокоить, отметила в заключение профессор Т.С. Перепанова.
Профессор кафедры урологии и хирургической андрологии РМАПО, д.м.н. Л.А. СИНЯКОВА начала свое выступление с рассказа о пациентке, которой диагноз «цистит» был поставлен ошибочно. Боли в нижней части живота и недержание мочи у нее были обусловлены тазовым венозным полнокровием и опущением передней стенки влагалища. На основании этого частного случая докладчица сделала вывод о необходимости более тесного сотрудничества врачей разных специальностей, в особенности урологов и гинекологов. «Если использовать комплексный подход к анализу жалоб пациентов, а также общий план обследования этих больных, диагностических ошибок будет гораздо меньше», – заявила Л.А. Синякова. Докладчица привела эпидемиологические данные. Около 20–25% женщин переносят цистит в той или иной форме, а 10% страдают хроническим рецидивирующим циститом. Частота рецидивов после первого эпизода цистита составляет 50%. Рецидивы обычно наблюдаются чаще трех раз в год.
В США ежегодно около 8 млн женщин обращаются к врачам с симптомами инфекции МВП. У девочек цистит диагностируется в 3 раза чаще, чем у мальчиков, и выявляется, главным образом, в возрасте от 4 до 12 лет. Аномалии расположения наружного отверстия уретры служат фактором риска развития рецидивирующей и хронической инфекции МВП. Влагалищная дистопия выявлена у 43% больных, страдающих хроническим пиелонефритом с детского возраста, и у 26% больных с рецидивирующими ИНМП. У 87,5% женщин, у которых есть «вагинализация уретры» вследствие влагалищной дистопии, отмечаются инфекции, передаваемые половым путем. К факторам риска развития урогенитальных заболеваний относятся раннее начало половой жизни, количество половых партнеров свыше трех, аборты.
Одной из причин развития цистита и дизурии может быть генитальный герпес. При этом заболевании дизурия развивается в 58% случаев, цистит – в 47%, поражение шейки матки – в 88%. У беременных женщин при первой атаке генитального герпеса риск заражения плода достигает 50%, при рецидиве он снижается до 5%. «Таким образом, часть детей инфицированы этим вирусом с рождения», – отметила доктор Л.А. Синякова. Опросы больных позволили уточнить особенности течения циститов на фоне урогенитальных инфекций. 32% больных жаловались на поллакиурию (до 11–14 раз в сутки) вне периода обострений. 96% женщин отмечали боли во время полового акта (диспареуния), в связи с чем 92% избегали сексуальных отношений. У 86% опрошенных женщин наблюдались умеренные и выраженные боли в области мочевого пузыря, малого таза, влагалища, промежности, уретры, которые становились причиной сексуальной и социальной дезадаптации. Наличие императивных позывов к мочеиспусканию отмечали 88% женщин, однако как «выраженные» их оценили только 28% больных.
Опросы также показали неэффективность традиционной антибактериальной терапии. Одна из причин связана с неправильной диагностикой. Профессор Л.А. Синякова подчеркнула, что боль в мочевом пузыре при мочеиспускании и боль в мочевом пузыре при его наполнении являются симптомами двух разных заболеваний. Если одним больным можно проводить обычную цистоскопию в амбулаторных условиях, то в других случаях (при подозрении на интерстициальный цистит) необходимо тщательно обследовать мочевой пузырь под наркозом. Докладчица также решительно высказалась в пользу биопсии при серьезных заболеваниях мочевого пузыря. Резистентность патогенных микроорганизмов к антибиотикам – одна из самых серьезных проблем здравоохранения, которая становится причиной гибели до 25 000 пациентов ежегодно только в Европе и связана с дополнительными расходами в размере 15 млрд евро.
Одна из причин резистентности – быстрый отбор штаммов, устойчивых к широко используемым препаратам. Американское сообщество по инфекционным болезням и Евросоюз планируют к 2020 г. создать 10 новых антибактериальных препаратов, которые будут обладать активностью к таким основным возбудителям, как кишечная палочка, продуцирующая бета-лактамазы расширенного спектра действия, стафилококк, клебсиелла и ряд других. Другая причина резистентности связана с тем, что многие патогены обладают способностью к образованию биопленок. При наличии биопленок концентрация антибиотика, необходимая для эффективного лечения, повышается в сотни раз. При этом внутрь биопленок проникает очень малое количество молекул препаратов.
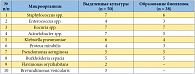
Л.А. Синякова привела результаты собственных исследований. Произведен посев биоптатов мочевого пузыря у 42 обследованных пациенток. У 20 из них отсутствовала бактериурия. В результате посева в 40 случаях получен рост микрофлоры в количестве 1000–100000 КОЕ/мл. Оценивали способность выделенных культур к образованию биопленки на абиогенных носителях в режиме бактериального анализатора BioTrack 4250. Результаты приведены в таблице 4. Л.А. Синякова обратила внимание слушателей на тот факт, что ни в одном случае в биоптатах мочевого пузыря у пациенток, страдающих рецидивирующим циститом, не высевалась кишечная палочка.
Алгоритм обследования пациенток со стойкой дизурией разработан кафедрой урологии и хирургической андрологии РМАПО в 2005 г., но серьезно переработан в 2011 г. в соответствии с результатами новых исследований. Он включает, прежде всего, тщательно собранный анамнез. Необходимо проверить наличие таких факторов риска, как раннее начало половой жизни, частая смена половых партнеров, наличие инвазивных манипуляций, сопутствующие хронические гинекологические заболевания, вирусные инфекции (герпес, цитомегаловирус), дисбиоз влагалища. Пациентки должны заполнять дневники мочеиспускания. Нужен влагалищный осмотр. Большое значение имеет общий анализ мочи. Производится посев мочи на флору и чувствительность к антибиотикам. Необходимо обследование на наличие инфекций, передаваемых половым путем (ИППП). Принципиально важно исследовать мазки из уретры, влагалища и цервикального канала, подчеркнула Л.А. Синякова.
Алгоритм диагностики включает ультразвуковое исследование (УЗИ) почек, мочевого пузыря с определением остаточной мочи, матки и придатков. Проводят и допплерографию сосудов малого таза. Необходима также цистоскопия с биопсией. Нормальная микрофлора влагалища – это микроэкологическая система, обеспечивающая защиту репродуктивных органов женщины. Ведущую роль в ней играют лактобактерии (95%) – L. acidofilus, L. plantarum, L. casei, L. fermentus, L. salivarius и др. Кроме них, в состав этой микрофлоры входят и другие микроорганизмы (5%) – бифидобактерии, пептококки, бактероиды, эпидермальные стафилококки, коринебактерии, гарднереллы, мобилункус, микоплазмы. Посев отделяемого из влагалища позволяет выявить, в норме ли микрофлора. «Если лактобактерий недостаточно, преобладает патогенная микрофлора, ее необходимо устранить, а потом восстанавливать нормальную флору влагалища», – объяснила профессор Л.А. Синякова.
Лечение НИМП включает целый ряд различных подходов. Этиологическое лечение – это антибактериальная терапия. Патогенетическое лечение включает коррекцию анатомических нарушений, лечение ИППП и коррекцию гормональных нарушений (применение эстрогенов в перименопаузе). Кроме того, определенное значение имеют посткоитальная профилактика, лечение воспалительных и дисбиотических гинекологических заболеваний, коррекция гигиенических и сексуальных факторов, коррекция иммунных нарушений и местное лечение. Однако первостепенное значение, по убеждению докладчицы, имеет антибактериальная терапия. Поскольку рецидивирующий цистит – инфекционное заболевание, только антимикробные препараты способны победить инфекцию и устранить причину заболевания.
Терапия НИМП антибиотиками преследует следующие основные цели: быстрое купирование симптомов, восстановление трудоспособности и социальной активности, предупреждение осложнений и профилактика рецидивов. При рецидивирующем цистите необходим длительный курс антибактериальной терапии лечения. Препарат выбирают с учетом выделенного возбудителя и антибиотикограммы. Антибиотики должны обладать сильным бактерицидным действием. Препаратами выбора являются фосфомицина трометамол (по 3 г 1 раз в 10 дней в течение 3 месяцев), Фурамаг, защищенные пенициллины, цефалоспорины (у детей и беременных), препараты бактериофагов, фторхинолоны.
Ключевое звено патогенеза ИМП – адгезия возбудителя (чаще всего E. coli) к клеткам уроэпителия благодаря взаимодействию между ворсинками бактерии и рецепторами эпителия. Монурал (фосфомицина трометамол) в субингибирующих концентрациях активно подавляет адгезивные свойства грамположительных и грамотрицательных бактерий на эпителиальных клетках мочевых путей. Для профилактики ИМП Европейская ассоциация урологов рекомендует (2010) длительное применение низких профилактических доз антибиотиков, вакцинопрофилактику или использование экстракта клюквы (Vaccinium macrocarpon) ежесуточно в количестве, содержащем как минимум 36–72 мг проантоцианидина A. Из этих рекомендаций профессор Л.А. Синякова решительно отвергла применение низких доз антибиотиков, поскольку это способствует отбору резистентных штаммов возбудителей.
Для повседневной практики рекомендуется ежедневное употребление клюквы. Однако содержание проантоцианидинов в свежей клюкве или клюквенном морсе неизвестно. Именно поэтому используют препарат Монурель, который состоит из экстракта клюквы и витамина С, содержит 36 мг проантоцианидина А и обладает профилактическим действием. Он препятствует адгезии кишечной палочки к клеткам уротелия. Монурель рекомендован в следующих случаях: для усиления эффекта антибиотикотерапии – по 1 таблетке в день течение недели; для профилактики развития рецидивирующих ИМП при неблагоприятных условиях – по 1 таблетке в день в течение неблагоприятного периода; как средство профилактики при часто рецидивирующих циститах (более 3 эпизодов в год) – по 1 таблетке в день 2 недели в течение 3 месяцев. Длительный прием препарата обеспечивает устойчивый противорецидивный эффект.
В заключение своего выступления профессор Л.А. Синякова напомнила о наиболее важных аспектах лечения НИМП. Во-первых, все пациентки со стойкой дизурией должны проходить комплексное обследование, включающее цистоскопию с биопсией и морфологическим исследованием биоптата. Морфологическое исследование позволяет определить степень диспластических процессов в уротелии, выраженность изменений в субэпителиальной основе, планировать вид и длительность терапии. Во-вторых, назначение эмпирической системной и внутрипузырной терапии женщинам со стойкой дизурией является недопустимым.
В начале своего доклада профессор кафедры урологии МГМСУ, д.м.н. А.В. ЗАЙЦЕВ высказал сомнение в инфекционной природе дизурии. Он сообщил, что было обследовано большое количество женщин с дизурией, у которых клинически подозревали наличие инфекции мочевых путей, цистита. Исследование проводилось во Франции, Венгрии, Италии и России. Выяснилось, что у каждой третьей пациентки с дизурией посев мочи оказался стерильным. Причины расстройств мочеиспускания у женщин разнообразны: ИМП, вагиниты, ИППП, дефицит эстрогенов, интерстициальный цистит, гиперактивный мочевой пузырь, химическое раздражение, системные заболевания, рак мочевого пузыря.
Интерстициальный цистит (ИЦ) относится к важнейшим причинам дизурии. Помимо дизурии симптомом интерстициального цистита являются мучительные тазовые боли, на сегодняшний день ИЦ – одна из четырех наиболее часто встречающихся причин тазовых болей у женщин. 9 млн женщин в США страдают от хронической тазовой боли, значительную долю среди них составляют больные ИЦ. В течение многих лет обсуждается роль лейкоплакии, эта тема обсуждалась еще на первом заседании Московского общества урологов в 1923 г. Однако до сих пор до конца не выяснены как причины возникновения этого явления, так и степень его связи с воспалением.
В Швейцарии проведено клиническое исследование с участием 103 пациенток в возрасте от 21 до 84 лет (средний возраст – 46 лет). Симптомы нижних мочевых путей (СНМП) у них наблюдались в среднем на протяжении 5 лет. При цистоскопии обнаружено наличие лейкоплакии в треугольнике Льето. Положительная урокультура отмечена в 15%, а лейкоцит-урия – в 30% случаев. Курс лечения включал прием доксициклина по 100 мг 2 раза в сутки в течение 2 недель, а затем по 100 мг 1 раз в день в течение еще 2 недель. Одновременно проводилась профилактика кандидоза влагалища таблетками гексетидина или циклопироксоламина в течение 10 дней. Аналогичному лечению подвергались и сексуальные партнеры пациенток, использование презерватива во время полового акта было обязательным на протяжении 4 недель.
Через 3 месяца из 103 пациенток 31 (30%) считали себя вылеченными. 42 женщины (41%) отмечали улучшение. В то же время 29 пациенток (28%) не отметили изменений, а 1 (1%) сообщила об усилении СНМП. У 8 из 31 пациентки (26%) при контрольной цистоскопии наблюдался полный регресс лейкоплакии в треугольнике Льето. В 12 случаях (39%) отмечено уменьшение степени выраженности симптомов лейкоплакии. В 10 случаях (32%) цистоскопическая картина не изменилась. Вывод швейцарских медиков: данное лечение следует предпринять прежде, чем ставить диагноз «интерстициальный цистит».
Интерстициальный цистит / синдром боли в мочевом пузыре диагностируется на основании хронической тазовой боли, давления или дискомфорта, связанных по ощущениям с мочевым пузырем и сопровождаемых, по крайней мере, одним из мочевых симптомов, таких как сильное, упорное желание мочиться или учащенное мочеиспускание. Должны быть исключены другие заболевания, имеющие похожие симптомы. Дальнейшее определение и классификация интерстициального цистита / синдрома боли в мочевом пузыре могут быть предприняты на основании данных цистоскопии с гидробужированием и морфологическим исследованием биоптатов.
Результаты зарубежных исследований не подтвердили наличия мочевой инфекции или колонизации мочевого пузыря простыми микроорганизмами. Вместе с тем незначительная бактериурия чаще наблюдается у пациенток с интерстициальным циститом, чем в контрольной группе. Не выявлена связь ИЦ с наличием вирусной или бактериальной ДНК в ткани мочевого пузыря. Наличие бактериурии в популяции больных интерстициальным циститом / синдромом болезненного мочевого пузыря не оказывает влияния на появление или исчезновение симптомов заболевания. Исследовали 314 пациенток с симптомами ИЦ. Влияние ИМП на начало ИЦ выявлено в 18–36% случаев. Ретроспективный анализ подтверждает, что часть женщин (возможно, меньшая) на момент возникновения ИЦ имели признаки ИМП или воспаления. Наличие ИМП в начале ИЦ может быть ключом к разгадке патогенеза заболевания. Профессор А.В. Зайцев также полагает, что у меньшей части больных ИЦ первопричиной болезни явилась инфекция, которая в дальнейшем исчезла, и их моча стала стерильной. Наличие ИМП в детском и подростковом возрасте увеличивает риск развития ИЦ в дальнейшем. У 41,6% из 125 пациенток с ИЦ в анамнезе имела место ИМП.
Провели микробиологическое исследование ткани мочевого пузыря у больных ИЦ. Всего обследовано 14 пациенток, средний возраст – 53 года, средняя продолжительность заболевания – 9 лет. В 9 из 14 случаев отмечена язвенная форма болезни. В количестве 1000–100000 КОЕ/мл выявлены такие микроорганизмы, как Staphylococcus spp., Kocuria spp., Acinetobacter spp., Klebsiella pneumoniae, Proteus mirabilis, Pseudomonas spp., Burkholderia cepacia, Flavimonas oryzihabitans и Brevundimonas vesicularis, а также Staphylococcus pasteuri, образующий биопленки. Докладчик призвал избегать длительного применения антибиотиков и оральных стероидов при таком заболевании, как ИЦ, и привел следующие показания к применению антимикробных препаратов у больных синдромом болезненного мочевого пузыря:
- профилактика ИМП при выполнении инвазивных эндовезикулярных манипуляций;
- доказанное наличие ИМП (3-кратная положительная урокультура, патоморфологическое исследование).
«В остальных случаях у больных с интерстициальным циститом назначать антибактериальные препараты не следует, чтобы не дискредитировать лекарственные средства», – сказал в завершение своего доклада профессор А.В. Зайцев.
Выступление профессора кафедры клинической фармакологии Первого МГМУ им. И.М. Сеченова, д.м.н. Д.А. СЫЧЕВА было целиком посвящено механизмам действия препаратов клюквы на мочевыводящие пути.
Клюква (Vaccinium macrocarpon, V. oxycoccus, V. microcarpum и V. erythrocarpum) – растение семейства вересковых, которое на протяжении тысячелетий использовалось в качестве средства лечения «мочевых проблем». Клюква обладает и другими полезными свойствами. Это важный источник витамина C и полифенолов. Доказано кардиопротективное действие клюквы, противораковые свойства, защитное действие против кариеса зубов. Но наибольший интерес вызывают проантоцианидины клюквы. В опытах in vitro доказано, что клюква за счет проантоцианидинов ингибирует адгезию многих микроорганизмов (Escherichia coli, Proteus spp., Pseudomonas aeruginosa, Staphylococcus aureus, S. typhymurium и Enterococcus faecalis) на различных поверхностях, в том числе даже синтетических. Предположительно, это происходит за счет ингибирования I- и P-типов фимбрий, утрачивающих способность прикрепляться к клеткам эпителия. Компоненты клюквы ингибируют развитие бактериальных биопленок у человека, но очень селективно. Биопленки, продуцируемые патогенами полости рта и уропатогенными штаммами E. coli, по-видимому, очень чувствительны к компонентам клюквы, их рост подавляется на 60–70%. А биопленки, продуцируемые Proteus mirabilis, нечувствительны. Активным действующим веществом клюквы является тримерный A-тип проантоцианидинов. Тип B (встречается в винограде, яблоках, чае) неактивен. Основной механизм действия клюквенных проантоцианидинов A-типа – это ингибирование связывания уропатогенов с P-типом фимбрий посредством маннозоспецифичных, лектиноподобных структур с маннозоподобными остатками на клетках слизистой оболочки. Ингибирование P-фимбрий обратимо. Есть данные, что проантоцианидины способствуют отделению P-фимбрий от бактерий, но по другим данным, плотность P-фимбрий не меняется. Меньше данных, что проантоцианидины ингибируют I-фимбрии.
Существует устаревшее представление, будто действие клюквенного сока связано с изменением реакции мочи. В действительности однократно и многократно применяемая клюква, свежая, сухая и в виде сока, не оказывает клинически значимого влияния на pH мочи. Процессы, с точки зрения клинической фармакологии происходящие в организме с компонентами клюквы, – это всасывание, распределение, биотрансформация, выведение. После приема добровольцами 480 мл клюквенного сока, содержащего 94,47 мг антоцианидинов, максимальная концентрация антоцианидинов в плазме крови достигалась через 1–4 часа и составляла 0,56–4,64 нмоль/л. Максимальная концентрация антоцианидинов в моче после приема добровольцами 200 мл клюквенного сока наблюдалась через 3–6 часов после приема сока, почечная экскреция была практически полной в течение первых 12 часов. Шесть из 12 антоцианидинов, идентифицированных в клюкве, обнаруживаются и в моче. Ферменты биотрансформации и транспортеры антоцианидинов неизвестны. О флавоноидах клюквы известно, что они могут являться субстратами транспортеров (SGLT1, MRP2, MRP3) и цитохрома P450.
Финское исследование 2001 г. эффективности клюквы в предотвращении рецидивов ИМП у женщин предусматривало деление пациенток на три равные группы по 50 человек: контрольную, группу пациентов, принимавших капсулы клюквы (Монурель), и группу, получавшую лактобактерии. Частота рецидивов в группе Монуреля составила всего 16%, в контрольной – 35%, а в группе больных, принимавших лактобактерии, – 39%. В другом исследовании сравнивалась эффективность экстракта клюквы (36 мг антоцианидинов в сутки в течение 6 месяцев) и триметоприма (100 мг/сут) для профилактики ИМП. Пациентки – женщины не моложе 45 лет с рецидивирующей ИМП (триметоприм – 68, клюква – 69). Рецидивы ИМП наблюдались у 14 женщин, получаших триметоприм, и у 25 пациенток, принимавших клюкву, но различия не были статистически достоверными. Не было различий во времени развития первого рецидива с момента начала применения триметоприма или клюквы. Частота отказа от применения составила 16% для триметоприма и 9% для клюквы.
Как отметил профессор Д.А. Сычев, при приблизительно одинаковой эффективности экстракта клюквы и низких доз антибактериального препарата следует сделать выбор в пользу клюквы хотя бы во избежание развития резистентных к антибиотику штаммов микробов. Докладчик напомнил, что Европейская ассоциация урологии в своих рекомендациях 2010 г. отнесла клюкву (Vaccinium macrocarpon) в дозировке проантоцианидинов 36–72 мг/сут к средствам профилактики ИМП. Переносимость клюквы, по данным клинических исследований, достаточно хорошая, но у детей хуже, чем у взрослых. Частота отказов от лечения колебалась от 5 до 47% (у детей) и была наибольшей при применении сока (из-за вкуса) и наименьшей – при использовании капсул. Докладчик прокомментировал эти данные, напомнив, что свежевыжатый сок горький и кислый, а потому дети его переносят с трудом. Отказы же от таблеток и капсул клюквы составляют лишь около 5%.
Зарегистрирован 1 случай иммуно-опосредованной тромбоцитопении у 68-летнего мужчины, который употреблял в пищу неизвестное количество клюквенного сока для облегчения симптомов дискомфорта, связанного с установкой мочевого катетера за 10 дней до госпитализации. В литературе не найдено прямых доказательств безопасности или вреда для матери или плода употребления клюквы во время беременности. Безопасность или вред клюквенного сока в период лактации не изучены. В этой связи в настоящее время назначать препараты клюквы беременным не разрешено, хотя Д.А. Сычев сомневается в пользе такого запрета. Следует избегать лечения клюквой пациентов с установленным нефролитиазом. Однако, по-видимому, клюква повышает вероятность образования только некоторых типов камней (уратных, оксалатных), а на другие типы (брушитный, апатитный, струвитный) оказывает антилитогенное действие.
В некоторых клинических исследованиях изучали фармакокинетическое взаимодействие клюквы с лекарственными средствами. Установлено, что клюквенный сок не влияет на всасывание амоксициллина и цефаклора. Биодоступность данных препаратов не изменялась, когда принятые внутрь лекарства запивали клюквенным соком. Не было обнаружено какого-либо влияния употребления клюквенного сока в течение 14 дней по 200 мл в сутки на фармакокинетику циклоспорина. Нельзя сочетать прием клюквы с применением варфарина. Большинство доступных в России продуктов клюквы не стандартизированы, содержание проантоцианидинов в них неизвестно. Это относится к таким продуктам, как клюква свежая, клюква замороженная, клюквенные соки. Между тем необходимая суточная доза проантоцианидинов составляет 36 мг, что соответствует 750 мл концентрированного клюквенного сока. Оптимальным выбором является применение клюквы в капсулах в виде препарата Монурель, заключил профессор Д.А. Сычев. Препарат рекомендуется принимать в следующих случаях:
- по 1 таблетке в день женщинам молодого и среднего возраста в течение неблагоприятного периода для профилактики рецидивирующих ИМП при неблагоприятных условиях;
- по 1 таблетке в день после курса антибиотикотерапии в течение 1 месяца;
- по 1 таблетке в день женщинам молодого и среднего возраста на срок до 3 месяцев при часто рецидивирующих циститах (более 3 эпизодов в год) с профилактической целью.
