количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Теория
Новые пероральные антикоагулянты для пациентов с фибрилляцией предсердий
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Кардиология и ангиология" №3 (25)
- Аннотация
- Статья
- Ссылки
- English
Новые пероральные антикоагулянты, в частности ривароксабан, более удобны в применении и имеют существенные преимущества в улучшении клинических исходов, в том числе уменьшении острых нарушений мозгового кровообращения (ОНМК), внутричерепных кровоизлияний, снижении летальности. Вероятно, новые пероральные антикоагулянты можно использовать в качестве препаратов первой линии для профилактики ОНМК при неклапанной фибрилляции предсердий.

Таблица 1. Дизайн, критерии включения и критерии оценки в крупных клинических исследованиях новых пероральных антикоагулянтов
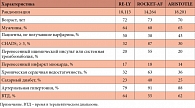
Таблица 2. Характеристика групп пациентов в крупных клинических исследованиях новых пероральных антикоагулянтов
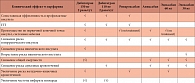
Таблица 3. Эффективность новых антикоагулянтных препаратов в профилактике ишемического инсульта и системных эмболий
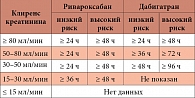
Таблица 4. Рекомендации по использованию дабигатрана и ривароксабана при хирургических вмешательствах

Таблица 5. Сводные данные о противопоказаниях к использованию НПАК
Актуальность проблемы
Острые нарушения мозгового кровообращения (ОНМК) являются важнейшей медико-социальной проблемой. По данным Американской ассоциации сердца (American Heart Association), инсульт встречается у 2,7% мужчин и 2,5% женщин старше 18 лет, с возрастом его частота увеличивается [1]. Одним из наиболее распространенных патогенетических подтипов ишемических нарушений мозгового кровообращения считается кардиоэмболический инсульт. Наиболее частая причина его развития – фибрилляция предсердий (ФП) [2]. Распространенность ФП увеличивается с возрастом, а также на фоне органической патологии сердца [3, 4]. ФП регистрируется у 0,4–2% взрослого населения [5, 6].
В отсутствие профилактического антикоагулянтного лечения среднегодовой риск ОНМК у пациентов с ФП составляет 5% [7]. Как показали результаты исследования AFFIRM [8], антиаритмические препараты не влияют на продолжительность жизни, а антикоагулянты заметно снижают риск смерти. Таким образом, у пациентов с ФП антитромботическую терапию следует расценивать как основную.
Согласно отечественным рекомендациям по диагностике и лечению ФП [9] для оценки риска тромбоэмболических осложнений у пациентов с ФП используется шкала CHA2DS2-VASc. Наличие таких факторов риска, как хроническая сердечная недостаточность (Congestive heart failure), артериальная гипертония (Hypertension) (АГ), возраст 65–74 года (Age), сахарный диабет (Diabetes mellitus), поражение сосудов (Vascular disease) (перенесенный инфаркт миокарда, перемежающаяся хромота, атеросклероз аорты), женский пол (Sex category), оценивается в 1 балл за каждый из факторов; возраст 75 лет и старше (Age) и наличие инсульта/транзиторной ишемической атаки (ТИА) в анамнезе (Stroke) – в 2 балла за каждый. При сумме баллов ≥ 1 назначаются пероральные антикоагулянты (ПАК), аспирин применять не рекомендуется.
Профилактика тромбоэмболических осложнений ассоциирована со значительным увеличением риска кровотечений. Именно поэтому такой риск необходимо оценивать перед назначением антикоагулянтной терапии. В соответствии с российскими рекомендациями 2012 г. [9] по ведению пациентов с ФП риск кровотечений оценивают по шкале HAS-BLED, которая характеризуется более высокой точностью и простотой в использовании. В шкалу HAS-BLED включены такие факторы риска, как АГ (Hypertension), нарушение функции печени и почек (Abnormal renal/liver function), перенесенный инсульт (Stroke), кровотечения в анамнезе или предрасположенность к ним (Bleeding history or predisposition), лабильное международное нормализованное отношение (МНО) (Labile international normalized ratio), возраст ≥ 65 лет (Elderly), сопутствующее применение лекарств или алкоголя (Drugs/alcohol concomitantly). Каждый фактор оценивается в 1 балл. Сумма ≥ 3 баллов по этой шкале свидетельствует о высоком риске кровотечений, что требует особой осторожности при назначении любого антитромботического препарата. Шкалу HAS-BLED следует использовать для идентификации модифицируемых факторов риска, которые можно корректировать.
На протяжении нескольких десятилетий антагонисты витамина K (АВК) считались стандартом в профилактике ОНМК. Их эффективность в профилактике кардиоэмболического инсульта у пациентов с ФП подтверждена клинически [10]. Несмотря на то что использование варфарина связано с улучшением выживаемости среди пациентов с ФП, фактическая частота назначения АВК явно недостаточна. Так, анализ применения варфарина в реальной клинической практике показал [11], что 58% пациентов высокого риска не получают терапию ПАК. Их реже используют пациенты с одним фактором риска (возраст ≥ 75 лет). ПАК достаточно редко назначают при пароксизмальной ФП. Уровни МНО в клинических исследованиях и реальной практике различны. Среди пациентов, перенесших ишемический инсульт, 10% не получают терапию ПАК. Отметим, что простое следование современным руководствам по антикоагулянтной терапии позволило бы предотвратить 20 (22%) инсультов из 89. Терапия АВК имеет ряд ограничений: непредсказуемый ответ, узкое терапевтическое окно (диапазон МНО 2,0–3,0), медленное развитие/окончание эффекта, постоянный контроль антикоагулянтного эффекта, необходимость частой коррекции дозы, взаимодействие с различными пищевыми продуктами и лекарственными препаратами, возможная резистентность к варфарину. Это затрудняет применение АВК в клинической практике.
В последние годы установлено, что достаточно часто (у европейцев более чем в четверти случаев) генетические особенности влияют на метаболизм S-изомера варфарина в печени при участии цитохрома Р4502С9 и молекулу-мишень – витамин К-эпоксидредуктазу. Кроме того, АВК снижают образование печенью и других витамин К-зависимых белков, включая компоненты противосвертывающей системы: белки С и S. Поэтому в случае неназначения парентеральных антикоагулянтов одновременно с АВК для быстрого достижения адекватной антикоагуляции у пациента может развиться тромбоз микроциркуляторного русла и некроз кожи [12].
Все усилия врачебного сообщества были направлены на разработку новых ПАК (НПАК) с более предсказуемым антикоагулянтным эффектом, что позволило бы отказаться от рутинного терапевтического мониторинга свертывания крови.
Учитывая доказанную антикоагулянтную эффективность варфарина, можно утверждать, что альтернативные НПАК должны характеризоваться по крайней мере эквивалентным антитромботическим эффектом, низким риском кровотечений (особенно интракраниальных), минимальным количеством побочных эффектов, отсутствием взаимодействия с пищевыми продуктами и лекарственными средствами, широким терапевтическим окном при применении в стандартной дозе, стабильной антикоагуляцией без необходимости частого лабораторного мониторинга. Кроме того, НПАК должны приниматься перорально (однократно или дважды в день).
Уже появились два основных класса антикоагулянтов на основе звеньев свертывания крови – ингибиторы тромбина (IIA) и активированного фактора Xa. Пероральный прямой ингибитор тромбина дабигатрана этексилат – представитель первого класса. Вторая группа включает ингибиторы фактора Ха – ривароксабан, апиксабан, эдоксабан. В ходе исследований RE-LY [13], ROCKET-AF [14], ARISTOTLE [15] и ENGAGE-AF [16] сравнивали эффективность и безопасность этих препаратов с таковой варфарина у пациентов с неклапанной ФП. В таблицах 1 и 2 приведены основные характеристики этих исследований, а также характеристики пациентов, принимавших в них участие.
Эффективность
В исследованиях RE-LY, ROCKET-AF, ARISTOTLE и ENGAGE-AF была убедительно показана не меньшая эффективность НПАК по сравнению с варфарином в сочетании с рядом преимуществ в отношении безопасности (табл. 3). Дабигатран, апиксабан и ривароксабан не уступали варфарину по эффективности в предотвращении ОНМК и системных тромбоэмболий. Терапия эдоксабаном в низкой дозе (30 мг) сопровождалась увеличением частоты ишемического инсульта на 41% (по сравнению с варфарином) [16]. Преимущество перед варфарином в предотвращении первичной конечной точки (инсульт и системная эмболия) продемонстрировали дабигатран 150 мг, ривароксабан, эдоксабан 60 мг (при проведении анализа в период лечения (on treatment)) и апиксабан.
Безопасность
Применение любого из четырех препаратов (дабигатран, ривароксабан, эдоксабан, апиксабан) снижает риск развития геморрагических ОНМК на 40–70%, а интракраниальных кровоизлияний на ~50%, что демонстрирует их преимущество перед варфарином в отношении интракраниальных кровоизлияний [13–16]. Апиксабан, дабигатран 110 мг и эдоксабан 60 и 30 мг уменьшают частоту серьезных кровотечений.
Эти важные преимущества, подтвержденные в клинических исследованиях, служат обоснованием использования указанных НПАК в качестве препаратов первой линии. Роль низкой дозы эдоксабана (30 мг) в лечении пациентов с ФП пока не установлена.
Влияние на показатель смертности
Как показал анализ, все НПАК примерно на 10% снижают риск смерти от сердечно-сосудистых или любых причин, хотя статистическая значимость такого снижения достигнута только для апиксабана и эдоксабана. И это неудивительно, учитывая поразительное сокращение частоты геморрагических ОНМК. Это преимущество было также отмечено при лечении дабигатраном и ривароксабаном в исследованиях RE-LY и ROCKET-AF.
Режим дозирования НПАК
Дабигатран и апиксабан при пероральном приеме следует проглатывать целиком с водой как натощак, так и во время еды, а ривароксабан необходимо принимать во время еды. Рекомендованная доза дабигатрана 300 мг в сутки назначается в два приема. Пациентам в возрасте 80 лет и старше, а также пациентам, получающим терапию верапамилом, дабигатран назначают в суточной дозе 220 мг – по 110 мг два раза в день.
Дневная доза 300 мг или 220 мг дважды в день выбирается индивидуально с учетом риска развития тромбоэмболии и кровотечений у следующих категорий пациентов:
- в возрасте от 75 до 80 лет;
- с умеренной формой хронической почечной недостаточности;
- с гастритом, эзофагитом и гастроэзофагеальным рефлюксом;
- с повышенным риском кровотечения.
Для ривароксабана рекомендованная доза – 20 мг один раз в день, для апиксабана – 5 мг два раза в день. Для пациентов с неклапанной ФП в возрасте 80 лет и старше, а также для пациентов с массой тела 60 кг и менее либо с уровнем креатинина сыворотки ≥ 133 мкмоль/л рекомендована доза апиксабана 2,5 мг два раза в день.
В случае низкой приверженности терапии пропущенную дозу дабигатрана можно принять не позднее чем за шесть часов до следующей плановой дозы. Если остается менее шести часов, пропущенная доза не принимается. Прием двойной дозы не допускается. В случае пропуска приема очередной дозы ривароксабана пациент должен принять препарат немедленно и продолжать на следующий день терапию в рекомендованной суточной дозе. Прием двойной дозы недопустим.
В случае пропуска приема дозы апиксабана его следует принять немедленно и затем продолжать прием два раза в день, как ранее.
При переходе с АВК на дабигатран прием АВК должен быть завершен. Дабигатран можно назначать при МНО < 2,0. При переходе с АВК на ривароксабан терапия АВК должна быть завершена, а прием ривароксабана начат при МНО ≤ 3,0. Если пациент переходит с терапии АВК на прием ривароксабана, уровень МНО может оказаться ложно повышенным. МНО не подходит для определения антикоагулянтной активности ривароксабана. При переходе с АВК на апиксабан следует прекратить прием АВК и начать терапию апиксабаном при МНО < 2,0.
Переход с дабигатрана на АВК осуществляется с учетом уровня скорости клубочковой фильтрации (СКФ):
- при СКФ ≥ 50 мл/мин – за три дня до окончания терапии дабигатраном;
- при СКФ 30–50 мл/мин – за два дня до окончания терапии дабигатраном.
Пациенты, перешедшие с ривароксабана на АВК, должны одновременно принимать АВК, пока МНО не достигнет ≥ 2,0. При комбинации ривароксабана и АВК МНО не следует контролировать ранее чем через 24 часа после предыдущей дозы, но до приема следующей дозы ривароксабана. При переходе с апиксабана на АВК прием апиксабана надо продолжать по крайней мере в течение двух дней после начала терапии АВК. После двух дней приема комбинации апиксабана и АВК необходим контроль МНО перед применением следующей плановой дозы апиксабана. Апиксабан в комбинации с АВК принимается до достижения МНО ≥ 2,0.
Особые группы пациентов
Пожилые пациенты (в возрасте от 75 до 80 лет) должны получать дабигатран в дозе 300 мг в сутки, престарелые (80 лет и старше) – 220 мг в сутки из-за повышенного риска развития кровотечения. Поскольку у пациентов в возрасте старше 75 лет часто имеет место почечная недостаточность, функция почек должна быть оценена путем определения СКФ на момент начала терапии для исключения пациентов с тяжелой хронической почечной недостаточностью (ХПН) (СКФ < 30 мл/мин). Корректировать дозу у пациентов с легкой ХПН (СКФ 50–80 мл/мин) не рекомендуется. Для больных с умеренной ХПН (СКФ 30–50 мл/мин) рекомендованная доза препарата составляет 300 мг в сутки, однако при высоком риске кровотечения ее снижают до 220 мг в сутки. У тех, кто получает дабигатран, почечную функцию необходимо контролировать один раз в год, а при необходимости и чаще.
При назначении ривароксабана не требуется корректировать дозу у пациентов с легкой ХПН (СКФ 50–80 мл/мин). Ривароксабан применяется с осторожностью у пациентов с СКФ 15–29 мл/мин. Его нецелесообразно назначать пациентам с СКФ < 15 мл/мин. У пациентов с тяжелой ХПН (СКФ 15–29 мл/мин) и неклапанной ФП для предупреждения ОНМК и системной эмболии рекомендуемая доза ривароксабана составляет 15 мг один раз в день.
Апиксабан не рекомендован пациентам с СКФ < 15 мл/мин, а также лицам, находящимся на гемодиализе. Не требуется коррекции дозы у пациентов с легкой или умеренной ХПН. У больных с уровнем креатинина сыворотки ≥ 1,5 мг/дл (133 мкмоль/л) в сочетании с возрастом 80 лет и старше или массой тела 60 кг и менее, а также у пациентов с тяжелой ХНП (СКФ 15–29 мл/мин) доза апиксабана снижается до 2,5 мг два раза в день.
Ривароксабан противопоказан пациентам с заболеваниями печени, сопровождающимися коагулопатиями и клинически значимым риском кровотечения, включая цирротическую стадию болезни. Апиксабан также противопоказан пациентам с заболеваниями печени, связанными с коагулопатиями и клинически значимым риском кровотечения, не рекомендован пациентам с тяжелой печеночной недостаточностью. Препарат следует использовать с осторожностью у пациентов с легкой или умеренной печеночной недостаточностью (А или B по шкале Чайлда – Пью).
Сложным остается выбор антикоагулянтного препарата у больных, перенесших ОНМК. Среди пациентов с ФП доля перенесших ОНМК/ТИА составляет от 15 до 25%. Как известно, такие пациенты имеют высокий риск рецидива цереброваскулярных событий, а значит, им показаны антикоагулянты. Одновременное повышение у них риска кровотечения, в частности интракраниального, менее изучено. В данной подгруппе больных обе дозы дабигатрана и ривароксабана не имеют преимуществ перед варфарином в снижении частоты первичной конечной точки. В то же время именно у этой сложной категории пациентов продемонстрировано существенное снижение частоты геморрагических осложнений на фоне НПАК по сравнению с варфарином [13, 14].
Очень важным представляется вопрос проведения тромболизиса на фоне применения НПАК. Данных, подтверждающих эффективность и безопасность тромболизиса, нет. Следовательно, не существует каких-либо универсальных рекомендаций. Согласно рекомендациям Европейского общества кардиологов (European Society of Cardiology) по ФП 2012 г. нецелесообразно проведение тромболизиса у пациентов с ишемическим инсультом, принимающих НПАК, если имеется удлинение протромбинового времени (для ривароксабана) или активированного частичного тромбопластинового времени (для дабигатрана) [17].
При хирургических вмешательствах использование НПАК также имеет свои особенности. Как следует из рекомендаций, хирургические вмешательства могут потребовать временной отмены дабигатрана. Если необходимо экстренное вмешательство, дабигатран может быть временно отменен. Если возможно, хирургическое вмешательство лучше отложить и провести через 12 часов после приема последней дозы препарата. При неотложном хирургическом вмешательстве надо учитывать, что риск кровотечения возрастает, и это должно быть соотнесено с необходимостью вмешательства.
Если инвазивная процедура или хирургическое вмешательство необходимы, прием ривароксабана должен быть приостановлен по крайней мере за 12 часов до вмешательства (табл. 4).
Апиксабан отменяется по крайней мере за 48 часов до вмешательства с умеренным или высоким риском кровотечения и за 24 часа – при вмешательстве с низким риском кровотечения. Если хирургическое вмешательство или инвазивная процедура не могут быть отменены, необходимо соблюсти все меры предосторожности с учетом повышенного риска кровотечения. После хирургического вмешательства прием препаратов следует возобновить как можно раньше, то есть как только разрешится клиническая ситуация и стабилизируется гемостаз.
Как уже отмечалось, рассматриваемые НПАК благодаря предсказуемой фармакодинамике не требуют регулярного мониторинга. Однако, несмотря на клинические преимущества этих препаратов, кровотечения остаются серьезным побочным эффектом. Дело в том, что сегодня стратегии реверсии антикоагулянтного эффекта этих препаратов ограниченны, особенно в экстренных случаях, при необходимости немедленной реверсии. Антикоагулянтный эффект можно контролировать с помощью активированного протромбинового и тромбинового времени, экаринового времени свертывания, хромогенного анализа фактора X или анти-фактора Xa, хотя ни один из этих методов не был стандартизирован и утвержден для оценки уровня антикоагуляции нового класса препаратов.
В случае развития кровотечения из-за отсутствия доступных антидотов отмена препарата, механическая компрессия и трансфузии представляют собой оптимальное начало лечения. На моделях у животных рекомбинантный фактор VIIa, концентрат активированного протромбинового комплекса (activated prothrombin complex concentrate, APCC) и концентрат протромбинового комплекса (prothrombin complex concentrate, PCC) обеспечили реверсию антикоагулянтного эффекта ингибиторов фактора Ха, что не наблюдалось при использовании этих препаратов с целью реверсии антикоагулянтного эффекта дабигатрана [18].
Для уменьшения риска развития хирургических кровотечений при применении НПАК следует учитывать геморрагические риски. Согласно европейским рекомендациям 2013 г. [17] хирургические вмешательства классифицируют по степени риска кровотечения:
- низкий: эндоскопия с биопсией; биопсия простаты, пузырная биопсия; электрофизиологическое исследование, радиочастотная аблация; ангиография, чрескожное коронарное вмешательство; имплантация электрокардиостимулятора, кардиовертера-дефибриллятора; холецистоэктомия, гистероэктомия; операция пластики грыж, малая пластическая хирургия; малая ортопедическая хирургия/артроскопия. Первые 48 часов вероятность серьезного кровотечения составляет 0–2%;
- высокий: осложненная аблация; спинальная или эпидуральная анестезия; люмбальная пункция, биопсия печени, почек; абдоминальная хирургия; сосудистая хирургия; трансуретральная резекция простаты; большие ортопедические операции; имплантация электрокардиостимулятора, кардиовертера-дефибриллятора в сложных случаях. Первые 48 часов вероятность серьезного кровотечения ≥ 2–4%;
- очень высокий: нейрохирургические операции (внутричерепные и на позвоночнике); кардиохирургия (коронарное шунтирование и операции на клапанах).
НПАК, как и все антикоагулянты, должны использоваться с осторожностью при состояниях, увеличивающих риск кровотечения, и ситуациях сопутствующего назначения препаратов, затрагивающих гемостаз путем ингибирования агрегации тромбоцитов. Так, дабигатран в целом не требует рутинного контроля МНО, однако оценка дабигатрансвязанной антикоагуляции позволит избежать чрезмерного воздействия препарата при наличии дополнительных факторов риска. Такие факторы, как снижение почечной функции (СКФ 30–50 мл/мин), возраст 75 лет и старше, снижение веса менее 50 кг или прием сильных ингибиторов P-гликопротеинов (амиодарон, хинидин или верапамил), связаны с увеличением уровня дабигатрана в плазме. Наличие состояний, повреждений, процедур и/или фармакологического лечения (нестероидные противовоспалительные препараты, антитромбоцитарная терапия, прием селективных ингибиторов обратного захвата серотонина и ингибиторов обратного захвата норадреналина), которые значительно увеличивают риск крупных кровотечений, требуют тщательной оценки соотношения пользы и риска. Ривароксабан при развитии тяжелой геморрагии должен быть отменен. Хотя терапия ривароксабаном не требует рутинного мониторинга, оценка уровня препарата на основе количественного анализа анти-фактора Ха может быть полезной в исключительных ситуациях. Информация об уровне ривароксабана может помочь определиться с клиническим решением (передозировка или экстренная хирургия). Особое внимание при длительной терапии ривароксабаном следует уделять кровотечениям слизистой оболочки (носовое кровотечение, кровотечение из десен, желудочно-кишечные кровотечения) и анемии.
Апиксабан используют с осторожностью при состояниях, увеличивающих риск геморрагии. При развитии тяжелой геморрагии препарат отменяют. Терапия апиксабаном не требует рутинного мониторинга. Между тем Rotachrom анти-фактор Xa-анализ может быть полезен в исключительных ситуациях. Информация об уровне апиксабана может помочь определиться с клиническим решением (передозировка или экстренная хирургия). В таблице 5 приведены сводные данные противопоказаний к использованию НПАК.
При применении НПАК особое внимание следует обращать на сопутствующую терапию: дабигатран не метаболизируется системой цитохрома CYP, однако служит субстратом для эффлюксного транспортного белка P-гликопротеинов. Последнее свойство препарата необходимо учитывать при его комбинировании с ингибиторами P-гликопротеинов, такими как амиодарон и верапамил. Одновременное применение дабигатрана с мощным индуктором P-гликопротеинов рифампином противопоказано. Прямые ингибиторы фактора Ха – ривароксабан и апиксабан – проявляют меньший потенциал лекарственных взаимодействий, чем варфарин и дабигатран. Метаболизм ривароксабана и апиксабана осуществляется ферментами CYP3A4/5, поэтому надо избегать их одновременного приема с мощными ингибиторами (кетоконазол) или индукторами CYP3A4/5 (рифампицин).
Заключение
Подводя предварительные итоги, следует констатировать, что по сравнению с варфарином НПАК более удобны и имеют существенные преимущества в улучшении клинических исходов, в том числе уменьшении частоты ОНМК, внутричерепных кровоизлияний, снижении летальности. Представляется, что НПАК можно использовать в качестве препаратов первой линии для профилактики ОНМК при неклапанной ФП. Рассматривая вопросы выбора между различными НПАК, нужно подчеркнуть, что поскольку прямые сравнительные исследования отсутствуют, приходится опираться на непрямое сравнение препаратов. Выбор препарата должен быть сугубо индивидуальным. Необходимо принимать в расчет возможность соблюдения режима лечения пациентом, предпочтительность однократного приема перед двукратным. Важно учитывать другие препараты, которые получает пациент, выявить у него риск кровотечений или нарушений со стороны желудочно-кишечного тракта (ЖКТ). Вместе с тем представляется, что три наиболее распространенных НПАК схожи, а основные различия в их эффектах, выявленные в ходе клинических исследований, обусловлены скорее дизайном и числом участников. При этом ингибиторы фактора Ха, вероятно, имеют некоторое преимущество, если говорить о нецелевой токсичности. Они в меньшей степени, чем ингибиторы IIa-фактора, зависят от почечной элиминации и оказывают меньше побочных эффектов в отношении ЖКТ: при наличии у пациента нарушений со стороны почек или склонности к развитию побочных эффектов со стороны ЖКТ предпочтение следует отдавать ривароксабану или апиксабану, нежели дабигатрану. В настоящее время ривароксабан выступает в качестве ценной альтернативы АВК у пожилых людей, пациентов с высокой оценкой по шкале CHA2DS2-VASc, а также с высоким риском острого коронарного синдрома или имеющих стабильные формы ишемической болезни сердца.
Вместе с тем варфарин все еще требуется пациентам, перенесшим протезирование клапанов сердца, о чем говорят отрицательные результаты исследований дабигатрана.
Кроме того, использование варфарина необходимо при тяжелых ревматических поражениях клапанов сердца, поскольку пока отсутствуют данные о действии новых препаратов в такой ситуации.
1. Roger V.L., Go A.S., Lloyd-Jones D.M. et al. Heart disease and stroke statistics--2011 update: a report from the American Heart Association // Circulation. 2011. Vol. 123. № 4. P. e18–e209.
2. Go A.S., Hylek E.M., Phillips K.A. et al. Prevalence of diagnosed atrial fibrillation in adults: national implications for rhythm management and stroke prevention: the AnTicoagulation and Risk Factors in Atrial Fibrillation (ATRIA) Study // JAMA. 2001. Vol. 285. № 18. P. 2370–2375.
3. Feinberg W.M., Blackshear J.L., Laupacis A. et al. Prevalence, age distribution, and gender of patients with atrial fibrillation. Analysis and implications // Arch. Intern. Med. 1995. Vol. 155. № 5. P. 469–473.
4. Stewart S., Hart C.L., Hole D.J., McMurray J.J. Population prevalence, incidence, and predictors of atrial fibrillation in the Renfrew/Paisley study // Heart. 2001. Vol. 86. № 5. P. 516–521.
5. Wolf P.A., Dawber T.R., Thomas H.E. Jr., Kannel W.B. Epidemiologic assessment of chronic atrial fibrillation and risk of stroke: the Framingham study // Neurology. 1978. Vol. 28. № 10. P. 973–977.
6. Guyatt G.H., Akl E.A., Crowther M. et al. Introduction to the ninth edition: antithrombotic therapy and prevention of thrombosis, 9th ed. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines // Chest. 2012. Vol. 141. Suppl. 2. P. 48S–52S.
7. Wolf P.A., Abbott R.D., Kannel W.B. Atrial fibrillation as an independent risk factor for stroke: the Framingham Study // Stroke. 1991. Vol. 22. № 8. P. 983–988.
8. Corley S.D., Epstein A.E., DiMarco J.P. et al. Relationships between sinus rhythm, treatment, and survival in the Atrial Fibrillation Follow-Up Investigation of Rhythm Management (AFFIRM) Study // Circulation. 2004. Vol. 109. № 12. P. 1509–1513.
9. Диагностика и лечение фибрилляции предсердий. Рекомендации РКО, ВНОА, АССХ, 2012. С. 1–64.
10. Hart R.G., Pearce L.A., Aguilar M.I. Meta-analysis: antithrombotic therapy to prevent stroke in patients who have nonvalvular atrial fibrillation // Ann. Intern. Med. 2007. Vol. 146. № 12. P. 857–867.
11. Gomes J. Warfarin for stroke prevention in an elderly community population with atrial fibrillation // Europace. 2010. Vol. 12. P. 779–784.
12. Odén A., Fahlén M., Hart R.G. Optimal INR for prevention of stroke and death in atrial fibrillation: a critical appraisal // Thromb. Res. 2006. Vol. 117. № 5. P. 493–439.
13. Connolly S.J., Ezekowitz M.D., Yusuf S. et al. Dabigatran versus warfarin in patients with atrial fibrillation // N. Engl. J. Med. 2009. Vol. 361. № 12. P. 1139–1151.
14. Patel M.R., Mahaffey K.W., Garg J. et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation // N. Engl. J. Med. 2011. Vol. 365. № 10. P. 883–891.
15. Granger C.B., Alexander J.H., McMurray J.J. et al. Apixaban versus warfarin in patients with atrial fibrillation // N. Engl. J. Med. 2011. Vol. 365. № 11. P. 981–992.
16. Giugliano R.P., Ruff C.T., Braunwald E. et al. Edoxaban versus warfarin in patients with atrial fibrillation // N. Engl. J. Med. 2013. Vol. 369. № 22. P. 2093–2104.
17. Heidbuchel H., Verhamme P., Alings M. et al. European Heart Rhythm Association Practical Guide on the use of new oral anticoagulants in patients with non-valvular atrial fibrillation // Europace. 2013. Vol. 15. № 5. P. 625–651.
18. Petzborn E., Harwardt M. Recombinant Factor VII apartially reverses the effects of the Factor Xa inhibitor rivaroxaban on thrombin generation, but not the effects of thrombin inhibitors, in vitro // J. Thromb. Haemost. 2007. Vol. 5. № 2. Abstr. P-W-640.
New Oral Anticoagulants for Patients with Atrial Fibrillation
Ye.V. Serdechnaya, B.A. Tatarsky
Northern State Medical University (Arkhangelsk)
Contact person: Yelena Valeryevna Serdechnaya, ekserdechny@yandex.ru
Compared to warfarin, new oral anticoagulants (NOACs), e.g. rivaroxaban, are charactirized by better usability and improved clinical efficacy (i.e. decreased stroke, intracranial bleeding and mortality risks). NOACs may be regarded as first-line therapies for the prevention of stroke in patients with non-valvular atrial fibrillation.
Новости на тему
09.09.2022 01:00:00
25.04.2022 10:00:00
08.04.2022 09:00:00
СТАТЬИ по теме
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
