Нужен ли контроль гликемии при сахарном диабете: «за» и «против»
- Аннотация
- Статья
- Ссылки


В то же время справедливо утверждение проф. Пьера Лефевра (Pierre Lefèbvre): мы можем лечить сахарный диабет, но не умеем его излечивать. Дело в том, что оптимальное лечение, увы, доступно не большинству больных, а лишь немногим. Причина заключается не только в большом объеме и сложности доказательной базы, но и в трудности оказания самой диабетологической помощи, отсутствии экономически обоснованного подхода к лечению больных диабетом и общепринятых стандартов клинической практики. В этой связи одним из путей решения проблемы представляется создание соответствующих руководств и методических указаний. В последние годы был опубликован целый ряд подобных документов, в том числе международных, национальных и локальных, однако большинство из них не учитывают новейшие строгие методические требования к идентификации и анализу получаемых данных.
В мире принята концепция медицины, основанная на доказательствах. В связи с этим Американская диабетическая ассоциация (АДА, 2009) предложила систему оценки качества научных данных, лежащих в основе клинических рекомендаций, – классификацию уровней доказательности (табл. 1). Рекомендации, обозначенные в таблице 1 как А, В или С, зависят от качества доказательности. Мнение экспертов (Е) представляет собой отдельную категорию рекомендаций, когда еще нет убедительных доказательств, полученных в результате клинических исследований, когда клинические исследования могут быть невыполнимы или имеются противоречивые доказательства.
В сегодняшней клинической практике актуальными и наиболее дискутируемыми мировой медицинской общественностью являются следующие вопросы. Какие целевые значения показателей гликемии являются безопасными и эффективными с точки зрения предотвращения развития сосудистых осложнений? Какие медикаментозные средства или их комбинации наиболее эффективны и безопасны? Насколько велик риск развития онкологической патологии при СД и какую роль могут играть в этих процессах различные антидиабетические препараты? В 2008 г. были обнародованы результаты 30-летнего наблюдения за больными с СД 2 в рамках исследования UKPDS (UK prospective diabetes study). Результаты исследования показали: хороший контроль гликемии в первые годы заболевания действенен и через многие годы. Установлено, что лица из группы интенсивного контроля имели в итоге и более низкую смертность, и меньшее количество сосудистых осложнений, чем пациенты из группы стандартного контроля.
Важнейшее значение также имели результаты исследования «Многофакторное управление и сердечно-сосудистая заболеваемость у пациентов с СД 2 типа», выполненного в STENO-центре (Копенгаген) и получившего название STENO-2. В рандомизированное, открытое исследование было включено 160 пациентов с микроальбуминурией, с исходным уровнем HbA1c ~ 8,4%. Активное наблюдение (лечение) продолжалось 7,8 лет, затем наблюдение продолжалось еще 5,2 лет (всего 13 лет). Пациенты были разделены на 2 группы – интенсивного и стандартного контроля. Основой интенсивного лечения в 1-й группе был препарат сульфонилмочевины Диабетон МВ. Установлена взаимосвязь интенсивной терапии с низким риском смертности от кардиоваскулярных причин (относительный риск (ОР) 0,43; 95-процентный доверительный интервал (ДИ) 0,19–0,94; p = 0,04). Установлена взаимосвязь интенсивной терапии с низким риском кардиоваскулярных эпизодов (ОР 0,41; 95% ДИ 0,25–0,67; p < 0,001). В группе интенсивной терапии умерли 24 пациента, а в группе стандартного лечения – 40 (ОР 0,54; 95% ДИ 0,32–0,89; p = 0,02). Только у одного пациента группы интенсивной терапии отмечено прогрессирование нефропатии до хронической почечной недостаточности (ХПН) против 6 пациентов в группе традиционной терапии (p = 0,04). Нескольким пациентам потребовалась лазерная фотокоагуляция сетчатки (ЛФК) (ОР 0,45; 95% ДИ 0,21–0,86; p < 0,02). Отмечено несколько серьезных побочных эффектов. Главные результаты исследования: обоснование для внедрения многофакторного подхода в лечении СД 2; достижение 50-процентного снижения риска развития макро- и микрососудистых осложнений.
В связи с результатами данных исследований возникли вопросы, которые требовали конкретных и своевременных ответов. Какие преимущества могут быть получены в результате жесткого контроля (более выраженного снижения) АД у пациентов с СД 2 типа, включая нормотензивных больных? Какие преимущества могут быть получены в результате более интенсивного гликемического контроля (HbA1c < 6,5%) в сравнении со стандартным? Какие преимущества могут быть получены в результате комбинации первых двух? В 2008 г. были завершены три крупнейших многоцентровых исследования: ADVANCE (Action in Diabetes and Vascular disease: Preterax and Diamicron MR Controlled Evaluation), ACCORD (Action to Control Cardiovascular Risk in Diabetes), VADT (Veterans Affairs Diabetes Trial). Цель этих работ – определить влияние различных терапевтических стратегий на развитие сердечно-сосудистых осложнений и смертности у больных с СД 2 типа с большим стажем диабета. Особый интерес представляют результаты исследования ADVANCE, которое по своему дизайну было наиболее продуманным, безопасным и «гуманным».
В исследовании ADVANCE в группе интенсивного гликемического контроля изучали последовательную стратегию, основанную на применении Диабетона МВ. Выбор Диабетона МВ в качестве основы интенсивной терапии в исследовании ADVANCE был определен уже известными свойствами данного препарата, а именно:
- оригинальная молекула и инновационная структура, что делает возможным эффективное 24-часовое действие при однократном приеме во время завтрака;
- доказанный эффективный и долгосрочный гликемический контроль;
- отличная переносимость даже в высоких дозах;
- антиоксидантные свойства, способность улучшать эндотелиальную функцию, что обеспечивает прямую сосудистую защиту;
- защищает β-клетки от апоптоза, индуцированного гипергликемией, сохраняя пул β-клеток. Наблюдение за включенными в исследование пациентами продолжалось 5 лет.
- основных микро- и макрососудистых осложнений на 10% (p = 0,013);
- микрососудистых осложнений на 14% (p = 0,01);
- уровня микроальбуминурии на 9% (p = 0,018);
- уровня макроальбуминурии на 30% (p < 0,001);
- развития новых случаев нефропатии и ее прогрессирования на 21% (p = 0,006).
В результате сердечно-сосудистая смертность снизилась на 12% (p = 0,12).
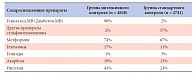
Выше перечисленные данные исследования ADVANCE конфликтуют с показателями избыточной сердечно-сосудистой смертности (ОР 1,35; p = 0,02) в исследовании ACCORD. Более того, такая высокая частота случаев смертности послужила причиной преждевременного прекращения гипогликемической ветви исследования ACCORD. В нем пациенты в группе интенсивного контроля получали один или несколько стимуляторов секреции инсулина (глимепирид 78,2%, репаглинид 50,2%). Кроме того, недостоверная тенденция к избыточной сердечно-сосудистой смертности (ОР 1,32; ДИ 0,81–2,14; р = 0,26) наблюдалась в исследовании VADT, в котором в качестве препарата из группы ПСМ использовали глимепирид. Отсутствие статистической значимости этого результата, вероятно, может объясняться недостаточной численностью групп пациентов. Таким образом, стратегия интенсивной терапии, основанная на Диабетоне МВ в исследовании ADVANCE, оказалась наиболее перспективной и безопасной.
Полученные результаты, тем не менее, поставили ряд актуальных проблем. Главным является вопрос, какой уровень HbA1c является необходимым и безопасным для предотвращения сосудистых осложнений? Следующий по важности вопрос – какую следует выбирать тактику сахароснижающей терапии? Таким образом, исходя из вышесказанного, становится понятным, почему необходимо создание четких и понятных рекомендаций по лечению СД 2:
- рекомендации разъясняют имеющиеся доказательства для всех врачей;
- в связи с появлением новых препаратов возможности лечения расширяются;
- рекомендации нуждаются в пересмотре по мере появления новых доказательств.
Однако при этом не стоит забывать, что рекомендации не заменяют клиническое решение при лечении конкретного пациента. Согласованный алгоритм оказания медицинской помощи при лечении сахарного диабета 2 типа, созданный группой экспертов Американской диабетической ассоциации (АDА) и Европейской ассоциации по изучению сахарного диабета (EASD), был опубликован впервые в августе 2006 г. Этот документ вызвал широкий резонанс и активную критическую дискуссию во всем мире. Учитывая результаты исследований ADVANCE, ACCORD, VADT, UKPDS, эксперты ADA совместно с EASD опубликовали новый вариант рекомендаций «Консенсус (Согласованный алгоритм) по ведению гипергликемии при СД 2 (начальная и дополнительная терапия)». Согласно Консенсусу, эффективным и безопасным следует признать уровень HbA1c < 7%, но при этом необходимо особо подчеркнуть, что целевые значения HbA1c должны быть индивидуализированы.
Сформулированная документом цель лечения:
- у всех больных: уровень HbA1c < 7%;
- у конкретного пациента следует стремиться к снижению уровня HbA1c как можно ближе к норме (< 6 %), по возможности избегая значимой гипогликемии;
- указанием к усилению терапии является повышение уровня HbA1c >7%.
В ряде случаев целесообразно установление менее строгих целевых уровней HbA1c для следующих категорий пациентов:
- пациенты с тяжелой гипогликемией в анамнезе;
- пациенты с небольшой ожидаемой продолжительностью жизни;
- дети и лица пожилого возраста;
- пациенты с сопутствующими сердечно-сосудистыми заболеваниями.
При выборе соответствующего сахароснижающего препарата необходимо учитывать ряд факторов:
- эффективность в снижении уровня глюкозы крови. При HbA1c ≥ 8,5% рекомендуются классы препаратов с более выраженным и более быстрым гипогликемическим действием; возможно более раннее начало комбинированной терапии;
- экстрагликемические эффекты, которые способны снизить риск развития поздних осложнений: артериальная гипертензия, дислипидемия, индекс массы тела, резистентность к инсулину, способность к секреции инсулина;
- безопасность;
- переносимость;
- простота применения;
- стоимость.
Основополагающими принципами лечения СД 2 в предложенном Согласованном алгоритме ADA/EASD являются следующие:
- раннее медикаментозное вмешательство сразу после установления диагноза;
-
активное участие пациента (обу-чение, самоконтроль глюкозы крови, коррекция лечения);
- сокращение задержек в изменении терапии;
- достижение и поддержание целевых нормальных уровней гликемии;
- добавление необходимых препаратов;
- быстрый переход на новые режимы лечения во всех ситуациях, когда уровень HbA1c ≥ 7%.
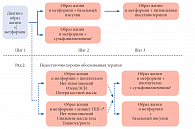
Согласованный алгоритм предлагает два варианта (ряда) терапии: хорошо обоснованная терапия и недостаточно хорошо обоснованная терапия (рис. 1). Первый вариант (хорошо обоснованная терапия) предусматривает последовательное использование хорошо известных и доказанных по эффективности препаратов и схем. Это наиболее изученная, эффективная, а также оптимальная по соотношению затрат и эффективности терапевтическая стратегия достижения целевых уровней гликемии.
Вариант 1 включает в себя ступенчатое и своевременное усиление терапии, борьбу с «клинической инертностью». На каждом визите предусматривается усиление мероприятий по изменению образа жизни. Контроль HbA1c проводится каждые 3 месяца, пока его уровень не снизится менее 7% либо не будет как можно более близким к недиабетическому диапазону. Затем этот анализ повторяется как минимум каждые 6 месяцев. Указанием для активного действия является уровень HbA1c ≥ 7%. Изменение вмешательств должно производиться в этих случаях в настолько быстром темпе, насколько это позволяет режим титрования доз препаратов.
Подводя итог самых первых лечебных мероприятий, выполняемых у больных СД 2 в период манифестации заболевания, необходимо особо подчеркнуть, что выбор врача зависит от предписанной схемы лишь отчасти. Главенствующую роль будут играть степень декомпенсации заболевания и состояние пациента. Нередки случаи, когда в дебюте заболевания мы видим не только резкую декомпенсацию СД, но и обострение сопутствующих заболеваний, таких как мочевые инфекции, туберкулез и др. В этих ситуациях необходимо активно снижать уровень гликемии, а метформин может быть противопоказан. В этой связи в конечном итоге выбор всегда остается за врачом. Выбор второго препарата – препараты сульфонилмочевины или базальный инсулин – будет зависеть (частично) от уровня HbA1c.
Большинство пациентов с впервые диагностированным диабетом 2 типа обычно хорошо отвечают на лечение препаратом сульфонилмочевины. Производные сульфонилмочевины обладают выраженным гипогликемическим действием из-за влияния на секрецию инсулина β-клетками (снижение гликемии до 3%), поэтому главными побочными эффектами являются гипогликемия и прибавка массы тела. Поскольку глибенкламид и хлорпропамид ассоциируются с очень высоким риском гипогликемических реакций, их использование не рекомендуется. Важно отметить, что в новой редакции Согласованного алгоритма ADA/EASD отдается предпочтение производным сульфонилмочевины новой генерации (гликлазид и глимепирид), они на равных конкурируют с инсулинотерапией за позицию первого шага в комбинированной терапии.
У пациентов с HbA1c > 8,5% предпочтительно назначение базального инсулина. В том случае если уровень HbA1c > 8,5% или имеются какие-либо иные показания, следует безотлагательно назначать инсулинотерапию. Главным побочным эффектом инсулинотерапии несомненно является гипогликемия. Описанный выше алгоритм лечения СД 2 вызвал достаточно бурную и продолжительную дискуссию. Были высказаны различные мнения по срокам начала комбинированной терапии и ее характера. В этом смысле особый интерес представляют результаты исследования ADVANCE, где были применены разнообразные схемы комбинированной терапии, но было доказано, что комбинации разных препаратов с Диабетоном МВ позволяют достичь целевых значений гликемии практически в любых случаях. Известными свойствами Диабетона МВ являются его селективность по отношению только к β-клеткам поджелудочной железы и интактность в отношении рецепторов сульфонилмочевины в кардиомиоцитах и др. Все это делает данный препарат незаменимым при проведении как моно-, так и комбинированной терапии у больных СД 2.
Таким образом, наиболее целесообразным и достаточным для предотвращения развития и прогрессирования сосудистых осложнений сахарного диабета следует признать уровень HbA1c равный 7% с оговоркой о необходимости индивидуализации этого критерия для конкретного больного. Выбор начальной и дальнейшей комбинированной терапии не должен быть ориентирован исключительно на конкретный или единственный алгоритм, поскольку в конечном итоге выбор всегда остается за врачом. Темпы достижения компенсации не должны быть слишком быстрыми, но и не могут быть растянуты на годы. Лечение должно быть эффективным, безопасным и удобным для больного, ибо в противном случае желаемый или ожидаемый результат не будет достигнут никогда.
NB
Rомбинации разных препаратов с Диабетоном МВ позволяют достичь целевых значений гликемии практически в любых случаях. Известными свойствами Диабетона МВ являются его селективность по отношению только к β-клеткам поджелудочной железы и интактность в отношении рецепторов сульфонилмочевины в кардиомиоцитах и др. Все это делает данный препарат незаменимым при проведении как моно-, так и комбинированной терапии у больных СД 2.
*К концу наблюдения 70% больных получали Диабетон МВ в дозе 120 мг утром перед завтраком. - Прим. авт.
