Омализумаб в лечении пациентов с хронической крапивницей
- Аннотация
- Статья
- Ссылки
- English
Цель. Исследование эффективности и безопасности омализумаба у больных хронической крапивницей, рефрактерных к антигистаминным препаратам, в реальной клинической практике.
Материал и методы. В ретроспективном клиническом исследовании приняли участие 17 пациентов: 16 с хронической идиопатической крапивницей, четверо из которых страдали и физической крапивницей, и одна пациентка с физической крапивницей.
Результаты. Полный эффект терапии достигнут у 70,6% пациентов, значительный – у 17,7%. Лечение оказалось неэффективным в 11,7% случаев. У восьми участников положительный эффект отмечен в течение 24 часов, у двух – в течение двух-трех дней, у двух – в течение двух недель, у одного – в течение четырех недель, у двух участников – в течение восьми недель. 11 пациентов применяли препарат в дозе 300 мг весь период наблюдения, одна пациентка – в дозе 150 мг, четыре пациента – две инъекции по 300 мг, затем две инъекции по 150 мг, одна пациентка начала лечение с дозы 150 мг, затем доза была увеличена до 300 мг. Терапия омализумабом характеризовалась как безопасная. На эффективность лечения омализумабом не влияли уровень общего иммуноглобулина Е и результаты теста с аутосывороткой.
Заключение. Наблюдение за больными хронической идиопатической крапивницей с сопутствующей или самостоятельной физической крапивницей, получавших омализумаб, позволяет рекомендовать препарат пациентам, рефрактерным к терапии первой и второй линии.
Цель. Исследование эффективности и безопасности омализумаба у больных хронической крапивницей, рефрактерных к антигистаминным препаратам, в реальной клинической практике.
Материал и методы. В ретроспективном клиническом исследовании приняли участие 17 пациентов: 16 с хронической идиопатической крапивницей, четверо из которых страдали и физической крапивницей, и одна пациентка с физической крапивницей.
Результаты. Полный эффект терапии достигнут у 70,6% пациентов, значительный – у 17,7%. Лечение оказалось неэффективным в 11,7% случаев. У восьми участников положительный эффект отмечен в течение 24 часов, у двух – в течение двух-трех дней, у двух – в течение двух недель, у одного – в течение четырех недель, у двух участников – в течение восьми недель. 11 пациентов применяли препарат в дозе 300 мг весь период наблюдения, одна пациентка – в дозе 150 мг, четыре пациента – две инъекции по 300 мг, затем две инъекции по 150 мг, одна пациентка начала лечение с дозы 150 мг, затем доза была увеличена до 300 мг. Терапия омализумабом характеризовалась как безопасная. На эффективность лечения омализумабом не влияли уровень общего иммуноглобулина Е и результаты теста с аутосывороткой.
Заключение. Наблюдение за больными хронической идиопатической крапивницей с сопутствующей или самостоятельной физической крапивницей, получавших омализумаб, позволяет рекомендовать препарат пациентам, рефрактерным к терапии первой и второй линии.

Введение
Хроническая идиопатическая (спонтанная) крапивница – редко встречающееся заболевание. По некоторым данным, им страдают в среднем 0,1–1% популяции. Однако за последнее десятилетие наблюдается рост заболеваемости [1].
Поставить диагноз «крапивница» несложно. Гораздо труднее установить причину ее развития [2]. Само слово «идиопатическая» (или «спонтанная») предполагает отсутствие клинически обоснованных причин развития заболевания. Объем диагностических мероприятий диктуется спектром возможных этиологических факторов. Однако в такой ситуации весьма вероятно назначение лишних и неоправданных с диагностической и (или) экономической точки зрения исследований [3].
Недостаточное понимание механизмов патогенеза крапивницы и отсутствие биомаркеров эффективности лечения привели к тому, что сегодня терапия пациентов с хронической идиопатической крапивницей предполагает несколько этапов. При этом переход на следующий этап происходит из-за неэффективности предыдущего [4].
Сначала назначают неседативные Н1-антигистаминные средства (нс Н1-АГ) (первый этап). В случае отсутствия эффекта лицензированной дозы дозу препаратов увеличивают до четырехкратной (второй этап). Далее предлагается терапия омализумабом, циклоспорином А, монтелукастом (третий этап). Циклоспорин А эффективен в лечении торпидной хронической крапивницы, однако на фоне его применения могут развиться потенциально опасные побочные эффекты. Монтелукаст эффективен в небольшом проценте случаев, хотя и обладает хорошим профилем безопасности. Кроме того, применение этих препаратов относится к категории «не по показаниям».
Для купирования обострения хронической крапивницы на любом этапе лечения коротким курсом (в целях предотвращения осложнений) могут применяться глюкокортикостероиды (ГКС) [4].
В 2014 г. на российском фармацевтическом рынке появился препарат для лечения пациентов с хронической крапивницей, рефрактерных к антигистаминным средствам, – омализумаб.
Омализумаб – терапевтические моноклональные антитела к иммуноглобулину E (IgE) человека. Указанные антитела уже несколько десятилетий применяются при лечении бронхиальной астмы среднетяжелого и тяжелого течения. Гуманизированные анти-IgE антитела содержат 95% человеческого белка и 5% белка мыши в Fab-области. Fab-фрагмент связывается с Fc-областью IgE и действует как конкурентный ингибитор: связывает только свободный IgE и образует биологически инертную молекулу. Это предотвращает взаимодействие свободного IgE с высокоаффинными и низкоаффинными IgE-рецепторами (FcεRI и FcεRII) [5, 6]. Снижение уровня циркулирующего свободного IgE приводит к уменьшению FcεRI на тучных клетках, базофилах, дендритных клетках. Таким образом предупреждается высвобождение провоспалительных медиаторов. Показано, что снижение FcεRI на дендритных клетках может привести к истощению дифференцировки Th2-лимфоцитов [7].
Лечение омализумабом снижает активацию и чувствительность тучных клеток, активацию эозинофилов и эозинофильную инфильтрацию [8, 9]. Возможность применения омализумаба в терапии ряда аллергических заболеваний (например, аллергический ринит, пищевая аллергия, анафилаксия, атопический дерматит, полипозный риносинусит, мастоцитоз, реакция на ужаление инсектами, аллергический бронхолегочный аспергиллез) обусловлена вовлечением в их патогенез IgE.
Первые доказательства эффективности омализумаба при разных видах крапивницы (спонтанной, холодовой, холинергической, солнечной) были получены из клинической практики и небольших клинических исследований, опубликованных в 2006–2011 гг. [10–14]. Кроме того, были опубликованы результаты трех плацебоконтролируемых исследований эффективности и безопасности омализумаба у пациентов с хронической крапивницей.
Наиболее показательными с точки зрения доказательной медицины были три исследования: ASTERIA I, ASTERIA II и GLACIAL [15, 16]. Необходимо отметить, что лечение хронической крапивницы омализумабом является симптоматическим, а не болезньмодифицирующим. При этом не решен вопрос о длительности терапии.
В работе I. Fiorino описан случай успешного лечения омализумабом 54-летней пациентки с хронической идиопатической крапивницей в течение четырех лет [17].
Данные о продолжительности ремиссии на фоне терапии омализумабом противоречивы – от четырех до восьми недель [18] и более [19].
Вышесказанное послужило поводом проведения ретроспективного анализа эффективности и безопасности омализумаба у больных хронической крапивницей, рефрактерных к антигистаминным препаратам, в реальной клинической практике.
Материал и методы
Эффективность и безопасность омализумаба оценивалась у 17 пациентов, из них 14 женщин и трое мужчин. Возраст больных – от 27 до 67 лет. Длительность заболевания составляла от полугода до 16 лет.
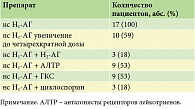
До начала исследования пациенты получали лечение первой, второй, а некоторые и третьей линии (кроме омализумаба) (табл. 1).
Все участники наблюдались в клинике Института иммунологии с февраля 2014 г. по февраль 2015 г. Клинический диагноз поставлен на основании изучения анамнеза и клинической картины.
У 16 пациентов выявлена хроническая идиопатическая крапивница. Кроме того, у одного из них обнаружены три сопутствующие формы физической (индуцированной) крапивницы (холинергическая, дермографическая, замедленная от давления), у двух – замедленная крапивница от давления, у одной пациентки – дермографическая. Одна пациентка из 17 страдала только физической крапивницей (холодовой и холинергической). В 11 (60%) случаях наблюдался ангиоотек.
Пациенты помимо стандартного прошли расширенное клинико-лабораторное обследование.
Омализумаб применяли в дозе 300 или 150 мг. Первая рекомендована в инструкции по применению препарата. Выбор второй продиктован клинической ситуацией. Интервал между инъекциями в большинстве случаев составлял четыре недели.
Для оценки эффективности проводимой терапии применялся индекс активности крапивницы за семь дней (Urticaria Activity Score 7 – UAS 7). UAS 7 определялся до лечения и в течение семи дней до следующей инъекции [4].
Полный ответ на терапию омализумабом характеризовался как снижение индекса от 90% и более, значительный – от 90 до 30%, незначительное улучшение – менее 30% [18]. Оценить аналогичным образом физическую крапивницу не удалось в связи с невозможностью определить пороговый уровень раздражения.
Результаты
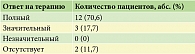
Анализ результатов свидетельствовал об эффективности обеих доз препарата (табл. 2). У пациентов с сопутствующими ангиоотеками отмечена аналогичная эффективность.
У пациентки, страдавшей только физической крапивницей, симптомы холодовой крапивницы стали менее интенсивными, холинергической – исчезли полностью.
У пациентов с сопутствующими формами крапивницы значительное улучшение всех трех форм зафиксировано у одного больного. Кроме того, у одного пациента не выявлена замедленная крапивница от давления, еще у одной пациентки – дермографическая крапивница.
Все пациенты переносили омализумаб хорошо.
Нежелательных явлений не наблюдалось.
Терапевтический эффект у восьми пациентов отмечен уже в первые 24 часа, у двух – в течение двух-трех дней, у двух – двух недель, у одного – четырех недель, у двух пациентов – в течение восьми недель.
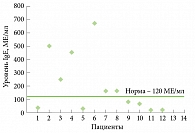
В ходе исследования у 12 пациентов измеряли уровень общего IgE (рис. 1). Минимальное значение составило 18 МЕ/мл, максимальное – 672 МЕ/мл при норме 120 МЕ/мл. У половины обследованных данный показатель оказался повышенным. Заметной корреляции между уровнем общего IgE и эффективностью омализумаба зафиксировано не было.
Тест с аутосывороткой проведен 13 пациентам. В восьми случаях он был отрицательным, в пяти – положительным. Связь между результатами теста и эффективностью терапии не выявлена.
В качестве примера приведем клинический случай. Пациентка Я., 1987 года рождения.
Диагноз: хроническая идиопатическая аутореактивная крапивница, ангиоотеки, обострение.
Анамнез: первый кратковременный эпизод крапивницы в девять лет. Обострение произошло после родов. Длительность заболевания – шесть лет. Н1-АГ препараты первого и второго поколения в стандартной дозе не дали положительного результата. В июне 2011 г. пациентка госпитализирована в клинику Института иммунологии в связи с тяжелым течением крапивницы и неэффективностью проводимой терапии. При поступлении жалобы на генерализованные зудящие волдыри, отеки мягких тканей.
Проведено стандартное и расширенное обследование. В клиническом анализе крови лейкоцитоз до 22,6 × 109/л, уровень С-реактивного белка – 3,69 мг/дл (0–0,75 мг/дл).
Биохимический анализ крови (общий белок, мочевина, креатинин, гамма-глутамилтрансфераза, аланинаминотрансфераза, аспартатаминотрансфераза, амилаза, общий билирубин, прямой билирубин, глюкоза, железо, С-реактивный белок), электрофорез белков сыворотки крови, общий анализ мочи, коагулограмма, ревмопробы (выполнены в Институте ревматологии): антитела к dsDNA, АНФ-Нер-2, криоглобулины (отрицательные), pANCA, cANCA, общий IgE – 61 МЕ/мл (15–130 МЕ/мл) в пределах референсных значений.
Лечение: Н1-АГ препараты в стандартной дозе, Н2-АГ препараты, ε-аминокапроновая кислота, антибактериальные препараты, иммуноглобулин 15 г в/в, дексаметазон в/в (общая доза 8 мг), монтелукаст 10 мг, метилпреднизолон 12 мг в сутки, тонзиллэктомия.
В результате лечения полный контроль над крапивницей не достигнут. Следующим шагом было назначение циклоспорина А в дозе 175 мг (3,5 мг/кг) в сутки. Высыпания прекратились на следующий день после приема. Регулярно проводился контроль лабораторных показателей: клинический и биохимический анализы крови, общий анализ мочи. В мае 2013 г. циклоспорин А был отменен. Через месяц произошло обострение, в связи с чем прием препарата возобновлен в дозе 150 мг. Отсутствие ремиссии обусловило увеличение дозы до 175 мг. Отмечен положительный эффект.
12 июля 2014 г. пациентка начала применять омализумаб в дозе 300 мг. Активность крапивницы по UAS 7 – 25 баллов. Высыпания исчезли уже на вторые сутки. Через две недели после первого введения циклоспорин А был отменен. После третьей инъекции отмечено кратковременное обострение крапивницы (UAS 7 – 21 балл) – в течение двух дней. Далее – 1–2 балла до пятого введения. Первые два раза омализумаб вводили по 300 мг, затем – по 150 мг. Нежелательных явлений на фоне проводимой терапии не отмечено (рис. 2).
Обсуждение
Предыдущая терапия, рекомендованная согласительным документом по лечению крапивницы, оказалась неэффективной [4]. Результаты исследования свидетельствуют о быстром и эффективном действии омализумаба у большинства пациентов.
Эффективность омализумаба составила 88,3%. При этом полное исчезновение симптомов отмечено в 70,6% случаев, в 17,7% – наблюдалось значительное их уменьшение.
Аналогичные данные получены и в зарубежных исследованиях. M. Metz зафиксировал полный эффект у 83% пациентов, значительное улучшение – у 10% [18]. В работе M. Maurer, проведенной в группе больных крапивницей с IgE-антителами против тиреопероксидазы, полная эффективность достигнута в 70% случаев [19]. В исследовании S. Saini у 76% пациентов с хронической крапивницей, получавших 300 мг омализумаба, состояние улучшилось более чем в 90% случаев [20]. Эффективность омализумаба при физической крапивнице столь же велика. Наше исследование продемонстрировало высокую эффективность омализумаба у больных с физической крапивницей. Это соотносится с данными M. Metz: у 71% пациентов зафиксирован полный ответ на терапию, у 12% – значительный [18].
Необходимо отметить, что принципы подбора дозы при хронической идиопатической крапивнице иные, чем при бронхиальной астме. Так, в первом случае не следует ориентироваться на уровень общего IgE и вес пациента. У больных хронической крапивницей омализумаб одинаково эффективен как при повышенных, так и нормальных значениях указанного показателя. В клинических исследованиях эффективности и безопасности омализумаба у больных хронической крапивницей показана эффективность двух доз препарата – 300 и 150 мг [15]. Для больных крапивницей в инструкции по применению препарата рекомендована доза 300 мг каждые четыре недели. Именно эта доза должна обеспечить максимальный эффект лечения.
Результатом постмаркетинговых исследований, проведенных сотрудниками клиники Шарите, стал протокол дозирования омализумаба для больных хронической крапивницей: первая инъекция 150 мг с последующей оценкой эффекта в течение четырех недель. В случае полного эффекта необходимо продолжать применять препарат в той же дозе каждые четыре недели. Если у пациента нет ответа или он слабый, необходимо повысить дозу до 300 мг и оценить эффект в течение двух недель. Если ответ на лечение не получен, пациент признается не ответившим на терапию. Полный или достаточный эффект служит основанием для уменьшения дозы или увеличения интервала между введениями [18].
При выборе дозы в первую очередь следует ориентироваться на рекомендации, содержащиеся в инструкции по применению препарата, а также учитывать тяжесть течения крапивницы.
В нашем исследовании 11 пациентов получали 300 мг препарата без изменения дозы, одна пациентка начала лечение омализумабом в дозе 150 мг и продолжила лечение той же дозой, четырем пациентам после двух инъекций по 300 мг доза была снижена до 150 мг, только одна пациентка после введения 150 мг омализумаба была переведена на большую дозу из-за недостаточного ответа на терапию.
Важная характеристика эффективности – скорость нивелирования симптомов заболевания. В нашей работе у восьми пациентов отмечен эффект в течение 24 часов. В исследовании M. Metz получены аналогичные результаты: полный контроль симптомов достигался в течение первых 24 часов у 12 из 21 пациента с хронической идиопатической крапивницей [18].
Не менее важен вопрос переносимости и безопасности омализумаба, в частности возможность развития анафилаксии после введения омализумаба (препарата Ксолар). В результате наблюдения 57 300 пациентов (июнь 2003 г. – декабрь 2006 г.) частота развития анафилаксии достигала 0,2% [21]. В опубликованных отчетах по исследованиям эффективности и безопасности омализумаба в лечении хронической крапивницы анафилаксия не отмечена ни у одного пациента.
Тем не менее есть рекомендации наблюдать пациентов после введения омализумаба в течение 2 часов после первых трех инъекций и 30 минут после последующих инъекций [16].
Мы придерживались этих рекомендаций. Все 17 пациентов переносили омализумаб хорошо. Нежелательные явления не зафиксированы.
Заключение
Результаты наблюдения пациентов с хронической идиопатической крапивницей с ангиоотеками и без них, с сопутствующей или самостоятельной физической крапивницей, получавших лечение омализумабом, позволяют рекомендовать препарат больным, рефрактерным к терапии Н1-АГ средствами.
I.V. Danilycheva, O.G. Yеlisyutina, N.I. Ilina, Yе.А. Latysheva, Т.V. Latysheva, Yе.S. Fedenko, А.Yе. Shulzhenko
Institute of Immunology
Contact person: Inna Vladimirovna Danilycheva, ivdanilycheva@mail.ru
Study objective. Study of the efficacy and safety of omalizumab in patients with chronic urticarial, refractory to antihistamines in clinical practice.
Materials and methods. In this retrospective clinical analysis, we assessed effectiveness, time to relief of symptoms, dose change after omalizumab administration, and safety in 17 chronic urticarial patients, 16 with chronic spontaneous urticaria, 1 with different forms of chronic inducible urticaria and 4 with both.
Results. Treatment with omalizumab led to full effect in 70.6% of patients, a significant – in 17.7%, was ineffective in 11.7%. Eight patients marked effect for 24 hours at 2 – within 2 – 3 days, 2 – during 2 weeks, 1 – 4 weeks, at 2 – 8 weeks. Eleven patients were receiving 300 mg of the entire period of observation, one patient - 150 mg, 4 patients 2 injections of 300 mg, followed by 150 mg of 2, one patient had started treatment with a dose of 150 mg, continued treatment with omalizumab 300 mg. Omalizumab was safe. Efficacy was not correlated to baseline IgE levels and the test results with autosyvorotkoy not affect the effectiveness of treatment with omalizumab.
Conclusion. Our observation of patients with chronic spontaneous urticaria, with the concomitant or separate physical hives treated with omalizumab can recommend widespread use of the drug in patients, torpid to the therapy of first and second-line treatment of urticaria.
