количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Опыт применения препарата Витапрост® Форте у пациентов с доброкачественной гиперплазией предстательной железы
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Урология и Нефрология" №1
- Аннотация
- Статья
- Ссылки
В статье приведены результаты российских исследований по изучению эффективности и безопасности препарата Витапрост® Форте суппозитории ректальные 100 мг у больных с доброкачественной гиперплазией предстательной железы (ДГПЖ). Было показано, что препарат снижает клинические проявления заболевания, способствует значительному улучшению показателей урофлоуметрии и уменьшению объема предстательной железы.
В связи с этим Витапрост® Форте рекомендуется к применению в монотерапии ДГПЖ у пациентов с умеренно выраженной инфравезикальной обструкцией вне зависимости от возраста и наличия сопутствующих заболеваний.
В статье приведены результаты российских исследований по изучению эффективности и безопасности препарата Витапрост® Форте суппозитории ректальные 100 мг у больных с доброкачественной гиперплазией предстательной железы (ДГПЖ). Было показано, что препарат снижает клинические проявления заболевания, способствует значительному улучшению показателей урофлоуметрии и уменьшению объема предстательной железы.
В связи с этим Витапрост® Форте рекомендуется к применению в монотерапии ДГПЖ у пациентов с умеренно выраженной инфравезикальной обструкцией вне зависимости от возраста и наличия сопутствующих заболеваний.
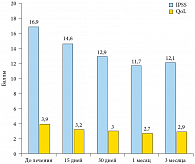
Рис. 1. Динамика показателей IPSS и Qol анкетирования пациентов, получающих препарат Витапрост® Форте
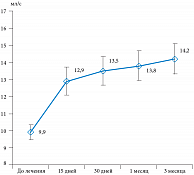
Рис. 2. Динамика показателей объемной скорости мочеиспускания после приема препарата Витапрост® Форте

Таблица 1. Динамика значений объема простаты по данным ТРУЗИ

Таблица 2. Результаты лечения препаратом Витапрост® Форте больных ДГПЖ
Доброкачественная гиперплазия предстательной железы – наиболее распространенное урологическое заболевание пожилых мужчин [1, 2]. Для ДГПЖ характерны жалобы на затрудненное, учащенное мочеиспускание, чувство неполного опорожнения мочевого пузыря, вынужденное ночное мочеиспускание и другие симптомы, которые значительно снижают качество жизни больных. По мнению ряда авторов, клинические проявления ДГПЖ имеют место у 34% мужчин в возрасте 40–50 лет, у 67% мужчин в возрасте 51–60 лет, у 77% мужчин в возрасте 61–70 лет и у 83% мужчин в возрасте старше 70 [3]. Гиперплазия простаты развивается у всех мужчин, при этом 25% из них в дальнейшем потребуется медикаментозное или хирургическое лечение. J. Isaacs и D. Coffey (1989) на основании аутопсийных исследований заключают, что при профилактическом обследовании мужчин старше 50 лет ДГПЖ обнаруживается в 10–15% случаев, однако клинические проявления болезни наблюдаются далеко не у всех [2]. У 80–85% мужчин 60 лет и старше имеет место в той или иной степени увеличение предстательной железы [4]. Учитывая, что население Земли стареет, лечение пациентов с ДГПЖ является важной задачей современной урологии.
В настоящее время выбор терапии при ДГПЖ чаще делается в пользу фармакотерапии, чем хирургического вмешательства. Между тем механизм действия некоторых препаратов изучен недостаточно, у многих отсутствуют четкие показания к применению. Основными группами лекарственных средств, которые применяются при ДГПЖ, являются гормональные препараты (аналоги гонадотропных рилизинг-гормонов, антиандрогены, гестагены, антиэстрогены, ингибиторы ароматазы, антагонисты пролактина); ингибиторы 5-альфа-редуктазы; альфа-адреноблокаторы; прочие (полиеновые антибиотики, аминокислотные комплексы и экстракты органов животных) [5, 6]. Используются также разнообразные лекарственные препараты растительного и животного происхождения. Один из них – Витапрост® Форте, активным веществом которого является эндогенная субстанция Сампрост (экстракт простаты) – комплекс водорастворимых биологически активных пептидов, выделенных из предстательной железы ткани простаты быков и бычков, достигших половой зрелости, путем жесткого кислотного гидролиза, глубоко разрушающего клеточные структуры. Особенности выделения этих пептидов нивелируют их молекулярную видоспецифичность, в результате чего полученные препараты лишаются антигенных свойств и ассоциированных с ними побочных эффектов [3].
Экстракт простаты оказывает органотропное действие на предстательную железу [7]. Как все пептидные биорегуляторы, он обладает антиагрегантными и антикоагулянтными свойствами, усиливает синтез антигистаминовых и антисеротониновых антител, улучшает микроциркуляцию в пораженном органе, что способствует уменьшению отека и активности воспалительных процессов при заболеваниях предстательной железы. Существенным является также наличие у экстракта простаты иммуномодулирующих свойств [8]. Компанией ОАО «Нижфарм» разработана новая форма препарата – Витапрост® Форте суппозитории ректальные 100 мг, что позволяет врачу и пациенту варьировать режим дозирования препарата, осуществляя патогенетическую терапию заболеваний предстательной железы и функционально связанных с ней органов. Витапрост® Форте суппозитории ректальные 100 мг показан при различных заболеваниях и патологических состояниях мужской урогенитальной сферы, в том числе и при гиперплазии предстательной железы.
В России за последние годы накоплен большой опыт применения препарата Витапрост® Форте при лечении ДГПЖ. Препарат применялся во многих клиниках нашей страны. В частности, эффективность препарата при лечении ДГПЖ была доказана в ГБУЗ здравоохранения «Городской гериатрический медико-социальный центр» (Санкт-Петербург) [9], где было проведено лечение препаратом Витапрост® Форте 40 пациентов c ДГПЖ в возрасте от 55 до 77 лет (средний возраст 67,6 ± 0,9 лет). Для оценки эффективности и безопасности применения лекарственного препарата Витапрост® Форте у пациентов с ДГПЖ использовались следующие критерии:
- динамика симптомов ДГПЖ по Международной шкале суммарной оценки простатических симптомов (IPSS/QоL) на фоне терапии препаратом Витапрост® Форте;
- определение степени выраженности инфравезикальной обструкции, обусловленной ДГПЖ, по данным УЗИ, урофлоуметрии, определения объема остаточной мочи в результате лечения препаратом Витапрост® Форте;
-
анализ динамики самооценки пациентами в процессе лечения степени беспокойства и дискомфорта из-за расстройств мочеиспускания с помощью опросника ICIQ-MLUTS (пациент оценивает не только выраженность симптомов нарушения мочеиспускания, но и степень причиняемого каждым симптомом беспокойства по 10-балльной шкале),визуальной аналоговой шкалы степени дискомфорта из-за симптомов (UB-VAS) и визуальной аналоговой шкалы оценки лечения (TS-VAS);
- оценка безопасности и переносимости препарата Витапрост® Форте для пациентов, страдающих ДГПЖ.
До получения препарата пациенты были дважды обследованы с интервалом в 5–10 дней. Пациенты заполняли несколько опросников, в которых оценивали качество мочеиспускания и качество жизни. Больным были выполнены УЗИ мочевого пузыря и предстательной железы, определен объем остаточной мочи после урофлоуметрии. Данные первых двух обследований при анализе были усреднены и признаны исходными. Все пациенты применяли суппозитории Витапрост® Форте 1 раз в сутки на ночь в течение 30 дней. Проводилась оценка мочеиспускания до лечения, через 15 и 30 дней применения суппозиториев, а также через 1 и 3 месяца после курса лечения. По итогам исследования были получены следующие результаты. В процессе лечения суммарный балл IPSS снизился с 16,9 до 14,6 через 15 дней и до 12,9 через 30 дней, в итоге на 23,7% (рис. 1). Через месяц после лечения балл IPSS еще уменьшился до 11,7 (на 30,8% от исходного), немного увеличившись через 3 месяца – до 12,1. Индекс оценки качества жизни (QоL) соответственно улучшился с 3,9 до 3,3 и в итоге лечения – до 3 (на 23,1%). Через месяц – также улучшение до 2,7 (на 30,8%), через 3 месяца – до 2,9. Оценка пациентом степени дискомфорта из-за симптомов нарушения мочеиспускания (UB-VAS) уменьшилась в процессе лечения с 54,3% до 44,3% и 41,5% через месяц (в 1,3 раза).
Через месяц после лечения достигнутое улучшение сохранялось (40,3%), а через 3 месяца дискомфорт вырос до 45,2%. Интересен анализ данных, полученных с помощью опросника ICIQ-MLUTS по симптомам нарушения мочеиспускания и связанному с ними беспокойству. Суммарный балл опросника в процессе лечения сократился с 15,8 до 14,0 и 13,2 балла, в итоге на 16,5%. Достигнутое улучшение сохранялось через месяц после лечения (13,1) и достигло 12,9 через 3 месяца. Суммарный балл степени беспокойства из-за симптомов нарушения мочеиспускания уменьшился с 39 до 32,3 и 28,5 балла, в итоге на 27,2%. Через месяц после лечения степень беспокойства – 29,3 балла, а через 3 месяца – 28,6 балла, практически сохраняясь на уровне, достигнутом в результате лечения. Таким образом, по самооценке пациентов, уменьшение беспокойства из-за симптомов нарушения мочеиспускания практически в 1,5 раза опережает саму положительную динамику этих симптомов. При этом суммарный балл опросника ICIQ-MLUTS по обструктивным симптомам нарушения мочеиспускания снизился в процессе лечения с 8,6 до 7,4 и 7,1 балла, в итоге на 17,4%, достигнутое улучшение сохранялось через 1 и 3 месяца (7,2 и 7,0 балла). Беспокойство из-за обструктивных симптомов уменьшилось в процессе лечения с 19,7 до 15,7 и 13,9 балла, в итоге на 29,4%, также почти сохраняя достигнутое улучшение через 1 и 3 месяца (14,5 и 14,7 балла).
Суммарный балл опросника ICIQ-MLUTS по ирритативным симптомам нарушения мочеиспускания снизился в процессе лечения с 7,2 до 6,6 и 6,1 балла, в итоге на 15,3%, также сохраняя достигнутое улучшение через 1 и 3 месяца (5,9 балла). Беспокойство из-за ирритативных симптомов уменьшилось в процессе лечения с 19,3 до 16,6 и 14,5 баллов, в итоге на 24,9%, сохраняя достигнутое улучшение через 1 и 3 месяца (14,8 и 14,0 балла). Таким образом, положительная динамика обструктивных и ирритативных симптомов развивалась практически параллельно, а уменьшение беспокойства значительно опережало улучшение симптоматики, что очень важно для повышения качества жизни пациентов с ДГПЖ. Это заключение подтверждали данные опросника TS-VAS, по которым оценка лечения пациентами составила через 15 дней 58%, в конце курса лечения – 64,2%, а через 1 месяц еще выросла до 69,7%, немного уменьшившись (до 64,1%)через 3 месяца.
Очень важная положительная динамика наблюдалась по объективным параметрам мочеиспускания (рис. 2). При анализе данных урофлоуметрии использовался показатель максимальной объемной скорости мочеиспускания (Qmax) потока мочи (при объеме мочеиспускания более 150 мл) как единственный достоверно суммарно отражающий изменения функционального состояния детрузора (тонус, сократительная активность) и проходимость (резистентность) мочеиспускательного канала [8]. Показатель Qmax вырос с 9,9 до 12,8 мл/с через 15 дней и 13,5 мл/с в конце лечения (на 36,4%). Через месяц скорость еще увеличилась до 13,8 мл/с, а через 3 месяца – до 14,2 мл/с (на 43,4% от исходной). Все изменения статистически достоверны. При этом объем остаточной мочи сократился практически в три раза, с 37,7 до 13,4 мл и 10,1 мл через 30 дней приема препарата, что сохранялось и через 3 месяца. Такая стойкая положительная динамика свидетельствовала не только о снижении инфравезикальной обструкции, но и в значительной степени о стимулирующем влиянии на мышечный тонус мочевого пузыря Витапрост® Форте, терапевтическое действие которого продолжается после прекращения курса лечения. По данным УЗИ средний объем предстательной железы составил 48,62 ± 6,54 см3 (от 34,6 до 87,8 см3). В процессе лечения и дальнейшего наблюдения достоверной динамики объема простаты выявлено не было.
За время наблюдения у пациентов, применявших Витапрост® Форте, отмечалось только одно нежелательное явление легкой степени тяжести, связанное с терапией данным препаратом, – аллергическая реакция, быстро прекратившаяся после отмены препарата. Отсутствие у других пациентов какой-либо отрицательной динамики свидетельствовало о хорошей переносимости и безопасности Витапрост® Форте. Изучение эффективности и безопасности препарата Витапрост® Форте суппозитории ректальные 100 мг у пациентов с ДГПЖ также было проведено на кафедре урологии и нефрологии ГБОУ ВПО АГМУ Минздравсоцразвития России (Барнаул) [10]. Целями данного исследования были:
- оценка динамики симптомов ДГПЖ по шкалам IPSS и QоL на фоне терапии препаратом Витапрост® Форте суппозитории ректальные 100 мг;
- определение степени выраженности инфравезикальной обструкции, обусловленной ДГПЖ, по данным трансректального УЗИ, урофлоуметрии, определения объема остаточной мочи на фоне терапии препаратом Витапрост® Форте суппозитории ректальные 100 мг.
В исследование были включены 15 пациентов (мужчины с диагнозом ДГПЖ, находящиеся на амбулаторном лечении и наблюдении, с умеренно выраженной инфравезикальной обструкцией (Qmax 5,0–15,0 мл/с)). Пациенты получали препарат Витапрост® Форте суппозитории ректальные 100 мг по 1 суппозиторию 1 раз в сутки. Длительность лечения составляла 30 дней. В качестве параметров эффективности терапии препаратом Витапрост® Форте были выбраны оценка терапевтического эффекта, оценка степени выраженности симптомов ДГПЖ. Для оценки терапевтического эффекта были использованы данные, полученные в результате пальцевого ректального исследования, трансректального УЗИ простаты, урофлоуметрии, а также определения объема остаточной мочи. Оценка степени выраженности симптомов ДГПЖ проводилась на основании регистрации обструктивной и ирритативной симптоматики с использованием шкал IPSS и QоL.
Негативные изменения в общем состоянии пациента, возникновение новых жалоб, патологические отклонения лабораторных показателей (клинического исследования крови и клинического исследования мочи) в ходе исследования фиксировались как нежелательные явления. Выявлялась взаимосвязь между нежелательными явлениями и терапией препаратом Витапрост® Форте, определялась степень тяжести нежелательных явлений (слабая, умеренная, тяжелая), их продолжительность и серьезность. Данные трансректального УЗИ простаты являлись одним из параметров эффективности, используемых для оценки терапевтического эффекта терапии и степени выраженности воспалительного процесса в предстательной железе. На фоне приема препарата Витапрост® Форте было достигнуто незначительное, но статистически достоверное снижение среднего значения объема предстательной железы (табл. 1).
Оценивались показатели урофлоуметрии и величины объема остаточной мочи, характеризующие степень нарушения мочеиспускания на фоне развития ДГПЖ и функциональное состояние детрузора. У пациентов, получавших препарат Витапрост® Форте, достигнуто увеличение среднего значения Qmax с 9,94 мл/с на визите 0 до 12,81 мл/с к визиту 2 и 13,09 мл/с на визите 4. Эти изменения были статистически достоверны. При этом максимальные значения этого параметра среди пациентов, принимавших Витапрост® Форте, возросли до 16,8 и 17,1 мл/с на визитах 2 и 4 соответственно, достигнув нормальных значений. Зафиксировано статистически достоверное выраженное снижение среднего значения объема остаточной мочи от визита 0 к визиту 2 с 27,07 до 10,67 мл и далее к визиту 4 до 10,43 мл.
У пациентов, получавших Витапрост® Форте, от нулевого к 4-му визиту достоверно снижалось среднее значение объема остаточной мочи, несмотря на прекращение приема препарата на 2-м визите, что может свидетельствовать о том, что терапевтическое действие препарата Витапрост® Форте продолжается после курса лечения еще некоторое время. Одним из параметров эффективности терапии, используемых при статистическом анализе данных исследования для оценки степени выраженности обструктивной и ирритативной симптоматики ДГПЖ, являлась сумма баллов по шкале IPSS. При анализе результатов исследования отдельно оценивалось количество пациентов с незначительной (сумма баллов 0–7), умеренной (сумма баллов 8–19) и выраженной (сумма баллов 20–35) симптоматикой ДГПЖ. Количество пациентов с незначительными симптомами последовательно увеличивалось от визита 0 к визиту 4 с 2 до 3, в то время как число пациентов с выраженными симптомами снижалось с 3 до 0.
Это связано с тем, что препарат влияет на субъективную симптоматику и достоверно уменьшает симптоматику исходного заболевания, в результате чего количество пациентов с незначительными симптомами последовательно увеличилось от визита 0 к визиту 4 с 2 до 3. Дополнительным подтверждением субъективных параметров мочеиспускания является оценка суммарного балла по шкале IPSS. Среднее значение суммарного показателя по шкале IPSS снизилось с 15,67 на визите 0 до 12,4 и 11,13 баллов на визитах 2 и 4. Таким образом, у пациентов прослеживается достоверное снижение суммарного балла по шкале IPSS от нулевого к 4-му визиту. В оценке степени выраженности симптомов ДГПЖ немаловажную роль играет и оценка пациентом качества жизни (QоL). Количество пациентов со сглаженностью срединной бороздки, свидетельствующей о развитии узлов гиперплазии и/или отеке тканей простаты, уменьшилось на фоне приема препарата Витапрост® Форте с 3 (20%) перед проведением терапии до 2 (13,3%) после окончания исследования.
В урологической ГОУ ВПО «СПбГМУ им. акад. И.П. Павлова» [11] было проведено исследование по изучению эффективности препарата Витапрост® Форте суппозитории ректальные. Под наблюдением находились 30 больных ДГПЖ, которые получали Витапрост® Форте в виде ректальных суппозиториев в дозе 100 мг 1 раз в сутки непрерывно в течение 60 дней. Средний возраст пациентов составил 63,5 ± 2,4 года. В результате проведенного исследования все 30 пациентов с ДГПЖ, получавших Витапрост® Форте в течение 60 дней, к моменту завершения лечения отметили положительный эффект. При этом выраженный положительный эффект отметили 8 (26,7%), хороший эффект – 12 (40%), а удовлетворительный – 10 (33,3%) пациентов. К моменту окончания приема препарата все показатели клинического течения заболевания улучшились. Так, средний балл по шкале IPSS через 30 дней лечения снизился с 13,9 ± 2,1 до 11,8 ± 2,3 балла, то есть на 2,1 балла (p < 0,05), а к 60-му дню лечения – до 9,7 ± 1,9 балла, то есть на 4,2 балла (p < 0,01). Через 60 дней после завершения лечения отмечен такой же (9,8 ± 1,7) уровень балла симптоматики, как и к моменту окончания лечения. У больных ДГПЖ, получающих Витапрост® Форте суппозитории ректальные, выявлено статистически достоверное улучшение качества жизни. Qmax через 30 дней лечения препаратом Витапрост® Форте возросла с 9,3 ± 0,9 до 10,5 ± 0,6 мл/с (p < 0,05), а через 60 дней терапии – до 12,9 ± 0,4 мл/с (то есть на 3,6 мл/с), p < 0,01. Этот показатель клинического течения заболевания еще более существенно улучшился спустя 60 дней после лечения Витапрост® Форте, составив 14,0 ± 0,7 мл/с (p < 0,001).
У больных ДГПЖ, получающих Витапрост® Форте, отмечено снижение количества остаточной мочи. Если до лечения среднее значение объема остаточной мочи составило 65,5 ± 12,9 мл, то через 30 дней лечения – 42,4 ± 10,5 мл, через 60 дней лечения – 33,8 ± 9,1 мл, а через 2 месяца после прекращения приема препарата – 25,6 ± 7,5 мл. Разница статистически достоверна (p < 0,001). Положительные изменения в клиническом течении заболевания сохранялись в течение 2 месяцев после приема препарата, что подтверждает высокую оценку эффективности Витапрост® Форте у больных ДГПЖ (табл. 2). В 2008 г. на кафедре урологии ГБОУ ВПО УГМА Минздравсоцразвития России (Екатеринбург) было проведено исследование [12] по изучению эффективности применения препарата Витапрост® Форте у больных ДГПЖ. Исследование включало 35 больных с ДГПЖ, получавших препарат Витапрост® Форте суппозитории ректальные 100 мг по 1 суппозиторию 1 раз в сутки в течение 30 дней. Результаты исследования препарата показали его общий положительный эффект, заключающийся в умеренном уменьшении объема предстательной железы, что может быть объяснено органотропным действием, которое обусловливает снижение пролиферативной активности клеток предстательной железы. Было отмечено также усиление синтеза антигистаминных и антисеротониновых антител, что в конечном итоге приводит к уменьшению отека, снижению активности воспалительного процесса и уменьшению объема предстательной железы.
Уменьшение объема предстательной железы отразилось и на уменьшении инфравезикальной обструкции, что подтверждали данные исследования: уменьшился объем остаточной мочи, увеличилась максимальная и средняя объемная скорость мочеиспускания, эффект сохранился к 4-му визиту (30 дней после окончания приема препарата). Уменьшение ирритативной и обструктивной симптоматики также свидетельствовало о стабилизации процессов и после отмены препарата. Нежелательных явлений средней и тяжелой степени выявлено не было. В ГОУ ДПО «Институт повышения квалификации специалистов здравоохранения» (Хабаровск) на базе урологического отделения Краевой клинической больницы № 1 также исследовалась эффективность препарата Витапрост® Форте суппозитории ректальные [13]. Под наблюдением находились 30 больных с ДГПЖ, которые получали Витапрост® Форте в виде ректальных суппозиториев в дозе 100 мг 1 раз в сутки непрерывно в течение 30 дней, двумя курсами с интервалом в 30 дней.
В результате проведенного лечения 29 пациентов с ДГПЖ, получающих Витапрост® Форте в течение двух курсов по 30 дней, к моменту завершения лечения отметили положительный эффект, один пациент отметил неудовлетворительный эффект от применения препарата. При этом выраженный положительный эффект отметили 9 (30%) пациентов, хороший эффект – 13 (43,4%) больных, удовлетворительный – 7 (23,3%) больных, неудовлетворительный – 1 (3,3%) пациент. Так, средний балл симптоматики заболевания по шкале IPSS через 30 дней от начала лечения снизился с 15,9 ± 2,11 до 15,23 ± 1,55 балла, то есть на 0,7 балла (p < 0,05), а к 60-му дню от начала лечения – до 14,33 ± 1,83 балла, то есть на 1,6 балла (p < 0,01). Через 120 дней после начала лечения отмечено продолжающееся снижение показателей до 13,6 ± 1,94, то есть на 2,3 (p < 0,01). У больных ДГПЖ, получающих Витапрост® Форте суппозитории ректальные, выявлено статистически достоверное улучшение качества жизни. Среднее значение показателя качества жизни к 30-му дню лечения снизилось с 3,97 ± 0,96 до 3,93 ± 0,94 баллов (p < 0,05), а к 60-му дню от начала терапии – до 3,57 ± 1,14 баллов (p < 0,05). Показатель качества жизни к 120-му дню от начала лечения составил 2,93 ± 0,87 балла (p < 0,001). Qmax через 30 дней лечения препаратом Витапрост® Форте суппозитории ректальные 100 мг возросла с 11,45 ± 2,92 до 12,64 ± 2,61 мл/с (p < 0,05), а через 60 дней от начала проведения терапии – до 14,00 ± 2,64 мл/с, т.е. на 1,2 мл/с (p < 0,001). Этот показатель клинического течения заболевания еще более существенно улучшился спустя 120 дней после лечения Витапрост® Форте, составив 15,08 ± 3,37 мл/с (p < 0,001).
У больных ДГПЖ, получающих Витапрост® Форте, отмечено снижение количества остаточной мочи. Если до лечения среднее значение объема остаточной мочи составляло 41,17 ± 18,6 мл, то через 30 дней от начала лечения – 28,5 ± 12,6 мл, через 60 дней от начала лечения – 23,17 ± 12,7 мл, а через 120 дней от начала лечения – 18,67 ± 10,74 мл, разница статистически достоверна (p < 0,001). На фоне приема Витапрост® Форте статистически достоверно объем предстательной железы у больных ДГПЖ снизился лишь через 60 дней от начала лечения – с 41,17 ± 7,85 до 37,73 ± 7,46 см³ (p < 0,05) и практически оставался на этом же уровне и в течение 120 дней после прекращения лечения, составив 37,06 ± 7,75 (p < 0,05). У двоих пациентов из 30 наблюдаемых нами больных с ДГПЖ в процессе лечения Витапрост® Форте отмечены незначительные нежелательные явления в виде мацерации кожных покровов анальной области, которые были легко устранимы путем применения гигиенических процедур, что свидетельствует о хорошей переносимости и безопасности препарата. Эффективность препарата Витапрост® Форте суппозитории ректальные изучалась на кафедре урологии ГОУ ВПО «Казанский ГМУ» Росздрава [14] у пациентов с ДГПЖ. Пациенты (30 человек) получали препарат Витапрост® Форте суппозитории ректальные 100 мг по 1 суппозиторию 1 раз в сутки в течение 60 дней. Затем наблюдались в течение 30 дней, контрольный визит – еще через 30 дней.
Проведенное исследование эффективности и переносимости препарата Витапрост® Форте суппозитории ректальные 100 мг у пациентов с ДГПЖ в качестве монотерапии подтвердило его эффективность в медикаментозной терапии у больных с умеренно выраженной симптоматикой. В ходе исследования улучшились показания уродинамики нижних мочевых путей, выражающиеся при объективном уродинамическом обследовании в увеличении средней скорости мочеиспускания и уменьшении объема остаточной мочи. У пациентов, принимавших Витапрост® Форте суппозитории ректальные 100 мг (n = 30), не отмечено ни одного нежелательного явления, связанного с его приемом. Легкий дискомфорт в прямой кишке в начале применения наблюдается у всех пациентов при использовании ректальной формы медицинских препаратов. Кроме того, о хорошей переносимости и безопасности препарата свидетельствует отсутствие изменений параметров диагностического комплекса во время проведения исследования, а также изменений со стороны других органов и систем.
В ФГБУ «НИИ урологии» Минздравсоцразвития России (Москва) в 2006 г. [15] было проведено сравнительное рандомизированное плацебоконтролируемое клиническое исследование эффективности и безопасности препарата Витапрост® Форте суппозитории ректальные 100 мг производства ОАО «Нижфарм» (Россия) у пациентов с ДГПЖ. В исследование было включено 120 пациентов. Все пациенты, соответствовавшие критериям включения и принявшие участие в исследовании, были рандомизированы на три группы по 40 человек в каждой:
-
пациенты основной группы получали препарат Витапрост® Форте суппозитории ректальные 100 мг по 1 суппозиторию1 раз в сутки;
- пациенты первой контрольной группы – препарат тамсулозин (Омник) из группы альфа-адреноблокаторов по 1 таблетке 1 раз в сутки;
- пациенты второй контрольной группы – плацебо по 1 суппозиторию 1 раз в сутки.
Длительность лечения во всех трех группах составляла 30 дней. Исследование включало 5 визитов, в ходе которых проводились сбор анамнеза и физикальный осмотр пациента, регистрация симптоматики ДГПЖ с использованием шкал IPSS и QоL, пальцевое ректальное и трансректальное ультразвуковое исследование с допплерографией сосудов предстательной железы, клинические и биохимические лабораторные исследования крови и мочи, анализ на простатспецифический антиген, определение объема остаточной мочи, урофлоуметрия.
В ходе проводимого исследования и пациенты, и врачи отмечали высокую эффективность терапии препаратом Витапрост® Форте, а также Омником по сравнению с плацебо. За период лечения от 2-го к 3-му визиту констатирована положительная динамика в оценке эффективности как в основной группе, так и в группе пациентов, получавших Омник. При этом в основной группе на 2-м визите у подавляющего большинства пациентов эффект расценен как удовлетворительный (87,5% – 35 пациентов), однако к 3-му визиту преобладают пациенты с хорошим эффектом (47,5% – 19 пациентов). После прекращения терапии к 4-му визиту в группе Витапрост® Форте отмечено такое же количество пациентов с выраженным эффектом, как и на 3-м визите (1 пациент), количество пациентов с хорошим эффектом увеличилось с 3-го визита к 4-му с 12 до 14. Это подтверждает, что терапевтическое действие препарата Витапрост® Форте продолжается после курса лечения.
После прекращения терапии к 4-му визиту в группе Омника отмечается увеличение числа пациентов с неудовлетворительным эффектом – на 3-м визите это был 1 пациент, а к 4-му визиту их стало 18, что указывает на прекращение действия препарата Омник сразу после завершения терапии. В группе плацебо, по мнению пациентов, неудовлетворительный эффект зафиксирован в 90% (36 пациентов) случаев, удовлетворительный – в 10% (4 пациента). Хорошего, а также выраженного эффекта не выявлено ни в одном из случаев. По оценке врача, ко времени 4-го визита у пациентов основной группы удовлетворительный, выраженный, а также хороший эффекты распределились практически в равных долевых пропорциях: удовлетворительный – 35% (14 пациентов), хороший – 30% (12 пациентов), выраженный – 32,5% (13 пациентов) при 1 неудовлетворительном результате. После прекращения терапии к 4-му визиту в группе Витапрост® Форте отмечается увеличение числа пациентов с выраженным эффектом – на 3-м визите их было 10, а к 4-му визиту стало 13, что также свидетельствует о терапевтическом последействии исследуемого препарата.
В группе Омника частота встречаемости эффектов от проведенного лечения иная: удовлетворительный и неудовлетворительный эффекты преобладают – 17 и 16 пациентов соответственно (42,5 и 40%). Хороший эффект отмечен в 12,5% (5 пациентов) случаев, выраженный эффект был у 2 (5%) пациентов. В группе плацебо неудовлетворительный эффект отмечен в 85% (34 пациента) случаев, удовлетворительный – в 10% (4 пациента), хороший и выраженный эффекты – по 1 наблюдению (по 2,5%). Таким образом, через 15 дней после окончания лечения в группе Омника наблюдается тенденция к снижению эффективности проведенной терапии на фоне завершения использования препарата по сравнению с плацебо, низкая эффективность которого была заведомо ожидаемой и подтверждена документально в данном исследовании. Выраженное и резкое снижение оценки эффективности лечения после прекращения приема препарата в группе Омника объяснимо с позиции рассмотрения принципов проведения симптоматического лечения, механизма действия и периода полувыведения препарата. Применение препарата Витапрост® Форте суппозитории ректальные в качестве монотерапии ДГПЖ вызывает умеренное статистически достоверное уменьшение объема предстательной железы. Положительный эффект может быть объяснен специфическим прямым и непрямым органотропным действием основного действующего вещества препарата (экстракта простаты) на простату, что приводит к снижению пролиферативной активности клеток предстательной железы и торможению развития ДГПЖ, усилению синтеза антигистаминовых и антисеротониновых антител, что в конечном счете способствует уменьшению отека органа и снижению активности сопутствующих воспалительных процессов. Немалую роль играет и способность экстракта простаты уменьшать отек и активность воспалительных процессов в органе за счет улучшения в нем микроциркуляции. С антиагрегантными и антикоагулянтными свойствами экстракта простаты связано и умеренное улучшение кровообращения в органе, проявившееся статистически достоверным увеличением максимальной линейной скорости кровотока после первых 15 дней терапии.
Выводы
Анализ результатов исследований и объективные данные, подтвержденные стандартными методами исследования, принятыми к использованию в международной практике (IPSS, QoL), однозначно свидетельствуют о положительной динамике обструктивных и ирритативных симптомов у пациентов в период приема препарата Витапрост® Форте суппозитории ректальные 100 мг и после окончания лечения. Продолжение терапевтического эффекта после двухмесячного приема препарата пациентами с ДГПЖ свидетельствует о патогенетически направленном действии препарата, обусловленном органотропными свойствами. Данный положительный эффект может быть объяснен специфическим органотропным действием основного вещества препарата на предстательную железу, способствующим уменьшению отека органа и снижению активности сопутствующих воспалительных процессов. Такой патогенетический механизм действия Витапрост® Форте подтверждает и наблюдаемая положительная динамика, продолжающаяся в течение нескольких месяцев по окончании курса лечения.
Увеличение Qmax на 36,4% в конце двухмесячного курса лечения и еще на 7% через три месяца параллельно с уменьшением более чем в 3 раза объема остаточной мочи свидетельствуют о значительном снижении инфравезикальной обструкции в результате действия Витапрост® Форте. Его антиагрегантные и антикоагулянтные свойства способствуют улучшению кровообращения в предстательной железе и мочевом пузыре. Именно снижением ишемии детрузора, играющей значительную роль в патогенезе ДГПЖ, можно объяснить такое выраженное повышение мышечного тонуса мочевого пузыря, которое продолжается и после окончания приема препарата. Следует также учитывать полученные экспериментальные данные об увеличении почти в 2 раза максимального напряжения, развиваемого мышцей детрузора крыс, при добавлении экстракта простаты в перфузат. Результаты анкетирования пациентов по нескольким опросникам показывают, что применение Витапрост® Форте практически одинаково улучшает обструктивную и ирритативную симптоматику. При этом уменьшение беспокойства из-за симптомов нарушения мочеиспускания и изменение по шкале QoL в 1,5 раза больше, чем само улучшение симптоматики, что говорит о значительном повышении качества жизни пациентов в результате лечения.
В исследованиях за время наблюдения у пациентов, применявших Витапрост® Форте суппозитории ректальные, нежелательных явлений зафиксировано не было. Отсутствие статистически достоверных отрицательных изменений клинических и биохимических параметров крови и мочи у пациентов за время наблюдения также свидетельствует о хорошей переносимости и безопасности препарата. Статистически достоверное подтверждение уменьшения объема предстательной железы в процессе проводимой терапии в ходе исследований подтвердило наличие антипролиферативной активности эндогенного субстрата Сампрост (экстракт простаты) по отношению к клеткам предстательной железы и аденоматозной ткани. Вторичный эффект, связанный со снижением и устранением конгестивных изменений в простате, связан со способностью препарата улучшать микроциркуляцию и активизировать внутритканевые антигистаминные процессы за счет выработки специфических антител. Полученные данные убедительно показывают, что применение препарата Витапрост® Форте в суточной дозе 100 мг в течение 30 дней у пациентов с ДГПЖ улучшает параметры мочеиспускания, снижает обструктивную и ирритативную симптоматику, значительно повышает качество жизни. Патогенетический механизм действия препарата на ДГПЖ обусловливает сохранение и развитие терапевтического эффекта через 3 месяца по окончании курса лечения. Терапия препаратом Витапрост® Форте хорошо переносится, благоприятно воспринимается пациентами и может быть рекомендована при неосложненных формах ДГПЖ вне зависимости от сопутствующих заболеваний для периодического курсового лечения.
На основании проведенных исследований применения препарата (в результате которых была изучена эффективность и безопасность препарата Витапрост® Форте суппозитории ректальные 100 мг у больных с ДГПЖ) было доказано, что препарат снижает клинические проявления заболевания, улучшает качество жизни больных, способствует значительному улучшению показателей урофлоуметрии и уменьшает объем предстательной железы. Витапрост® Форте более эффективен у больных с ДГПЖ в сочетании с хроническим простатитом. Препарат обладает антиагрегантными и антикоагулянтными свойствами, усиливает синтез антигистаминовых и антисеротониновых антител, улучшает микроциркуляцию в пораженном органе, что приводит к уменьшению отека и активности воспалительных процессов при заболеваниях предстательной железы. Все вышеизложенное позволяет рекомендовать препарат Витапрост® Форте суппозитории ректальные к применению в монотерапии ДГПЖ у пациентов с умеренно выраженной инфравезикальной обструкцией вне зависимости от возраста и наличия сопутствующих заболеваний.
1. Barry M.J. Epidemiology and natural history of benign prostatic hyperplasia // Urol. Clin. North Am. 1990. Vol. 17. № 3. P. 495–507.
2. Доброкачественная гиперплазия предстательной железы / под ред. Н.А. Лопаткина. 2-e изд. М.: Медицина, 1999. 216 с.
3. Schroder F., Altwein I. Development of benign prostatic hyperplasia // Benign prostatic hyperplasia. A diagnosis and treatment primer. Oxford, 1992. P. 31–50.
4. Шабад А.Л. Учебное пособие по урологии с уходом за больными. М.: Медицина, 1980. 240 с.
5. Ткачук В.Н., Аль-Шукри С.Х., Лукьянов А.Э. Медикаментозное лечение больных доброкачественной гиперплазией предстательной железы. СПб., 2000. 104 c.
6. Souverein P.C., Erkens J.A., de la Rosette J.J. et al. Drug treatment of benign prostatic hyperplasia and hospital admission for BPH-related surgery // Eur. Urol. 2003. Vol. 43. № 5. P. 528–534.
7. Ткачук В.Н., Горбачев А.Г., Хавинсон В.Х. Применение простатилена при лечении больных хроническим простатитом // Урол. и нефрол. 1991. № 6. С. 40–43.
8. Аль-Шукри С.Х., Горбачев А.Г., Кузьмин И.В., Хавинсон В.Х. Введение в биорегулирующую терапию при урологических болезнях. СПб.: Наука, 1996. 93 с.
9. Гомберг В.Г., Надь Ю.Т. Эффективность применения препарата Витапрост® Форте при доброкачественной гиперплазии предстательной железы // Урология. 2010. № 5. С. 35–39
10. Неймарк А.И., Ноздрачев Н.А. Отчет изучения эффективности применения препарата Витапрост® Форте суппозитории ректальные 100 мг производства ОАО «Нижфарм» у пациентов с добро- качественной гиперплазией предстательной железы // URL: http:// medi.ru/doc/g2401304.htm.
11. Ткачук В.Н., Ткачук И.Н. Эффективность препарата Витапрост Форте у больных с доброкачественной гиперплазией предстательной железы // URL: http://ukonkemerovo.com/sprawka/g2401204.htm.
12. Журавлев В.Н., Баженов И.В., Журавлев О.В., Бурцев С.А. Изучение эффективности применения препарата Витапрост® Форте суппозитории ректальные 100 мг производства ОАО «Нижфарм» у пациентов с доброкачественной гиперплазией предстательной железы // URL: http://medi.ru/doc/g2401305.htm.
13. Миллер А.М., Ярошенко В.П., Сорока П.В., Стахнев Е.Ю. Изучение эффективности применения препарата Витапрост Форте суппозитории ректальные 100 мг производства ОАО «Нижфарм» у пациентов с доброкачественной гиперплазией предстательной железы // Материалы 3-й конференции «Рациональная фармакоте- рапия в урологии», 2009. С. 3.
14. Ситдыкова М.Э., Зубков А.Ю. Изучение эффективности препарата Витапрост Форте суппозитории ректальные 100 мг производства ОАО «Нижфарм» у пациентов с доброкачественной гиперплазией предстательной железы // Урология. 2009. № 6. С. 3–6.
15. Камалов А.А., Ефремов Е.А., Дорофеев С.Д. и соавт. Витапрост Форте в лечении больных с аденомой предстательной железы // Урология. 2007. № 3. С. 39–47.
Новости на тему
17.02.2023
08.12.2022
12.09.2022 01:00:00
СТАТЬИ по теме
СТАТЬИ этих авторов
Отправить статью по электронной почте
Ваш адрес электронной почты:
В статье приведены результаты российских исследований по изучению эффективности и безопасности препарата Витапрост® Форте суппозитории ректальные 100 мг у больных с доброкачественной гиперплазией предстательной железы (ДГПЖ).
Было показано, что препарат снижает клинические проявления заболевания, способствует значительному улучшению показателей урофлоуметрии и уменьшению объема предстательной железы. В связи с этим Витапрост® Форте рекомендуется к применению в монотерапии ДГПЖ у пациентов с умеренно выраженной инфравезикальной обструкцией вне зависимости от возраста и наличия сопутствующих заболеваний.
" id="sender_art_description" name = "SENDER_ART_DESCRIPTION" />
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
