количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
Опыт ведения детей с последствиями перинатального поражения нервной системы в течение первого года жизни в амбулаторных условиях
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Педиатрия" №1
- Аннотация
- Статья
- Ссылки
Дети, у которых диагноз перинатальной энцефалопатии поставлен в течение первых месяцев жизни и которым в комплекс лечения введен современный полипептидный препарат Кортексин, имели более короткие сроки лечения, более быструю ликвидацию задержки становления моторных функций, психоэмоционального, предречевого развития, а редукция патологических ультразвуковых паттернов проходила без формирования сосудистых дистоний.
Авторами обоснована важность своевременной диагностики и раннего лечения детей с диагнозом перинатальной энцефалопатии.
Дети, у которых диагноз перинатальной энцефалопатии поставлен в течение первых месяцев жизни и которым в комплекс лечения введен современный полипептидный препарат Кортексин, имели более короткие сроки лечения, более быструю ликвидацию задержки становления моторных функций, психоэмоционального, предречевого развития, а редукция патологических ультразвуковых паттернов проходила без формирования сосудистых дистоний.
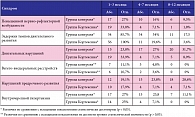
Таблица 1. Динамика частоты выявления синдромов негрубых неврологических нарушений у детей первого года жизни с диагнозом ПЭП в исследуемых группах в зависимости от возраста

Рис. Динамика основных синдромов негрубых неврологических нарушений: А – в группе Кортексина, Б – в контрольной группе
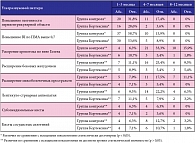
Таблица 2. Динамика частоты выявления патологических ультразвуковых паттернов у детей первого года жизни с диагнозом ПЭП в исследуемых группах в зависимости от возраста
Актуальность проблемы перинатальной энцефалопатии (ПЭП) в педиатрии обусловлена тем, что ПЭП оказывает влияние на качество жизни детей и формирование различных повреждений нервной системы, в тяжелых случаях приводящих к инвалидности. В настоящее время в Российской Федерации дети-инвалиды составляют от 1,5 до 4,5% детского населения. За период с 1980 по 2009 г. распространенность детской инвалидности возросла почти в 12 раз. Общее число детей с ограниченными возможностями превысило полумиллионную отметку [1]. В структуре детской инвалидности первое место принадлежит врожденным аномалиям развития, второе – психическим расстройствам, третье – заболеваниям нервной системы. Среди последних 35–40% составляют поражения, возникающие в перинатальном периоде вследствие влияния различных неблагоприятных факторов на процессы развития нервной системы. Так, в частности, по данным Муниципального бюджетного учреждения здравоохранения «Детская городская поликлиника № 1» (МБУЗ ДГП № 1) г. Краснодара, структуру общей детской инвалидности за 2011 г. составили следующие заболевания:
- заболевания нервной системы – 38,6% (половина из таких пациентов – дети, страдающие последствиями перинатальных поражений центральной нервной системы (ЦНС));
- врожденные аномалии – 17,1%;
- эндокринные заболевания и нарушения обмена веществ – 11,9%.
В поликлинической практике отмечаются проявления ПЭП легкой и средней степени тяжести, поэтому адекватная терапия может снизить частоту условно инвалидизирующих состояний. Для этого необходима своевременная диагностика и назначение корригирующего лечения в ранний восстановительный период – от 0 до 4 месяцев. Условно инвалидизирующие состояния представляют собой негрубые неврологические нарушения, развивающиеся преимущественно в детском возрасте. К ним относят задержку речевого развития, задержку формирования двигательных навыков, способности к концентрации внимания, дислексию, дисграфию, нарушение поведения (гиперактивность, неуправляемость, агрессивность, жестокость, плаксивость, истероидность), неврозоподобные нарушения (заикания, тики, энурез, нарушения сна), астено-невротические состояния. Эти негрубые неврологические нарушения не приводят к инвалидности, но в плане социальной адаптации значительно снижают качество жизни пациентов. Несмотря на нормальные интеллектуальные функции, такие дети при обучении в школе испытывают значительные трудности, что является причиной школьной и социальной дезадаптации, а в более зрелом возрасте приводит к ограничению в профессиональной ориентации [2].
В основе патогенеза негрубых неврологических нарушений лежат структурные, биохимические, гемодинамические и нейрофизиологические изменения. Инструментальная диагностика, позволяющая выявить факторы развития заболевания у такого больного, дает важную информацию для назначения патогенетически обоснованного лечения. Прежде всего, при помощи исследования мозгового кровотока требуется исключить структурные поражения головного мозга [3–6]. В условиях поликлиники это можно сделать методом ультразвуковой визуализации с применением допплерографии. Этот метод диагностики не является нозологически специфичным, не позволяет поставить диагноз, но помогает выявить группу детей, у которых отклонения в развитии возникли на фоне тех или иных нарушений органического характера, изменений кровотока. Необходимо помнить о том, что терапевтические воздействия, направленные на коррекцию высших корковых функций, не дадут желаемого результата при наличии неустраненных нарушений гемодинамики, а эффективность лечебных мероприятий зависит от своевременной диагностики.
Методы исследования
В работе у детей с диагнозом ПЭП определялась взаимосвязь неврологического статуса с данными нейровизуализации в течение первого года жизни и оценивалась эффективность разных способов ведения этих пациентов. Отобрана группа детей в возрасте от 1 месяца до 1 года с диагнозом ПЭП. Дети были доношенными, с массой тела 3000–3850 г. С рождения у всех пациентов зарегистрированы клинические признаки перинатального поражения ЦНС гипоксически-ишемического генеза. Оценивались соматический статус, анамнез, неврологический статус, моторное развитие, предречевое развитие пациента, данные нейровизуализации и допплерометрии. Наблюдение велось в течение первого года жизни. В рамках национального проекта «Здоровье» введен план диспансерного ведения детей от 0 месяцев до 12 месяцев, включающий обязательный осмотр детей в возрасте 1 месяца, ультразвуковую диагностику с применением допплерографии. На протяжении 1 года невролог оценивал состояние детей в возрасте 3 месяцев, 6 месяцев, 12 месяцев. При выявлении ПЭП осмотр неврологом осуществляется по мере необходимости, нейросонография проводится в возрасте 1 месяца, далее – по показаниям. Группа обследованных детей состояла из 119 пациентов, у которых была диагностирована ПЭП трех степеней тяжести:
В работе у детей с диагнозом ПЭП определялась взаимосвязь неврологического статуса с данными нейровизуализации в течение первого года жизни и оценивалась эффективность разных способов ведения этих пациентов. Отобрана группа детей в возрасте от 1 месяца до 1 года с диагнозом ПЭП. Дети были доношенными, с массой тела 3000–3850 г. С рождения у всех пациентов зарегистрированы клинические признаки перинатального поражения ЦНС гипоксически-ишемического генеза. Оценивались соматический статус, анамнез, неврологический статус, моторное развитие, предречевое развитие пациента, данные нейровизуализации и допплерометрии. Наблюдение велось в течение первого года жизни. В рамках национального проекта «Здоровье» введен план диспансерного ведения детей от 0 месяцев до 12 месяцев, включающий обязательный осмотр детей в возрасте 1 месяца, ультразвуковую диагностику с применением допплерографии. На протяжении 1 года невролог оценивал состояние детей в возрасте 3 месяцев, 6 месяцев, 12 месяцев. При выявлении ПЭП осмотр неврологом осуществляется по мере необходимости, нейросонография проводится в возрасте 1 месяца, далее – по показаниям. Группа обследованных детей состояла из 119 пациентов, у которых была диагностирована ПЭП трех степеней тяжести:
- легкая степень ПЭП – у 81 ребенка (68,1%). Отмечены небольшие отклонения в процессе беременности и родов, легкие симптомы поражения ЦНС, быстрое восстановление кровотока, умеренные структурные нарушения;
- средняя степень ПЭП – у 35 детей (29,4%). Отмечены комбинированные факторы повреждения ЦНС – внутриутробные и родовые, но без реанимационных мероприятий. Дети имели структурные изменения головного мозга, нарушения церебральной гемодинамики;
- тяжелая степень ПЭП – у 3 детей (2,5%). В этой группе выявлены: отягощенный акушерский анамнез, глубокая недоношенность, внутриутробные инфекции, реанимационные мероприятия после родов, структурные нарушения головного мозга, нарушения гемодинамики [7].
Результаты исследования и обсуждение
В течение периода наблюдения в группах исследования у 2 детей отмечена аллергическая реакция на сироп Пантогам, у 1 ребенка – на Элькар. Случаев непереносимости Кортексина не зафиксировано. В таблице 1 представлено распределение пациентов в зависимости от основных клинических синдромов, наблюдаемых у них в период от 1 до 12 месяцев: синдром повышенной нервно-рефлекторной возбудимости (СПНРВ), синдром двигательных нарушений (СДН) (гиперкинетический синдром, синдром мышечной гипотонии, мышечного гипертонуса, гемипареза), синдром задержки темпов двигательного развития (СЗТДР), синдром вегето-висцеральных расстройств (СВВР), синдром нарушений предречевого развития (СНПРР), синдром внутричерепной гипертензии (СВЧГ). Часть пациентов имели сочетание данных синдромов в различных комбинациях. Более наглядно клиническая динамика распространенности тех или иных неврологических синдромов ПЭП у детей в двух группах за период наблюдения от 1–3 месяцев до 8–12 месяцев представлена на рисунке.
Как видно из представленных данных, в течение года статистически значимое (p < 0,05) изменение частоты встречаемости тех или иных синдромов отмечено у детей как в 1-й, так и во 2-й группе. При этом уменьшение доли пациентов с синдромами повышенной нервно-рефлекторной возбудимости, задержки темпов двигательного развития, внутричерепной гипертензии происходило достоверно быстрее в группе применения Кортексина (p < 0,05). В ходе исследования было установлено, что динамика синдрома вегето-висцеральных расстройств не зависела от проводимого лечения, так как в обеих группах к 1 году (8–12 месяцев) произошло снижение доли детей с этим синдромом до 0%. Выявление достоверных различий между группами в отношении синдрома вегето-висцеральных расстройств на фоне терапии Кортексином или без терапии Кортексином было затруднено в связи с низкой частотой синдрома в обеих группах (у 11,1% детей в 1-й группе, у 10,7% во 2-й группе).
У детей, пролеченных Кортексином, распространенность синдрома двигательных нарушений снизилась с 33,9% в возрасте 1–3 месяцев до 8,9% в возрасте 8–12 месяцев (p < 0,05), а в контрольной группе, наоборот, отмечен достоверный рост частоты этого нарушения с 23,8 до 31,8% (p < 0,05). Аналогичная тенденция наблюдается и в динамике синдрома нарушения предречевого развития: у детей контрольной группы отмечен достоверный рост (p < 0,05) частоты данного синдрома, в то время как в группе Кортексина – достоверное снижение (p < 0,05) доли детей с нарушениями предречевого развития. Данные по выявленным при ультразвуковом исследовании измененным ультразвуковым паттернам отображены в таблице 2. Как видно из представленных данных, у детей обеих групп исследования в течение года имело место изменение распространенности ультразвуковых синдромов. Достоверное снижение (p < 0,05) частоты таких ультразвуковых паттернов, как повышение эхогенности перивентрикулярной области и повышение индекса резистентности (RI, resistance index) по ПМА более 0,7 за период от 1–3 месяцев до 8–12 месяцев, отмечается у представителей обеих групп; доля пациентов с этими синдромами в обеих группах уменьшается до 0%, поэтому эффективность лечения по этому критерию оценить невозможно. Но темпы редукции этих синдромов во 2-й группе были выше, чем в 1-й группе.
В отношении остальных ультразвуковых синдромов у пациентов обеих групп наблюдается недостоверное снижение доли детей с выявленными нарушениями (p > 0,05), что связано с исходно низкой частотой данных ультразвуковых нарушений в обеих группах. При оценке динамики такого ультразвукового паттерна, как ускорение кровотока по вене Галена, можно отметить рост частоты выявления этого синдрома у детей 1-й группы с 6,3% в возрасте 1–3 месяца до 33,3% в возрасте 4–7 месяцев, а к 8–12 месяцам частота выявления данного паттерна снижалась до 15,9%, что более чем в 2 раза превосходило частоту в период 1–3 месяца. У детей 2-й группы частота обнаружения этого нарушения исходно составляла 10,7% в 1–3 месяца и постепенно снижалась до 1,8% к 8–12 месяцам, то есть частота паттерна ускорения кровотока по вене Галена у детей с ПЭП в возрасте 8–12 месяцев на фоне терапии Кортексином была в 8,8 раз ниже, чем у пациентов контрольной группы. Сходная картина динамики распространенности патологических паттернов в сравниваемых подгруппах отмечена для всех ультразвуковых паттернов. Таким образом, характеризуя неврологический статус у детей двух групп исследования, необходимо отметить, что пациенты, получавшие Кортексин в ранний восстановительный период, в целом показывали более стабильные результаты в отношении формирования навыков моторного развития, становления речевой функции, психоэмоционального фона; у них отмечался более быстрый регресс патологической неврологической симптоматики по сравнению с пациентами группы контроля.
В группе детей, не получавших лечение Кортексином, кроме задержки редукции неврологической симптоматики можно отметить следующие особенности динамики ультразвуковых паттернов: повышение эхогенности перивентрикулярной области и повышение индекса резистентности, выявленные в период 1–3 месяца, сменялись в последующем расширением боковых желудочков и межоболочечных пространств, появлением анэхогенных включений в сосудистых сплетениях, повышением скорости венозного оттока по большой мозговой вене (вене Галена). Напротив, у детей, получавших Кортексин, признаки перивентрикулярной ишемии и повышение индекса резистентности по ПМА исчезали без формирования других патологических ультразвуковых паттернов. А положительная динамика данных нейровизуализации опережала положительную динамику клинической картины. Из представленного материала следует, что более быстрая ликвидация неврологических синдромов у детей из 2-й группы и благополучное разрешение явлений перивентрикулярной ишемии обусловлены включением на ранних этапах в комплексную терапию пептидного препарата Кортексин. Добавление Кортексина в схему терапии позволяет сократить сроки лечения, уменьшить количество назначаемых пероральных препаратов, количество курсов медикаментозной терапии, немедикаментозного лечения, включающего физиотерапевтическое лечение, лечебную физкультуру и массаж.
В течение периода наблюдения в группах исследования у 2 детей отмечена аллергическая реакция на сироп Пантогам, у 1 ребенка – на Элькар. Случаев непереносимости Кортексина не зафиксировано. В таблице 1 представлено распределение пациентов в зависимости от основных клинических синдромов, наблюдаемых у них в период от 1 до 12 месяцев: синдром повышенной нервно-рефлекторной возбудимости (СПНРВ), синдром двигательных нарушений (СДН) (гиперкинетический синдром, синдром мышечной гипотонии, мышечного гипертонуса, гемипареза), синдром задержки темпов двигательного развития (СЗТДР), синдром вегето-висцеральных расстройств (СВВР), синдром нарушений предречевого развития (СНПРР), синдром внутричерепной гипертензии (СВЧГ). Часть пациентов имели сочетание данных синдромов в различных комбинациях. Более наглядно клиническая динамика распространенности тех или иных неврологических синдромов ПЭП у детей в двух группах за период наблюдения от 1–3 месяцев до 8–12 месяцев представлена на рисунке.
Как видно из представленных данных, в течение года статистически значимое (p < 0,05) изменение частоты встречаемости тех или иных синдромов отмечено у детей как в 1-й, так и во 2-й группе. При этом уменьшение доли пациентов с синдромами повышенной нервно-рефлекторной возбудимости, задержки темпов двигательного развития, внутричерепной гипертензии происходило достоверно быстрее в группе применения Кортексина (p < 0,05). В ходе исследования было установлено, что динамика синдрома вегето-висцеральных расстройств не зависела от проводимого лечения, так как в обеих группах к 1 году (8–12 месяцев) произошло снижение доли детей с этим синдромом до 0%. Выявление достоверных различий между группами в отношении синдрома вегето-висцеральных расстройств на фоне терапии Кортексином или без терапии Кортексином было затруднено в связи с низкой частотой синдрома в обеих группах (у 11,1% детей в 1-й группе, у 10,7% во 2-й группе).
У детей, пролеченных Кортексином, распространенность синдрома двигательных нарушений снизилась с 33,9% в возрасте 1–3 месяцев до 8,9% в возрасте 8–12 месяцев (p < 0,05), а в контрольной группе, наоборот, отмечен достоверный рост частоты этого нарушения с 23,8 до 31,8% (p < 0,05). Аналогичная тенденция наблюдается и в динамике синдрома нарушения предречевого развития: у детей контрольной группы отмечен достоверный рост (p < 0,05) частоты данного синдрома, в то время как в группе Кортексина – достоверное снижение (p < 0,05) доли детей с нарушениями предречевого развития. Данные по выявленным при ультразвуковом исследовании измененным ультразвуковым паттернам отображены в таблице 2. Как видно из представленных данных, у детей обеих групп исследования в течение года имело место изменение распространенности ультразвуковых синдромов. Достоверное снижение (p < 0,05) частоты таких ультразвуковых паттернов, как повышение эхогенности перивентрикулярной области и повышение индекса резистентности (RI, resistance index) по ПМА более 0,7 за период от 1–3 месяцев до 8–12 месяцев, отмечается у представителей обеих групп; доля пациентов с этими синдромами в обеих группах уменьшается до 0%, поэтому эффективность лечения по этому критерию оценить невозможно. Но темпы редукции этих синдромов во 2-й группе были выше, чем в 1-й группе.
В отношении остальных ультразвуковых синдромов у пациентов обеих групп наблюдается недостоверное снижение доли детей с выявленными нарушениями (p > 0,05), что связано с исходно низкой частотой данных ультразвуковых нарушений в обеих группах. При оценке динамики такого ультразвукового паттерна, как ускорение кровотока по вене Галена, можно отметить рост частоты выявления этого синдрома у детей 1-й группы с 6,3% в возрасте 1–3 месяца до 33,3% в возрасте 4–7 месяцев, а к 8–12 месяцам частота выявления данного паттерна снижалась до 15,9%, что более чем в 2 раза превосходило частоту в период 1–3 месяца. У детей 2-й группы частота обнаружения этого нарушения исходно составляла 10,7% в 1–3 месяца и постепенно снижалась до 1,8% к 8–12 месяцам, то есть частота паттерна ускорения кровотока по вене Галена у детей с ПЭП в возрасте 8–12 месяцев на фоне терапии Кортексином была в 8,8 раз ниже, чем у пациентов контрольной группы. Сходная картина динамики распространенности патологических паттернов в сравниваемых подгруппах отмечена для всех ультразвуковых паттернов. Таким образом, характеризуя неврологический статус у детей двух групп исследования, необходимо отметить, что пациенты, получавшие Кортексин в ранний восстановительный период, в целом показывали более стабильные результаты в отношении формирования навыков моторного развития, становления речевой функции, психоэмоционального фона; у них отмечался более быстрый регресс патологической неврологической симптоматики по сравнению с пациентами группы контроля.
В группе детей, не получавших лечение Кортексином, кроме задержки редукции неврологической симптоматики можно отметить следующие особенности динамики ультразвуковых паттернов: повышение эхогенности перивентрикулярной области и повышение индекса резистентности, выявленные в период 1–3 месяца, сменялись в последующем расширением боковых желудочков и межоболочечных пространств, появлением анэхогенных включений в сосудистых сплетениях, повышением скорости венозного оттока по большой мозговой вене (вене Галена). Напротив, у детей, получавших Кортексин, признаки перивентрикулярной ишемии и повышение индекса резистентности по ПМА исчезали без формирования других патологических ультразвуковых паттернов. А положительная динамика данных нейровизуализации опережала положительную динамику клинической картины. Из представленного материала следует, что более быстрая ликвидация неврологических синдромов у детей из 2-й группы и благополучное разрешение явлений перивентрикулярной ишемии обусловлены включением на ранних этапах в комплексную терапию пептидного препарата Кортексин. Добавление Кортексина в схему терапии позволяет сократить сроки лечения, уменьшить количество назначаемых пероральных препаратов, количество курсов медикаментозной терапии, немедикаментозного лечения, включающего физиотерапевтическое лечение, лечебную физкультуру и массаж.
Выводы
В проведенном исследовании показана возможность эффективного амбулаторного лечения детей с ПЭП. При этом выявлено следующее:
В проведенном исследовании показана возможность эффективного амбулаторного лечения детей с ПЭП. При этом выявлено следующее:
- Применение Кортексина в раннем восстановительном периоде способствует регрессу неврологической симптоматики и сокращению сроков лечения перинатальных поражений ЦНС, снижает частоту формирования сосудистых дистоний.
- Кортексин не дает осложнений, аллергических реакций, хорошо сочетается с другими методами лечения.
1. Батышев А.С., Батышева Т.Т. Врач + пациент: философия успеха. М.: ВК, 2011.
2. Росин Ю.А. Ультразвуковая и функциональная диагностика в «малой» детской неврологии. СПб.: Гиппократ, 2008. С. 3–5.
3. Лучевая диагностика в педиатрии: национальное руководство / Гл. редактор А.Ю. Васильев. М.: ГЭОТАР-Медиа, 2010. С. 13–40.
4. Бадалян Л.О., Журба Л.Т., Тимонина О.В. Детский церебральный паралич. Киев: Здоровье, 1988. С. 99–111, 129–149.
5. Долгих Г.Б. Цереброваскулярные дистонии у детей. Казань: Медлитература, 2007. С. 86–111.
6. Лечение заболеваний нервной системы у детей / Под ред. В.П. Зыкова. М.: Триада-Х, 2009. С. 20–32.
7. Белоусова Т.В., Ряжина Л.А. Перинатальные поражения центральной нервной системы у новорожденных. Методические рекомендации. СПб.: Коста, 2010. С. 21–29.
Новости на тему
СТАТЬИ по теме
05.04.2023
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
