Патогенетическая терапия новым отечественным антиоксидантом Этоксидолом при цереброваскулярной болезни
- Аннотация
- Статья
- Ссылки
В настоящее время одной из важнейших проблем здравоохранения в мире, в том числе в России, являются вопросы патогенетической терапии и профилактики цереброваскулярных заболеваний (ЦВЗ). Их рост обусловлен множеством причин: артериальной гипертензией, в том числе вариабельной, ишемической болезнью сердца, церебральным атеросклерозом, дислипопротеинемией, сахарным диабетом, гемостатическими нарушениями, злоупотреблением алкоголем, стрессом и др. Согласно статистическим данным, смертность от ЦВЗ в экономически развитых странах достигает 11–12% и более. В Российской Федерации первичная заболеваемость и показатели смертности от ЦВЗ одни из самых высоких в мире. В связи с этим вопросы лечения и профилактики данной патологии остаются крайне актуальными [1, 2].
В настоящее время одной из важнейших проблем здравоохранения в мире, в том числе в России, являются вопросы патогенетической терапии и профилактики цереброваскулярных заболеваний (ЦВЗ). Их рост обусловлен множеством причин: артериальной гипертензией, в том числе вариабельной, ишемической болезнью сердца, церебральным атеросклерозом, дислипопротеинемией, сахарным диабетом, гемостатическими нарушениями, злоупотреблением алкоголем, стрессом и др. Согласно статистическим данным, смертность от ЦВЗ в экономически развитых странах достигает 11–12% и более. В Российской Федерации первичная заболеваемость и показатели смертности от ЦВЗ одни из самых высоких в мире. В связи с этим вопросы лечения и профилактики данной патологии остаются крайне актуальными [1, 2].
По характеру клинического течения выделяют острые и хронические формы ЦВЗ. Патогенетические механизмы одинаковы:
-
нарушение тонуса сосудов;
-
морфологическое изменение сосудистой стенки;
-
недостаточность коллатерального кровообращения;
-
ухудшение реологических свойств крови;
-
нарушение церебральной микроциркуляции и ауторегуляции мозгового кровообращения и нейрогенной регуляции системной и церебральной гемодинамики.
Как следствие – гипоксия головного мозга, окислительный стресс и нарушения связей между корой и подкорковыми образованиями [3, 4].
К острым формам относят острое нарушение мозгового кровообращения (инсульт) и преходящее нарушение мозгового кровообращения. Инсульт характеризуется быстрым началом и очаговой неврологической симптоматикой, сохраняющейся свыше 24 часов или заканчивающейся в тяжелых случаях смертью в течение суток.
Преходящие нарушения мозгового кровообращения подразделяют на транзиторную ишемическую атаку, церебральный сосудистый криз и острую гипертоническую энцефалопатию. Очаговый неврологический дефицит регрессирует в течение нескольких часов [4–6].
К хроническим формам относят хроническую ишемию мозга – медленно прогрессирующую недостаточность кровоснабжения головного мозга. Выделяют три стадии: легкую, выраженную и резко выраженную.
Для первой стадии характерны, в частности, головная боль, головокружение, шум в голове, рассеянная неврологическая симптоматика субсиндромального характера в виде легкой асимметрии носогубных складок, девиации языка, анизорефлексии. Когнитивные расстройства минимальны, отмечаются незначительное снижение оперативной памяти, нарушение концентрации внимания. Превалируют жалобы на повышенную утомляемость, слабость, раздражительность, снижение работоспособности, которые ухудшают качество жизни пациента. Легкие когнитивные расстройства носят субъективный характер и практически незаметны для окружающих. Диагностика основана на жалобах пациента и специальных нейропсихологических методиках. Выявляется замедление выполнения заданий из-за снижения концентрации внимания и скорости психомоторных реакций. Типичны также астенические проявления от легких в виде повышенной утомляемости, слабости, раздражительности, вегетативной дисфункции до выраженных с формированием астенического синдрома.
Хроническая ишемия мозга имеет неуклонно прогредиентный тип течения, одна стадия плавно переходит в другую.
При второй стадии формируется неврологический синдром: цефалгический, вестибулярный, пирамидный и др. Умеренные когнитивные нарушения не ограничивают повседневную активность, но в отличие от легких заметны окружающим в повседневном общении и представляют недостаточность нескольких когнитивных функций. Они характеризуются трудностями сосредоточения и переключения с одной деятельности на другую, вязкостью мышления, сужением круга интересов, снижением мыслительной продукции, памяти, критики. При нейропсихологическом тестировании выявляются изменения, указывающие на затруднения в профессиональной и социальной сферах. Развиваются тревожные, впоследствии депрессивные реакции. Отмечается также нарушение циркадианных ритмов – дневная сонливость и ночное бодрствование [4, 7].
Для третьей стадии характерны несколько неврологических синдромов и выраженные нарушения когнитивных функций: памяти, внимания, мышления, пространственной ориентации. Формируются изменения личности с трудностями в общении, зависимостью от окружающих, с немотивированными поступками, неадекватными реакциями и изменением психики вплоть до развития профессиональной и социальной дезадаптации и деменции.
Изменения вследствие болезни социального статуса больного и утрата трудоспособности являются психогенно травмирующими факторами, провоцирующими возникновение разнообразных аффективных нарушений депрессивного круга. Наличие органически измененной почвы значительно облегчает возникновение реакций на психотравмирующие ситуации, приводит к их фиксации. Наблюдаются протрагированные депрессивные реакции, для которых характерны сниженное настроение, чувство беспокойства, тревога, мысли о бесперспективности существования, пессимистическая оценка будущего. При депрессивно-ипохондрических реакциях на первый план выходят тревожные опасения за здоровье, фобические эпизоды. В отдельных случаях реакция личности на болезнь принимает характер стойкого гипотимического сдвига настроения с идеями собственной неполноценности, инвалидизированности, ограничением круга интересов и общей активности.
Хронической ишемии мозга свойственно несколько типов течения:
-
ремитирующий, когда эпизоды декомпенсации в виде церебрально-сосудистого криза, транзиторной ишемической атаки или инсульта чередуются с компенсацией;
-
медленнопрогредиентный – без эпизодов декомпенсации;
-
быстропрогредиентный – с быстрым типом прогрессирования [4, 6].
Диагноз ЦВЗ ставят на основании клинического осмотра и результатов дополнительного обследования, включающего дуплексное обследование сосудов шеи и головного мозга, компьютерную томографию (КТ) или магнитно-резонансную томографию (МРТ) головного мозга, биохимического анализа крови. При МРТ определяются периваскулярные лакуны (постишемические кисты), атрофия коры полушарий, расширение желудочковой системы, изменение плотности ткани мозга, особенно в перивентрикулярных образованиях по типу лейкоареоза. КТ или МРТ проводятся также для дифференциальной диагностики с другими заболеваниями [4, 6].
Механизм развития и принципы патогенетического лечения
Цель лечения ЦВЗ состоит в коррекции факторов риска, восстановлении гемодинамики. Окислительный стресс, приводящий к образованию избыточного количества свободных радикалов, способствует прогрессированию церебральной ишемии и играет негативную роль в патогенезе ЦВЗ. При гипоксии основным патогенетическим звеном повреждения является активация процессов перекисного окисления липидов. Одним из вариантов снижения уровня метаболического ацидоза и пролонгации энергопродукции считается использование промежуточных веществ цикла Кребса. Этим обусловлено включение в комплексное лечение антиоксидантов, химических соединений, механизм действия которых основан на торможении свободнорадикальных процессов в тканях.
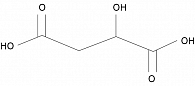
Широко назначаемые в последние десятилетия производные янтарной кислоты, сукцинаты, не всегда отвечали современным требованиям и ожиданиям клиницистов и пациентов. Поэтому возникла проблема поиска новых, более эффективных лекарственных средств, сочетающих в себе энергообеспечивающие и антиоксидантные свойства. Предметом исследования стал энергетический субстрат цикла Кребса – 2-этил-6-метил-3-гидроксипиридина малат, соединение яблочной кислоты (рис. 1). Впервые эта кислота была выделена шведским химиком Карлом Шееле в XVIII в. из незрелых яблок. Исключительная роль малата определяется высоким содержанием малатдегидрогеназы. Результаты сравнительных клинических исследований свидетельствуют в пользу более высокой биодоступности и эффективности малатов по сравнению с сукцинатами. Малат легко проникает через гематоэнцефалический барьер. В физиологических условиях малат является промежуточным компонентом цикла Кребса, но становится дефицитным при прогрессирующей гипоксии. Доказана уникальность механизма действия малата: при гипоксии он подвергается метаболизму с образованием аденозинтрифосфата (АТФ) в 2,5 раза больше, чем сукцинат. В зависимости от степени гипоксии малат обратимо перестраивается, благодаря чему клетка продолжает получать энергию даже в отсутствие кислорода. Таким образом, чем выше гипоксия, тем эффективнее проявляется действие малата. Преимущество малата заключается в том, что он способен восстанавливаться в фумарат и даже сукцинат. В зависимости от степени ишемии и потребности клетки в энергии малат может окисляться с высвобождением АТФ при достаточном количестве кислорода в митохондриях и даже при недостаточном количестве кислорода в цитоплазме или восстанавливаться до сукцината «про запас». Сукцинат способен только окисляться и не так эффективен при выраженной гипоксии. Установлено, что клетка не затрачивает энергию АТФ для переноса малата в митохондрию. Для этого существует специальный малат-аспартатный челнок. Доказана способность малата повышать коэффициент дыхательного контроля митохондрий, восстанавливать цитохром b5 в присутствии никотинамидадениндинуклеотида, кофермента, участвующего в окислительно-восстановительных реакциях [3, 5, 8].
Учитывая уникальные свойства малата, в научном центре биологически активных веществ российскими учеными был разработан новый отечественный лекарственный препарат, антиоксидант второго поколения, этилметилгидроксипиридина малат – Этоксидол®. Кроме малата в состав препарата входят глицин, N-ацетил-L-глутаминовая кислота (ацеглумат), 2-(диметиламино)этанол, пиридоксин витамин В6. Благодаря фармакологическому синергизму компонентов препарата обеспечиваются интенсификация процессов клеточного метаболизма и обмена веществ, окислительно-восстановительных процессов, регенерация клеток, нормализация липидного обмена. Глицин нормализует многие функции мозга, сон, улучшает когнитивные функции, снижает токсическое действие ряда веществ, в том числе антиаритмиков. Деанол (ацеглумат) является нейрометаболическим стимулятором, имеет структурное сходство с ГАМК и глутаминовой кислотой. Обладает ноотропным, церебропротективным, антиастеническим, антидепрессивным и гепатопротективным свойствами. Благодаря комбинированному составу препарат Этоксидол® способствует улучшению процесса обучения, сохранению и воспроизведению информации, снижает уровни маркеров старения в головном мозге и крови, уменьшает проявления неврологического дефицита.
Этоксидол® выпускается в виде жевательных таблеток по 100 мг и раствора в ампулах по 2,0 и 5,0 мл, в 1,0 мл содержится 50 мг вещества. Курс лечения и доза препарата подбираются индивидуально. При инфузионном способе введения препарат разводят в 0,9%-ном растворе натрия хлорида. Начинают терапию с дозы 50–100 мг, постепенно повышая ее до получения терапевтического эффекта. Внутривенно струйно препарат вводят медленно в течение пяти – семи минут, капельно – со скоростью 40–60 капель в минуту. Раствор можно вводить и внутримышечно по 100 мг при необходимости до трех раз в день. Рекомендуемая максимальная суточная доза – не более 800 мг. Впоследствии возможен переход на таблетированную форму по одной таблетке три раза в день. Таблетки разжевывают и запивают водой. Длительность курса зависит от тяжести состояния и эффективности терапии.
Комплексный механизм действия Этоксидола подтвержден результатами многочисленных клинических исследований. Л.Н. Сернов в ходе эксперимента изучал возможность пролонгации энергопродукции в ишемизированной клетке при накоплении недоокисленных продуктов и снижении уровня рН. Было доказано, что энергопродукция служит ключевым механизмом для обеспечения выживаемости клетки и снижения уровня метаболического ацидоза. Благодаря этому Этоксидол® оказывает противоишемическое действие: улучшает кровоток в зоне ишемии, ограничивает зону ишемического повреждения, препятствует накоплению первичных продуктов перекисного окисления липидов в мозге, повышает активность ферментов антиоксидантной защиты и снижает степень эксцесс-лактата.
В ряде исследований доказана высокая гиполипидемическая эффективность. В.Г. Кукес и соавт. в экспериментах на животных продемонстрировали липидрегулирующее действие Этоксидола при гиперлипидемии. Впоследствии клинически была подтверждена способность Этоксидола снижать в крови уровень триглицеридов, холестерина, атерогенных липопротеинов.
Показано также, что Этоксидол® характеризуется выраженным анксиолитическим действием. При назначении 100–200 мг два-три раза в день внутримышечно или перорально в течение 14–30 дней уменьшаются тревога, раздражительность, нарушения сна.
В.В. Архипов и А.С. Кузьменко проводили сравнительное исследование различных групп пациентов с инсультом. Как показали результаты, Этоксидол® достоверно ускорял регресс не только двигательных, но и когнитивных нарушений при назначении 200–300 мг внутривенно капельно в первые два – четыре дня и 100 мг внутримышечно три раза в сутки 10–14 дней с последующим переходом на пероральный прием 100 мг три раза в сутки, в тяжелых случаях – до 800 мг/сут. Побочных симптомов даже при назначении высоких доз не отмечалось.
В других исследованиях изучали антиалкогольное действие Этоксидола. Экспериментально была доказана способность препарата за пять – семь дней при назначении 100–200 мг внутримышечно два-три раза в день или внутривенно капельно один-два раза в день восстанавливать вызванные этанолом нарушения двигательной активности, уменьшать миорелаксацию и расстройства координации. Препарат может быть использован для купирования абстинентного синдрома с неврозоподобными и вегетативными расстройствами или лечения алкогольной зависимости [3, 8, 9].
Как правило, препарат хорошо переносится пожилыми пациентами и не требует коррекции дозы.
С целью изучения эффективности и переносимости препарата Этоксидол® нами было проведено обследование больных с вариабельной гипертензией и когнитивными расстройствами при хронической ишемии мозга.
Материал и методы исследования
Обследовано 50 больных с вариабельной гипертензией (20 (40,01%) мужчин и 30 (60,0%) женщин) в возрасте от 40 до 65 лет (средний возраст – 55,0 ± 10,2 года). Все пациенты принимали гипотензивную терапию. На фоне нестабильности артериального давления отмечались головная боль, головокружение, ухудшение памяти, эмоциональные расстройства. Длительность когнитивных расстройств составила от года до 12 лет, в среднем 5,8 ± 6,4 года. Психоэмоциональные расстройства и нарушение сна имели место у всех больных. У 10 (20,0%) наблюдалось злоупотребление алкоголем. Курс лечения начинали с внутримышечных инъекций по 2,0 мл (100 мг) два раза в день с последующим переходом на прием Этоксидола внутрь по 100 мг три раза в день в течение трех месяцев.
Дизайн исследования
Критериями включения было наличие у больного вариабельной гипертензии и когнитивных расстройств, выявляемых после анкетирования и специального нейропсихологического тестирования. Критерием исключения служила деменция. Было запланировано четыре визита с периодичностью каждые четыре недели. На каждом визите проводилось нейропсихологическое тестирование.
Анкетирование
На первом визите проводили стандартный неврологический и физикальный осмотр пациентов, изучали анамнез. Физикальное обследование включало трехкратное измерение артериального давления (АД) (для определения «внутривизитной» вариабельности АД), суточное мониторирование АД.
Анкетирование предусматривало ответы на такие вопросы, как:
-
наличие жалоб на снижение памяти или умственной работоспособности со слов самого пациента или его родственников;
-
принимаемая пациентом медикаментозная терапия, в том числе гипотензивная и церебропротективная.
Тестирование
С целью объективизации когнитивных расстройств было выполнено нейропсихологическое тестирование с использованием тестов «Серийный счет» и «Часы».
При проведении теста «Серийный счет» пациента просят начиная от 100 пять раз подряд вычесть 7 (100 – 7 = 93; 93 – 7 = 86 и т.д.). Данный тест позволяет проверить у больного концентрацию внимания.
При проведении теста «Часы» пациента просят нарисовать циферблат и отметить стрелками предлагаемое исследователем время. Ошибки, допущенные пациентом при проведении нейропсихологического тестирования, свидетельствуют о когнитивных расстройствах.
Динамика когнитивных расстройств при терапии Этоксидолом
При терапии Этоксидолом на каждом визите выполняли нейропсихологическое тестирование в динамике для изучения влияния препарата на когнитивные функции.
Результаты
Все пациенты завершили исследование. Отмечалась хорошая переносимость препарата. У одного (2%) пациента имели место побочные симптомы в виде диспепсических расстройств, тошноты, сухости во рту, которые быстро прошли самостоятельно и не потребовали коррекции. У двух (4%) пациентов в течение первых пяти дней от начала приема препарата наблюдались расстройства сна в виде дневной сонливости и нарушения засыпания в вечернее время, не потребовавшие отмены препарата.
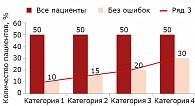
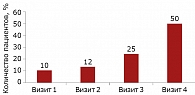
От первого к четвертому визиту постепенно увеличивалось количество больных, выполнявших тесты без ошибок (рис. 1 и 2). Все пациенты, включенные в исследование, отметили снижение тревоги, раздражительности, улучшение сна. У пяти (50%) из десяти пациентов наблюдалось снижение пристрастия к алкоголю. 20 (40%) отметили стабилизацию АД.
Заключение
Собственный опыт и результаты многочисленных исследований убедительно доказали, что синтезированное новое отечественное лекарственное средство этилметилгидроксипиридина малат (Этоксидол®) является оригинальным высокоэффективным антиоксидантом с комплексным механизмом действия. Благодаря антигипоксическому, противоишемическому, антиангинальному, ангиопротективному, гипохолестеринемическому, ноотропному и анксиолитическому действию Этоксидол® может широко применяться в клинической практике при различной патологии, в том числе цереброваскулярной.
Препарат оказывает церебропротективное действие, восстанавливает психическую активность, стабилизирует артериальное давление, оказывает положительное анксиолитическое действие при невротических состояниях, антиалкогольное – при алкогольно-абстинентном синдроме.
Фармакологические свойства Этоксидола позволяют использовать его в качестве монотерапии, а также в комплексном лечении острых и хронических форм ЦВЗ. Уникальный состав препарата обеспечивает интенсификацию метаболизма головного мозга и окислительно-восстановительных процессов, нормализацию липидного и углеводного обмена.
