Препарат Санпраз в лечении пациентов с ГЭРБ и с НПВП-индуцированной гастропатией
- Аннотация
- Статья
- Ссылки


В конце XX столетия европейское сообщество гастроэнтерологов провозгласило: «XX век – век язвенной болезни, XXI – век гастроэзофагеальной рефлюксной болезни». Это утверждение обусловлено ростом распространенности ГЭРБ, тогда как в отношении язвенной болезни прослеживается тенденция к уменьшению частоты встречаемости. Вместе с тем данное высказывание по меньшей мере несколько преждевременно, поскольку XXI в. только начинается, а в клинической практике врача число пациентов с язвенной болезнью остается весьма значительным и, что наиболее драматично, возрастает удельный вес осложненных форм заболевания, нередко связанных с приемом лекарственных препаратов с ульцерогенными свойствами. В этой связи на современном этапе особенно важно подчеркнуть актуальность проблемы развития НПВП-индуцированной гастропатии (НПВП – нестероидные противовоспалительные препараты), которая к началу нового столетия приобретает все большую значимость не только с сугубо медицинских, но и с социальных позиций. При этом количество госпитализаций и смертей, связанных с приемом НПВП, а также экономические затраты на лечение НПВП-ассоциированных заболеваний c каждым годом неуклонно растут (16).
Спектр гастроинтестинальных нежелательных явлений, связанных с приемом НПВП, достаточно широк и варьирует от легкой диспепсии до развития эрозий (часто множественных), пептических язв, перфораций и тяжелых гастродуоденальных кровотечений. Механизмы возникновения данных побочных эффектов обусловлены ульцерогенным действием НПВП на слизистую оболочку ЖКТ. При этом вне зависимости от локализации эрозивно-язвенного поражения возможно развитие двух вариантов их воздействия: как непосредственного повреждения слизистой оболочки (что справедливо в отношении ацетилсалициловой кислоты и ее производных), так и связанного с ингибированием циклооксигеназы (ЦОГ: ЦОГ1 и ЦОГ2) – ключевого фермента в каскаде метаболизма арахидоновой кислоты, которая является предшественником простагландинов, простациклинов и тромбоксанов. Закономерность развития неблагоприятных эффектов, особенно на фоне длительного приема препаратов нестероидного противовоспалительного ряда, отмечается во всех отделах ЖКТ, но наиболее выражена в гастродуоденальной зоне и прежде всего в антральном отделе желудка, где более высокая плотность рецепторов простагландинов. К существенным особенностям относятся следующие критерии: язвы желудка при НПВП-гастропатии выявляются значительно чаще, в соотношении примерно 1,5 : 1 к дуоденальной язве, и имеют преимущественную локализацию в антральном отделе желудка, нежели при эссенциальной форме язвенной болезни желудка; язвенные дефекты чаще единичны, относительно небольшого размера и глубины, могут выявляться при минимальных изменениях слизистой оболочки, а эрозивные поражения в большинстве случаев множественные. Следует отметить, что зачастую отсутствие симптоматики у больных с НПВП (наличие в 70% случаев так называемых немых язв) обусловлено как торможением биосинтеза простагландинов – медиаторов боли и воспаления, так и сугубо субъективными ощущениями, проявляющимися не истинным отсутствием проявлений, а тем, что жалобы, связанные с основным заболеванием, беспокоят пациента существенно больше, нежели симптоматика со стороны ЖКТ (3).
Вместе с тем важно подчеркнуть, что НПВП являются каузальным фактором повреждения слизистой оболочки не только желудка и/или ДПК, но и пищевода. Последние проявляются симптоматикой ГЭРБ. Так, результаты анализа 3-месячного исследования, проведенного во Франции в конце 2005 г., показали, что среди 10 тыс. респондентов 6823 (72,6%) принимали НПВП и имели клинические проявления ГЭРБ в виде изжоги и/или регургитации кислого желудочного содержимого в пищевод. При этом превалирование симптомов ГЭРБ отмечалось у 27% пациентов, принимающих НПВП в возрасте старше 65 лет, среди которых преобладали женщины.
Ныне общепризнанной является точка зрения, согласно которой возможно прогнозировать развитие НПВП-индуцированной гастропатии. Известно, что побочное действие НПВП проявляется не у всех пациентов, принимающих эти лекарственные средства. Объяснение данного феномена связано с наличием факторов риска развития повреждений слизистой оболочки ЖКТ. Важнейшими среди них считаются пожилой возраст (старше 65 лет) и язвенный анамнез, высокие дозы или одновременный прием нескольких НПВП (кроме низких доз аспирина), тяжелые сопутствующие заболевания в виде застойной сердечной недостаточности и т.д., сочетанный прием ингибиторов ангиотензинпревращающего фермента, диуретиков, b-адреноблокаторов, сочетанный прием глюкокортикоидов или антикоагулянтов, длительный прием НПВП, особенно неселективных в отношении изоформ ЦОГ и с большим периодом полувыведения. К дополнительным факторам риска относят наличие ревматоидного артрита, женский пол, курение, прием алкоголя, инфекции Н. pylori (4, 5, 16). В соответствии с выводами Американской ревматологической ассоциации (2002) у пациентов с двумя и более факторами риск развития НПВП-гастропатий очень высок и не зависит от избирательности действия НПВП. Следовательно, пациенты, нуждающиеся в длительном применении НПВП, должны быть обеспечены высококачественным лечением и эффективной лекарственной профилактикой.
Общеизвестно, что для лечения «кислотозависимых заболеваний» в течение длительного периода времени применялись антациды (с античных времен), М-холинолитики (с начала XX в.) и блокаторы Н2-гистаминовых рецепторов (70-е гг. XX в.). Однако было показано, что данные группы препаратов не способны длительно и полностью блокировать выработку соляной кислоты, поскольку воздействуют только на часть механизма, участвующего в синтезе желудочного биомаркера. Так, антацидные средства прямо взаимодействуют с хлористоводородной кислотой в желудке, инактивируя ее на короткий период времени, М-холинолитики блокируют М-холинорецепторы, делая их нечувствительными к ацетилхолину, уменьшая тем самым путем ингибирования нервно-вегетативного механизма секрецию желудочных желез, однако часто при этом приводят к большому количеству нежелательных побочных явлений, а парциальное воздействие на данные рецепторы париетальных клеток не дает выраженного желаемого эффекта для подавления выработки соляной кислоты. Блокаторы Н2-рецепторов гистамина, которые в течение продолжительного периода времени являлись препаратами выбора в терапии кислотозависимых заболеваний, ингибируют гуморальный путь стимуляции и более эффективно тормозят выработку париетальными клетками соляной кислоты и пепсина. Вместе с тем действие Н2-блокаторов также является парциальным, при их применении париетальная клетка остается чувствительной к действию гастрина и ацетилхолина. Кроме того, в виду особенностей фармакодинамики данные лекарственные средства вызывают «феномен усталости (привыкания) рецепторов», а также для них характерен «синдром отмены» препарата.
В этой связи в начале 80-х гг. прошлого столетия были синтезированы новые соединения, избирательно воздействующие на ключевой и конечный этап выработки соляной кислоты – так называемую протонную помпу (Н+, К+-АТФазу), в силу функционирования которой происходит замена иона водорода на ион калия, ион водорода выходит за пределы париетальной клетки, где связывается с анионом хлора и секретируется в форме хлористоводородной кислоты в просвет желудка (13). На сегодняшний день ингибиторы протонной помпы (ИПП), как самые мощные подавители желудочной секреции, являются основными средствами лечения «кислотозависимых заболеваний». Ввиду широкого представительства препаратов данной группы на фармацевтическом рынке, врач зачастую стоит перед выбором назначения того или иного ИПП и в большинстве случаев данный выбор обуславливают не только аспекты клинической эффективности, но и соображения рентабельности.
В настоящее время в гастроэнтерологической практике используются ИПП с несколько различающимися химической структурой и механизмом действия. Широко применяются омепразол (исторически первый – «эталонный» – ИПП), лансопразол, пантопразол, рабепразол, а также эзомепразол. Несмотря на тот факт, что пантопразол был третьим, синтезированным после омепразола и лансопразола ИПП, на фармацевтическом рынке России данный препарат появился относительно недавно. От своих предшественников пантопразол отличается только структурой радикалов на пиридиновом и бензимидазольном кольцах (2). Тем не менее данное химическое строение препарата обуславливает несколько иные свойства пантопразола, являясь более стабильным при значениях рН, близких к нейтральным. Было показано, что при более широком диапазоне значений рН может увеличиваться селективность накопления препарата в канальцах париетальных клеток, поскольку у более стабильного соединения меньше шансов прореагировать с тиольными группами белков вне париетальной клетки (9).
Антисекреторный эффект пантопразола при приеме препарата от 20-60 мг/сут является дозозависимым, а увеличение дозы до 80-120 мг/сут способствует лишь минимальному дальнейшему усилению ингибирования желудочной секреции (10, 11).
Показания к применению пантопразола не отличаются от таковых при назначении других ИПП. Вместе с тем долгое время в США приоритетным считалось использование данного препарата в лечении ГЭРБ с эрозивно-язвенным поражением пищевода (14). По данным ряда рандомизированных многоцентровых исследований, отмечена равнозначная клиническая эффективность использования 40 и 20 мг/сут пантопразола при рефлюкс-эзофагите средней и тяжелой степени выраженности (8, 11).
С учетом всех изложенных обстоятельств, целью настоящей работы явилось изучение эффективности (по динамике симптоматики и эндоскопической картины) и безопасности дженерика пантопразола препарата Санпраз у больных с различными формами ГЭРБ – эрозивным (ЭРБ) и неэрозивным (НЭРБ) ее вариантами, а также у пациентов с НПВП-индуцированной гастропатией с эрозивно-язвенными поражениями слизистой желудка и двенадцатиперстной кишки (ДПК), страдающих ревматоидным артритом и постоянно принимающих препараты нестероидного противовоспалительного ряда.
Материалы и методы исследования
В исследование были включены 35 человек, из них 17 пациентов с ГЭРБ (8 человек с ЭРБ (степени А и В по Лос-Анджелесской классификации) и 9 – с НЭРБ с признаками поверхностного воспаления (отек, гиперемия) слизистой оболочки нижних отделов пищевода) и 18 – с НПВП-индуцированной гастропатией с эрозивно-язвенными поражениями слизистой желудка (11 человек ) и ДПК (7 человек). В обеих подгруппах пациенты были пропорционально представлены в возрастном диапазоне от 18 до 70 лет (средний возраст составил 49 ± 15 лет), наблюдались преимущественно женщины (60%).
Всем пациентам проводился осмотр и стандартизированный расспрос для оценки динамики клинических проявлений заболевания на фоне лечения. Степень выраженности клинических проявлений определялась методом субъективной самооценки больными собственных ощущений с использованием градации в баллах: 0 баллов – отсутствие признака, 1 – признак выражен слабо, 2 – признак выражен умеренно, 3 – признак резко выражен. Осмотр и опрос проводился на 1, 2, 7, 14 дни и далее каждые 2 недели до 8 недель наблюдения. Эндоскопическое исследование верхних отделов ЖКТ (ФГДС) выполнялось до начала терапии, контроль – через 2 недели от начала лечения. При сохранении эрозивных (язвенных) дефектов слизистой пищевода, желудка или ДПК – каждые 2 недели до их эпителизации (рубцевания). Для оценки степени выраженности эндоскопических изменений в пищеводе использовалась Лос-Анжелесская классификация (2002).
Всем пациентам производилось 24-часовое мониторирование интрагастрального и интрапищеводного рН с помощью автономного ацидогастрометра «Гастроскан-24» по общепринятой методике. Контроль суточного рН-мониторирования назначался через 7 дней от начала терапии. Если пациенты получали антисекреторные препараты ранее, то последние отменяли за неделю до начала участия в исследовании.
Кроме того, производилась оценка показателей качества жизни по опроснику SF-36 у всех пациентов до начала терапии и после достижения клинико-эндоскопической ремиссии.
Все пациенты получали препарат Санпраз в дозе 40 мг/сут в течение 8 недель.
Результаты исследования и их обсуждение
На момент включения в исследование все пациенты с ГЭРБ испытывали изжогу, причем 8 из них и в ночное время. Помимо изжоги 10 пациентов предъявляли жалобы на регургитацию (отрыжку), 3 – на осиплость голоса, 2 – на периодические приступы удушья и кашля, преимущественно в ночные часы. Кроме того, 5 больных жаловались на загрудинные боли некардиального характера. Среди пациентов с НПВП-индуцированной гастропатией 8 человек отмечали боли в эпигастральной области и 10 – дискомфорт и тяжесть данной локализации.
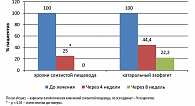
На фоне проводимой терапии уже к 3-му дню лечения у большинства пациентов ГЭРБ (11 человек, 64,7%) отмечалась статистически достоверная положительная динамика (р < 0,05), что проявлялось уменьшением выраженности изжоги. У 15 (88,2%) пациентов полное нивелирование изжоги было отмечено к 5 дню лечения. К концу первой недели терапии изжога была купирована у 94,1% пациентов с ГЭРБ (рисунок 1). Через 2 недели приема данный симптом не регистрировался.
Полнота купирования отрыжки и загрудинной (пищеводной) боли имела несколько иную динамику. Так, на 3-й день от начала лечения отрыжка регистрировалась у 35,3% пациентов, к 5-му дню – у 23,5% больных. Через 2 недели данные жалобы периодически отмечались у 12,7% пациентов. Данное обстоятельство объясняется, вероятно, выраженными двигательными расстройствами пищевода и кардиального жома. Жалобы на загрудинную (пищеводную) боль на 5-й день сохранялись у 11,7% пациентов, тогда как уже к концу первой недели отмечалось нивелирование последних.
Кроме того, важно подчеркнуть, что пациенты, имеющие внепищеводные проявления ГЭРБ, к концу первой недели терапии Санпразом отметили уменьшение осиплости голоса по утрам, а к 14-му дню терапии данный симптом не проявлялся ни у кого. Приступы удушья также уменьшились к 7-му дню терапии с 4 ± 0,3 до 2,3 ± 0,5 в неделю. К концу 3-й недели терапии во всех случаях увеличилась продолжительность сна за счет исчезновения ночных приступов удушья и кашля.
При лечении пациентов с НПВП-гастропатией уже на 2-й день от начала терапии Санпразом 67% пациентов отметили уменьшение болей в эпигастральной области, а к 7-му дню лечения жалобы данного характера были купированы у всех пациентов. Чувство дискомфорта и тяжесть в эпигастрии значительно уменьшились к 4-му дню терапии.
При оценке результатов эндоскопического обследования было установлено, что через 4 недели лечения полное заживление эрозий в пищеводе отмечалось у 75% пациентов. Через 8 недель терапии у всех больных эрозивные дефекты в слизистой пищевода не выявлялись. Кроме того, выраженность гиперемии слизистой пищевода значительно уменьшилась через 4 недели лечения, при этом у 77,8% больных к 8-й неделе от начала терапии эндоскопических изменений не определялось (рисунок 2).
Данные ФГДС у пациентов с НПВП-гастропатией, принимавших Санпраз в дозе 40 мг/сут, распределились следующим образом. Заживление язв ДПК было достигнуто через 2 недели у 86% пациентов и через 4 недели – в 100% случаев. Клиническая эффективность Санпраза в терапии НПВП-гастропатии с локализацией эрозивно-язвенного дефекта в желудке также была достаточной и показала, что частота заживления повреждений слизистой желудка через 4 и 8 недель лечения составила 86,7 и 100% соответственно.
Данные суточного рН-мониторирования (таблица 1) выявили факт исходного повышения желудочной кислотности у большинства пациентов с ГЭРБ (среднесуточный интрагастральный рН – 2,27 ± 0,46), что совпадает с результатами ряда исследований (17), подтверждающих ведущую роль уровня секреции соляной кислоты париетальными клетками желудка в патогенезе ГЭРБ. Безусловно, эффективный контроль интрагастрального, а следовательно, и интрапищеводного рН на уровне 4 и выше принципиально важен не только для ускорения восстановления структурных изменений слизистой оболочки пищевода, но и для быстрого и длительного купирования клинической симптоматики рефлюкс-эзофагита.
Динамика оценки суточного рН-мониторирования показала, что Санпраз обладает выраженным антисекреторным эффектом. Так, % суточного времени с рН > 4 ед. в желудке увеличился более чем вдвое, а % времени с рН < 4 в пищеводе уменьшился в среднем с 8,82 до 3,76. Общее число рефлюксов за сутки с 82,5 сократилось до 21.
Кроме того, как видно из данных таблицы 1, Санпраз оказывает опосредованное влияние и на количество гастроэзофагеальных рефлюксов в течение суток, уменьшая число последних более чем наполовину.
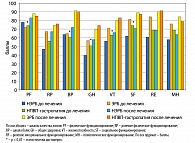
При анализе показателей качества жизни больных ГЭРБ, в зависимости от эндоскопической картины, отмечено статистически достоверное (р < 0,05) их снижение при НЭРБ по сравнению с ЭРБ по всем шкалам, кроме шкалы физического функционирования и шкалы боли (рисунок 3). При этом у пациентов, страдающих НПВП-гастропатией, которые вынуждены длительно принимать препараты нестероидного противовоспалительного ряда, уровень качества жизни оказался выше, чем у больных с НЭРБ, но ниже по сравнению с ЭРБ. На фоне лечения дженериком пантопразола препаратом Санпраз отмечалась положительная динамика по всем показателям качества жизни у всех 3 групп пациентов, с наибольшей выраженностью по шкалам боли, жизнеспособности, социального и ролевого эмоционального функционирования, особенно у больных ЭРБ и НПВП-индуцированной гастропатией.
Более чем 15-летний опыт использования ИПП показал безопасность применения данных лекарственных препаратов. Вместе с тем побочные эффекты приема ИПП изредка встречаются и могут проявляться головной болью, диспептическими явлениями, абдоминальной болью, повышением печеночных трансаминаз. При этом по данным ряда исследований, наибольшее количество нежелательных явлений зарегистрировано в связи с приемом ланзопразола и эзомепразола, наименьшее – пантопразола и рабепразола (6, 12). При оценке побочных эффектов при приеме ИПП Санпраз за время наблюдения нежелательных явлений отмечено не было.
Таким образом, наш ограниченный опыт применения антисекреторного препарата Санпраз у пациентов с ГЭРБ и НПВП-индуцированной гастропатией, безусловно, не претендующий на широкие экстраполяции и обобщения, тем не менее продемонстрировал не только достаточно высокие клинические возможности препарата, но и его хорошую переносимость.
