Мы изучили обоснованность применения в терапии кашля при легком или среднетяжелом ОРЗ вследствие ларингита, ринофарингита, трахеита, бронхита комбинированного препарата Аскорил экспекторант (сальбутамол, бромгексин, гвайфенезин, рацементол) на основании клинической эффективности и безопасности у 75 детей в возрасте от 2 до 10 лет (1-я группа). Группу сравнения (2-я группа) составили 30 детей такого же возраста и со сходной клинической симптоматикой, получавших Бромгексин (в 5 мл сиропа 4 мг бромгексина гидрохлорида). Аскорил экспекторант является комбинированным препаратом, который воздействует на различные звенья патогенеза бронхолегочных заболеваний, сопровождающихся бронхиальной обструкцией, образованием трудноотделяемого вязкого секрета [6]. В 10 мл сиропа входят сальбутамол (2 мг), бромгексина гидрохлорид (4 мг), гвайфенезин (100 мг), рацементол (1 мг).
Бромгексина гидрохлорид оказывает муколитическое и отхаркивающее действие посредством деполимеризации и разрушения мукопротеинов и мукополисахаридов, входящих в состав мокроты, стимулирует деятельность секреторных клеток слизистых оболочек бронхов, продуцирующих сурфактант, который обеспечивает стабильность альвеол в процессе дыхания, защиту от неблагоприятных факторов, а также улучшение реологических свойств бронхиальной слизи [7]. Назначается внутрь 3 раза в сутки взрослым и детям старше 14 лет по 8–16 мг, детям до 14 лет и пациентам с массой тела менее 50 кг – по 8 мг; детям до 6 лет – по 4 мг. Сальбутамол является селективным β2-агонистом, оказывает бронхолитический эффект; также влияет на мукоцилиарный клиренс за счет стимуляции секреции слизи и активности реснитчатого эпителия; тормозит выброс медиаторов из тучных клеток и базофилов; устраняет антигензависимое подавление мукоцилиарного клиренса и выделение факторов хемотаксиса нейтрофилов [8, 9]. Согласно инструкции сальбутамол в ингаляциях назначается детям старше 18 мес. в дозе 2,5 мг (при необходимости – 5 мг) до 4 раз в сутки, при назначении внутрь детям 2–6 лет доза составляет 1–2 мг (0,1 мг/кг) 3–4 раза в сутки, 6–12 лет – 2 мг 3–4 раза в сутки. Максимальная доза – 24 мг/сут, детям старше 12 лет – по 2–4 мг 3–4 раза в сутки, максимальная разовая доза – 8 мг, максимальная суточная доза – 32 мг.
Гвайфенезин – эффективное отхаркивающее средство, оказывает секретолитическое и секретомоторное действие, подавляющее позывы к кашлю и частоту приступов, уменьшает беспокойство, тревожность, вегетативные нарушения в виде нейроциркуляторной астении, сердцебиений, одышки, головных болей, нарушения сна [10]. Назначается внутрь после еды 3–4 раза в сутки детям старше 12 лет по 200–400 мг, 6–12 лет – по 100–200 мг, 2–6 лет – по 50–100 мг.
Ментол (рацементол) оказывает эффект в основном вследствие рефлекторных реакций, связанных с раздражением чувствительных нервных окончаний: легкое рефлекторное сосудорасширяющее, мягкое спазмолитическое, легкое мочегонное, потогонное действие. Оказывает мягкий седативный эффект при повышенной возбудимости, нарушении сна, раздражении чувствительных рецепторов слизистых оболочек, стимулирует секрецию бронхиальных желез, обладает слабыми антисептическими свойствами вследствие неизбирательного действия на микробные клетки, уменьшает колики при метеоризме.
Пациенты получали Аскорил экспекторант 3 раза в сутки в возрастной дозировке: от 2 до 6 лет по 5 мл (1 чайная ложка), от 6 до 10 лет – по 5–10 мл (1–2 чайные ложки). Курс лечения был начат в первые сутки от начала заболевания, его продолжительность составила 7–10 дней в зависимости от динамики состояния пациентов. Детям второй группы назначался Бромгексин на такой же период. Наблюдаемые дети в обеих группах были сопоставимы по возрасту и полу. Средний возраст детей в 1-й группе составил 4 ± 2 года (мальчиков 51 (68%) и девочек 24 (32%), во 2-й группе – 4,1 ± 1,9 лет (20 (66,7%) и 10 (33,3%) соответственно). Наличие аллергического фона отмечалось в 1-й группе у 55,4% и во 2-й – у 53,3% детей. В исследование не включались пациенты, принимавшие бронхолитические, муколитические, антигистаминные препараты, ингаляционные и системные глюкокортикостероиды, другие противокашлевые препараты, а также пациенты, принимавшие антибиотики в течение предшествующих 10 дней. Врач наблюдал каждого ребенка не менее четырех-пяти раз (1, 3, 5, 7–10-й день терапии). В дневниках ежедневно регистрировалась выраженность симптомов ОРЗ (кашель, одышка, отхождение мокроты) родителями. Каждый симптом оценивался в баллах (0 – отсутствуют; 1 – слабо выражены, кратковременные, не нарушают самочувствие ребенка; 2 – умеренно выражены в течение дня, а также ночью; 3 – сильно выражены в течение дня и ночи, существенно нарушают самочувствие ребенка, аппетит, сон). Затем проводилась суммарная балльная оценка симптомов.
Всем детям проводилось исследование функции внешнего дыхания с помощью бронхофонографии (БФГ) до приема и через час после приема препаратов, а у детей старше 6 лет оценивались также показатели спирометрии. БФГ проводилась с помощью компьютерного акустического диагностического комплекса (КАДК) «Паттерн-01» (регистрационное удостоверение № ФСР 2009/04789). Принцип метода заключается в регистрации дыхательных шумов c помощью специальных микрофонов-датчиков, обладающих высокой чувствительностью в широком спектре частот, включая те частоты, которые не выявляются при аускультации, но имеют важное диагностическое значение. Компьютерный комплекс «Паттерн-01» позволяет отображать фиксируемые дыхательные шумы на экране монитора, объективно оценивать характеристики дыхательных шумов. Сканирование респираторного цикла производится в частотном диапазоне от 200 до 12 600 Гц. Выделяются три зоны частотного спектра: 200–1200 (низкочастотный диапазон), > 1200–5000 (среднечастотный диапазон) и > 5000–12 600 Гц (высокочастотный диапазон). Зо-на высоких частот (выше 5000 Гц) отражает обструктивные изменения в дыхательных путях [11, 12]. С помощью БФГ оценивались следующие параметры: частотно-амплитудные характеристики дыхательных шумов; длительность респираторного цикла; длительность и соотношение фаз выдоха и вдоха; наличие высокочастотных колебаний; акустический компонент работы дыхания (АКРД – итоговая интегральная характеристика экспираторной дыхательной волны, составляющей часть работы легких, рассчитываемая как площадь под кривой в частотно-временной области, измеряется в мкДж).
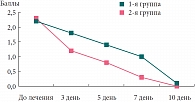
Спирография проводилась на аппарате «Spirosift-3000» (Fukuda denchi, Япония). Регистрировали форсированную жизненную емкость легких (ФЖЕЛ), объем форсированного выдоха (ОФВ) за первую секунду, пиковую скорость выдоха (ПСВ), минимальную объемную скорость на уровне 25, 50 и 75% ЖЕЛ. Мониторинг нежелательных эффектов проводился в течение всего периода наблюдения. У 40 детей 1-й группы в возрасте от 2 до 5 лет измерялись также частота сердечных сокращений, систолическое и диастолическое давление до приема препарата и через 20 и 60 минут после его приема в первый день лечения и на 7–10-й день терапии. У 10 детей одновременно проводилась запись показателей ЭКГ до приема Аскорила экспекторанта и через 20 и 60 минут после его приема в первый день лечения и на 7–10-й день терапии. У детей в 1-й группе наблюдалась более быстрая положительная динамика клинических симптомов, чем в группе сравнения. Значительное снижение тяжести симптомов дневного кашля (с 2,3 ± 0,6 до 1,0 ± 0,3 балла) отмечалось уже к 4-му дню приема Аскорила экспекторанта, а во 2-й (с 2,2 ± 0,8 до 1,0 ± 0,4 балла) – только к 7-му дню лечения; p < 0,05. Полное исчезновение симптомов дневного кашля (у 93% больных) в 1-й группе отмечалось к 6–7-му дню наблюдения, во 2-й такой же результат (у 93%) был к 9–10-му дню лечения; p < 0,05 (рис. 1).
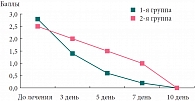
Выраженность симптомов ночного кашля до начала терапии в 1-й группе была 2,7 ± 0,7 балла, во 2-й – 2,5 ± 0,5. Значительное снижение тяжести симптомов ночного кашля (до 1,0 ± 0,4 баллов) в 1-й группе наблюдалось уже к 4-му дню приема Аскорила экспекторанта, во 2-й (до 1,0 ± 0,3 балла) – к 7-му дню лечения; p < 0,05. Полное исчезновение симптомов ночного кашля у 93% больных в 1-й группе отмечалось к 5–6-му дню наблюдения, во 2-й такой же результат (93%) был к 8–10-му дню лечения; p < 0,05 (рис. 2). У детей, получавших Аскорил экспекторант, исчезновение симптомов кашля отмечалось на 3–4 дня раньше, чем у больных в группе сравнения (p < 0,05). До начала лечения у всех детей имелись затруднения при откашливании мокроты. После назначения терапии у детей 1-й группы кашель становился влажным, наблюдалось улучшение в откашливании мокроты ко 2–3-му дню лечения, во 2-й группе – к 4–5-му (p < 0,05). При суммарной балльной оценке клинических симптомов при назначении Аскорила экспекторанта эффективность лечения была больше по сравнению с группой, в терапии которой присутствовал только муколитик (p < 0,05). Выздоровление отмечалось к 6–7-му дню лечения, у детей 2-й группы – к 9–10-му (p < 0,05).
Трем детям 1-й группы (4%) в связи с недостаточной эффективностью терапии была добавлена антибактериальная составляющая, однако необходимость ее проведения была существенно ниже, чем во 2-й группе (у 3 детей – 10%; p < 0,05). Ответ на вопрос о том, с чем связана бóльшая эффективность комбинированного препарата, мы получили при оценке функции дыхания. Согласно проведенным ранее исследованиям рост АКРД в высокочастотной части спектра (> 5 кГц) характеризует наличие обструкции бронхов [11]. Клиническое улучшение в 1-й группе сопровождалось достоверным снижением показателей АКРД в высокочастотном диапазоне, при том что они до начала лечения (> 5–12,6 кГц) достоверно превышали норму, составляя в этой группе 0,32 ± 0,16 мкДж, во 2-й – 0,29 ± 0,18 при норме 0,07 ± 0,04 мкДж (р < 0,05), что свидетельствовало о наличии у детей бронхиальной обструкции. Клинически мы регистрировали синдром легкой бронхиальной обструкции у 11 детей (15%) в 1-й группе и у 4 во 2-й (13%). Однако, как сказано выше, согласно анатомо-физиологическим особенностям бронхиальная обструкция может быть у значительно большего процента детей.
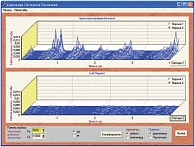
По данным БФГ мы выявили повышение АКРД в высокочастотном диапазоне (> 5–12,6 кГц) у 46 детей (62%) в 1-й группе и у 17 (57%) во 2-й. Уже в первый день приема Аскорила экспекторанта наблюдалось значительное снижение АКРД в высокочастотном диапазоне до 0,18 ± 0,08 мкДж (р < 0,05), что, по-видимому, было обусловлено наличием в препарате селективного β2-агониста. На 3–5-й день терапии бронхиальная проходимость существенно улучшилась, но показатели АКРД до приема Аскорила экспекторанта были 0,16 ± 0,05 мкДж, а при исследовании через час после приема препарата приблизились к норме (0,09 ± 0,02 мкДж). На 7–10-й день терапии показатели АКРД (0,08 ± 0,02 мкДж) были в норме уже до приема Аскорила экспекторанта и не изменялись (0,07 ± 0,03 мкДж) после приема препарата (р ± 0,05). На рис. 3 показаны паттерны дыхания больного 4 лет до и после приема Аскорила экспекторанта. До приема Аскорила экспекторанта наблюдались волновые колебания в высокочастотной части спектра (> 5–12,6 кГц) (верхний график), через 60 минут после приема препарата в 1-й день терапии отмечалось значительное улучшение бронхофонографических показателей с приближением их к норме (нижний график).
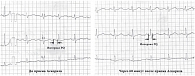
Данные БФГ у детей старше 6 лет соответствовали спирографическим показателям. До приема Аскорила экспекторанта в первый день терапии ОФВ1 был 85,7% ± 4,9%, а через час после приема препарата – 92,3 ± 3,8% (р < 0,05). В группе сравнения достоверной разницы в показателях до (87,7 ± 3,5%) и после (89,1 ± 4,8%) приема Бромгексина не было (р > 0,05). При лечении детей Аскорилом экспекторантом 96% их родителей оценили эффективность препарата как высокую. Действительно, переносимость Аскорила экспекторанта у больных была хорошей. У 1 ребенка наблюдалась аллергическая реакция на препарат в виде сыпи, у остальных детей побочных эффектов и нежелательных реакций при назначении Аскорила не было. После приема этого препарата не отмечалось достоверного изменения частоты сердечных сокращений (у 4 детей (10%) присутствовало недостоверное увеличение частоты сердечных сокращений; р ± 0,05), а также систолического и диастолического давления. Учитывая упоминание возможных нарушений ритма среди побочных эффектов β2-агонистов при ингаляционном применении, мы оценивали данные ЭКГ преимущественно у детей раннего возраста при энтеральном поступлении β2-агониста в комбинированном препарате. У наблюдавшихся детей после приема Аскорила экспекторанта не отмечалось изменений показателей ЭКГ: частоты сердечных сокращений, интервала PQ (рис. 4). Таким образом, применение комбинированного препарата эффективно при кашле вследствие ОРЗ у детей. Назначение Аскорила экспекторанта снижает длительность заболевания, уменьшает проявления бронхиальной гиперреактивности, способствует более быстрому клиническому выздоровлению, что, в свою очередь, снижает риск неадекватного использования системных антибиотиков. В рекомендуемых дозах комбинация «β2-агониста + гвайфенезин + бромгексин + рацементол» является безопасной при лечении кашля у детей.