количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Применение средств наружной терапии в лечении ограниченных форм склеродермии
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Дерматология" №2
- Аннотация
- Статья
- Ссылки
Ограниченная склеродермия (ОС) (шифр L94 по МКБ-10) – хроническое заболевание соединительной ткани, принадлежащее к семейству коллагенозов и характеризующееся формированием в коже и подлежащих тканях воспалительно-склеротических изменений ограниченного (очагового) характера, без вовлечения в процесс внутренних органов. Этиология и патогенез ОС не уточнены. Имеются предположения об инфекционном происхождении заболевания, поскольку в ряде случаев оно ассоциируется с острыми и хроническими инфекциями, что не исключает роли наследственных факторов, генетически обусловленных детерминант, эндокринопатий, аутоиммунных патогенетических процессов. Таким образом, склеродермия в целом и ОС в частности могут быть отнесены к мультифакторным заболеваниям, в которых значение отдельных факторов, инициирующих либо промотирующих, не может быть четко определено.
Ключевую роль в патогенезе данного дерматоза играют аутоиммунные реакции к коллагену, возникающие вследствие высокого уровня антигенной коллагеновой стимуляции.

Таблица 1. Последовательность обследования больных

Таблица 2. Распределение больных по группам сравнения
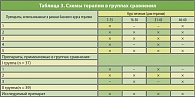
Таблица 3. Схемы терапии в группах сравнения

Таблица 4. Изменения горизонтальных размеров (площади) очагов поражения в группах в зависимости от используемого средства наружной терапии

Таблица 5. Изменения толщины (вертикальных границ) индуративных очагов поражения в группах в зависимости от используемого средства наружной терапии (по данным УЗ-морфометрии, гистомикрометрии)

Таблица 6. Оценка влияния используемого средства наружной терапии на величину показателя плотности очага поражения (по данным соноэластографии)

Таблица 7. Совокупная оценка степени выраженности индурации (глубина инвазии + интенсивность) до и после лечения

Таблица 8. Изменения показателей интенсивности эритемы в очагах ОС в зависимости от используемого средства наружной терапии на основании различия цветовых характеристик зоны поражения до и после лечения (по данным колориметрии)

Таблица 9. Изменения показателей интенсивности кровотока в зоне поражения в зависимости от используемого средства наружной терапии до и после лечения (по данным ЛДФ)

Таблица 10. Глобальная оценка терапевтического эффекта в группах сравнения

Таблица 11. Побочные эффекты терапии в группах наблюдения

Таблица 12. Анализ силы влияния использованного метода терапии (препарата) на качество жизни пациентов в группах сравнения (ДИКЖ до и после лечения)

Таблица 13. Оценка потребительских свойств препаратов наружного применения в группах сравнения
Инспирируемые ими функциональные изменения деятельности фибробластов и других коллагенобразующих клеток приводят к глубоким нарушениям внутриклеточного метаболизма коллагена. Об этом свидетельствуют данные, демонстрирующие высокой уровень цитотоксической активности сывороток больных в отношении фибробластов, величины титров антинуклеарных антител, дисиммуноглобулинемия и пр. (1). Для лечения ОС представляется весьма перспективным применение отечественного препарата Эгаллохит (галадерм), активной субстанцией которого является 10% эпигаллокатехин-3-галлат.
Клинически различают две формы ОС – бляшечную (sclerodermia en plaque, morfea) и линейную (sclerodermia en band, sclerodermia en coup de sabre). Иногда в качестве отдельных форм или разновидностей ОС рассматривают так называемую поверхностную (каплевидную) склеродермию – склероатрофический лихен, белый лишай Цимбуша (lichen albus Zumbusch), идиопатическую атрофодермию Пазини Пьерини, склередерму новорожденных, склередерму взрослых Бушке (scleroederma adultorum Buschke) и пр.
Клиническая картина ОС вполне характерна. В классическом варианте течения болезни очаги поражения в своем развитии проходят 3 стадии: пятна, бляшки, атрофии (4). Процесс начинается с появления одного (реже – нескольких) розовато-красного с фиолетовым оттенком пятна, почти без уплотнения, округлой или овальной формы, с сиреневым ободком по периферии, за более или менее продолжительное время достигающего размеров ладони и более (стадия 1 – пятна, эритематозная). В дальнейшем в центре пятна формируется уплотнение, которое может быть поверхностным либо проникающим глубоко в дерму, иногда до фасций и мышц. Вскоре очаг превращается в плотную (деревянистой консистенции) бляшку характерного желтовато-белого цвета с гладкой поверхностью, напоминающей слоновую кость. В таком состоянии он может сохраняться без видимых изменений месяцами и годами (стадия 2 – бляшки, индуративная). Поздняя эволюция очагов состоит в исчезновении сиреневого кольца, постепенном размягчении и рассасывании уплотнения от центра к периферии, в результате чего центр бляшки начинает западать, а вскоре и весь очаг превращается в участок атрофии (стадия 3 – атрофия). Имеются наблюдения, когда при рано начатом и адекватном лечении очаг бляшечной склеродермии может исчезнуть, не оставляя атрофии.
В нетипичных случаях исходом процесса может явиться формирование в зоне поражений плотной грубой рубцовой ткани по типу гипертрофического или келоидного рубца – «келоидоподобная склеродермия», отложение в коже извести, изъязвление очага, малигнизация.
Несмотря на очевидный прогресс в изучении склеродермии, в целом, вопросы профилактики рецидивов, трудоспособности и качества жизни больных с ОС по-прежнему нуждаются в анализе и разработке (6). Существует мнение о том, что ОС, в особенности бляшечная форма болезни, является достаточно редкой, изолированной патологией с благоприятным течением и прогнозом, мало влияющей на качество жизни пациентов, уровень их социальной и профессиональной адаптации. Вместе с тем, по мнению ряда исследователей, вероятность трансформации ОС в системную склеродермию составляет до 40%, а распространенность данного дерматоза такова, что доля его в структуре дерматологической патологии достигает 1% и имеет неуклонную тенденцию к росту (1, 2).
Даже при наличии потенциальных возможностей раннего выявления, полноценной диагностики и адекватной терапии диагноз «бляшечной склеродермии» нередко устанавливается с большим опозданием. Этому способствует ряд обстоятельств, в частности, сложность, многоэтапность диагностики и терапии, преимущественная ориентированность лечебных мероприятий на воспрепятствование и исключение предпосылок к приобретению процессом системного характера. Они сложны, дорогостоящи, инвазивны (инъекции, местные обкалывания, электро- и фонофорез, УФА и ПУВА-терапия и пр.), имеют ряд серьезных противопоказаний, могут быть выполнены только в условиях стационара, а потому ограничены по времени, подразумевают под собой необходимость госпитализации, отказа от бытовой и профессиональной деятельности. Местные же процедуры в виде мазей и аппликаций, в основном, гормоносодержащих (мометазон, гидрокортизон, метилпреднизолон и пр.), пугают пациентов приобретением зависимости, заставляя уклоняться от выполнений данных рекомендаций врача. Следствием этого становятся рецидивирование и прогрессирование заболевания, повторные, по истечении месяцев и лет обращения к специалистам, когда и диагноз, и прогноз уже однозначно неблагоприятны и свидетельствуют о наличии тяжелого терапевтического недуга из группы коллагенозов (6). В сложившихся условиях очевидна необходимость поиска новых препаратов и лекарственных форм, применение которых в создавшихся условиях являлось бы адекватной альтернативой уже имеющимся средствам и отвечало бы следующим требованиям: патогенетическая направленность терапии, безопасность, удобство и простота применения, возможность длительного использования в амбулаторных условиях.
В этом смысле применение оте-чественного препарата «Эгаллохит» (Галадерм), активной субстанцией которого является 10% эпигаллокатехин-3-галлат, представляется весьма перспективным. Механизмы действия данного препарата, направленные на основные звенья патогенеза патологического рубцевания, а именно: влияние на активность факторов роста, особенно VEGF, синтез и метаболизм коллагена, подавление синтеза цитокинов (ИЛ-1, 6, 8; ФНО-α, циклооксигеназы второго типа и простагландинов), поглощение пероксидных радикалов, снижение уровня чувствительности рецепторов клетки к Ig E и пр., дают основание к предположению о патогенетической обоснованности использования его при лечении склеродермии. Тем более, благодаря своей безопасности и эффективности, подтвержденной клиническими исследованиями, данный препарат давно и широко применяется как средство предотвращения патологического рубцевания после пластических операций, лазерных шлифовок кожи, фотодинамической терапии и пр., а также используется в комплексной терапии уже имеющихся гипертрофических, келоидных и атрофических рубцов совместно с инъекционной, лучевой терапией и другими методами (5).
В связи с этим целью настоящей работы явилось научно–практическое обоснование целесообразности применения крема (геля) «Эгаллохит» в комплексной терапии ОС как патогенетически оправданного неинвазивного средства лечения. В ходе исследования были поставлены и нашли свое решение следующие задачи:
- сравнительная оценка кожного статуса в очагах склеродермии до и после лечения: площадь эритемы и индурации кожи; выраженность индурации (плотность и вертикальные размеры зоны поражения), степень интенсивности эритемы;
- сравнительный анализ клинической эффективности применения изучаемого препарата и традиционных препаратов наружного применения в группах сравнения;
- сравнительная оценка безопасности и переносимости традиционных препаратов местного применения и изучаемого препарата при лечении ограниченных форм склеродермии;
- оценка психосоматического статуса у больных с ОС до и после лечения. Анализ силы влияния различных по своей природе средств наружной терапии на уровень и качество физического, психического, социального и ролевого или функционально-ассоциированного образа жизни индивидуума;
- изучение реакции и отношения пациентов на использование нового для них средства наружной терапии хронического дерматоза.
Построенное в рамках программы клинических испытаний на предмет оценки применимости и безопасности выше обозначенного препарата в сравнении с традиционно используемыми наружным средствами данное исследование осуществлялось в группах пациентов с использованием следующих клинических критериев эффективности терапии:
влияние используемых средств терапии на выраженность основных клинических признаков патологического процесса (критерий 1);
- терапевтический эффект (ГОТЭ) (вариант адаптации применительно к условиям данного исследования) (критерий 2);
- частота возникновения побочных эффектов терапии (критерий 3);
- качество жизни пациентов в группах сравнения (ДИКЖ) (критерий 4);
- потребительские свойства препарата «Эгаллохит» (критерий 5).
Объект, объем, материалы и методы исследования
Работа выполнялась в течение 2008-2009 гг. сотрудниками Северо-Западного центра лазерной хирургии кожи на базе кафедры кожных и венерических болезней СПбГМА им. И.И. Мечникова.
Объектом исследования стали амбулаторные больные в количестве 76 лиц мужского (21 случай наблюдения) и женского (55 случаев наблюдения) пола в возрасте от 18 до 69 лет (средний возраст 39,5 ± 3,4 года), страдающие ОС (бляшечная форма), имевшие очаги поражения 1 (эритематозной) и 2 (индуративной) стадии, не имевшие признаков системности процесса с продолжительностью заболевания от 3 мес. до 20 лет. Ввиду критического сокращения числа участников испытания вследствие использования критериев включения (исключения), в качестве альтернативного рандомизации способа распределения участников по группам наблюдения был использован метод минимизации как единственно способный обеспечить сопоставимость групп по признакам, предположительно влияющим на исход терапии (пол, возраст, продолжительность, клиническая форма заболевания и пр.). Таким образом, при распределении участников по группам наблюдения были сформированы 2 равноценные группы сравнения: группа I (контрольная) и группа II (таблица 2). Значимых различий в степени выраженности оцениваемых клинических проявлений заболевания – эритемы, индурации, площади поражения кожи и пр., а также существенных расхождений в оценке качества жизни на долечебном этапе у представителей обеих групп отмечено не было – исходные показатели в группах сравнения статистически значимо не различаются, p < 0,05; (см. таблицу. 4 – 9, 12).
В целях верификации диагноза в комплекс предварительных диагностических мероприятий, наряду со сбором анамнеза и физикальным обследованием, были включены обязательные исследования, выполненные в соответствии с ныне действующими рекомендациями по диагностике ОС (3, 7).
В качестве используемых методов лечения применялись:
Общая терапия ОС, применя-емая ко всем участникам клинических испытаний (базовый курс).
Препарат 1 – бензилпенициллина натриевая соль в/м по 1 млн ЕД 2 раза в сутки, 15 дней, 2 курса с интервалом в 30 дней.
Препарат 2 – гиалуронидаза в/м по 64 УЕ 1 раз в сутки через день, № 30.
Препарат 3 – пентоксифиллин внутрь по 400 мг 1-2 раза в сутки ежедневно, 60 дней.
Препарат 4 – депротеинизированный гемодериват из крови телят (Актовегин) в/м по 5 мл ежедневно, 15 дней, 2 курса с интервалом в 15 дней.
Препарат 5 – α-токоферола ацетат внутрь по 200 мг 2 раза в сутки ежедневно, 60 дней.
Местная терапия ОС, применяемая в зависимости от принадлежности участников к группе сравнения.
В I группе:
Препарат 1 – гидрокортизона бутират – аппликации или окклюзионные повязки 1 раз в сутки, 15 дней, 2 курса с интервалом в 15 дней.
Препарат 2 – депротеинизированный гемолизат из крови телят (Солкосерил) мазь 5% 2 раза в сутки ежедневно, 60 дней.
Препарат 3 – гепарин натрия + бензокаин + бензилникотинат (мазь) 2 раза в сутки 15 дней, 2 курса с интервалом в 15 дней.
Во II группе:
Изучаемый препарат – крем (гель) «Эгаллохит» (Галадерм) – 10% эпигаллокатехин-3-галлат; 2 раза в сутки ежедневно, 60 дней (таблица 3).
В качестве методов инструментальной (аппаратной) диагностики были использованы:
- бинокулярная дистанционная дермоскопия, дигитальная фотосъемка, фотопротокол с последующим вычислением площадей поражения на основании их графических TIFF-изображений с использованием программы Data Master 2000 (© 1993, 2003 RRR), предназначенной для визуального редактирования и численной обработки данных;
- ультрасонография, УЗ-мор-фометрия, трепанационная биопсия, ультразвуковая денсиметрия, гистомикрометрия (выборочно);
- дигитальная видео- и фотосъемка, фиксация изображений в формате TIFF с последующей обработкой компьютерными методами, включающими в себя анализ цветовых характеристик (колориметрия) объекта;
- лазерная доплеровская флоуметрия (ЛДФ). Анализ изменений степени интенсивности кровотока в сосудах кожи в очаге поражения и за его пределами до и после лечения.
Методы получения информации: данные клинического наблюдения, анкетирование (таблица 1). Методики – самостоятельное заполнение универсальной формы стандартного опросника, представляющего собой русифицированную версию Dermatology Life Quality Index (DLQI) и опросника, содержащего вопросы, оценива-ющие используемый препарат.
При выборе статистических процедур для регистрации достоверности полученных результатов были учтены методологические требования Международного конгресса по гармонизации GCP («Статистические принципы для клинических исследований»; ICH Guidelines. Good Clin Pract J 1998). Обработку полученных данных проводили с использованием общепринятых методов параметрической и непараметрической статистики с использованием пакетов прикладных программ для статистического анализа: «Excel» и «Statistica 6.0».
Результаты и обсуждение
1. Анализ влияния используемого средства наружной терапии на величину площади очагов поражения (таблица 4) продемонстрировал положительную динамику у пациентов в обеих группах. Однако сила влияния метода терапии на оцениваемый клинический признак патологического процесса оказалась различной. Так, у пациентов I группы наблюдения использование заявленных препаратов в совокупности привело к сокращению площадей поражения на 56% и к моменту окончания исследования составило 44% от исходного уровня, что может быть интерпретировано лишь как клинически значимый позитивный результат (p > 0,05). В то же время, у пациентов II группы наблюдения отмечалось более выраженное сокращение величины исследуемого параметра – до 19% от исходного уровня (p < 0,001), что является не только клинически, но и статистически значимым показателем эффективности примененного метода лечения. Кроме того во II группе интенсивность снижения величины изучаемого параметра была более выраженной, нежели в I группе. Так, статистически значимое сокращение показателя площади поражения отмечалось уже к 45 дню исследования (4 контрольный пункт наблюдения).
2. Анализ влияния используемого метода терапии (препарата) на изменение величины вертикальных границ очага поражения (таблица 5) выявил факт отсутствия в группе I статистически значимых различий показателя глубины инвазии в контрольных точках регистрации за весь период наблюдения (p > 0,05), наряду с чем у пациентов группы II наблюдалась выраженное, клинически значимое сокращение величины данного параметра (до 24% от исходного уровня) и статистически значимое уменьшение его абсолютной величины в конечной точке регистрации по сравнению с исходным уровнем (p < 0,001).
3. При оценке влияния метода терапии на величину показателя плотности очага поражения (таблица 6) были установлены вполне отчетливые различия результатов в группах наблюдения.
Так, несмотря на положительную в целом динамику процесса, у пациентов группы I в заключительном пункте регистрации сохранялись статистически значимые (p < 0,05) различия величины изучаемого параметра относительно контрольной группы при отсутствии таковых по сравнению с исходными показателями (p > 0,05).
Во II же группе, напротив, удалось констатировать достоверное, клинически и статистически значимое (p < 0,05) сокращение абсолютной и относительной величины изучаемого параметра в конечной точке регистрации, а так же отсутствие значимых различий данных показателей относительно контрольной группы наблюдения.
4. Интеграционный анализ, суммирующий результаты динамики показателей индурации в процессе лечения, в целом, подтвердил мнение о более высокой эффективности метода (препарата) терапии, использованного пациентами группы наблюдения II (таблица 7). Сила влияния его на выраженность изучаемого клинического признака оказалась достоверно более высокой, нежели препаратов, использованных больными I группы.
Свидетельством этого может служить средняя величина совокупного показателя (балла) интенсивности индурации в конечной точке регистрации (после лечения), равного 0,5, статистически значимо (p < 0,05) отличающегося от такового в группе I (1, 6) и исходных значений (2, 7) до лечения (p < 0,001).
5. Получены данные, свидетельствующие о выраженном влиянии обоих методов лечения на интенсивность эритемы, что подтверждается статистически значимыми различиями величин оцениваемых показателей во всех контрольных точках регистрации относительно исходного уровня (таблица 8). Несмотря на отсутствие достоверных свидетельств большей эффективности метода (препарата), использовавшегося в группе II (отсутствие статистически значимых различий величин сравниваемых показателей после лечения, (p > 0,05)), клинические преимущества его очевидны. Основаниями для данного вывода являются статистически значимые различия величин оцениваемых показателей в промежуточной контрольной точке регистрации, а также отчетливо более выраженное и клинически значимое снижение интенсивности эритемы (до 10% от исходного уровня) по завершении курса терапии.
6. При исследовании базовых показателей ЛДФ у пациентов, страдающих ОС, в зависимости от фазы развития очага поражения (эритематозная/индуративная), изменения носили разнонаправленный характер. Так, в индуративных очагах, до лечения, ПМ оказался достоверно более чем на 2σ ниже, чем в контрольной группе и колебался в диапазоне от 4,55 до 5,75 пф. ед., что соответствовало картине ангиоспастического синдрома. Резкое снижение ПМ, подавление амплитуд всех видов ритмов кровотока по сравнению с контрольной группой позволил интерпретировать данные показатели двумя возможными вариантами: стазический или смешанный, стазический-спастический тип нарушения микрогемодинамики (классиф. В.И. Маколкин и соавт., 1999 г.). В эритематозных очагах поражения ПМ был зарегистрирован на уровне, в 1,5 раза превышающем средние значения в контрольной группе и составлял величины в пределах от 23,8 до 25,1 пф. ед. (в норме – 16,7 ± 1,5), что соответствовало картине периферического ангиодистонического синдрома, с характерным и типичным гиперемическим типом нарушения микроциркуляции. Таким образом, у всех больных до лечения имелись выраженные, клинически и статистически достоверные изменения показателей кровотока в очагах поражения, в основном обусловленные депрессией медленных ритмов кровотока, характеризующих нейрогенный и миогенный тонус, а также признаки микроциркуляторного стаза, являющегося свидетельством наличия внутрисосудистых изменений (нарушения реологических свойств крови, агрегации форменных элементов, сладж-синдрома). В результате проведенного лечения у пациентов обеих групп сравнения удалось констатировать более или менее выраженные позитивные изменения ПМ. Однако в I группе наблюдения они могли быть расценены лишь как клинически значимые (различия показателей с контрольной группой статистически недостоверно (p ≥ 0,05), в то время как во II группе отмечалось достоверное, статистически значимое улучшение базовых показателей М, σ и Кv, в финальных измерениях не отличавшихся от таковых в контрольной группе.
7. Сравнительный анализ эффективности лечения ограниченных форм склеродермии в зависимости от используемого средства наружной терапии выявил явные преимущества метода лечения (препарата), использованного во II группе наблюдения. Свидетельством этого явились результаты глобальной оценки терапевтического эффекта (индекс ГОТЭ).
Согласно полученным данным, величина данного показателя в II группе составила 1,97 балла, тогда как в I группе лишь 1,41 балла (таблица 10). При этом состояние клинического выздоровления (уменьшение выраженности клинического признака от 75% и выше от исходного уровня) было зарегистрировано у 8 (20,5%), значительного улучшения (уменьшение выраженности клинического признака от 50% до 75% от исходного уровня) – у 23 (59,0%) пациентов II группы. В то же время в группе I доля лиц с подобным результатом оказалась почти в 2 раза меньше (5,4% и 37,8% соответственно). Доля пациентов с отличным и хорошим результатом лечения была статистически значимо выше во II группе (p = 0,0012 по критерию x²). Это, в свою очередь, позволяет говорить о наличии прямой положительной корреляционной связи между результатами оценки динамики клинических проявлений заболевания и данными ГОТЭ.
8. Сравнительная оценка безопасности и переносимости препаратов местного применения, использованных при лечении ОС, представленная на основании показателя «частота развития нежелательных побочных эффектов терапии» выявила существенные различия величины данного показателя в группах сравнения (таблица 11).
Полученные результаты свидетельствуют как о большем числе возможных вариантов осложнений, возникших у представителей группы I (10 против 4), так и о большей частоте случаев их регистрации (14 против 5) по сравнению со II группой.
Полученные результаты свидетельствуют как о большем числе возможных вариантов осложнений, возникших у представителей группы I (10 против 4), так и о большей частоте случаев их регистрации (14 против 5) по сравнению со II группой.
Существенно большее абсолютное количество случаев регистрации нежелательных побочных эффектов терапии и значимо больший удельный вес случаев применения метода лечения (препарата), осложненных развитием побочных эффектов в I группе (37,8% против 12,8%, p = 0,0118 по критерию x²), дает основания к выводу о значительно лучшей переносимости и большей безопасности метода лечения (препарата), использованного во II группе сравнения.
9. Детальный анализ ДИКЖ, проведенный по 6 основным разделам, показал наличие клинически значимых различий в оценке качества жизни до и после проведенного лечения абсолютным большинством пациентов в обеих группах наблюдения (таблица 12). Исключением из этого явились различия в оценке степени влияния на данный показатель метода терапии (раздел 6).
Так, если больные I группы с учетом предшествующего опыта лечения не изменили своего отношения к нему и после настоящих клинических испытаний (средний балл до и после лечения составил 2,1 ± 0,8 и 2,1 ± 1,1 соответственно), то у больных II группы можно констатировать явные позитивные сдвиги в оценке влияния терапии на качество их жизни (2,3 ± 0,7 балла – до лечения и 1,2 ± 0,5 балла – после лечения). Несмотря на отсутствие достоверных различий цифровых значений показателя качества жизни до и после лечения по 4 из 6 разделов, у пациентов в обеих группах наблюдения зарегистрировано статистически значимое снижение совокупного показателя (индекса) качества жизни после проведенной терапии: в I группе с 12,2 ± 1,3 балла до 6,9 ± 0,6 балла (p < 0,05); во II группе – с 12,0 ± 1,0 баллов до 3,7 ± 0,3 балла (p < 0,001), что можно интерпретировать как почти двукратное улучшение качества жизни по критерию ДИКЖ (43,4%) у больных в I группе и почти трехкратное (69,2%) – у больных во II группе.
10. При сравнительном анализе потребительских свойств лекарственных форм крема (геля) «Эгаллохит», реализованном посредством заполнения индивидуальной карты-опросника, выдаваемой каждому участвующему в исследовании респонденту, были получены следующие данные.
Респонденты, принадлежавшие к II группе, значительно реже (в 12,8% случаев), нежели представители I группы (37,8%), акцентировали внимание на наличии нежелательных побочных эффектов лечения. Существенно реже (лишь в 7,7% против 73,0% случаев) предъявляли претензии к удобству применения препарата. Объективно реже (в 17,9% против 43,2% случаев, p = 0,0061 по критерию x²) изъявляли дополнительные пожелания во время лечения. Значимо чаще, нежели их оппоненты (в 87,2% против 59,5% случаев), позитивно оценивали результаты терапии (таблица 13).
Выводы
Препарат Эгаллохит (галадерм), использованный в качестве средства наружной терапии у пациентов с бляшечной формой ОС, продемонстрировал значительно более высокий уровень эффективности, нежели традиционно применяемые в этих целях препараты.
Об этом свидетельствуют результаты клинических наблюдений в группах сравнения, позволяющие констатировать факт значительного сокращения числа и степени выраженности клинических проявлений заболевания на фоне его применения:
- значительное, до 19% от исход-ного уровня, сокращение горизонтальных размеров (площадей) очагов поражения в основной группе против 44% в группе сравнения;
- выраженное, до 24% от исходного уровня, уменьшение вертикальных границ (глубины инвазии) индуративных очагов поражения в основной группе против 67% в группе сравнения;
- достоверное в основной группе наблюдения снижение плотности (интенсивности индурации) тканей в очагах поражения (с 2,7 баллов до 0,5 баллов), что на момент завершения терапии оказалось сопоставимым с таковой у здоровых лиц и статистически значимо отличалось от аналогичных показателей (1,6 балла) в группе сравнения;
- клинически более выраженное (при отсутствии статистически значимых различий), нежели в группе сравнения, снижение показателей интенсивности эритемы у пациентов основной группы (до 20,7% против 39,3% от исходного уровня);
- достоверное, статистически значимое улучшение у пациентов основной группы наблюдения, изменения базовых показателей микроциркуляции крови в очагах поражения (М, σ и Кv), которые в результате лечения перестали отличаться от таковых у здоровых лиц. Эти наблюдения являются так же косвенным свидетельством патогенетической обоснованности применения препарата «Эгаллохит» при данном заболевании;
- существенно большая величина индекса ГОТЭ, составившая в основной группе 1,97 балла против 1,41 балла в группе сравнения;
- существенно меньшее число случаев регистрации нежелательных побочных эффектов терапии в основной группе наблюдения – 4 против 10 – в группе сравнения, а так же значимо меньший показатель частоты возникновения осложнений, который при использовании данного препарата составил 12,8% против 37,8% при применении традиционных средств терапии;
- статистически значимое, на 69,2% (с 12,0 ± 1,0 баллов до 3,7 ± 0,3 балла) снижение совокупного показателя (индекса) качества жизни больных основной группы против 43,4% (с 12,2 ± 1,3 балла до 6,9 ± 0,6 балла) в группе сравнения.
Заключение
Все выше изложенное, а также признание факта удобства применения изучаемого препарата 36 из 39 (92,3%) респондентами, невысокая частота выявления нежелательных побочных эффектов лечения, зарегистрированная у 5 из 39 (12,8%) пациентов, незначительность претензий и дополнительных пожеланий во время лечения, возникшая у 7 из 39 (17,9%) опрашиваемых, высокая степень позитивности в оценке результатов терапии, отмечаемая в 87,2% случаев наблюдений, является достаточным основанием к положительному заключению об эффективности, безопасности и переносимости препарата Эгаллохит (галадерм) при использовании его в качестве средства наружной терапии у пациентов с бляшечной формой ОС. Отмеченная, по результатам проведенных исследований, высокая степень патогенетической обоснованности и применимости, а также положительная оценка потребительских свойств позволяют рассматривать данную лекарственную форму как перспективное средство в комплексной терапии ограниченных форм склеродермии.
1. Дворников А.С., Круглова Л.С. // Клин. дерматол. и венерол. 2008. № 2. С. 58-62.
2. Дифференциальная диагностика кожных болезней. Руководство для врачей / Под ред. проф. Б.А. Беренбейна, проф. А.А. Студницина. 2-е изд. М., 1989. С. 454-464.
3. Клинические рекомендации. Дерматовенерология. / Под ред. А.А. Кубановой. М.: ДЭКС-Пресс, 2007. С. 106-116.
4. Кожные и венерические болезни: справочник / Под ред. проф. О.Л. Иванова. М., 1997. С. 273-275.
5. Применение препарата Галадерм для профилактики патологического рубцевания. // Клин. дерматол. и венерол. 2009. № 4. С. 80-82.
6. Романенко Г.Х., Покхарел Арбинд. Показания к проведению реабилитационных мероприятий у больных склеродермией с элементами системности // Рос. журн. кож. и вен. бол. 2007. № 5. С. 28-31.
7. Современные клинические рекомендации. Дерматовенерология / Под ред. А.А. Кубановой. М.: ГЭОТАР-Медиа. 2006-2007. С. 75-91
СТАТЬИ по теме
04.10.2010
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
