Продолжительность терапии Герцептином при HER2-позитивном раке молочной железы
- Аннотация
- Статья
- Ссылки



![Таблица 4. Трастузумаб: механизмы действия и резистентности [3]](/upload/resize_cache/iblock/9e6/195_350_1/9e6ecd41ca033ec1ed5494afc05e559d.png)


Лиганды к HER2 пока еще не идентифицированы. Предполагается, что он участвует в процессе димеризации в качестве корецептора, образуя гетеродимеры с другими представителями семейства EGFR. Помимо этого HER2, обладая конститутивной активностью, может принимать участие в лиганд-независимой гомо- или гетеродимеризации. Полагают, что HER2 является наиболее частым партнером для димеризации со всеми другими рецепторами, включая HER3. В отличие от других EGFR, HER3-рецептор не обладает собственной тирозинкиназной активностью, и для генерации сигнала ему необходима гетеродимеризация.
Кроме того, он содержит по крайней мере 6 доменов для связывания с регуляторной субъединицей PI3K: p85 и является наиболее мощным из всех EGFR активатором PI3K-пути. HER3 играет важную роль в реализации биологической активности HER2. Появились экспериментальные данные о том, что клеточные линии РМЖ, экспрессирующие как HER2-, так и HER3-рецепторы, обладают более высокой степенью фосфорилирования Akt. По данным некоторых исследований, гиперэкспрессия HER3 ассоциирована с плохим прогнозом и снижением выживаемости больных [1].
Основным механизмом гиперэкспрессии белка HER2 считается амплификация гена. Известно, что экспрессия HER2 способствует канцерогенезу. Так, в экспериментальных исследованиях показано, что трансфекция HER2 в эпителиальные клетки молочной железы индуцирует опухолевую трансформацию. Однако для стимуляции клеточной пролиферации РМЖ рецептору HER2 необходим HER3, что подчеркивает значимость гетеродимерного комплекса HER2/HER3 [2].
С развитием и прогрессированием РМЖ связана также активация рецепторов инсулиноподобного фактора роста 1 (IGF-1R). IGF-1R также относится к числу тирозинкиназных рецепторов, связываясь с IGF-1 и IGF-2, он регулирует клеточную пролиферацию и выживание. Существуют доказательства перекрестного взаимодействия между путями проведения сигнала, активированными семейством EGFR и IGF-1R. Так, в клетках РМЖ, резистентных к трастузумабу, выявлена гетеродимеризация между IGF-1R и HER2, что может являться одной из причин резистентности [1].
Внедрение в клиническую практику трастузумаба (Герцептин) – гуманизированного моноклонального антитела к экстрацеллюлярному домену белка HER2 – кардинально повлияло на выживаемость пациенток с HER2-положительным РМЖ, существенно улучшив как непосредственные, так и отдаленные результаты лечения.
Трастузумаб. Механизм противоопухолевого действия
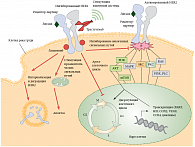
Трастузумаб обладает комплексным механизмом противоопухолевого действия, который обусловлен блокадой внутриклеточных путей передачи сигнала, которые запускает HER2, а также стимуляцией противоопухолевого иммунного ответа (рис. 1) [3]. В результате клинических исследований доказаны следующие эффекты трастузумаба:
- промотирует интернализацию и деградацию HER2;
- подавляет пролиферацию и восстанавливает способность опухолевых клеток к апоптозу за счет блокады PI3K/Akt сигнального пути, которая также обусловливает синергизм трастузумаба с химиотерапией;
- ингибирует HER2-регулируемый ангиогенез;
- предотвращает формирование HER2p95 – транкированной активной формы HER2-рецептора, которая характеризуется отсутствием экстрацеллюлярного домена при наличии тирозинкиназной активности, ингибируя таким образом развитие опухоли;
- индуцирует противоопухолевый иммунный ответ за счет активации антителозависимой клеточной цитотоксичности. В структуре трастузумаба, который представляет собой иммуноглобулин подкласса G1, присутствует домен Fc. Именно его распознают эффекторные клетки иммунной системы, экспрессирующие рецептор Fcγ. Вследствие связывания естественных киллеров с доменом Fc трастузумаба происходит лизис опухолевой клетки.
Эффективность лечения трастузумабом при диссеминированном HER2-позитивном раке молочной железы
Клинические исследования показали, что при диссеминированном HER2-позитивном РМЖ монотерапия трастузумабом эффективна как в первой, так и в последующих линиях лечения (табл. 2). В таблице 3 представлены результаты рандомизированных исследований, в которых сравнивалась эффективность таксанов и их комбинации с трастузумабом в первой линии лечения HER2-положительного рака молочной железы. По сравнению со стандартной химиотерапией (ХТ) (табл. 3) и монотерапией трастузумабом (табл. 2) использование комбинации трастузумаба с цитостатиками достоверно повышает эффективность первой линии лечения HER2-положительного рака молочной железы.
В последующих клинических исследованиях было показано, что трастузумаб хорошо переносим и эффективен в комбинации с винорельбином, платиновыми производными, капецитабином, гемцитабином, ингибиторами ароматазы [9]. Добавление карбоплатина [10] или капецитабина [11] к комбинации трастузумаба с доцетакселом не привело к повышению эффективности лечения, за исключением достоверного увеличения медианы времени до прогрессирования болезни с 12,8 до 17,9 мес. при использовании трехкомпонентного режима с капецитабином. Добавление паклитаксела к комбинации Герцептина с карбоплатином позволило повысить частоту достижения объективного эффекта с 36 до 52% (p = 0,04), медианы времени до прогрессирования болезни с 7,1 до 10,7 мес. (p = 0,03) без увеличения медианы продолжительности жизни (32,2 и 35,7 мес., p = 0,73) больных [12].
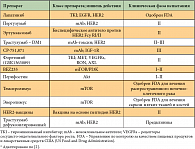
В настоящее время Герцептин является стандартом как адъювантной терапии, так и терапии первой линии HER2-позитивного РМЖ. Трастузумаб обычно назначают до прогрессирования болезни, которое неизбежно наступает вследствие развития резистентности опухоли к лекарственным препаратам. Механизмы развития резистентности представлены в таблице 4. Вопрос о дальнейшей терапевтической тактике HER2-позитивного РМЖ весьма актуален, особенно в лечении метастатических форм.
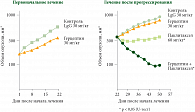
Имеет ли смысл продолжать введение Герцептина после регистрации прогрессирования болезни? Этот вопрос был исследован в эксперименте на перевиваемых опухолях HER2-позитивного РМЖ (рис. 2). После развития резистентности опухоли к Герцептину максимальное подавление опухолевого роста вызывала комбинация Герцептина с паклитакселом, паклитаксел в монорежиме был достоверно менее эффективен [13]. Экспериментальные данные были подтверждены в небольшом клиническом исследовании GBG-26/BIG03-06, посвященном сравнительному изучению эффективности капецитабина в монорежиме или в комбинации с Герцептином при диссеминированном HER2-позитивном РМЖ, резистентном к терапии первой линии Герцептином в комбинации с ХТ [14].
В исследование было включено 156 пациенток, 78 из которых после рандомизации была назначена терапия Кселодой в стандартном режиме (Х), другим 78 – Кселодой на фоне продолжения введения Герцептина (Х + Н). Основной целью исследования было сравнение времени до прогрессирования болезни. Комбинация Кселоды с Герцептином по сравнению с монотерапией Кселодой привела к увеличению медианы времени до прогрессирования болезни с 5,6 до 8,2 мес. (HR = 0,69; 95% ДИ 0,48–0,97; двухсторонний log-rank p = 0,0338), повышению частоты достижения объективного эффекта с 27,0 до 48,1% (OR = 2,50; p = 0,0115) и контроля роста опухоли, включающего частоту объективного эффекта и стабилизации болезни длительностью более 24 недель, с 54,1 до 75,3% (p = 0,0068). Медиана общей выживаемости больных на фоне лечения капецитабином и Герцептином составила 25,5 мес., на фоне капецитабина в монорежиме – 20,4 мес. (p = 0,257).
Другое рандомизированное исследование III фазы EGF 104-900, в которое было включено 296 пациенток с HER2-позитивным РМЖ, резистентным к Герцептину, было посвящено изучению эффективности «максимальной» HER2-блокады [15, 16]. Выбор лечения осуществлялся путем рандомизации, после которой больные получали либо тирозинкиназный ингибитор HER1- и HER2-рецепторов лапатиниб в стандартной дозе 1500 мг/день, либо лапатиниб по 1000 мг/день на фоне продолжения еженедельного введения трастузумаба. Главной целью исследования было сравнение выживаемости больных без прогрессирования болезни. Согласно результатам исследования, комбинация двух таргетных препаратов является достоверно более эффективной, чем монотерапия лапатинибом. Медиана выживаемости больных без прогрессирования болезни, получавших лапатиниб на фоне продолжения введения трастузумаба, составила 12,0 недель, у больных на монотерапии лапатинибом – 8,1 недели (HR = 0,73; 95% ДИ 0,57–0,93; p = 0,008), объективный эффект – 10 и 7%, медиана общей выживаемости – 52 и 39 недель соответственно, хотя разница была статистически недостоверной.
Таким образом, результаты обоих клинических исследований свидетельствуют о том, что после наступления прогрессирования на фоне лечения трастузумабом в комбинации с химиотерапией Герцептин целесообразно оставлять в качестве одного из компонентов последующей лекарственной терапии. В этом случае в комбинации с Герцептином может применяться цитостатик, который ранее не получала пациентка, либо один из таргетных препаратов.
До настоящего времени для лечения HER2-позитивного РМЖ, резистентного к трастузумабу, чаще всего назначалась комбинация лапатиниба с Кселодой. Основанием для подобного выбора послужили данные рандомизированного исследования EGF100151, главной целью которого являлось сравнение времени до прогрессирования болезни при лечении капецитабином в монорежиме или в комбинации с лапатинибом [17]. Медиана времени до прогрессирования болезни была достоверно (p < 0,001) выше у больных, получавших капецитабин с лапатинибом (8,4 мес.), чем у пациенток, получавших монотерапию капецитабином (4,4 мес.), объективный эффект (23,7 против 13,9%, p = 0,017) также был достоверно выше при использовании комбинированного режима, чем монотерапии. Медианы общей выживаемости достоверно не различались.
Таким образом, при развитии резистентности к трастузумабу у пациенток с HER2-позитивным РМЖ для продолжения лечения можно использовать по крайней мере 3 комбинированных режима со сходной эффективностью (табл. 5) в зависимости от наличия того или иного препарата. Предклинические результаты свидетельствуют о том, что лечение лапатинибом HER2-позитивного РМЖ способствует восстановлению чувствительности HER2-рецепторов опухолевых клеток к трастузумабу. На этом основании итальянские ученые проводят изучение целесообразности повторного назначения трастузумаба после прогрессирования HER2-позитивного РМЖ во второй линии лечения лапатинибом и капецитабином. В настоящее время из 179 пациенток оценено 69, у 51 из них (74%) были обнаружены висцеральные метастазы, у 16 (23%) – метастазы в головной мозг. Все больные ранее получали лечение, включающее и трастузумаб, и лапатиниб.
В результате повторного лечения трастузумабом у 1 (2%) больной была достигнута полная регрессия болезни, у 18 (29%) – частичная, у 10 (14%) отмечена стабилизация болезни на протяжении 6 и более месяцев, у 47% больных – клиническое улучшение. Медиана продолжительности эффекта составила 8,1 мес. При медиане наблюдения 13 мес. медиана выживаемости больных без прогрессирования болезни составила 4,9 мес., медиана общей выживаемости – 19,4 мес. Медиана общей выживаемости была достоверно выше у больных, имевших клиническое улучшение (не достигнута), чем у пациенток без него (13,4 мес., p = 0,002). Метастатическое поражение головного мозга было ассоциировано с более низкой медианой выживаемости больных (17,3 против 23,3 мес., p = 0,021). По мнению авторов, повторное назначение трастузумаба позволяет достичь клинического улучшения у 47% пациенток с HER2-позитивным РМЖ, резистентным к ранее проводимой терапии трастузумабом и лапатинибом, и способствует увеличению продолжительности жизни [18]. Дальнейший прогресс в преодолении резистентности к трастузумабу может быть связан с развитием и изучением препаратов таргетной терапии (табл. 6).
Трастузумаб в адъювантной терапии HER2-позитивного операбельного рака молочной железы
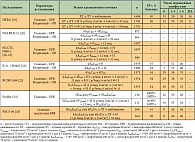
Оценке роли трастузумаба в адъювантной терапии операбельного HER2-позитивного рака молочной железы посвящены 6 крупных международных рандомизированных контролируемых исследований: HERA (the Herceptin Adjuvant trial) [19], NSABP B-31 (the National Surgical Adjuvant Breast and Bowel Project B-31 trial) [20], NCCTG N9831 (the North Central Cancer Treatment Group N9831 trial) [20, 21], BCIRG-006 (the Breast Cancer International Research Group 006 trial) [22], FinHer (the Finland Herceptin trial) [23], PACS-04 (the Protocolе Adjuvant dans le Cancer du Sein trial) [24]. Всего в эти исследования включено более 14 000 женщин и оценена целесообразность добавления трастузумаба к различным режимам ХТ в различной их последовательности (табл. 7).
В четырех из упомянутых международных клинических исследований было показано, что добавление трастузумаба к химиотерапии приводит к достоверному увеличению безрецидивной выживаемости, в трех испытаниях – помимо увеличения БРВ к достоверному увеличению общей выживаемости (табл. 8). Данные, полученные в этих исследованиях, а также результаты метаанализа на основе индивидуальных данных больных, включенных в исследования, подтверждают позитивное влияние Герцептина на эффективность адъювантной терапии. Согласно результатам метаанализа, включение Герцептина в адъювантную терапию приводит к достоверному снижению смертности (p < 0,00001), частоты рецидивов (p < 0,00001), частоты развития отдаленных метастазов (p < 0,00001) и вторых злокачественных опухолей [25].
Заключение
В большинстве исследований, результаты которых легли в основу существующих рекомендаций, продолжительность назначения трастузумаба составляла 1 год. Более длительный период введения трастузумаба (2 года) изучается в исследовании HERA, результаты которого пока не опубликованы. В исследовании FinHer использовали более короткий курс введения Герцептина, равный 9 неделям. Результаты двухлетнего наблюдения за больными показали, что добавление Герцептина к адъювантной химиотерапии способствует достоверному увеличению 2-летней безрецидивной выживаемости с тенденцией к увеличению общей продолжительности жизни. Однако 5-летние результаты наблюдения показали, что 9-недельный курс введения трастузумаба не приводит к достоверному увеличению безрецидивной и общей выживаемости больных [26]. В настоящее время продолжаются исследования по изучению оптимальной длительности введения трастузумаба в составе адъювантной терапии, результаты которых, возможно, изменят наши представления о рациональной длительности введения Герцептина. На сегодняшний день оптимальной продолжительностью введения Герцептина в составе адъювантной терапии считается 1 год.
