Развивающая и поддерживающая гормональная терапия у пациенток с XY-дисгенезией гонад
- Аннотация
- Статья
- Ссылки
с препаратами, способствующими репарации костной ткани.
с препаратами, способствующими репарации костной ткани.


Нарушение дифференцировки половых желез, исходом которой является дисгенезия гонад, относится к группе заболеваний, сопровождающихся гипоэстрогенией. Гипоэстрогенное состояние характеризуется отсутствием полового развития, менструаций и феминизации фигуры; гиперлипидемией; снижением минеральной плотности костной ткани и др. В отсутствие своевременной коррекции гормональные и метаболические нарушения могут привести к развитию раннего атеросклероза, нарушению деятельности сердечно-сосудистой системы, снижению когнитивных функций, значительному увеличению риска переломов костей.
Дисгенезия гонад с наличием в кариотипе больной Y-хромосомы (XY-ДГ) связана с мутациями генов, отвечающих за половую дифференцировку по мужскому типу, и наследуется по мужской линии. Она характеризуется наличием двусторонних дисгенетичных тестикулов, персистенцией мюллеровых протоков и крипторхизмом у индивидуумов с кариотипом 46,ХY (или с мозаичным присутствием Y-хромосомы) и возможным неопределенным строением наружных половых органов. Данная форма XY-реверсии пола заслуживает особого внимания в связи с высоким риском малигнизации неполноценных половых желез, находящихся в брюшной полости. Риск неопластической трансформации увеличивается с возрастом – от 2% в 10-летнем возрасте до 27% в 30-летнем [1, 8, 6]. Более того, в литературе имеются данные об обнаружении опухолевых процессов в гонадах при XY-ДГ у детей в возрасте до 1 года жизни [5, 6, 10]. В связи с высокой частотой малигнизации гонад лечение данного контингента больных состоит из двух этапов – хирургического (двустороннего удаления половых желез) и последующей заместительной гормональной терапии (ЗГТ), направленной на возмещение дефицита эстрогенов. В последние годы рядом исследователей показана большая эффективность ЗГТ препаратами, имеющими в своем составе натуральные эстрогены [3, 4].
Принимая во внимание длительность (с пубертатного периода до возраста физиологической менопаузы) заместительной гормональной терапии, актуален вопрос ее корректного подбора. Целью нашего исследования явился поиск препаратов для ЗГТ, имеющих наименьшее число побочных реакций, но обеспечивающих достаточный эстрогенный фон.
Пациенты и методы исследования
Нами было проведено комплексное клинико-лабораторное обследование 40 пациенток (согласно паспортному полу), у которых был выявлен мужской кариотип 46,XY. Пациентки характеризовались задержкой полового созревания при нормально выраженном оволосении по женскому типу и наличии матки и влагалища.
Поводом для обращения в преобладающем большинстве случаев были проблемы, связанные c отсутствием самостоятельных менструаций. В единичных случаях больные обратились в ФГУ «НЦАГиП им. В.И. Кулакова» в связи с выявленным аномальным строением наружных половых органов или после удаления объемных образований органов малого таза.
Исходно, до обращения в Центр, заболевание было правильно диагностировано лишь у 12,5% пациенток с XY-ДГ, что привело к назначению неверного лечения. Впоследствии у 2 больных с XY-ДГ, получавших ЗГТ, были обнаружены опухолевые процессы в гонадах, что свидетельствует об опасности назначения пациенткам с задержкой полового созревания гормональной терапии без предварительного генетического исследования. Такое лечение может спровоцировать развитие неопластического процесса в дисгенетичных гонадах, что коррелирует с данными литературы [2, 7].
Всем больным было произведено удаление половых желез с последующим морфологическим исследованием и назначением заместительной гормональной терапии, направленной на возмещение дефицита эстрогенов. В ходе обследования проводился динамический контроль содержания гонадотропных и половых стероидных гормонов крови, состояния липидного спектра крови, эхографическое исследование органов малого таза и молочных желез, денситометрия.
Результаты исследования
У всех пациенток биологический возраст отставал от календарного на 2–5 лет и соответствовал в среднем 12,1 ± 1,3 годам. При этом разница календарного и биологического возрастов составила 4,9 ± 1,27 лет. Антропометрическое обследование выявило задержку формирования костного таза и интерсексуальный тип телосложения. Индекс таза к 18–19 годам жизни у них оказался меньше нормативных значений для женщин этого возраста, а тазово-плечевой коэффициент имел промежуточное – между мужскими и женскими нормативами – значение.
Развитие и строение молочных желез, по данным эхографического исследования, у пациенток с XY-ДГ, не получавших ЗГТ, в основном соответствовало периоду детства. Исключение составили больные с неопластическим процессом в дисгенетичных гонадах, у которых молочные железы достигли 2–3 степени развития по Таннеру (72,2% при опухолях). Зрелость молочных желез у этих пациенток подтверждалась большей толщиной опорной стромы по данным эхомаммографии (0,49 ± 0,2 см), чем у пациенток без опухолевого процесса (0,3 ± 0,07 см; р < 0,05). Ни у одной больной с ХY-ДГ не было обнаружено сетчатого строения молочных желез.
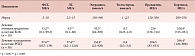
Исследование гормонального профиля крови выявило выраженную гипоэстрогению при высоких показателях содержания гонадотропных гормонов с периода полового созревания (табл. 1).
Значения уровня холестерина, его липопротеидных фракций и триглицеридов, а также коэффициента атерогенности до начала терапии в основном не выходили за рамки нормы.
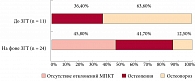
Исследование минеральной плотности костной ткани (МПКТ) до удаления гонад и назначения ЗГТ выявило у всех обследованных больных с XY-ДГ снижение плотности костной массы, в том числе у 63,6% – до степени остеопороза (Z = -4,3 ± 0,6) и у 36,4% – до степени остеопении (Z = -1,6 ± 0,3). Показатели Z-критерия области второго – четвертого поясничных позвонков (L2–L4) у пациенток с XY-ДГ составили в среднем 3,3 ± 1,4 (от 1,3 до 5,2) стандартных единиц.
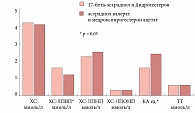
Первый этап лечения больных с XY-реверсией пола заключался в двустороннем удалении половых желез, преимущественно эндоскопическим доступом. Частота неопластической трансформации дисгенетичных гонад при XY-кариотипе, по данным нашего исследования, составила 47,5%. Максимальная частота выявления опухолевого процесса (53%) приходилась на календарный возраст 15–18 лет, но в двух случаях опухоли гонад (дисгерминомы) были обнаружены в детском периоде жизни. Морфологически опухоли дисгенетичных гонад были представлены гонадобластомами в 52,6%, дисгерминомами – в 10,5% и комбинированными опухолями (дисгерминома с гонадобластомой) – в 36,9% случаев. У 29,4% больных были обнаружены патологические изменения маточных труб и мезосальпинксов.
Вторым этапом лечения явилось назначение развивающей и поддерживающей гормональной терапии (РПГТ). При выборе препаратов для РПГТ было учтено, что сочетанное влияние эстрогенов и прогестерона позволит обеспечить более физиологичное развитие молочных желез; прогестерон сенсибилизирует рецепторный аппарат головного мозга к влиянию эстрогенов, способствуя тем самым формированию адекватного полу воспитания полоролевого поведения с пубертатного периода. При этом часть пациенток вначале получали эстрогены (этинилэстрадиол) в составе комбинированных оральных контрацептивов, но в последующем были переведены на заместительную гормональную терапию препаратами, содержащими натуральные эстрогены в сочетании с прогестагенами.
Наиболее существенные изменения в содержании гормонов наблюдались к концу первого полугодия от начала терапии. Показатели липидного обмена на фоне ЗГТ у пациенток обеих групп колебались в пределах нормативных возрастных значений.
Сравнительный анализ уровня содержания гормонов в крови больных с XY-ДГ на фоне применения различных препаратов, содержащих комбинацию эстрогенов и прогестагенов, показал, что комбинированные оральные контрацептивы обладали большей антигонадотропной активностью, но меньшим эффектом эстрогенизации, чем препараты, содержащие натуральные эстрогены (табл. 2).
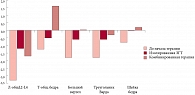
Сопоставление результатов применения РПГТ у больных с XY-ДГ выявило, что 17-бета-эстрадиол в комбинации с дидрогестероном (Фемостон® 2/10) обеспечивал более высокую эстрогенную насыщенность, чем эстрадиол валерат в комбинации с медроксипрогестерона ацетатом (рис. 1).
При этом Фемостон® 2/10, содержащий аналог натурального прогестерона – дидрогестерон, не имел андрогенного эффекта и обладал большей метаболической нейтральностью, что особенно важно в условиях длительной (с пубертатного периода до возраста физиологического климактерия) РПГТ (рис. 2). Дидрогестерон является уникальным аналогом (пространственным изомером) натурального прогестерона. Обладая высоким сродством к прогестероновым рецепторам, дидрогестерон оказывает все необходимые прогестагенные эффекты при приеме в небольшой дозировке. Благодаря высокой селективности дидрогестерона к рецепторам прогестерона препарат не влияет на углеводный, водно-солевой обмен, а обеспечивает благоприятное действие эстрогенов на липидный обмен и костную ткань.
Постоянное применение эстрадиола и дидрогестерона в последовательном режиме оказывало более благотворное влияние на состояние молочных желез, не вызывая развитие аденоза и выраженной гиперплазии железистой ткани, которое было выявлено у больных с ХY-ДГ, применявших эстрадиол в сочетании с медрокспрогестерона ацетатом.
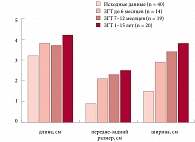
Увеличение размеров матки у больных с XY-ДГ, особенно ширины и передне-заднего размера, было наиболее выражено в первые 6 мес. от начала РПГТ с последующим замедлением скорости роста (рис. 3).
Молочные железы пациенток за первые 2–3 года лечения увеличились с 1 до 4–5 степени по Таннеру. Тем не менее у 74,1% больных с XY-ДГ даже на фоне длительной (10 и более лет) РПГТ молочные железы не достигли завершающей стадии структурного развития, характеризующейся появлением сетчатого типа строения.
У больных с XY-ДГ РПГТ способствовала значительному восстановлению МПКТ (рис. 4).
Однако наиболее оптимальные результаты возрастания МПКТ отмечены при использовании ЗГТ в комбинации с препаратами, способствующими регенерации костной ткани. Больные, имевшие снижение МПКТ до степени выраженного остеопороза, получали оссеин-гидроксиапатитное соединение (остеогенон) в суточной дозе 2490 мг (в три приема) в первые 6 мес. терапии, остальным проводилась терапия препаратом, содержащим 600 мг элементарного кальция и витамин Д3 в дозе 400 МЕ (Натекаль Д3). Наилучший эффект наблюдался в первые 2 года лечения от начала РПГТ (рис. 5).
Натекаль Д3 назначался в суточной дозе 1200 мг кальция и 800 МЕ витамина Д3 в два приема (день и вечер) курсами по 6 мес. с полугодовым перерывом.
Как показали наши исследования, своевременная коррекция состояния минеральной плотности костной ткани приводила к уменьшению риска возникновения переломов и болей в позвоночнике в будущем.
На фоне терапии значительно улучшилось и психологическое состояние девочек. Феминизация фигуры, увеличение молочных желез и размеров матки до степени, позволяющей выносить беременность, появление менструально-подобных реакций способствовало окончательной половой самоидентификации пациенток. Они становились более уверенными, возрастала их социальная активность, что подтверждалось результатами проведенного психологического тестирования.
В результате разработанной в отделении гинекологии детского и юношеского возраста комплексной РПТ девушки, достигшие половой зрелости, смогли создать семью и с помощью вспомогательных репродуктивных технологий стать матерями. К сегодняшнему дню все пациентки с Хy-ДГ, обратившиеся по поводу экстракорпорального оплодотворения донорской яйцеклетки, имеют детей, которые растут и развиваются нормально.
Заключение
Проведенное нами исследование показало, что врожденное эстрогендефицитное состояние у больных с ХY-ДГ приводит к гормональным и метаболическим нарушениям; отсутствию полового развития, менструаций и феминизации фигуры; к задержке формирования костного скелета, маскулинному типу телосложения и выраженному снижению МПКТ; развитию раннего атеросклероза; к снижению когнитивных функций. Высокий процент выявленной неопластической трансформации гонад у пациенток различных возрастных групп требует проведения билатеральной гонадэктомии в момент диагностирования патологии, независимо от возраста пациентки. На втором, консервативном, этапе лечения необходимо учитывать длительность предполагаемой РПГТ (на протяжении 30 лет), отдавая предпочтение препаратам, содержащим «натуральные» эстрогены и метаболически нейтральные гестагены. Результаты проведенного нами исследования показали, что Фемостон® 2/10, содержащий 17-бета-эстрадиол с дидрогестероном, обеспечивает достаточную эстрогенизацию и обладает максимальной метаболической нейтральностью. С целью восстановления МПКТ в комплекс терапии необходимо включать препараты, способствующие репарации костной ткани – элементарный кальций и витамин Д3 – Натекаль Д3 курсами по 6 мес. с полугодовым перерывом, а при выраженном остеопорозе – в первые полгода от начала ЗГТ – с предшествующей терапией оссеин-гидроксиапатитным соединением (остеогеноном).
Таким образом, гипоэстрогения, даже абсолютная, как у больных с ХY-ДГ, – это не приговор, а состояние, подлежащее и поддающееся коррекции с помощью правильно подобранной терапии. В данной связи подчеркнем важность своевременной диагностики заболевания, хирургического лечения, а также раннего, с пубертатного периода, назначения заместительной гормональной терапии.
