количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Результаты применения препарата Семакс при когнитивных нарушениях в остром периоде ишемического инсульта и при хронической ишемии мозга
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Неврология и Психиатрия" №2
- Аннотация
- Статья
- Ссылки
На базе Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова было проведено исследование, которое показало высокую клиническую эффективность препарата Семакс в терапии когнитивных и неврологических нарушений как при острой, так и при хронической ишемии головного мозга.
Препарат Семакс относится к классу лекарственных средств, являющихся аналогами нейропептидов мозга. Препарат обладает нейропротективным, нейрометаболическим, ноотропным и антиастеническим действием, способствует синтезу важнейших нейротрофических факторов мозга, угнетает процессы первичной и отсроченной нейрональной гибели.
На базе Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова было проведено исследование, которое показало высокую клиническую эффективность препарата Семакс в терапии когнитивных и неврологических нарушений как при острой, так и при хронической ишемии головного мозга.
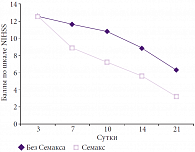
Рис. 1. Динамика клинического балла по шкале NIHSS при инсульте легкой степени тяжести (n = 35, p < 0,05)
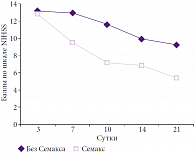
Рис. 2. Динамика клинического балла по шкале NIHSS при инсульте средней степени тяжести (n = 34, p < 0,05)
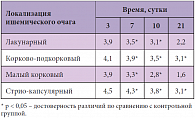
Таблица 1. Динамика функционального восстановления больных, получавших Семакс, в зависимости от локализации ишемического очага (по модифицированной шкале Рэнкина, n = 69)
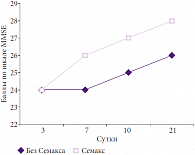
Рис. 3. Динамика когнитивных нарушений по шкале MMSE при инсульте легкой степени тяжести в основной и контрольной группах
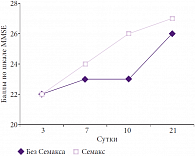
Рис. 4. Динамика когнитивных нарушений по шкале MMSE при инсульте средней степени тяжести в основной и контрольной группах
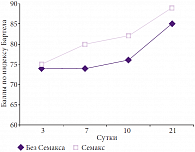
Рис. 5. Динамика фукционального восстановления больных по индексу Бартела в группе с инсультом легкой степени тяжести (n = 35, p < 0,05)
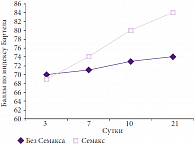
Рис. 6. Динамика фукционального восстановления больных по индексу Бартела в группе с инсультом средней степени тяжести (n = 34, p < 0,05)
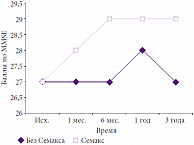
Рис. 7. Динамика когнитивных нарушений при хронической ишемии мозга II степени в основной (n = 31) и контрольной группах (p < 0,05)
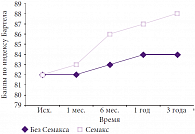
Рис. 8. Динамика функционального восстановления больных, получавших Семакс, при хронической ишемии мозга III степени (последствия ишемического инсульта, основная группа, n = 89, p < 0,05) по индексу Бартела
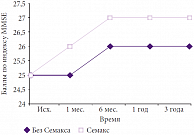
Рис. 9. Динамика когнитивных нарушений у больных, получавших Семакс, при хронической ишемии мозга III степени (последствия ишемического инсульта, основная группа, n = 89, p < 0,05) по шкале MMSE
Нейропротекция – одно из важнейших направлений патогенетической терапии ишемии мозга. Единственной группой препаратов, обладающих свойствами первичных и вторичных нейропротекторов, являются лекарственные средства, созданные на основе регуляторных олигопептидов (нейропептидов) мозга. В малых дозах (доли миллиграмма – миллиграммы) они легко проникают через гематоэнцефалический барьер, обладают выраженной физиологической активностью, комплексным воздействием на различные звенья патогенеза, длительным терапевтическим последействием на фоне высокого уровня безопасности приема [4, 5].
Семакс является первым (и пока единственным) препаратом группы нейропептидов, нашедшим широкое применение в медицинской практике. Семакс оказывает нейропротективное, нейрометаболическое, ноотропное и антиастеническое действие, способствует синтезу важнейших нейротрофических факторов мозга (фактор роста нервов – nerve growth factor (NGF), нейротрофический фактор мозга – brain-derived neurotrophic factor (BDNF) и др.), угнетает процессы первичной и отсроченной нейрональной гибели [6–10]. Эффективность препарата Семакс доказана в терапии острого периода ишемического и геморрагического инсульта, в профилактике инсульта и транзиторной ишемической атаки, а также при лечении хронической ишемии мозга и когнитивных нарушений различного генеза [11–13]. На базе Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова было проведено исследование с целью оценки динамики когнитивных и неврологических нарушений в результате применения препарата Семакс в терапии острого нарушения мозгового кровообращения и хронической ишемии мозга.
Материалы и методы
В исследовании приняли участие две группы пациентов: в первой группе Семакс в комплексной терапии получали больные с ишемическим инсультом, во второй – с хронической ишемией мозга. Для динамического наблюдения использовался диагностический нейрохирургический комплекс, включающий общеклиническое обследование, неврологическое исследование с использованием шкальных оценок (модифицированная шкала Multicentre Acutу Stroke Trial (MAST), шкала National Institutes of Health Stroke Scale (NIHSS), модифицированная шкала Рэнкина, индекс Бартела), а также исследование когнитивных функций с использованием шкалы Mini-mental State Examination (MMSE). С целью верификации первичного диагноза использовались данные компьютерной (КТ) и магнитно-резонансной томографии (МРТ), транскраниальной допплерографии и дуплексного сканирования.
В связи с разной степенью тяжести состояния больных, особенностями патогенеза и неврологической симптоматики, а также различными схемами применения препарата Семакс, анализ результатов проводился отдельно для группы с острым ишемическим инсультом и группы с хронической ишемией мозга. В первую группу вошли 87 пациентов с острым ишемическим инсультом. Основную группу составили 69 пациентов (39 мужчин, 30 женщин) в возрасте от 42 до 73 лет, средний возраст – 58,3 ± 5,9 года.У всех пациентов группы острое нарушение мозгового кровообращения развилось в каротидном бассейне с формированием лакунарного (n = 9), малого коркового (n = 19), корково-подкоркового (n = 21) инфарктов, у 20 пациентов имелись обширные глубинные (стрио-капсулярные) инфаркты. Левосторонняя локализация процесса установлена у 35, правосторонняя – у 34 больных. У всех пациентов имелся множественный стенозирующий процесс с наличием тандемных и циркулярных стенозов, а также гомогенных и гетерогенных бляшек в экстракраниальных отделах внутренних сонных артерий.
Все пациенты поступили в сосудистое отделение Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова в сроки 3–5 суток от начала инсульта. Инсульты легкой степени тяжести по модифицированной шкале MAST (100 баллов и выше) были диагностированы у35 больных, инсульты средней степени тяжести (от 50 до 100 баллов по MAST) – у 34 пациентов. Неврологическая симптоматика у больных была представлена сочетанием общемозговых симптомов в виде головной боли, нарушения сознания от умеренного оглушения (n = 39) до сопора (n = 4), нарушением функций черепных нервов (III, VI, VII, XII пары), а также двигательными и чувствительными нарушениями различной степени выраженности. У всех пациентов имелись нарушения когнитивных функций в виде интеллектуально-мнестических расстройств, а также сенсорная, моторная и амнестическая афазии (n = 19), апракто-гностический синдром (n = 9). Структура синдрома когнитивных нарушений коррелировала с локализацией и степенью выраженности ишемии мозга. Степень выраженности когнитивных нарушений оценивалась по шкале MMSE (от 22 до 28 баллов).
В исследовании приняли участие две группы пациентов: в первой группе Семакс в комплексной терапии получали больные с ишемическим инсультом, во второй – с хронической ишемией мозга. Для динамического наблюдения использовался диагностический нейрохирургический комплекс, включающий общеклиническое обследование, неврологическое исследование с использованием шкальных оценок (модифицированная шкала Multicentre Acutу Stroke Trial (MAST), шкала National Institutes of Health Stroke Scale (NIHSS), модифицированная шкала Рэнкина, индекс Бартела), а также исследование когнитивных функций с использованием шкалы Mini-mental State Examination (MMSE). С целью верификации первичного диагноза использовались данные компьютерной (КТ) и магнитно-резонансной томографии (МРТ), транскраниальной допплерографии и дуплексного сканирования.
В связи с разной степенью тяжести состояния больных, особенностями патогенеза и неврологической симптоматики, а также различными схемами применения препарата Семакс, анализ результатов проводился отдельно для группы с острым ишемическим инсультом и группы с хронической ишемией мозга. В первую группу вошли 87 пациентов с острым ишемическим инсультом. Основную группу составили 69 пациентов (39 мужчин, 30 женщин) в возрасте от 42 до 73 лет, средний возраст – 58,3 ± 5,9 года.У всех пациентов группы острое нарушение мозгового кровообращения развилось в каротидном бассейне с формированием лакунарного (n = 9), малого коркового (n = 19), корково-подкоркового (n = 21) инфарктов, у 20 пациентов имелись обширные глубинные (стрио-капсулярные) инфаркты. Левосторонняя локализация процесса установлена у 35, правосторонняя – у 34 больных. У всех пациентов имелся множественный стенозирующий процесс с наличием тандемных и циркулярных стенозов, а также гомогенных и гетерогенных бляшек в экстракраниальных отделах внутренних сонных артерий.
Все пациенты поступили в сосудистое отделение Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова в сроки 3–5 суток от начала инсульта. Инсульты легкой степени тяжести по модифицированной шкале MAST (100 баллов и выше) были диагностированы у35 больных, инсульты средней степени тяжести (от 50 до 100 баллов по MAST) – у 34 пациентов. Неврологическая симптоматика у больных была представлена сочетанием общемозговых симптомов в виде головной боли, нарушения сознания от умеренного оглушения (n = 39) до сопора (n = 4), нарушением функций черепных нервов (III, VI, VII, XII пары), а также двигательными и чувствительными нарушениями различной степени выраженности. У всех пациентов имелись нарушения когнитивных функций в виде интеллектуально-мнестических расстройств, а также сенсорная, моторная и амнестическая афазии (n = 19), апракто-гностический синдром (n = 9). Структура синдрома когнитивных нарушений коррелировала с локализацией и степенью выраженности ишемии мозга. Степень выраженности когнитивных нарушений оценивалась по шкале MMSE (от 22 до 28 баллов).
Контрольная группа состояла из 18 пациентов и была сопоставима по всем оцениваемым критериям.
Все больные контрольной и основной групп получали максимально унифицированную консервативную терапию с применением низкомолекулярных декстранов, гемодилюции, препаратов, стабилизирующих жизненно важные функции, а также антиоксидантов (Мексидол, Цитофлавин) и дезагрегантов. Препарат Семакс в основной группе пациентов с острым ишемическим инсультом применялся интраназально в виде 1% раствора в дозе 12 мг в сутки в течение 21 дня. Во вторую группу вошли 152 пациента с хронической ишемией мозга II–III степени. Основную группу составили 120 пациентов (70 мужчин, 50 женщин) c хронической ишемией головного мозга вследствие стенозирующих процессов экстра- и интракраниальных сосудов. Возраст больных – от 48 до 71 года, средний возраст – 55,6 ± 4,9 года.
Все больные контрольной и основной групп получали максимально унифицированную консервативную терапию с применением низкомолекулярных декстранов, гемодилюции, препаратов, стабилизирующих жизненно важные функции, а также антиоксидантов (Мексидол, Цитофлавин) и дезагрегантов. Препарат Семакс в основной группе пациентов с острым ишемическим инсультом применялся интраназально в виде 1% раствора в дозе 12 мг в сутки в течение 21 дня. Во вторую группу вошли 152 пациента с хронической ишемией мозга II–III степени. Основную группу составили 120 пациентов (70 мужчин, 50 женщин) c хронической ишемией головного мозга вследствие стенозирующих процессов экстра- и интракраниальных сосудов. Возраст больных – от 48 до 71 года, средний возраст – 55,6 ± 4,9 года.
У всех пациентов наблюдалась хроническая ишемия головного мозга II–III степени, у 89 из них в анамнезе были ишемические инсульты с формированием умеренного неврологического дефицита и наличием умеренных (n = 56) и выраженных (n = 64) когнитивных нарушений в сочетании с афатическими расстройствами (n = 19) и апракто-гностическим синдромом (n = 12). Нарушения речи, гнозиса и праксиса были умеренно выраженными. В большинстве случаев (n = 81) наблюдалась патология экстракраниальных отделов сонных артерий, которая у 15 пациентов сочеталась с наличием стенозирующего процесса на уровне супраклиноидного отдела внутренних сонных артерий. У 39 больных имелась патологическая извитость позвоночных артерий на экстракраниальном уровне.
Нарушения функции черепных нервов были выражены минимально и в основном представлены установочным нистагмом при взгляде в сторону, слабостью конвергенции, недостаточностью иннервации мимической мускулатуры и некоторым снижением глоточного рефлекса. Пирамидная симптоматика проявлялась в виде рефлекторной асимметрии, а также остаточными явлениями моно- и гемипарезов в пределах 4–4,5 баллов без изменения мышечного тонуса (n = 11). У 39 пациентов были отмечены умеренные нарушения статики и координации в виде неустойчивости в усложненной позе Ромберга, дискоординации при пальце-носовой пробе и незначительной шаткости походки.
По данным КТ и МРТ у 19 пациентов с инсультом в анамнезе наблюдались рубцово-атрофические изменения, соответствующие локализации очага ишемии в остром периоде инсульта. У остальных 70 пациентов отмечались только признаки умеренной заместительной гидроцефалии, множественные очаги демиелинизации сосудистого характера и невыраженные кистозно-спаечные изменения. У пациентов, не имевших в анамнезе инсульта, посредством нейровизуализационных методов выявлялись признаки дисциркуляторной энцефалопатии, умеренно выраженной заместительной гидроцефалии и мелких очагов демиелинизации в подкорковых структурах.
Нарушения функции черепных нервов были выражены минимально и в основном представлены установочным нистагмом при взгляде в сторону, слабостью конвергенции, недостаточностью иннервации мимической мускулатуры и некоторым снижением глоточного рефлекса. Пирамидная симптоматика проявлялась в виде рефлекторной асимметрии, а также остаточными явлениями моно- и гемипарезов в пределах 4–4,5 баллов без изменения мышечного тонуса (n = 11). У 39 пациентов были отмечены умеренные нарушения статики и координации в виде неустойчивости в усложненной позе Ромберга, дискоординации при пальце-носовой пробе и незначительной шаткости походки.
По данным КТ и МРТ у 19 пациентов с инсультом в анамнезе наблюдались рубцово-атрофические изменения, соответствующие локализации очага ишемии в остром периоде инсульта. У остальных 70 пациентов отмечались только признаки умеренной заместительной гидроцефалии, множественные очаги демиелинизации сосудистого характера и невыраженные кистозно-спаечные изменения. У пациентов, не имевших в анамнезе инсульта, посредством нейровизуализационных методов выявлялись признаки дисциркуляторной энцефалопатии, умеренно выраженной заместительной гидроцефалии и мелких очагов демиелинизации в подкорковых структурах.
Контрольную группу составили 32 пациента с хронической ишемией мозга (у 12 из них в анамнезе было нарушение мозгового кровообращения).
Основная и контрольная группы были сопоставимы по полу, возрасту, стадии ишемической болезни головного мозга, характеру и тяжести неврологической симптоматики. Все больные контрольной и основной групп получали максимально унифицированную консервативную терапию с применением антиоксидантов (Мексидол, Цитофлавин), гипотензивных средств по показаниям (Теветен, Амлодипин, Энап, Конкор и т.д.), ноотропов (Ноотропил, Нобен, Луцетам), препаратов Танакан, Билобил, Мемоплант, Гинкго-билоба, а также и при необходимости препаратов Бетасерк, Вертигохель. Препарат Семакс в виде 0,1% раствора применяли в дозе 0,1 мг (по 2 капли в каждый носовой ход) 3 раза в сутки в течение месяца, затем повторяли курс лечения до 6 раз в год в течение 3 лет.
Основная и контрольная группы были сопоставимы по полу, возрасту, стадии ишемической болезни головного мозга, характеру и тяжести неврологической симптоматики. Все больные контрольной и основной групп получали максимально унифицированную консервативную терапию с применением антиоксидантов (Мексидол, Цитофлавин), гипотензивных средств по показаниям (Теветен, Амлодипин, Энап, Конкор и т.д.), ноотропов (Ноотропил, Нобен, Луцетам), препаратов Танакан, Билобил, Мемоплант, Гинкго-билоба, а также и при необходимости препаратов Бетасерк, Вертигохель. Препарат Семакс в виде 0,1% раствора применяли в дозе 0,1 мг (по 2 капли в каждый носовой ход) 3 раза в сутки в течение месяца, затем повторяли курс лечения до 6 раз в год в течение 3 лет.
Результаты исследования и их обсуждение
При клиническом анализе результатов, полученных у больных первой группы, было установлено, что использование препарата Семакс приводит к более быстрому улучшению (р < 0,05) состояния сознания больных к концу первой недели. Регресс очаговых симптомов выпадения функций центральной нервной системы (оценка по шкале NIHSS, функциональное восстановление по индексу Бартела и модифицированной шкале Рэнкина) у 83% больных начинался уже с середины первой недели применения препарата, в то время как в контрольной группе положительная динамика по этим оценочным шкалам наблюдалась с 7–12-х суток и была менее выраженной (рис. 1, 2). При оценке зависимости функционального восстановления от локализации ишемического очага по шкале Рэнкина лучшие результаты на фоне применения Семакса были получены при малом корковом и лакунарном инсультах. Лучшие результаты по шкале Рэнкина статистически достоверно наблюдались с 7-х суток применения препарата, достигая максимальных различий к 21-м суткам (табл. 1).
Наиболее выраженный терапевтический эффект имелся у больных, поступивших в отделение в состоянии ясного сознания, с умеренно выраженным неврологическим дефицитом в виде когнитивных нарушений. Динамика когнитивных нарушений по шкале MMSE в группе Семакса начиналась с 3–7-х суток (на 4–7 дней раньше, чем при базисной терапии) и достоверно отличалась по приросту среднего балла на 2– 3 единицы от аналогичных результатов в контрольной группе (рис. 3, 4). Так, при инсульте легкой степени тяжести в группе базисной терапии положительная динамика была зарегистрирована только на 10-й день, при использовании Семакса – на 5-е сутки, а к концу лечения (21-е сутки) у пациентов, применяющих регуляторный пептид, скорость восстановительных процессов была в два раза выше, чем в контрольной группе. У пациентов с инсультом средней степени тяжести положительная динамика когнитивных нарушений по шкале MMSE (+2 балла) при использовании Семакса регистрировалась на 7-е сутки, а в группе сравнения – только на 14-й день.
Динамика функционального восстановления больных оценивалась по индексу Бартела. Полученные данные коррелировали с данными оценки динамики неврологического статуса по шкале NIHSS и когнитивных функций по шкале MMSE. Результаты при применении препарата Семакс оказались достоверно лучшими, чем в контрольной группе (рис. 5, 6). Так, при инсульте легкой степени тяжести в группе Семакса положительная динамика регистрировалась уже на 5-й день терапии (+2,5 балла), а при использовании базисной терапии – только на 10-е сутки (+2 балла). При этом на 10-е сутки лечения Семаксом положительная динамика по шкале Бартела была +7 баллов, то есть интенсивность восстановительных процессов была в 3,5 раза выше, чем в контрольной группе. Наиболее значимые результаты были получены у больных с инсультом средней степени тяжести: к концу лечения (21-е сутки) у пациентов, применяющих регуляторный пептид, динамика функционального восстановления составляла +15 баллов, а в контрольной группе, получавшей только базисную терапию, – только +4 балла.
Следует отметить, что наиболее торпидными были апракто-гностические расстройства, хотя и при этой форме нарушений высших корковых функций степень восстановления в основной группе была выше (при апракто-гностических нарушениях была визуализирована зона инфаркта в правой теменной доле головного мозга, что, как известно, является морфологическим субстратом одного из наиболее стойких неврологических синдромов). Существенным положительным результатом исследования явилось отсутствие летальных исходов в анализируемой группе. В контрольной группе больных был один летальный исход на 18-е сутки от начала инсульта в связи с тромбоэмболией легочной артерии. Таким образом, результаты применения препарата Семакс у пациентов в остром периоде ишемического инсульта достоверно доказали его выраженное нейропротективное, нейрометаболическое и ноотропное действие, особенно при наличии когнитивных нарушений.
Во второй группе больных с хронической ишемией мозга применение препарата Семакс также показало выраженную положительную динамику состояния здоровья пациентов по всем использованным оценочным шкалам. В подгруппе больных с хронической ишемией мозга без инсульта в анамнезе отмечался статистически достоверный регресс когнитивных нарушений с 22 до 28 баллов (практически полное отсутствие когнитивных нарушений) по шкале MMSE. Восстановление состояния когнитивных функций пациентов начиналось с 10–14-х суток применения препарата Семакс и коррелировало с положительной динамикой нарушений статики и координации по шкале NIHSS и индексу Бартела. Качество жизни в данной группе пациентов сохранялось на должном уровне в течение 3 лет (рис. 7). В то же время у пациентов, которым проводилась только базисная терапия, положительная динамика когнитивных нарушений была выражена менее значимо (в 2 раза ниже по сравнению с группой Семакса) и наблюдалась только первые 1–1,5 года лечения, а затем возвращалась к исходному уровню.
В подгруппе пациентов с инсультом в анамнезе результаты были несколько менее значимы, что было обусловлено наличием стойких постишемических изменений, визуализированных по данным КТ и МРТ. Однако и у этих больных отмечалась отчетливая и статистически достоверная (р < 0,05) положительная динамика когнитивных нарушений (интеллектуально-мнестические расстройства, снижение внимания) по сравнению с контрольной группой (рис. 8, 9). Анализируя динамику функционального восстановления больных, получавших Семакс, при хронической ишемии мозга III степени (рис. 8), можно утверждать, что в группе Семакса результаты появились в первый месяц, в контрольной – на 7-й месяц; через год положительная динамика у пациентов в группе Семакса была в 2,5 раза выше, чем в контрольной. При этом в контрольной группе максимальный прирост показателей наблюдался в конце первого года (на 2 ед.), а затем на протяжении последующих 2 лет оставался на том же уровне. В группе Семакса в течение трех лет наблюдения происходил непрерывный рост показателя, и в конце исследования его положительная динамика в 3 раза превышала показатель в группе контроля.
Восстановительная динамика когнитивных нарушений (рис. 9) как в группе Семакса, так и в группе базисной терапии наблюдалась в течение первого года лечения, а затем ее показатели оставались на том же уровне, но при использовании регуляторного пептида они была достоверно выше в 2 раза. Необходимо отметить, что при стойких афатических нарушениях и апракто-гностическом синдроме существенного улучшения изучаемых показателей выявлено не было. Таким образом, результаты применения препарата Семакс при хронической ишемии мозга II–III степени показали его высокую клиническую эффективность.
Проведенный анализ результатов применения Семакса в двух группах больных подтвердил существующие литературные данные о безопасности данного препарата: с высокой степенью достоверности установлено отсутствие клинически значимых осложнений в процессе его использования. Примерно у 7% больных наблюдался побочный эффект в виде субъективных жалоб на парестезии (чувство «похолодания») в области носа и объективного побледнения слизистой носа в зоне воздействия препарата Семакс. Данный побочный эффект легко купировался 1–2-дневной отменой препарата и применением масляных растворов типа Пинасола.
При клиническом анализе результатов, полученных у больных первой группы, было установлено, что использование препарата Семакс приводит к более быстрому улучшению (р < 0,05) состояния сознания больных к концу первой недели. Регресс очаговых симптомов выпадения функций центральной нервной системы (оценка по шкале NIHSS, функциональное восстановление по индексу Бартела и модифицированной шкале Рэнкина) у 83% больных начинался уже с середины первой недели применения препарата, в то время как в контрольной группе положительная динамика по этим оценочным шкалам наблюдалась с 7–12-х суток и была менее выраженной (рис. 1, 2). При оценке зависимости функционального восстановления от локализации ишемического очага по шкале Рэнкина лучшие результаты на фоне применения Семакса были получены при малом корковом и лакунарном инсультах. Лучшие результаты по шкале Рэнкина статистически достоверно наблюдались с 7-х суток применения препарата, достигая максимальных различий к 21-м суткам (табл. 1).
Наиболее выраженный терапевтический эффект имелся у больных, поступивших в отделение в состоянии ясного сознания, с умеренно выраженным неврологическим дефицитом в виде когнитивных нарушений. Динамика когнитивных нарушений по шкале MMSE в группе Семакса начиналась с 3–7-х суток (на 4–7 дней раньше, чем при базисной терапии) и достоверно отличалась по приросту среднего балла на 2– 3 единицы от аналогичных результатов в контрольной группе (рис. 3, 4). Так, при инсульте легкой степени тяжести в группе базисной терапии положительная динамика была зарегистрирована только на 10-й день, при использовании Семакса – на 5-е сутки, а к концу лечения (21-е сутки) у пациентов, применяющих регуляторный пептид, скорость восстановительных процессов была в два раза выше, чем в контрольной группе. У пациентов с инсультом средней степени тяжести положительная динамика когнитивных нарушений по шкале MMSE (+2 балла) при использовании Семакса регистрировалась на 7-е сутки, а в группе сравнения – только на 14-й день.
Динамика функционального восстановления больных оценивалась по индексу Бартела. Полученные данные коррелировали с данными оценки динамики неврологического статуса по шкале NIHSS и когнитивных функций по шкале MMSE. Результаты при применении препарата Семакс оказались достоверно лучшими, чем в контрольной группе (рис. 5, 6). Так, при инсульте легкой степени тяжести в группе Семакса положительная динамика регистрировалась уже на 5-й день терапии (+2,5 балла), а при использовании базисной терапии – только на 10-е сутки (+2 балла). При этом на 10-е сутки лечения Семаксом положительная динамика по шкале Бартела была +7 баллов, то есть интенсивность восстановительных процессов была в 3,5 раза выше, чем в контрольной группе. Наиболее значимые результаты были получены у больных с инсультом средней степени тяжести: к концу лечения (21-е сутки) у пациентов, применяющих регуляторный пептид, динамика функционального восстановления составляла +15 баллов, а в контрольной группе, получавшей только базисную терапию, – только +4 балла.
Следует отметить, что наиболее торпидными были апракто-гностические расстройства, хотя и при этой форме нарушений высших корковых функций степень восстановления в основной группе была выше (при апракто-гностических нарушениях была визуализирована зона инфаркта в правой теменной доле головного мозга, что, как известно, является морфологическим субстратом одного из наиболее стойких неврологических синдромов). Существенным положительным результатом исследования явилось отсутствие летальных исходов в анализируемой группе. В контрольной группе больных был один летальный исход на 18-е сутки от начала инсульта в связи с тромбоэмболией легочной артерии. Таким образом, результаты применения препарата Семакс у пациентов в остром периоде ишемического инсульта достоверно доказали его выраженное нейропротективное, нейрометаболическое и ноотропное действие, особенно при наличии когнитивных нарушений.
Во второй группе больных с хронической ишемией мозга применение препарата Семакс также показало выраженную положительную динамику состояния здоровья пациентов по всем использованным оценочным шкалам. В подгруппе больных с хронической ишемией мозга без инсульта в анамнезе отмечался статистически достоверный регресс когнитивных нарушений с 22 до 28 баллов (практически полное отсутствие когнитивных нарушений) по шкале MMSE. Восстановление состояния когнитивных функций пациентов начиналось с 10–14-х суток применения препарата Семакс и коррелировало с положительной динамикой нарушений статики и координации по шкале NIHSS и индексу Бартела. Качество жизни в данной группе пациентов сохранялось на должном уровне в течение 3 лет (рис. 7). В то же время у пациентов, которым проводилась только базисная терапия, положительная динамика когнитивных нарушений была выражена менее значимо (в 2 раза ниже по сравнению с группой Семакса) и наблюдалась только первые 1–1,5 года лечения, а затем возвращалась к исходному уровню.
В подгруппе пациентов с инсультом в анамнезе результаты были несколько менее значимы, что было обусловлено наличием стойких постишемических изменений, визуализированных по данным КТ и МРТ. Однако и у этих больных отмечалась отчетливая и статистически достоверная (р < 0,05) положительная динамика когнитивных нарушений (интеллектуально-мнестические расстройства, снижение внимания) по сравнению с контрольной группой (рис. 8, 9). Анализируя динамику функционального восстановления больных, получавших Семакс, при хронической ишемии мозга III степени (рис. 8), можно утверждать, что в группе Семакса результаты появились в первый месяц, в контрольной – на 7-й месяц; через год положительная динамика у пациентов в группе Семакса была в 2,5 раза выше, чем в контрольной. При этом в контрольной группе максимальный прирост показателей наблюдался в конце первого года (на 2 ед.), а затем на протяжении последующих 2 лет оставался на том же уровне. В группе Семакса в течение трех лет наблюдения происходил непрерывный рост показателя, и в конце исследования его положительная динамика в 3 раза превышала показатель в группе контроля.
Восстановительная динамика когнитивных нарушений (рис. 9) как в группе Семакса, так и в группе базисной терапии наблюдалась в течение первого года лечения, а затем ее показатели оставались на том же уровне, но при использовании регуляторного пептида они была достоверно выше в 2 раза. Необходимо отметить, что при стойких афатических нарушениях и апракто-гностическом синдроме существенного улучшения изучаемых показателей выявлено не было. Таким образом, результаты применения препарата Семакс при хронической ишемии мозга II–III степени показали его высокую клиническую эффективность.
Проведенный анализ результатов применения Семакса в двух группах больных подтвердил существующие литературные данные о безопасности данного препарата: с высокой степенью достоверности установлено отсутствие клинически значимых осложнений в процессе его использования. Примерно у 7% больных наблюдался побочный эффект в виде субъективных жалоб на парестезии (чувство «похолодания») в области носа и объективного побледнения слизистой носа в зоне воздействия препарата Семакс. Данный побочный эффект легко купировался 1–2-дневной отменой препарата и применением масляных растворов типа Пинасола.
Выводы
Наиболее оптимальным сроком лечения острого инсульта являются первые три часа заболевания, до запуска процесса первичной гибели нейронов. Именно это время является наилучшим для начала тромболитической терапии и использования нейропротекторов и нейрометаболиков. Однако чаще всего больные поступают в стационар и получают патогенетическое противоинсультное лечение в более позднее время (в нашем исследовании – 3–5-е сутки от начала заболевания). К этому времени процесс гибели нейронов (первичной и в основной массе отсроченной) практически завершен, что определяет рамки формирования когнитивного и неврологического дефицита и одновременно сужает терапевтические возможности врача.
Наиболее оптимальным сроком лечения острого инсульта являются первые три часа заболевания, до запуска процесса первичной гибели нейронов. Именно это время является наилучшим для начала тромболитической терапии и использования нейропротекторов и нейрометаболиков. Однако чаще всего больные поступают в стационар и получают патогенетическое противоинсультное лечение в более позднее время (в нашем исследовании – 3–5-е сутки от начала заболевания). К этому времени процесс гибели нейронов (первичной и в основной массе отсроченной) практически завершен, что определяет рамки формирования когнитивного и неврологического дефицита и одновременно сужает терапевтические возможности врача.
Поэтому весьма ценным является появление в медицинской практике препаратов, обладающих выраженной терапевтической активностью именно в подострый период развития ишемического инсульта, к которым относится аналог регуляторных пептидов мозга Семакс. При его использовании на 3–5-й день после развития ишемического инсульта положительная достоверная динамика когнитивных нарушений наблюдалась с середины первой недели применения. При этом она коррелировала с положительной динамикой двигательных нарушений и нарастала на протяжении всей 21-дневной терапии. Высокоэффективным было применение Семакса и при хронической ишемии мозга II–III степени: препарат достоверно положительно влиял на состояние когнитивных функций пациентов; лучшие результаты лечения получены при мнестических нарушениях у больных с дисциркуляторной энцефалопатией.
Анализ результатов применения препарата Семакс в остром периоде ишемического инсульта и при хронической ишемии мозга показал, что препарат обладает выраженным нейропротективным, нейрометаболическим, ноотропным и нейротрофическим действием. Учитывая данные литературы [7, 8, 10], можно утверждать, что высокая терапевтическая эффективность Семакса как при ишемическом инсульте, так и при хронической ишемии мозга связана с инициацией им выработки ряда нейротрофических факторов (в особенности BDNF), роль которых значимо возрастает при патологии мозговой ткани. Таким образом, проведенное исследование свидетельствует о высокой клинической эффективности препарата Семакс как при острой, так и при хронической ишемии головного мозга.
Анализ результатов применения препарата Семакс в остром периоде ишемического инсульта и при хронической ишемии мозга показал, что препарат обладает выраженным нейропротективным, нейрометаболическим, ноотропным и нейротрофическим действием. Учитывая данные литературы [7, 8, 10], можно утверждать, что высокая терапевтическая эффективность Семакса как при ишемическом инсульте, так и при хронической ишемии мозга связана с инициацией им выработки ряда нейротрофических факторов (в особенности BDNF), роль которых значимо возрастает при патологии мозговой ткани. Таким образом, проведенное исследование свидетельствует о высокой клинической эффективности препарата Семакс как при острой, так и при хронической ишемии головного мозга.
1. Инсульт: диагностика, лечение, профилактика / под ред. З.А. Суслиной, М.А. Пирадова. М.: МЕДпресс-информ, 2008. 288 с.
2. Суслина 3.А., Варакин Ю.Я. Эпидемиологические аспекты изучения инсульта. Время подводить итоги // Анналы клинической и экспериментальной неврологии. 2007. Т. 1. № 2. С. 22–28.
3. Feigin V., Lawes C.M.M., Bennett D.A. et al. Worldwide stroke incidence and early case fatality reported in 56 population-based studies: a systematic review // Lancet Neurol. 2009. № 8. Р. 355–369.
4. Ворлоу Ч.П., Деннис М.С., Ж. Ван Гейн и др. Инсульт: практическое руководство для ведения больных. СПб.: Политехника, 1998. 629 с.
5. История создания препарата Семакс // Неотложная терапия. 2004. № 3-4. URL: http://proformula.kiev.ua/semax_history.html.
6. Ашмарин И.П., Незавибатьков Н.Н., Мясоедов Н.Ф. и др. Ноо- тропный аналог адренокортикотропина 4-10 – Семакс (15-летний опыт разработки и изучения) // Журнал высшей нервной деятельности. 1997. Т. 47. С. 419–425.
7. Гривенников И.А. Молекулярно-генетические подходы к пептидной фармакотерапии нейродегенеративных заболеваний: автореф. дисс. ... д-ра мед. наук. М., 2006. 46 с.
8. Долотов О.В. Механизмы действия пептида Семакс на центральную нервную систему: роль нейротрофинов: автореф. дисс. … канд. мед. наук. М., 2004. 24 с.
9. Еремин К.О. Влияние Семакса (АКТГ4-7–pro-gly-pro) на нейрохимические характеристики серотонин- и дофаминергичеких систем мозга и оценка его нейропротективной активности: автореф. дисс. ... канд. мед. наук. М., 2004. 25 с.
10. Левицкая Н.Г., Глазова Н.Ю., Себенцова Е.А. и др. Исслелование спектра физиологической активности аналога АКТГ4-10 гептапептида Семакс // Нейрохимия. 2008. Т. 25. № 1. С. 111–118.
11. Гусев Е.И., Скворцова В.И., Чуканова Е.И. Семакс в профилактике прогрессирования и развития обострений у больных с дисциркуляторной энцефалопатией // Журнал неврологии и психиатрии им. С.С. Корсакова. 2005. № 2. С. 35–40.
12. Заец Т.Я., Потапова А.А., Руднева В.В., Лобанова И.В. Применение препарата Семакс 0,1% в раннем восстановительном периоде ишемического инсульта // Кремлевская медицина. Клинический вестник. 2001. № 2. URL: http://www.vatros.ru/SEMAX/kremlin_med.htm.
13. Потапова А.А. Комплексное лечение ишемических инсультов с применением нейропептидных препаратов // Кремлевская медицина. Клинический вестник. 2003. № 2. URL: http://semaks.ru/SEMAX/semax_01_articles_kremlin_med_1.htm.
Новости на тему
СТАТЬИ по теме
09.04.2024
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
