количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Практика
Результаты сочетанного применения холинергических препаратов и ингибиторов ацетилхолинэстеразы при посттравматических когнитивных нарушениях
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Неврология и Психиатрия" №3 (32)
- Аннотация
- Статья
- Ссылки
- English
В статье приведены результаты комплексного применения пресинаптических холинергических препаратов и ингибиторов ацетилхолинэстеразы при когнитивных нарушениях в системе нейрореабилитации пациентов с последствиями тяжелой черепно-мозговой травмы.
Выявлены особенности динамики когнитивных нарушений в отдаленном периоде тяжелой черепно-мозговой травмы у пациентов с внутричерепными гематомами и очагами размозжения. Анализ динамики когнитивных нарушений при последствиях тяжелой черепно-мозговой травмы показал, что сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы является перспективным направлением как для профилактики, так и для лечения выраженных нарушений интеллектуально-мнестических функций.
Выявлены особенности динамики когнитивных нарушений в отдаленном периоде тяжелой черепно-мозговой травмы у пациентов с внутричерепными гематомами и очагами размозжения. Анализ динамики когнитивных нарушений при последствиях тяжелой черепно-мозговой травмы показал, что сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы является перспективным направлением как для профилактики, так и для лечения выраженных нарушений интеллектуально-мнестических функций.
В статье приведены результаты комплексного применения пресинаптических холинергических препаратов и ингибиторов ацетилхолинэстеразы при когнитивных нарушениях в системе нейрореабилитации пациентов с последствиями тяжелой черепно-мозговой травмы.
Выявлены особенности динамики когнитивных нарушений в отдаленном периоде тяжелой черепно-мозговой травмы у пациентов с внутричерепными гематомами и очагами размозжения. Анализ динамики когнитивных нарушений при последствиях тяжелой черепно-мозговой травмы показал, что сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы является перспективным направлением как для профилактики, так и для лечения выраженных нарушений интеллектуально-мнестических функций.
Выявлены особенности динамики когнитивных нарушений в отдаленном периоде тяжелой черепно-мозговой травмы у пациентов с внутричерепными гематомами и очагами размозжения. Анализ динамики когнитивных нарушений при последствиях тяжелой черепно-мозговой травмы показал, что сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы является перспективным направлением как для профилактики, так и для лечения выраженных нарушений интеллектуально-мнестических функций.
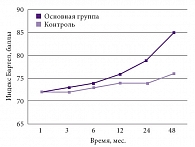
Рис. 1. Динамика неврологических нарушений и уровень адаптации по индексу Бартел: очаги размозжения и внутричерепные гематомы (p < 0,05)
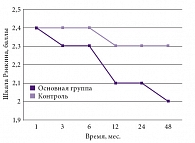
Рис. 2. Динамика неврологических нарушений по шкале Рэнкина: очаги размозжения и внутричерепные гематомы (p < 0,05)
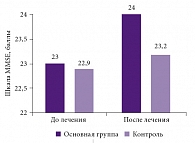
Рис. 3. Динамика когнитивных нарушений по шкале MMSE: очаги размозжения и внутричерепные гематомы (p < 0,05)
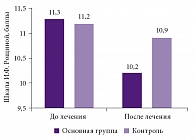
Рис. 4. Динамика когнитивных нарушений по шкале И.Ф. Рощиной: очаги размозжения и внутричерепные гематомы (p < 0,05)
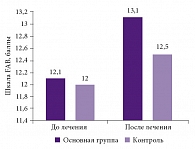
Рис. 5. Динамика когнитивных нарушений по шкале FAB: очаги размозжения и внутричерепные гематомы (p < 0,05)
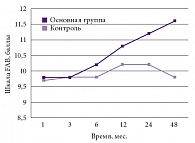
Рис. 6. Динамика выраженных когнитивных нарушений по шкале FAB: очаги размозжения и внутричерепные гематомы (p < 0,01)
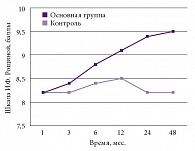
Рис. 7. Динамика выраженных когнитивных нарушений по шкале И.Ф. Рощиной: очаги размозжения и внутричерепные гематомы (p < 0,01)
Введение
Диагностика и лечение когнитивных нарушений – одна из актуальных проблем нейрореабилитации при неврологической и нейрохирургической патологии. Постоянный рост нейротравматизма, широкая распространенность когнитивных нарушений, в значительной мере отягощающих реабилитационный прогноз при последствиях черепно-мозговой травмы, высокая степень инвалидизации пострадавших, в том числе и в результате интеллектуально-мнестических нарушений, обусловливают социальную значимость проблемы диагностики и лечения когнитивной дисфункции.
В последние годы значительные успехи нейрохирургии, анестезиологии и реаниматологии привели к росту выживаемости пациентов с нейрохирургической патологией и сохранению у них удовлетворительного качества жизни, в результате чего у пациентов пожилого и старческого возраста увеличился риск развития цереброваскулярной патологии. Развивающаяся сосудистая деменция приводит к корковой и субкортикальной атрофии вещества головного мозга, причем особое значение имеет атрофия медиальных отделов височной доли. Следует учитывать также наличие множественных корковых инфарктов, лакунарных инфарктов и субкортикальной лейкоэнцефалопатии. В условиях нарастающего дефицита мозгового кровотока вследствие атеросклероза магистральных артерий мозга и повреждения мелких сосудов с последующим развитием лейкоареоза нарастают сосудистые когнитивные расстройства, иногда достигающие степени деменции [1–7].
У пациентов, перенесших тяжелую черепно-мозговую травму с наличием внутричерепных гематом и очагов размозжения головного мозга, развиваются как кистозно-спаечные процессы и внутренняя наружная гидроцефалия, так и выраженные атрофические изменения в зоне наиболее пострадавшего мозгового вещества. Следует подчеркнуть, что единичные постишемические очаги достаточно часто обнаруживаются в таких стратегически важных зонах, как таламус, базальные ганглии и медиобазальные отделы височных долей, а также в лобных долях и гиппокампе. Указанные зоны являются чрезвычайно значимыми для интеллектуально-мнестической деятельности. Сочетание двух процессов – посттравматического и сосудистого, имеющих определенную патоморфологическую основу, у пациентов пожилого и старческого возраста приводит к значительному нарастанию выраженности когнитивных нарушений [8].
Современная стратегия нейропротективной терапии строится на основе анализа результатов клинико-нейрофизиологических, нейровизуализационных и нейропсихологических исследований, но терапевтические возможности коррекции посттравматических когнитивных нарушений, особенно коморбидных с сосудистыми когнитивными нарушениями, изучены еще недостаточно.
При диффузно-очаговых повреждениях в коре большого мозга в течение длительного периода на фоне значительного дефицита межнейронных синапсов происходит сначала репаративная, а затем, вероятно, и репаративно-адаптивная реорганизация нейронных сетей [9].
Нейропротекторы, сохраняя значительную часть нейронов и межнейронных синапсов, обеспечивают структурный гомеостаз нейронных сетей и уменьшают степень неконтролируемой реорганизации межнейронных отношений в поврежденном головном мозге. Все это способствует сохранению уже существующих функциональных систем мозга, облегчает их реабилитацию и препятствует формированию патологических систем мозга [10, 11].
Достаточно часто в отдаленном периоде тяжелой черепно-мозговой травмы назначаются ноотропные препараты (препараты первой линии терапии), однако эффективность этого класса препаратов, так же как и целесообразность их назначения, по-прежнему остается одним из дискуссионных вопросов. Особенно неоднозначным является назначение ноотропных препаратов при наличии посттравматической эпилепсии и специфических изменений биоэлектрической активности головного мозга с наличием высокой судорожной готовности и очагов эпилептической активности. Дискуссионным также остается вопрос эффективности применения статинов, поскольку в настоящее время нет достаточных данных, полученных в рандомизированных исследованиях и подтверждающих целесообразность их использования [12–14].
Базовой терапией при посттравматических когнитивных нарушениях, особенно при присоединении сосудистых нарушений (деменция), остаются вазоактивные препараты, антиоксиданты и блокаторы кальциевых каналов. Но применение только этих групп препаратов также не позволяет добиться клинически значимого результата при выраженной когнитивной дисфункции.
Особого внимания заслуживают результаты применения нейромедиаторной терапии в отдаленном периоде тяжелой черепно-мозговой травмы. Однако, несмотря на несомненные успехи в лечении препаратами медиаторного ряда в остром периоде, клинически значимых результатов в отдаленном периоде черепно-мозговой травмы получено не было [15].
Большие надежды возлагались на применение препаратов с доказанным нейротрофическим действием (Церебролизин), однако возможности этой группы препаратов требуют дальнейшего изучения и, что чрезвычайно важно, оценки результатов сочетанного применения нейромедиаторных и нейротрофических препаратов [16–17].
Обнадеживающими были признаны результаты применения холинергических препаратов в комплексной терапии последствий черепно-мозговой травмы, однако при развитии умеренной и выраженной деменции изолированное применение этой группы препаратов также недостаточно эффективно [18–19].
В последние годы делаются попытки одновременного применения препаратов, оказывающих модулирующее действие как на холинергическую, так и на глутаматергическую систему [20].
Известно, что применение ингибиторов ацетилхолинэстеразы при деменции типа Альцгеймера является практически последней терапевтической стратегией у этих пациентов. Появились сообщения об эффективности применения галантамина (Реминил) при смешанной деменции, а также ривастигмина (Экселон), однако существенных различий результатов назначения этих препаратов отмечено не было. Весьма перспективным остается применение модуляторов глутаматергической системы (антагонисты NMDA-рецепторов) [21].
Назначение пациентам с последствиями тяжелой черепно-мозговой травмы пресинаптического холинергического препарата Глиатилин обусловлено тем, что препарат участвует в регуляторных процессах, активирует фактор роста нервной ткани, улучшает ментальные и когнитивные функции, препятствует развитию амнезии, повышает текучесть мембран в холинергических нейронах, нейрометаболическую защиту мозга [22]. Глиатилин проникает через гематоэнцефалический барьер, способствует сохранению цитоскелета нейрона, сохранению органелл и обладает способностью экономить клеточные энергоресурсы.
Для оценки результатов эффективности сочетанного применения холина альфосцерата (препарат Глиатилин) и ингибиторов ацетилхолинэстеразы (Реминил, Экселон) при умеренных и выраженных когнитивных нарушениях, достигающих степени деменции, у пациентов с последствиями черепно-мозговой травмы было проведено длительное исследование в отдаленном периоде после хирургического лечения внутричерепных гематом и очагов размозжения.
Материалы и методы
В исследование было включено 45 пациентов с последствиями тяжелой черепно-мозговой травмы (29 мужчин, 16 женщин в возрасте от 60 до 79 лет, средний возраст 74 ± 5 года). Срок наблюдения составил 48 месяцев. В основную группу вошли 33 пациента с внутричерепными гематомами (эписубдуральными) и очагами размозжения головного мозга, в контрольную – 12 пациентов с аналогичной степенью тяжести травмы. Все больные были прооперированы.
Первичный результат оценивался на момент выписки из стационара и в процессе лечения; контрольные сроки осмотра были установлены через 1, 3, 6, 12, 24 и 48 месяцев от начала лечения. Проводился анализ структуры и степени выраженности неврологических нарушений и уровня бытовой адаптации с использованием индекса Бартел. Кроме того, интеллектуально-мнестические нарушения оценивались по Краткой шкале оценки психических нарушений (Mini-Mental State Examination, MMSE), исходы и уровень адаптации – по модифицированной шкале Рэнкина, уровень интеллектуально-мнестических нарушений – по шкале батареи тестов лобной дисфункции (Frontal Assessment Battery, FAB). Учитывая целесообразность проведения тщательного нейропсихологического тестирования с уточнением специфики когнитивного синдрома у пациентов с деменцией, также дополнительно использовалась шкала И.Ф. Рощиной. Шкала И.Ф. Рощиной позволяет оценить регуляторные составляющие психической деятельности (контроль за деятельностью, программирование деятельности, динамические параметры деятельности) и операционные составляющие психической деятельности (праксис позы пальцев рук, зрительный гнозис, динамический праксис, письмо, речь, оптико-пространственная деятельность, непосредственное запоминание пяти слов) [23]. Анализировались данные компьютерной и магнитно-резонансной томографий, электроэнцефалографии. Проведена статистическая обработка материала с использованием методов вариационной статистики, а также корреляционный анализ с использованием критериев Пирсона и Спирмена.
Результаты и обсуждение
Был проведен анализ динамики интеллектуально-мнестических (когнитивных) нарушений в течение 48 месяцев после комбинированного применения препарата холина альфосцерата (Глиатилин) и ингибиторов ацетилхолинэстеразы – ривастигмина (Экселон) и галантамина (Реминил). Глиатилин назначался по 400 мг 3 р/сут курсами по 4 месяца с перерывом в один месяц. Реминил применялся по 24 мг/сут в течение 6 месяцев с перерывом в один месяц и повторным курсом. Препарат Экселон применялся в дозировке 3–12 мг/сут по аналогичной схеме.
Все пациенты получали комплексное лечение с учетом основного клинического синдрома и сопутствующей патологии с применением вазоактивных, нейротрофических, ноотропных препаратов и антиоксидантов.
В структуре неврологических нарушений доминировали интеллектуально-мнестические (когнитивные), афатические и двигательные нарушения. Были выделены 2 группы больных с умеренно выраженными когнитивными нарушениями (25 больных в основной группе и 8 больных в контрольной) и выраженными когнитивными нарушениями, достигающими уровня деменции (8 больных в основной группе и 4 больных в контрольной). В клинической картине доминировал церебрально-очаговый синдром (22 больных в основной группе и 7 в контрольной) и гидроцефальный синдром (11 больных в основной группе и 5 в контрольной). Гидроцефальный синдром в основном был представлен нормотензивной гидроцефалией с синдромом Хакима – Адамса.
Анализ уровня бытовой адаптации и динамики неврологических нарушений по индексу Бартел показывает, что сочетанное применение препарата Глиатилин и ингибиторов ацетилхолинэстеразы привело к удовлетворительным результатам лечения (результаты через 48 месяцев достоверно отличались в основной группе по сравнению с контрольной). Индекс Бартел в основной группе составил 85 баллов, а в контрольной – 76. Лучшие результаты были получены при правополушарной локализации процесса и кистозно-атрофических изменениях в области полюса височной доли. Худшие результаты установлены в группе больных с изменениями по данным компьютерной и магнитно-резонансной томографий в медиобазальных отделах височных долей, субкортикально и в области подкорковых ганглиев при значительной распространенности очагов лейкоареоза (рис. 1).
Был проведен анализ исходов по модифицированной шкале Рэнкин. Лучшие результаты также получены в основной группе. Средний балл по шкале Рэнкин в конце лечения составил 2, а в контрольной – 2,3 балла. Существенная положительная динамика в основной группе отмечалась после 6 и 24 месяцев лечения, а в контрольной группе – к концу первого года (средний балл составил 2,3), далее положительной динамики не отмечалось. Худшие результаты были зафиксированы при правополушарной локализации процесса и нормотензивной гидроцефалии. Полученная разница в результатах статистически достоверна (рис. 2).
При оценке динамики когнитивных нарушений по шкале MMSE установлена статистически достоверная разница в результатах лечения основной и контрольной групп. Сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы дало возможность сохранить удовлетворительный уровень когнитивных функций в основной группе, несмотря на то что у значительного числа пациентов изначально были выраженные когнитивные нарушения. Следует отметить, что наличие афатических нарушений в 5 наблюдениях (3 в основной и 2 в контрольной группе) создавало определенные трудности в быту и осложняло достоверность комплексной оценки динамики когнитивных нарушений. В этих 5 наблюдениях при наличии смешанной формы афазии (очаги размозжения лобной доли и постишемические изменения височной доли) отмечался наиболее низкий уровень по шкале MMSE, не превышавший 21,9 балла (рис. 3).
При оценке динамики когнитивных нарушений по шкале И.Ф. Рощиной лучшие результаты также установлены в основной группе (р < 0,05). В целом отмечалось снижение функций программирования и контроля за протеканием психической деятельности. Обнаруживались изменения работы модально-специфических факторов в виде дефектов гнозиса и праксиса. Более скромные результаты были получены при наличии лакунарного поражения передних и базальных отделов лобных и височных долей в сочетании с кистозно-атрофическими (посттравматическими) изменениями полюсов лобных и височных долей, а также при наличии нормотензивной гидроцефалии (рис. 4).
Проведенная оценка динамики когнитивных нарушений по шкале FAB позволила получить результаты, аналогичные оценкам по шкале MMSE и шкале И.Ф Рощиной (p < 0,05). Установлена достоверная корреляционная связь со степенью распространенности лейкоареоза – при умеренной степени распространенности лейкоареоза преобладали умеренные когнитивные нарушения, при выраженном лейкоареозе имели место выраженные когнитивные нарушения, достигающие умеренной и выраженной деменции. Следует отметить, что сочетание посттравматических кистозно-атрофических изменений и выраженного лейкоареоза ухудшало прогноз, и результаты были хуже, чем у пациентов с сочетанием посттравматических кистозно-атрофических и постишемических атрофических изменений. У 2 пациентов, перенесших ишемический полушарный инсульт с массивным инфарктом в бассейне средней мозговой артерии, также были установлены наихудшие результаты динамики когнитивных нарушений по FAB (рис. 5).
Отдельный анализ проводился в группе пациентов с выраженными когнитивными нарушениями (смешанная деменция), в основной группе было 8 пациентов, в контрольной – 4 (возраст – старше 70 лет). В клинической картине у всех пациентов имелся синдром Хакима – Адамса. По данным нейровизуализационных методов обследования была диагностирована нормотензивная гидроцефалия. Анализ результатов динамики когнитивных нарушений по шкале FAB продемонстрировал статистически достоверную разницу между исходами в основной и контрольной группах. Обращает внимание тенденция к устойчивой положительной динамике в основной группе начиная с 3 месяцев лечения. В контрольной группе, несмотря на активное комплексное лечение, существенной положительной динамики достигнуто не было, а начиная с 24 месяцев получена отрицательная динамика когнитивных нарушений с нарастанием деменции. Одному пациенту из этой подгруппы была проведена шунтирующая операция с установкой вентрикулоперитонеального шунта среднего давления, однако позитивного результата получено не было.
В целом следует отметить, что у пациентов с выраженными когнитивными нарушениями не отмечено существенной разницы в зависимости от право- или левосторонней локализации изменений вещества мозга. Существенное значение имели выраженность и распространенность лейкоареоза и множественность лакунарных субкортикальных и подкорковых очагов (рис. 6).
В этой же группе пациентов дополнительно проводилась оценка динамики когнитивных нарушений по шкале И.Ф. Рощиной. Статистически достоверно установлено, что лучшие результаты получены также в основной группе, имелась тенденция к снижению когнитивных функций и в основной, и в контрольной группах при наличии внутримозговых кист в лобных долях (как посттравматических, так и постишемических). Несмотря на относительно невысокий уровень положительной динамики когнитивных нарушений (особенно при наличии нарушений гнозиса и праксиса), уровень бытовой адаптации у пациентов основной группы был выше, чем у пациентов контрольной группы (рис. 7).
Заключение
Проведенное исследование динамики когнитивных нарушений у пациентов с последствиями тяжелой черепно-мозговой травмы при сочетании внутричерепных гематом и очагов размозжения с сосудистым поражением вещества мозга (лакунарные инфаркты, лейкоареоз, постишемические кисты) показало, что включение в комплексное лечение одновременно ингибиторов ацетилхолинэстеразы и холинергических препаратов (Глиатилин) позволяет не только уменьшить степень выраженности когнитивных нарушений, но и повысить уровень бытовой адаптации даже при глубокой деменции.
Таким образом, целесообразно комбинированное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы при выраженных посттравматических нарушениях, особенно у лиц пожилого и старшего возраста.
Диагностика и лечение когнитивных нарушений – одна из актуальных проблем нейрореабилитации при неврологической и нейрохирургической патологии. Постоянный рост нейротравматизма, широкая распространенность когнитивных нарушений, в значительной мере отягощающих реабилитационный прогноз при последствиях черепно-мозговой травмы, высокая степень инвалидизации пострадавших, в том числе и в результате интеллектуально-мнестических нарушений, обусловливают социальную значимость проблемы диагностики и лечения когнитивной дисфункции.
В последние годы значительные успехи нейрохирургии, анестезиологии и реаниматологии привели к росту выживаемости пациентов с нейрохирургической патологией и сохранению у них удовлетворительного качества жизни, в результате чего у пациентов пожилого и старческого возраста увеличился риск развития цереброваскулярной патологии. Развивающаяся сосудистая деменция приводит к корковой и субкортикальной атрофии вещества головного мозга, причем особое значение имеет атрофия медиальных отделов височной доли. Следует учитывать также наличие множественных корковых инфарктов, лакунарных инфарктов и субкортикальной лейкоэнцефалопатии. В условиях нарастающего дефицита мозгового кровотока вследствие атеросклероза магистральных артерий мозга и повреждения мелких сосудов с последующим развитием лейкоареоза нарастают сосудистые когнитивные расстройства, иногда достигающие степени деменции [1–7].
У пациентов, перенесших тяжелую черепно-мозговую травму с наличием внутричерепных гематом и очагов размозжения головного мозга, развиваются как кистозно-спаечные процессы и внутренняя наружная гидроцефалия, так и выраженные атрофические изменения в зоне наиболее пострадавшего мозгового вещества. Следует подчеркнуть, что единичные постишемические очаги достаточно часто обнаруживаются в таких стратегически важных зонах, как таламус, базальные ганглии и медиобазальные отделы височных долей, а также в лобных долях и гиппокампе. Указанные зоны являются чрезвычайно значимыми для интеллектуально-мнестической деятельности. Сочетание двух процессов – посттравматического и сосудистого, имеющих определенную патоморфологическую основу, у пациентов пожилого и старческого возраста приводит к значительному нарастанию выраженности когнитивных нарушений [8].
Современная стратегия нейропротективной терапии строится на основе анализа результатов клинико-нейрофизиологических, нейровизуализационных и нейропсихологических исследований, но терапевтические возможности коррекции посттравматических когнитивных нарушений, особенно коморбидных с сосудистыми когнитивными нарушениями, изучены еще недостаточно.
При диффузно-очаговых повреждениях в коре большого мозга в течение длительного периода на фоне значительного дефицита межнейронных синапсов происходит сначала репаративная, а затем, вероятно, и репаративно-адаптивная реорганизация нейронных сетей [9].
Нейропротекторы, сохраняя значительную часть нейронов и межнейронных синапсов, обеспечивают структурный гомеостаз нейронных сетей и уменьшают степень неконтролируемой реорганизации межнейронных отношений в поврежденном головном мозге. Все это способствует сохранению уже существующих функциональных систем мозга, облегчает их реабилитацию и препятствует формированию патологических систем мозга [10, 11].
Достаточно часто в отдаленном периоде тяжелой черепно-мозговой травмы назначаются ноотропные препараты (препараты первой линии терапии), однако эффективность этого класса препаратов, так же как и целесообразность их назначения, по-прежнему остается одним из дискуссионных вопросов. Особенно неоднозначным является назначение ноотропных препаратов при наличии посттравматической эпилепсии и специфических изменений биоэлектрической активности головного мозга с наличием высокой судорожной готовности и очагов эпилептической активности. Дискуссионным также остается вопрос эффективности применения статинов, поскольку в настоящее время нет достаточных данных, полученных в рандомизированных исследованиях и подтверждающих целесообразность их использования [12–14].
Базовой терапией при посттравматических когнитивных нарушениях, особенно при присоединении сосудистых нарушений (деменция), остаются вазоактивные препараты, антиоксиданты и блокаторы кальциевых каналов. Но применение только этих групп препаратов также не позволяет добиться клинически значимого результата при выраженной когнитивной дисфункции.
Особого внимания заслуживают результаты применения нейромедиаторной терапии в отдаленном периоде тяжелой черепно-мозговой травмы. Однако, несмотря на несомненные успехи в лечении препаратами медиаторного ряда в остром периоде, клинически значимых результатов в отдаленном периоде черепно-мозговой травмы получено не было [15].
Большие надежды возлагались на применение препаратов с доказанным нейротрофическим действием (Церебролизин), однако возможности этой группы препаратов требуют дальнейшего изучения и, что чрезвычайно важно, оценки результатов сочетанного применения нейромедиаторных и нейротрофических препаратов [16–17].
Обнадеживающими были признаны результаты применения холинергических препаратов в комплексной терапии последствий черепно-мозговой травмы, однако при развитии умеренной и выраженной деменции изолированное применение этой группы препаратов также недостаточно эффективно [18–19].
В последние годы делаются попытки одновременного применения препаратов, оказывающих модулирующее действие как на холинергическую, так и на глутаматергическую систему [20].
Известно, что применение ингибиторов ацетилхолинэстеразы при деменции типа Альцгеймера является практически последней терапевтической стратегией у этих пациентов. Появились сообщения об эффективности применения галантамина (Реминил) при смешанной деменции, а также ривастигмина (Экселон), однако существенных различий результатов назначения этих препаратов отмечено не было. Весьма перспективным остается применение модуляторов глутаматергической системы (антагонисты NMDA-рецепторов) [21].
Назначение пациентам с последствиями тяжелой черепно-мозговой травмы пресинаптического холинергического препарата Глиатилин обусловлено тем, что препарат участвует в регуляторных процессах, активирует фактор роста нервной ткани, улучшает ментальные и когнитивные функции, препятствует развитию амнезии, повышает текучесть мембран в холинергических нейронах, нейрометаболическую защиту мозга [22]. Глиатилин проникает через гематоэнцефалический барьер, способствует сохранению цитоскелета нейрона, сохранению органелл и обладает способностью экономить клеточные энергоресурсы.
Для оценки результатов эффективности сочетанного применения холина альфосцерата (препарат Глиатилин) и ингибиторов ацетилхолинэстеразы (Реминил, Экселон) при умеренных и выраженных когнитивных нарушениях, достигающих степени деменции, у пациентов с последствиями черепно-мозговой травмы было проведено длительное исследование в отдаленном периоде после хирургического лечения внутричерепных гематом и очагов размозжения.
Материалы и методы
В исследование было включено 45 пациентов с последствиями тяжелой черепно-мозговой травмы (29 мужчин, 16 женщин в возрасте от 60 до 79 лет, средний возраст 74 ± 5 года). Срок наблюдения составил 48 месяцев. В основную группу вошли 33 пациента с внутричерепными гематомами (эписубдуральными) и очагами размозжения головного мозга, в контрольную – 12 пациентов с аналогичной степенью тяжести травмы. Все больные были прооперированы.
Первичный результат оценивался на момент выписки из стационара и в процессе лечения; контрольные сроки осмотра были установлены через 1, 3, 6, 12, 24 и 48 месяцев от начала лечения. Проводился анализ структуры и степени выраженности неврологических нарушений и уровня бытовой адаптации с использованием индекса Бартел. Кроме того, интеллектуально-мнестические нарушения оценивались по Краткой шкале оценки психических нарушений (Mini-Mental State Examination, MMSE), исходы и уровень адаптации – по модифицированной шкале Рэнкина, уровень интеллектуально-мнестических нарушений – по шкале батареи тестов лобной дисфункции (Frontal Assessment Battery, FAB). Учитывая целесообразность проведения тщательного нейропсихологического тестирования с уточнением специфики когнитивного синдрома у пациентов с деменцией, также дополнительно использовалась шкала И.Ф. Рощиной. Шкала И.Ф. Рощиной позволяет оценить регуляторные составляющие психической деятельности (контроль за деятельностью, программирование деятельности, динамические параметры деятельности) и операционные составляющие психической деятельности (праксис позы пальцев рук, зрительный гнозис, динамический праксис, письмо, речь, оптико-пространственная деятельность, непосредственное запоминание пяти слов) [23]. Анализировались данные компьютерной и магнитно-резонансной томографий, электроэнцефалографии. Проведена статистическая обработка материала с использованием методов вариационной статистики, а также корреляционный анализ с использованием критериев Пирсона и Спирмена.
Результаты и обсуждение
Был проведен анализ динамики интеллектуально-мнестических (когнитивных) нарушений в течение 48 месяцев после комбинированного применения препарата холина альфосцерата (Глиатилин) и ингибиторов ацетилхолинэстеразы – ривастигмина (Экселон) и галантамина (Реминил). Глиатилин назначался по 400 мг 3 р/сут курсами по 4 месяца с перерывом в один месяц. Реминил применялся по 24 мг/сут в течение 6 месяцев с перерывом в один месяц и повторным курсом. Препарат Экселон применялся в дозировке 3–12 мг/сут по аналогичной схеме.
Все пациенты получали комплексное лечение с учетом основного клинического синдрома и сопутствующей патологии с применением вазоактивных, нейротрофических, ноотропных препаратов и антиоксидантов.
В структуре неврологических нарушений доминировали интеллектуально-мнестические (когнитивные), афатические и двигательные нарушения. Были выделены 2 группы больных с умеренно выраженными когнитивными нарушениями (25 больных в основной группе и 8 больных в контрольной) и выраженными когнитивными нарушениями, достигающими уровня деменции (8 больных в основной группе и 4 больных в контрольной). В клинической картине доминировал церебрально-очаговый синдром (22 больных в основной группе и 7 в контрольной) и гидроцефальный синдром (11 больных в основной группе и 5 в контрольной). Гидроцефальный синдром в основном был представлен нормотензивной гидроцефалией с синдромом Хакима – Адамса.
Анализ уровня бытовой адаптации и динамики неврологических нарушений по индексу Бартел показывает, что сочетанное применение препарата Глиатилин и ингибиторов ацетилхолинэстеразы привело к удовлетворительным результатам лечения (результаты через 48 месяцев достоверно отличались в основной группе по сравнению с контрольной). Индекс Бартел в основной группе составил 85 баллов, а в контрольной – 76. Лучшие результаты были получены при правополушарной локализации процесса и кистозно-атрофических изменениях в области полюса височной доли. Худшие результаты установлены в группе больных с изменениями по данным компьютерной и магнитно-резонансной томографий в медиобазальных отделах височных долей, субкортикально и в области подкорковых ганглиев при значительной распространенности очагов лейкоареоза (рис. 1).
Был проведен анализ исходов по модифицированной шкале Рэнкин. Лучшие результаты также получены в основной группе. Средний балл по шкале Рэнкин в конце лечения составил 2, а в контрольной – 2,3 балла. Существенная положительная динамика в основной группе отмечалась после 6 и 24 месяцев лечения, а в контрольной группе – к концу первого года (средний балл составил 2,3), далее положительной динамики не отмечалось. Худшие результаты были зафиксированы при правополушарной локализации процесса и нормотензивной гидроцефалии. Полученная разница в результатах статистически достоверна (рис. 2).
При оценке динамики когнитивных нарушений по шкале MMSE установлена статистически достоверная разница в результатах лечения основной и контрольной групп. Сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы дало возможность сохранить удовлетворительный уровень когнитивных функций в основной группе, несмотря на то что у значительного числа пациентов изначально были выраженные когнитивные нарушения. Следует отметить, что наличие афатических нарушений в 5 наблюдениях (3 в основной и 2 в контрольной группе) создавало определенные трудности в быту и осложняло достоверность комплексной оценки динамики когнитивных нарушений. В этих 5 наблюдениях при наличии смешанной формы афазии (очаги размозжения лобной доли и постишемические изменения височной доли) отмечался наиболее низкий уровень по шкале MMSE, не превышавший 21,9 балла (рис. 3).
При оценке динамики когнитивных нарушений по шкале И.Ф. Рощиной лучшие результаты также установлены в основной группе (р < 0,05). В целом отмечалось снижение функций программирования и контроля за протеканием психической деятельности. Обнаруживались изменения работы модально-специфических факторов в виде дефектов гнозиса и праксиса. Более скромные результаты были получены при наличии лакунарного поражения передних и базальных отделов лобных и височных долей в сочетании с кистозно-атрофическими (посттравматическими) изменениями полюсов лобных и височных долей, а также при наличии нормотензивной гидроцефалии (рис. 4).
Проведенная оценка динамики когнитивных нарушений по шкале FAB позволила получить результаты, аналогичные оценкам по шкале MMSE и шкале И.Ф Рощиной (p < 0,05). Установлена достоверная корреляционная связь со степенью распространенности лейкоареоза – при умеренной степени распространенности лейкоареоза преобладали умеренные когнитивные нарушения, при выраженном лейкоареозе имели место выраженные когнитивные нарушения, достигающие умеренной и выраженной деменции. Следует отметить, что сочетание посттравматических кистозно-атрофических изменений и выраженного лейкоареоза ухудшало прогноз, и результаты были хуже, чем у пациентов с сочетанием посттравматических кистозно-атрофических и постишемических атрофических изменений. У 2 пациентов, перенесших ишемический полушарный инсульт с массивным инфарктом в бассейне средней мозговой артерии, также были установлены наихудшие результаты динамики когнитивных нарушений по FAB (рис. 5).
Отдельный анализ проводился в группе пациентов с выраженными когнитивными нарушениями (смешанная деменция), в основной группе было 8 пациентов, в контрольной – 4 (возраст – старше 70 лет). В клинической картине у всех пациентов имелся синдром Хакима – Адамса. По данным нейровизуализационных методов обследования была диагностирована нормотензивная гидроцефалия. Анализ результатов динамики когнитивных нарушений по шкале FAB продемонстрировал статистически достоверную разницу между исходами в основной и контрольной группах. Обращает внимание тенденция к устойчивой положительной динамике в основной группе начиная с 3 месяцев лечения. В контрольной группе, несмотря на активное комплексное лечение, существенной положительной динамики достигнуто не было, а начиная с 24 месяцев получена отрицательная динамика когнитивных нарушений с нарастанием деменции. Одному пациенту из этой подгруппы была проведена шунтирующая операция с установкой вентрикулоперитонеального шунта среднего давления, однако позитивного результата получено не было.
В целом следует отметить, что у пациентов с выраженными когнитивными нарушениями не отмечено существенной разницы в зависимости от право- или левосторонней локализации изменений вещества мозга. Существенное значение имели выраженность и распространенность лейкоареоза и множественность лакунарных субкортикальных и подкорковых очагов (рис. 6).
В этой же группе пациентов дополнительно проводилась оценка динамики когнитивных нарушений по шкале И.Ф. Рощиной. Статистически достоверно установлено, что лучшие результаты получены также в основной группе, имелась тенденция к снижению когнитивных функций и в основной, и в контрольной группах при наличии внутримозговых кист в лобных долях (как посттравматических, так и постишемических). Несмотря на относительно невысокий уровень положительной динамики когнитивных нарушений (особенно при наличии нарушений гнозиса и праксиса), уровень бытовой адаптации у пациентов основной группы был выше, чем у пациентов контрольной группы (рис. 7).
Заключение
Проведенное исследование динамики когнитивных нарушений у пациентов с последствиями тяжелой черепно-мозговой травмы при сочетании внутричерепных гематом и очагов размозжения с сосудистым поражением вещества мозга (лакунарные инфаркты, лейкоареоз, постишемические кисты) показало, что включение в комплексное лечение одновременно ингибиторов ацетилхолинэстеразы и холинергических препаратов (Глиатилин) позволяет не только уменьшить степень выраженности когнитивных нарушений, но и повысить уровень бытовой адаптации даже при глубокой деменции.
Таким образом, целесообразно комбинированное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы при выраженных посттравматических нарушениях, особенно у лиц пожилого и старшего возраста.
1. Gorelick P.B., Pantoni L. Advances in vascular cognitive impairment // Stroke. 2013. Vol. 44. № 2. P. 307–308.
2. Schneider J.A., Arvanitakis Z., Bang W. et al. Mixed brain pathologies account for most dementia cases in community-dwelling older persons // Neurology. 2007. Vol. 69. № 24. P. 2197–2204.
3. Jokinen H., Lipsanen J., Schmidt R. et al. Brain atrophy accelerates cognitive decline in cerebral small vessel disease: the LADIS study // Neurology. 2012. Vol. 78. № 22. P. 1785–1792.
4. Nitkunan A., Lanfranconi S., Charlton R.A. et al. Brain atrophy and cerebral small vessel disease: a prospective follow-up study // Stroke. 2011. Vol. 42. № 1. P. 133–138.
5. Raji C.A., Lopez O.L., Kuller L.H. et al. White matter lesions and brain gray matter volume in cognitively normal elders // Neurobiol. Aging. 2012. Vol. 33. № 4. P. 834.
6. Kloppenborg R.P., Nederkoorn P.J., Grool A.M. et al. Cerebral small-vessel disease and progression of brain atrophy: the SMART-MR study // Neurology. 2012. Vol. 79. № 20. P. 2029–2036.
7. Jouvent E., Mangin J.F., Duchesnay E. et al. Longitudinal changes of cortical morphology in CADASIL // Neurobiol. Aging. 2012. Vol. 33. № 5. P. 1002.
8. Одинак М.М., Емелин А.Ю., Лобзин В.Ю. Нарушение когнитивных функций при цереброваскулярной патологии. СПб.: ВМедА, 2006. 158 с.
9. Семченко В.В., Степанов С.С., Боголепов Н.Н. Синаптическая пластичность головного мозга. Омск: Омская областная типография, 2008. 407 с.
10. Семченко В.В., Боголепов Н.Н., Степанов С.С. Структурно-функциональные закономерности реализации механизмов синаптической пластичности // Омский научный вестник. 2003. № 24. Приложение. С. 33–39.
11. Dobkin B.H. Neurobiology of rehabilitation // Ann. N. Y. Acad. Sci. 2004. Vol. 1038. P. 148–170.
12. Atri A., Shaughnessy L.W., Locascio J.J. et al. Long-term course and effectiveness of combination therapy in Alzheimer disease // Alzheimer Dis. Assoc. Disord. 2008. Vol. 22. № 3. P. 209–221.
13. Ballard C., Sauter M., Scheltens P. et al. Efficacy, safety and tolerability of rivastigmine capsules in patients with probable vascular dementia: the VantagE study // Curr. Med. Res. Opin. 2008. Vol. 24. № 9. P. 2561–2574.
14. Bernick C., Katz R., Smith N.L. et al. Statins and cognitive function in the elderly: the Cardiovascular health study // Neurology. 2005. Vol. 65. № 9. P. 1388–1394.
15. Chui H.C. Subcortical ischemic vascular dementia // Neurol. Clin. 2007. Vol. 25. № 3. P. 717–740.
16. Flicker L., Grimley E.G. Piracetam for dementia or cognitive impairment // Cochrane Database Syst. Rev. 2001. Vol. 2. CD001011.
17. Pantoni L. Treatment of vascular dementia: evidence from trials with non-cholinergic drugs // J. Neurol. Sci. 2004. Vol. 226. № 1–2. P. 67–70.
18. Parnetti L., Mignini F., Tomassoni D. et al. Cholinergic precursors in the treatment of cognitive impairment of vascular origin: ineffective approaches or need for re-evaluation? // J. Neurol. Sci. 2007. Vol. 257. № 1–2. P. 264–269.
19. Tomassoni D., Lanari A., Silvestrelli G. et al. Nimodipine and its use in cerebrovascular disease: evidence from recent preclinical and controlled clinical studies // Clin. Exp. Hypertens. 2008. Vol. 30. № 8. P. 744–766.
20. Wilkinson D., Doody R., Helme R. et al. Donepezil in vascular dementia: a randomized, placebo-controlled study // Neurology. 2003. Vol. 61. № 4. P. 479–486.
21. Winblad B., Fioravanti M., Dolezal T. et al. Therapeutic use of nicergoline // Clin. Drug Investig. 2008. Vol. 28. № 9. P. 533–552.
22. Иванова Н.Е. Результаты применения Глиатилина при когнитивных нарушениях у пациентов с последствиями тяжелой черепно-мозговой травмы // Эффективная фармакотерапия. Неврология и психиатрия. 2012. № 5. С. 8–12.
23. Рощина И.Ф., Жариков Г.А. Нейропсихологический метод в диагностике мягкой деменции у лиц пожилого и старческого возраста // Журнал невропатологии и психиатрии им. С.С. Корсакова. 1998. Т. 98. № 2. С. 34–39.
The use of choline donators and acetylcholinesterase inhibitors in the cognitive rehabilitation after Severe Brain Injury
N.Ye. Ivanova
Russian Polenov’s Neurosurgical Institute
Contact person: Natalya Yevgenyevna Ivanova, ivamel@yandex.ru
The author studied efficacy of the donors of choline and acetylcholinesterase inhibitors during neuro-rehabilitation of patients with cognitive impairment as the consequences of severe traumatic brain injury. Some particular features of the dynamics of cognitive impairment in the late period of severe traumatic brain injury in group of patients with combination of intracranial hematoma with focal contusions were identified. The analysis of the effects of treatment showed that the inclusion of donor of choline and acetylcholinesterase inhibitors is a promising direction for both prevention and treatment of mental disorders after severe traumatic brain injury.
Key words: the late period of severe traumatic brain injury, cognitive impairment, cholinomimetic, acetylcholinesterase inhibitors
N.Ye. Ivanova
Russian Polenov’s Neurosurgical Institute
Contact person: Natalya Yevgenyevna Ivanova, ivamel@yandex.ru
The author studied efficacy of the donors of choline and acetylcholinesterase inhibitors during neuro-rehabilitation of patients with cognitive impairment as the consequences of severe traumatic brain injury. Some particular features of the dynamics of cognitive impairment in the late period of severe traumatic brain injury in group of patients with combination of intracranial hematoma with focal contusions were identified. The analysis of the effects of treatment showed that the inclusion of donor of choline and acetylcholinesterase inhibitors is a promising direction for both prevention and treatment of mental disorders after severe traumatic brain injury.
Key words: the late period of severe traumatic brain injury, cognitive impairment, cholinomimetic, acetylcholinesterase inhibitors
Новости на тему
09.02.2023
СТАТЬИ по теме
09.04.2024
Отправить статью по электронной почте
Ваш адрес электронной почты:
В статье приведены результаты комплексного применения пресинаптических холинергических препаратов и ингибиторов ацетилхолинэстеразы при когнитивных нарушениях в системе нейрореабилитации пациентов с последствиями тяжелой черепно-мозговой травмы.
Выявлены особенности динамики когнитивных нарушений в отдаленном периоде тяжелой черепно-мозговой травмы у пациентов с внутричерепными гематомами и очагами размозжения. Анализ динамики когнитивных нарушений при последствиях тяжелой черепно-мозговой травмы показал, что сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы является перспективным направлением как для профилактики, так и для лечения выраженных нарушений интеллектуально-мнестических функций.
Выявлены особенности динамики когнитивных нарушений в отдаленном периоде тяжелой черепно-мозговой травмы у пациентов с внутричерепными гематомами и очагами размозжения. Анализ динамики когнитивных нарушений при последствиях тяжелой черепно-мозговой травмы показал, что сочетанное применение холинергических препаратов и ингибиторов ацетилхолинэстеразы является перспективным направлением как для профилактики, так и для лечения выраженных нарушений интеллектуально-мнестических функций.
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
