Шах и мат: Опдиво в лечении меланомы. XXII Российский онкологический конгресс. Сателлитный симпозиум компании Bristol-Myers Squibb
- Аннотация
- Статья
- Ссылки




Яркий дебют Опдиво в меланоме
Заместитель директора по онкологии Московского клинического научного центра им. А.С. Логинова, д.м.н., профессор Людмила Григорьевна ЖУКОВА рассказала о ярком дебюте Опдиво. Это один из первых препаратов, активирующих противоопухолевый иммунный ответ, продемонстрировавших эффективность не только в отношении меланомы, но и других злокачественных новообразований.
Еще 15 лет назад меланома считалась фатальным заболеванием: общая выживаемость больных метастатической меланомой не превышала 6–9 месяцев1. Появление в реальной клинической практике новых иммуноонкологических препаратов (ингибиторы CTLA-4, PD-1) позволило увеличить общую выживаемость пациентов с метастатической меланомой.
Меланома характеризуется максимальным количеством соматических мутаций. Высокая частота мутаций способствует повышенной экспрессии неоантигенов, которые могут запускать начальные процессы иммунной реакции организма. С последующим введением онкоиммунных препаратов эта реакция усиливается и улучшается ответ на иммунотерапию2–4.
Инфильтрация опухоли цитотоксическими (СD8+) Т-лимфоцитами определяет более благоприятный прогноз заболевания. Показатель выживаемости больных метастатической меланомой с высоким уровнем инфльтрации цитотоксическими T-клетками достоверно (р = 0,0001) выше, чем у больных с низким уровнем инфильтрации Т-клеток5.
Агрессивная атака меланомы требует активной защиты. Важно поддержать начавшуюся иммунную реакцию.
Ипилимумаб – первый иммуноонкологический препарат, ингибитор рецептора CTLA-4 на поверхности Т-лимфоцитов, блокирование которого приводит к активации противоопухолевого иммунитета. В клинических исследованиях у пациентов с метастатической меланомой, получавших ипилимумаб, трехлетняя общая выживаемость составила 22%, при этом кривая далее переходит на плато6. Открытие пути CTLA-4 принадлежит Джеймсу Эллисону.
Блокирование рецепторов PD-1, расположенных также на поверхности T-лимфоцитов, является вторым способом активации противоопухолевого иммунного ответа. За открытием этого пути активации стоит Тасуку Хондзе. Открытие этих рецепторов и разработка противоопухолевой терапии, в основе которой лежит ингибирование контрольных точек иммунного ответа, стали настоящим открытием в онкологии, за которое в 2018 г. ученые были удостоены Нобелевской премии по медицине.
Представителем блокаторов PD-1 является ниволумаб (Опдиво)7.
Ниволумаб – моноклональное антитело, которое связывается с рецептором PD-1 на поверхности Т-лимфоцитов и блокирует инактивирующее влияние этого рецептора на иммунный ответ. Опухолевые клетки, экспрессирующие на своей поверхности лиганды к PD-1-рецептору – PD-L1 и PD-L2, не могут ускользать от иммунного ответа7.
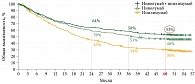
В рандомизированном клиническом исследовании III фазы CheckMatе 066 сравнивали эффективность монотерапии ниволумабом и дакарбазином у пациентов с BRAF-негативной меланомой. Ниволумаб продемонстрировал преимущество перед дакарбазином. Одногодичная общая выживаемость в группах ниволумаба и дакарбазина составила 71 и 45%, двухлетняя – 58 и 26%, трехлетняя – 51 и 22% соответственно (рис. 1).
Выживаемость без прогрессирования (ВБП) в группе ниволумаба была выше, чем в группе дакарбазина: одногодичная ВБП – 43 и 7%, двухлетняя – 35 и 6%, трехлетняя – 32 и 3% соответственно. В группе ниволумаба отмечалось снижение риска прогрессирования на 58%, смерти – на 54%. Частота объективного ответа на терапию ниволумабом зарегистрирована в 43% случаев, дакарбазином – в 14%8.
Согласно результатам исследования, большинство пациентов обеих групп после прогрессирования заболевания получали дополнительно иммунотерапию препаратами ипилимумаб, пембролизумаб, а также ниволумаб.
Медиана общей выживаемости пациентов группы ниволумаба, получавших после прогрессирования заболевания ипилимумаб, составила 21,5 месяца (95% доверительный интервал (ДИ) 14,2–28,3). Медиана общей выживаемости у больных группы дакарбазина, получавших после прогрессирования заболевания ниволумаб, достигла 35,4 месяца. Медиана общей выживаемости у больных, получавших после прогрессирования заболевания на фоне терапии ниволумабом последующую иммунотерапию ипилимумабом, составила 17,8 месяца (95% ДИ 11,7–22,1).
Анализ данных общей выживаемости и ВБП в зависимости от выраженности экспрессии PD-L1 показал, что терапия ниволумабом эффективнее, чем терапия дакарбазином, при любом уровне PD-L1.
Летальных исходов, обусловленных нежелательными явлениями, не зафиксировано. Нежелательные явления и частота их возникновения соответствовали ранее полученным результатам клинических исследований не только меланомы, но и других злокачественных новообразований8.
Проводились сравнительные исследования, в которых ингибиторы PD-1 сравнивали с ипилимумабом. В исследовании KEYNOTE 006, посвященном сравнительной оценке эффективности пембролизумаба в дозе 10 мг/кг и ипилимумаба, показатели трехлетней общей выживаемости на фоне терапии пембролизумабом были на 10% выше, чем при использовании ипилимумаба, – 48,1 и 37,8% соответственно.
В исследовании CheckMate 067 при сравнении эффективности монотерапии ниволумабом в дозе 3 мг/кг и ипилимумабом больных метастатической меланомой с медианой наблюдения 46,9 месяца четырехлетняя общая выживаемость на фоне применения ниволумаба составила 46% по сравнению с 30% при использовании ипилимумаба. Анализ эффективности терапии в зависимости от BRAF-статуса (дикий тип или мутация) продемонстрировал, что ниволумаб обеспечивает более высокие результаты в отношении четырехлетней выживаемости пациентов как при диком типе BRAF, так и при наличии BRAF-мутации по сравнению с ипилимумабом: 46 против 28% и 50 против 33% соответственно9.
Оценка безопасности терапии ниволумабом и ипилимумабом подтвердила лучший профиль безопасности ниволумаба, при этом спектр нежелательных явлений не отличался от ранее продемонстрированного для иммуноонкологических препаратов. Большинство нежелательных явлений были управляемы и разрешились через три-четыре недели10.
Безусловно, алгоритм лечения должен быть сугубо индивидуальным. В качестве примера были представлены два профиля пациентов, для которых ниволумаб в качестве препарата первой линии может оказаться наиболее оптимальным.
Профиль пациента 1. Клинические данные: меланома кожи туловища с поражением лимфатических узлов, множественные метастазы в подкожную клетчатку и кожу, солитарный метастаз в легкое, опухоль BRAF-мутированная, уровень лактатдегидрогеназы (ЛДГ) в пределах нормы.
Тем не менее при интерактивном голосовании большинство участников (56,8%) выбрали терапию комбинацией BRAF и МЕК-ингибиторов и лишь 35% – монотерапию ингибиторами PD-1.
Согласно комментариям профессора Л.Г. Жуковой, назначение монотерапии ингибиторами PD-1 (ниволумаб, пембролизумаб) для малосимптомного пациента с наличием BRAF-мутированной опухоли соответствует современным международным представлениям о ведении пациентов с метастатической меланомой в отсутствие признаков висцерального криза.
Профиль пациента 2. Клинические данные: меланома кожи голени с поражением девяти лимфатических узлов; через девять месяцев после операции метастазы в легких; солитарный метастаз в печени 3 см; опухоль BRAF-негативная; ЛДГ – в пределах нормы.
При интерактивном голосовании большинство участников симпозиума (56,8%) отдали предпочтение комбинации «ниволумаб + ипилимумаб», треть (31,1%) – монотерапии ингибиторами PD-1.
По словам профессора Л.Г. Жуковой, в такой ситуации исходные клинические данные крайне неблагоприятны. Резкое прогрессирование заболевания после иссечения первичной опухоли, множественное поражение лимфоузлов, значимая опухолевая масса дают основание для выбора максимально эффективного варианта лечения. На сегодняшний день это назначение двух иммунопрепаратов.
Итак, ниволумаб в качестве первой линии терапии следует назначать пациенту с BRAF-положительной меланомой в отсутствие значимых симптомов заболевания, уровень ЛДГ в норме или несколько повышен (хуже прогноз). Уровень экспрессии PD-L1 не имеет значения, в том числе при отсутствии данных. Меланома слизистых оболочек. Комплаентный пациент, поскольку возможность обратной связи позволяет обеспечить не только эффективное, но и безопасное лечение.
Завершая выступление, профессор Л.Г. Жукова перечислила основные преимущества препарата ниволумаб (Опдиво) при распространенной меланоме11–13:
- улучшение объективного ответа и выживаемости;
- эффективность, не зависящая от наличия мутации BRAF;
- оптимальное место – первая линия терапии;
- большинство иммуноопосредованных нежелательных реакций обратимы при использовании разработанных алгоритмов управления токсичностью;
- одинаковая доза и единый режим введения – 3 мг/кг каждые две недели, зарегистрированные в РФ, изучались во всех клинических исследованиях ниволумаба.
Комбинированная иммунотерапия метастатической меланомы
По словам заведующего отделением городской онкологической больницы № 62, к.м.н. Даниила Львовича СТРОЯКОВСКОГО, эффективное ведение больного меланомой иногда напоминает стратегически выверенную и успешно разыгранную шахматную партию.
Как уже отмечалось, ингибиторы различных контрольных точек действуют на разных этапах активации иммунного ответа. Если ипилимумаб, будучи ингибитором CTLA-4, действует на первичной фазе, когда опухолевый антиген презентируется неактивным Т-лимфоцитам, то ингибитор PD-1 ниволумаб работает в опухолевом микроокружении на эффекторной фазе7. Логично предположить, что комбинация этих двух препаратов способствует более эффективной работе иммунной системы.
В исследовании CheckMate 064 изучали возможности последовательного применения ниволумаба и ипилимумаба у больных метастатической меланомой независимо от статуса мутации BRAF. В отношении общей выживаемости показано преимущество назначения сначала ниволумаба, затем лечения ипилимумабом с последующим переходом снова на ниволумаб14.
Ключевым считается рандомизированное двойное слепое исследование CheckMate 067, в котором сравнивали эффективность комбинации ниволумаба и ипилимумаба или ниволумаба в монорежиме и монотерапии ипилимумабом9.
945 больных неоперабельной метастатической меланомой, ранее не получавших лечения, были рандомизированы на три равные группы. 314 пациентов первой группы получали лечение по схеме: ниволумаб 1 мг/кг + ипилимумаб 3 мг/кг каждые три недели, всего четыре введения, затем ниволумаб 3 мг/кг каждые две недели до прогрессии заболевания или неприемлемой токсичности, 316 пациентов второй группы – ниволумаб 3 мг/кг каждые две недели до прогрессии заболевания или неприемлемой токсичности и 315 пациентов третьей группы – ипилимумаб 3 мг/кг каждые три недели, всего четыре введения.
Уже доступны данные четырехлетнего наблюдения. Частота объективного ответа (ЧОО) в группе комбинации «ниволумаб + ипилимумаб» составила 58,3%, в группе ниволумаба – 44,6%, в группе ипилимумаба – 19%. Медиана длительности ответа (ДО) в группе комбинации не достигнута к четырем годам и на данном этапе, по предварительной оценке, составила 50,1 месяца. Медиана ДО в группе ниволумаба не достигнута, а в группе ипилимумаба – 14,4 месяца.
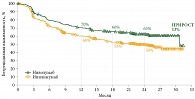
На момент первичного анализа медиана общей выживаемости не достигнута во всех группах, двухгодичная общая выживаемость составила 64% в группе комбинации, 59% в группе ниволумаба, 45% в группе ипилимумаба. При увеличении сроков наблюдения до 36 и 48 месяцев медиана общей выживаемости не достигнута в группе, получавшей комбинацию ниволумаба и ипилимумаба. В группе монотерапии ниволумабом к 48-му месяцу наблюдения медиана общей выживаемости достигла 36,9 месяца, в группе ипилимумаба – 19,9 месяца. Показатели четырехлетней общей выживаемости составили 53% в группе комбинации «ниволумаб + ипилимумаб», 46% в группе ниволумаба, 30% в группе ипилимумаба (рис. 2).
Четырехлетняя ВБП составила 37% в группе комбинации, 31% в группе ниволумаба и 9% в группе ипилимумаба.
Экспрессия PD-L1 считается одним из ведущих прогностических маркеров с точки зрения потенциала иммунотерапии. Дополнительный анализ влияния на эффективность терапии уровня экспрессии PD-L1 на опухолевых клетках показал, что комбинация более эффективна при любом уровне экспрессии: разница в показателях четырехлетней общей выживаемости при PD-L1 ≤ 5% и ≥ 5% составила 7% по сравнению с монотерапией ниволумабом.
Оценка эффективности иммунотерапии в зависимости от статуса мутации BRAF также продемонстрировала определенное преимущество комбинированной терапии перед ниволумабом. У пациентов с мутацией BRAF четырехлетняя общая выживаемость составила 62% в группе комбинации «ниволумаб + ипилимумаб», 50% в группе ниволумаба, 33% в группе ипилимумаба. У пациентов с диким типом BRAF четырехлетняя общая выживаемость в группе комбинации достигла 49%, в группе ниволумаба – 45% и в группе ипилимумаба – 28%.
Как выбрать терапию в зависимости от мутации BRAF? Согласно данным исследования, у больных метастатической меланомой с диким типом BRAF четырехлетняя ЧОО на фоне терапии пембролизумабом, ниволумабом и комбинацией «ниволумаб + ипилимумаб» не имеет существенных различий и составляет 42–53%. Показатели четырехлетней ВБП сопоставимы при монотерапии ниволумабом и комбинации «ниволумаб + ипилимумаб» – 34 и 35% соответственно9, 15. Таким образом, применима любая из трех иммунотерапевтических опций. Главное – учитывать токсичность и стоимость препарата.
В случае с BRAF-мутированной метастатической меланомой в распоряжении онкологов помимо трех опций иммунотерапии имеется еще одна опция – таргетная терапия. ЧОО на фоне таргетной терапии выше, чем на фоне монотерапии ниволумабом или пембролизумабом, но сопоставима с таковой на комбинации «ниволумаб + ипилимумаб»9, 15, 16. При этом комбинация «ниволумаб + ипилимумаб» выигрывает по показателю четырехлетней ВБП – 39%, при монотерапии ниволумабом – 22%.
Д.Л. Строяковский также проанализировал выбор терапии в зависимости от уровня ЛДГ. При нормальном уровне ЛДГ таргетная терапия позволяет достичь трехлетней ВБП 27%. Комбинация «ниволумаб + ипилимумаб» и монотерапия ниволумабом – 45 и 37% соответственно. Трехлетняя общая выживаемость на таргетной терапии при нормальном уровне ЛДГ составляет 54%, иммунотерапия демонстрирует схожую общую выживаемость как для комбинации ниволумаба и ипилимумаба, так и для монотерапии ниволумабом (66 и 61% соответственно). При ЛДГ выше нормы комбинация «ниволумаб + ипилимумаб» позволяет достичь трехлетней ВБП 28% и трехлетней общей выживаемости 44%. На таргетной терапии при высоком уровне ЛДГ трехлетняя ВБП составляет 13%, трехлетняя общая выживаемость – 21%9, 15, 16.
Согласно данным скорректированного непрямого сравнения комбинации «ниволумаб + ипилимумаб» и комбинации BRAF/MEK-ингибиторов, в первый год лечения обе комбинации демонстрируют сопоставимую эффективность. При более длительном периоде наблюдения (больше одного года) комбинация «ниволумаб + ипилимумаб» показывает преимущество по ВБП и общей выживаемости перед комбинацией BRAF/MEK-ингибиторов17.
B исследовании CheckMate 067 показано, что среди живых пациентов с метастатической меланомой к четвертому году наблюдения наибольшая доля пациентов, после отмены терапии сохранявших достигнутый ответ и не получавших последующую терапию (71%), была в группе комбинации «ниволумаб + ипилимумаб»9.
В отдельном исследовании (CA209–170) оценивали эффективность комбинации «ниволумаб + ипилимумаб» при метастазах в головном мозге. У пациентов с асимптомными метастазами в головном мозге эффективность комбинации «ниволумаб + ипилимумаб» более чем в два раза превышала таковую при монотерапии ниволумабом18.
B исследовании CheckMate 067 сравнивали безопасность комбинации ниволумаба и ипилимумаба с монотерапией ниволумабом и ипилимумабом9. Частота нежелательных реакций, связанных с лечением, составила 96% в группе комбинации «ниволумаб + ипилимумаб», 86% в группе ниволумаба и 86% в группе ипилимумаба.
Зарегистрировано два летальных исхода, обусловленных нежелательными реакциями: один в группе ниволумаба (нейтропения), другой – в группе ипилимумаба (перфорация кишки). В группе комбинации ниволумаба и ипилимумаба зафиксировано два летальных исхода (кардиомиопатия и некроз печени). Однако они наступили спустя более чем 100 дней после введения последней дозы препарата.
Несмотря на то что частота нежелательных реакций при назначении комбинации ниволумаба и ипилимумаба была выше, все нежелательные реакции управляемы и обратимы. В то же время данные свидетельствуют, что при прекращении терапии комбинацией «ниволумаб + ипилимумаб» в связи с развитием тяжелых нежелательных реакций эффект от лечения сохраняется19.
В исcледовании CheckMate 511 сравнивали эффективность комбинации ниволумаба и ипилимумаба в стандартной и низкой дозе20. Пациенты с неоперабельной меланомой стадии III–IV, ранее не получавшие лечения, были рандомизированы на две группы. Пациенты первой получали комбинацию ниволумаба 3 мг/кг и ипилимумаба 1 мг/кг, четыре введения, пациенты второй – комбинацию ниволумаба 1 мг/кг и ипилимумаба 3 мг/кг.
Показано, что снижение дозы ипилимумаба приводит к уменьшению токсичности терапии: в группе комбинации ниволумаба 3 мг/кг и ипилимумаба 1 мг/кг частота нежелательных реакций 3–5-й степени была на 14,4% меньше, чем в группе комбинации ниволумаба 1 мг/кг и ипилимумаба 3 мг/кг (33,9 против 48,3%).
На момент первичного анализа при минимальном периоде наблюдения 12 месяцев медиана общей выживаемости не достигнута в обеих группах. Одногодичная общая выживаемость в группе комбинации ниволумаба 3 мг/кг и ипилимумаба 1 мг/кг составила 79,7%, в группе комбинации ниволумаба 1 мг/кг и ипилимумаба 3 мг/кг – 81%. В обеих группах также отмечались сопоставимые результаты одногодичной ВБП – 47,2 и 46,4% соответственно. Наблюдение продолжается.
Кому целесообразно назначать комбинацию ниволумаба и ипилимумаба? Д.Л. Строяковский обсудил два возможных профиля пациентов.
Профиль пациента 1. Клинические данные: меланома кожи туловища; множественные метастазы в подкожной клетчатке и коже; солитарный метастаз в легком; BRAF-мутированная опухоль; ЛДГ выше нормы.
Согласно результатам интерактивного голосования, большинство участников симпозиума (72,3%) проголосовали за комбинацию «ниволумаб + ипилимумаб». Д.Л. Строяковский согласился, что в данном случае комбинированная иммунотерапия может увеличить продолжительность жизни.
Профиль пациента 2. Клинические данные: меланома кожи спины; множественные метастазы в легких; метастаз в печени 3 см; асимптомный метастаз в головном мозге 1,5 см; опухоль BRAF-негативная; ЛДГ в пределах нормы.
При голосовании 80,9% участников сделали выбор в пользу комбинации ниволумаба и ипилимумаба. Докладчик отметил, что этот вариант терапии, по данным клинических исследований, действительно наиболее предпочтителен.
Таким образом, в комбинированной терапии нуждаются пациенты со статусом ECOG 0–1, BRAF-негативной и BRAF-позитивной меланомой, ЛДГ в норме или выше нормы, любым PD-L1-статусом, меланомой слизистых оболочек, а также при наличии асимптомных метастазов в головном мозге менее 3 см, но не более пяти очагов.
В завершение Д.Л. Строяковский констатировал, что сегодня комбинация ниволумаба и ипилимумаба демонстрирует наилучшую отдаленную общую выживаемость у больных с практически некурабельным заболеванием.
Ход конем. Опдиво в адъювантном лечении меланомы
Заведующий хирургическим отделением № 10 Научно-исследовательского института клинической онкологии НМИЦ онкологии им. Н.Н. Блохина, профессор кафедры онкологии Первого Московского государственного медицинского университета им. И.М. Сеченова, председатель Ассоциации специалистов по проблемам меланомы, д.м.н. Лев Вадимович ДЕМИДОВ разыграл эндшпиль. Он представил данные об успешном применении ниволумаба в режиме адъювантной терапии больных меланомой III и IV стадии после полной резекции опухоли.
Результаты исследований и клинический опыт демонстрируют, что выживаемость пациентов с локализованной меланомой стадий II–III остается неудовлетворительной21.
На протяжении ряда лет, вплоть до 2017 г., выбор опций адъювантной терапии меланомы ограничивался интерфероном (ИФН) альфа и наблюдением, в США еще ипилимумабом в высокой дозе (10 мг/кг)22. Тем не менее в исследованиях применение ИФН далеко не всегда улучшало отдаленные результаты23. По словам докладчика, адъювантная терапия значимо не влияет на общую выживаемость.
Впервые существенное улучшение общей выживаемости при адъювантной терапии достигнуто в исследовании ипилимумаба 10 мг/кг: при пятилетнем наблюдении удалось добиться снижения риска прогрессирования заболевания на 24%, а смерти – на 28% по сравнению с плацебо24. Это было похоже на шах, хотя переносимость ипилимумаба в такой дозе была недостаточно хорошей – более чем у половины пациентов развились нежелательные явления 3–4-й степени, у 40% – иммуноопосредованные реакции.
Впечатляющие результаты получены при использовании комбинации таргетных препаратов дабрафениба и траметиниба в качестве адъювантной терапии BRAF-мутированной меланомы стадий IIIA/B/C. На фоне применения комбинации таргетных препаратов снижался риск прогрессирования заболевания на 53%, смерти – на 47% по сравнению с плацебо. Однако лечение также сопровождалось высокой частотой нежелательных явлений, потребовавших перерыва в лечении в 66% случаев и полной отмены – в 26%25.
Особый интерес представляет исследование адъювантной иммунотерапии ниволумабом (Опдиво). В рандомизированном двойном слепом исследовании CheckMate 238 участвовали 906 больных меланомой стадий III B/C или IV, перенесших полную хирургическую резекцию, без предшествующей системной терапии, со статусом по шкале ECOG 0–126. Они были рандомизированы на две равные группы. В одной группе назначали ниволумаб 3 мг/кг каждые две недели, далее – каждые 12 недель, начиная с 24-й недели, в другой – ипилимумаб 10 мг/кг каждые три недели, четыре введения, затем – каждые 12 недель, начиная с 24-й недели. Длительность терапии – до года.
Основным показателем эффективности была безрецидивная выживаемость (БРВ). Ниволумаб имел преимущество перед ипилимумабом в отношении прироста БРВ на 13%, а также снижения риска прогрессирования на 34% (рис. 3).
Во всех ключевых подгруппах ниволумаб (Опдиво) продемонстрировал преимущество перед ипилимумабом в отношении эффективности независимо от стадии заболевания, статуса BRAF и уровня экспрессии PD-L1.
Ниволумаб (Опдиво) характеризовался более благоприятным профилем безопасности. Нежелательные явления 3–4-й степени зарегистрированы у 14% пациентов группы ниволумаба и 46% пациентов группы ипилимумаба. Отмена терапии из-за любых нежелательных явлений в группе ниволумаба не превышала 10%, а в группе ипилимумаба составила 43%.
В группе ниволумаба смертельных исходов, связанных с нежелательными явлениями, не зафиксировано. Два летальных исхода, обусловленных нежелательными явлениями, зарегистрированы в группе ипилимумаба (аплазия костного мозга и колит). Но оба случая имели место более чем через 100 дней после последнего введения ипилимумаба26.
Профессор Л.В. Демидов также обсудил два профиля пациентов.
Профиль пациента 1. Клинические данные: меланома кожи, толщина по Бреслоу 2 мм с изъязвлением; опухоль BRAF-мутированная; поражение трех лимфатических узлов.
Согласно результатам интерактивного голосования, 58,6% участников сделали выбор в пользу адъювантной терапии ниволумабом, 32,8% – комбинации дабрафениб и траметидин, 5% – ИФН-альфа в разных дозах.
По мнению профессора Л.В. Демидова, оптимальной могла бы стать адъювантная терапия ниволумабом. Терапия ИФН-альфа не влияет на увеличение общей выживаемости и характеризуется высокой токсичностью. Терапия комбинацией дабрафениба и траметидина действительно снижает риск рецидива и смерти, но сопровождается высокой частотой нежелательных реакций и отменой терапии в 26% случаев. Ниволумаб не только значимо снижает риск рецидива, но и демонстрирует хороший профиль безопасности.
Профиль пациента 2. Клинические данные: меланома кожи туловища, толщина по Бреслоу 3 мм без изъязвления; дикий тип BRAF; поражение двух лимфоузлов; солитарный метастаз в подкожной клетчатке; полная резекция опухоли.
Большинство участников симпозиума (73,4%) проголосовало за назначение пациенту с резектабельной меланомой стадии IV адъювантной терапии ниволумабом. По словам профессора Л.В. Демидова, именно ниволумаб в данном случае наиболее предпочтителен, поскольку имеет соответствующие показания и характеризуется доказанными эффективностью и безопасностью. Комбинация дабрафениба и траметидина (как и ИФН-альфа) не рассматривается, поскольку не работает при диком типе BRAF и не изучалась при меланоме стадии IV.
Резюмируя сказанное, профессор Л.В. Демидов подвел итоги исследования CheckMate 238:
- ниволумаб (Опдиво) эффективнее ипилимумаба 10 мг/кг при меланоме стадий III и IV (снижение риска прогрессирования на 34% (95% ДИ 0,54–0,81; р < 0,0001), на 13% меньше риск прогрессирования заболевания при двухлетнем наблюдении (63 против 50%), эффективен во всех подгруппах пациентов независимо от мутации BRAF и экспрессии PD-L1);
- препарат Опдиво характеризуется благоприятным профилем безопасности;
Опдиво – новый стандарт адъювантной терапии меланомы стадий III и IV после полной резекции опухоли.
Заключение
Прогресс в терапии неоперабельной и метастатической меланомы обусловлен прежде всего применением нового класса иммуноонкологических препаратов. Впервые улучшение общей выживаемости больных метастатической меланомой отмечалось при использовании блокатора CTLA-4 ипилимумаба. Еще более высокой оказалась эффективность блокаторов PD-1 (ниволумаб, пембролизумаб). Ниволумаб (Опдиво) демонстрирует более благоприятный профиль безопасности.
Применение комбинации ниволумаба и ипилимумаба у пациентов с неоперабельной метастатической меланомой ассоциируется с увеличением ЧОО, безрецидивной и общей выживаемости (по сравнению с монотерапией ниволумабом и ипилимумабом). Нежелательные реакции при использовании комбинации ниволумаба и ипилимумаба легко управляемы и обратимы.
Ниволумаб (Опдиво) продемонстрировал более выраженный клинический эффект по сравнению с ипилимумабом также в адъювантном режиме у пациентов после полной хирургической резекции меланомы стадий III и IV.
Таким образом, результаты исследований дают основание рассматривать препарат Опдиво (ниволумаб) как в режиме монотерапии, так и в комбинации с ипилимумабом в качестве новой опции первой линии терапии метастатической меланомы независимо от статуса мутации BRAF и уровня экспрессии PD-L1, а монотерапию препаратом Опдиво – как новый стандарт адъювантной терапии меланомы стадий III и IV после полной резекции опухоли.
