количество статей
6422
Загрузка...
Пожалуйста, авторизуйтесь:
Медицинский форум
Современные подходы к терапии язвенного колита в педиатрии: от науки к практике. XVII Съезд педиатров России "Актуальные проблемы педиатрии":
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Педиатрия" №2
- Аннотация
- Статья
- Ссылки
На симпозиуме врачи делились с коллегами практическим опытом, когда инфликсимаб назначался детям с язвенным колитом по жизненным показаниям и его применение способствовало индукции и поддержанию длительной ремиссии, а также снижало риск или отсрочивало время проведения колэктомии. Напомним: в декабре 2012 г. инфликсимаб был зарегистрирован на территории Российской Федерации для применения у детей и подростков со среднетяжелым и тяжелым язвенным колитом при недостаточном ответе на стандартную терапию с применением глюкокортикостероидов, 6-меркаптопурина или азатиоприна, либо при наличии непереносимости или противопоказаний к стандартной терапии.
Язвенный колит – тяжелое воспалительное заболевание толстой кишки, поражающее и детей, и взрослых. В отсутствие адекватного лечения заболевание не только ухудшает качество жизни, но и может привести к инвалидизирующей операции с наложением постоянной стомы. Участники симпозиума «Современные подходы к терапии язвенного колита в педиатрии: от науки к практике», прошедшего в рамках XVII Съезда педиатров России (Москва, 14–17 февраля 2013 г.), обсуждали принятые на съезде Российские рекомендации по диагностике и лечению язвенного колита у детей. Особое внимание было уделено месту биологической терапии в алгоритмах ведения детей с язвенным колитом. Хотя до недавнего времени в России не было зарегистрировано ни одного биологического препарата для лечения детей с язвенным колитом, российские педиатры смогли накопить опыт применения инфликсимаба.
На симпозиуме врачи делились с коллегами практическим опытом, когда инфликсимаб назначался детям с язвенным колитом по жизненным показаниям и его применение способствовало индукции и поддержанию длительной ремиссии, а также снижало риск или отсрочивало время проведения колэктомии. Напомним: в декабре 2012 г. инфликсимаб был зарегистрирован на территории Российской Федерации для применения у детей и подростков со среднетяжелым и тяжелым язвенным колитом при недостаточном ответе на стандартную терапию с применением глюкокортикостероидов, 6-меркаптопурина или азатиоприна, либо при наличии непереносимости или противопоказаний к стандартной терапии.

Татьяна Викторовна ГАБРУССКАЯ
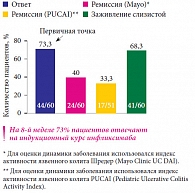
Рис. 1. Ответ на терапию инфликсимабом 5 мг/кг у детей со среднетяжелым и тяжелым язвенным колитом, пролеченных по тройной индукционной схеме (данные исследования T72)
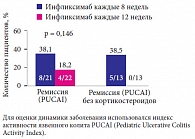
Рис. 2. Доля пациентов, достигших стойкой ремиссии в ходе исследования T72
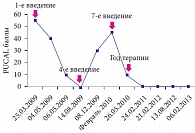
Рис. 3. Динамика индекса PUCAI у пациентки В., 17 лет, получавшей терапию инфликсимабом по поводу язвенного колита в течение 2 лет

Е.Г. Цимбалова

Э.Н. Федулова

О.В. Щербакова
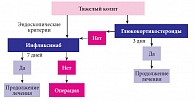
Рис. 4. Показания к оперативному вмешательству у детей с тяжелым язвенным колитом (Кливлендская клиника, 2011)

Профессор А.С,Потапов

Таблица 1. Переносимость терапии инфликсимабом: сравнение режимов инфузий каждые 8 и каждые 12 недель (данные исследования T72)
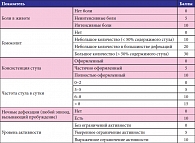
Таблица 2. Оценка педиатрического индекса активности язвенного колита (PUCAI)
Язвенный колит (ЯК) – хроническое рецидивирующее воспалительное заболевание толстой кишки. Воспалительный процесс при ЯК либо охватывает всю ободочную кишку сразу, либо начинается в ее дистальных отделах и постепенно распространяется в проксимальном направлении.
Как отметила в начале своего выступления врач Татьяна Викторовна ГАБРУССКАЯ (Санкт-Петербургский государственный педиатрический медицинский университет), вопрос лечения ЯК в педиатрической практике представляется весьма актуальным. Это обусловлено тем, что у 20% пациентов с данным диагнозом заболевание развивается в возрасте менее 18 лет. Кроме того, ЯК у детей характеризуется агрессивным течением. В 60–80% случаев наблюдается панколит, из-за чего риск колэктомии у детей с ЯК в 3 раза превышает аналогичный показатель для взрослых пациентов.
Фармакотерапия ЯК у детей также характеризуется рядом особенностей: показания к применению системных глюкокортикостероидов (ГКС) у 80% пациентов появляются уже в течение первого года после постановки диагноза. Примерно у половины детей с ЯК, принимающих системные ГКС, к концу первого года терапии формируется стероидозависимость. В этой связи особое значение получает область применения биологических препаратов, которые по причине целевого воздействия на провоспалительные цитокины получили название антицитокиновые препараты.
Наиболее востребованным ингибитором фактора некроза опухоли альфа (ФНО-альфа) – ключевого медиатора воспаления при многих аутоиммунных заболеваниях – является инфликсимаб (Ремикейд®): за 15 лет использования этого средства в клинической практике список показаний к его применению неоднократно расширялся. Зарегистрированный в 1998 г. в США для лечения болезни Крона у взрослых пациентов, к 2012 г. Ремикейд® в разных странах стал использоваться в терапии ряда ревматологических заболеваний (псориатический артрит, ревматоидный артрит), псориаза и болезни Крона у детей. Недавно список зарегистрированных показаний к применению инфликсимаба расширился еще одним – язвенный колит у детей.
Эффективность инфликсимаба в достижении ремиссии заболевания, преодолении глюкокортикостероидной зависимости и резистентности у взрослых пациентов с ЯК была доказана в ходе крупных исследований – АСТ 1 и АСТ 2 (Active Ulcerative Colitis Trials 1, 2). В этих исследованиях 364 пациента, резистентных к стандартной терапии ЯК, получали инфликсимаб (5 мг/кг или 10 мг/кг – 3 инфузии через две недели, затем повторные инфузии каждые 8 недель) или плацебо. После 8 недель клиническая и эндоскопическая ремиссия ЯК была достигнута у 60–62% пациентов, получавших инфликсимаб, и у 31–34% пациентов, получавших плацебо (p < 0,001). У 46% пациентов из группы терапии инфликсимабом против 18% пациентов из группы плацебо ремиссия сохранялась к 54-й неделе после первой инфузии1. Анализ данных 728 пациентов в отношении риска колэктомии при ЯК показал, что инфликсимаб снижает риск колэктомии у пациентов с ЯК на 41%2.
Целесообразность и безопасность применения инфликсимаба при ЯК у детей изучались в исследовании Т72, в которое были включены 60 пациентов в возрасте 6–17 лет с активным среднетяжелым и тяжелым ЯК, резистентных к одному из видов стандартной терапии и ранее не получавших терапии ингибиторами ФНО-альфа. Сначала участники исследования получали инфликсимаб по схеме индукционной терапии: в дозировке 5 мг/кг на 0, 2 и 6-й неделях. Ответившие на терапию пациенты (44 пациента, 73,3%) (рис. 1) были рандомизированы на две группы: в первой группе инфузии инфликсимаба проводились каждые 8 недель, а во второй – каждые 12. По таким схемам участники получали препарат на протяжении 42–46 недель. При потере ответа в первой группе удваивалась доза препарата, а во второй – увеличивалась частота инъекций до 1 укола в 8 недель, а в некоторых случаях еще и удваивалась доза. Оценка результативности лечения проводилась на 54-й неделе. Доля пациентов, достигших к этому моменту стойкой ремиссии (в том числе ремиссии без ГКС), оказалась выше в группе детей, получавших препарат 1 раз в 8 недель (рис. 2). При этом переносимость терапии в различных группах оказалась сравнимой: серьезные побочные эффекты развились в 21,7% случаев в группе, где пациенты получали препарат 1 раз в 12 недель, и в 18,2% случаев в группе, где инфузии проводились каждые 8 недель. Отмена терапии в связи с побочными эффектами была произведена в 13,6% и 26,1% соответственно, что говорит о хорошей переносимости препарата (табл. 1)3.
В целом исследование T72 показало, что инфликсимаб эффективен в индукции и поддержании ремиссии у детей со среднетяжелым и тяжелым ЯК. При этом эффективность поддерживающего режима, при котором инфузии инфликсимаба проводятся каждые 8 недель, предположительно, несколько выше по сравнению с режимом, предполагающим введение препарата 1 раз в 12 недель. Профиль безопасности инфликсимаба у детей с ЯК сопоставим с таковым при лечении взрослых пациентов с данным диагнозом и детей, страдающих болезнью Крона4.
Результаты исследований эффективности и безопасности применения инфликсимаба позволили включить этот препарат в европейские рекомендации по лечению ЯК у детей5. Препаратами первой линии терапии острого тяжелого ЯК у детей (оценка по педиатрическому индексу активности язвенного колита – PUCAI (Pediatric Ulcerative Colitis Activity Index) – более 65 баллов) по-прежнему остаются ГКС внутривенно, а также антибиотики в качестве эмпирической терапии инфекционных осложнений и токсического мегаколона. При недостаточном ответе на ГКС (отмечается у 30–40% детей) в течение 3–10 дней должна быть назначена вторая линия терапии: циклоспорин А, такролимус, инфликсимаб. Эти препараты демонстрируют сопоставимую эффективность в краткосрочном периоде (ответ на терапию наблюдается в 60–80% случаев)6, однако только инфликсимаб может использоваться длительно для поддержания ремиссии заболевания, поскольку и циклоспорин А, и такролимус характеризуются высокой токсичностью7.
В заключение своего выступления Т.В. Габрусская напомнила слушателям, что в декабре 2012 г. инфликсимаб был зарегистрирован на территории Российской Федерации для применения у детей и подростков со среднетяжелым и тяжелым язвенным колитом при недостаточном ответе на стандартную терапию с применением глюкокортикостероидов, 6-меркаптопурина или азатиоприна, либо при наличии непереносимости или противопоказаний к стандартной терапии. В настоящее время инфликсимаб является единственным представителем своей фармацевтической группы, применение которого у детей с ЯК официально разрешено в России и других странах мира.
Пациенты с язвенным колитом: клиническое наблюдение
Несмотря на то что ЯК у детей совсем недавно стал зарегистрированным показанием к применению инфликсимаба, опыт долговременного применения данного препарата при ЯК у российских педиатров имеется: в отдельных случаях препарат назначался по жизненным показаниям после получения информированного согласия родителей и самого ребенка, а также положительного заключения этической комиссии. Опыт применения Ремикейда у пациентки с ЯК описала к.м.н., старший научный сотрудник отделения гастроэнтерологии НИИ педиатрии Научного центра здоровья детей (НЦЗД) РАМН Екатерина Георгиевна ЦИМБАЛОВА.
Валя Б., 17 лет. Аллергоанамнез не отягощен, родилась и росла в сельской местности. В возрасте 14 лет (конец февраля 2009 г.) на фоне ОРВИ у ребенка возникли интенсивные усиливающиеся боли в животе, сопровождавшиеся повышенным газообразованием и жидким стулом. После нескольких госпитализаций по месту жительства (в ходе которых пациентке был впервые установлен диагноз «неспецифический язвенный колит») пациентка была направлена в гастроэнтерологическое отделение НЦЗД РАМН.
На момент поступления в НЦЗД РАМН (март 2009 г.) состояние девочки было тяжелым, наблюдалась фебрильная температура, дефицит массы тела (вес 34,5 кг, рост 160 см), жидкий стул с примесью крови 2–4 раза в сутки. Клинический анализ крови показал выраженное воспаление (скорость оседания эритроцитов (СОЭ) достигала 25 мм/ч), а видеокапсульная эндоскопия – эрозивный гастрит, эрозивный бульбит, дуоденогастральный рефлюкс, косвенные признаки патологии желчевыводящих путей и поджелудочной железы, еюнит, терминальный лимфофолликулярный илеит, а также эрозивный распространенный колит. Колоноскопия показала терминальный илеит, распространенный язвенный колит, афтозный сигмоидит и проктит. Морфологическое исследование биоптатов выявило: во всех отделах ободочной и прямой кишки отмечена умеренная деформация крипт, количество бокаловидных клеток на большем протяжении увеличено; в собственной пластинке – выраженная лимфоидная инфильтрация с примесью фибробластов; в прямой кишке определяются единичные мелкие крипт-абсцессы; в тонкой кишке ворсинки утолщены, в базальных отделах слизистой оболочки – сливающиеся гиперплазированные фолликулы. Заключение: хронический, тотальный ЯК с небольшими признаками обострения. Диагноз: неспецифический язвенный колит, панколит, высокая степень активности, обострение.
В связи с тяжелым состоянием пациентке была назначена пульс-терапия метилпреднизолоном в дозе 10 мг/кг (350 мг) в/в капельно 5 сеансов с переходом на пероральный прием преднизолона в дозе 1,5 мг/кг (55 мг/сут), месалазин 2 г/сут, азатиоприн 1,5 мг/кг (50 мг/сут), микроклизмы с гидрокортизоном 125 мг, а также симптоматическая и антибактериальная терапия (меропенем, метронидазол). На фоне лечения клиническое состояние пациентки сначала улучшилось, а впоследствии, после снижения дозы преднизолона до 30 мг/сут, вновь ухудшилось. Принимая во внимание сохраняющуюся на фоне противовоспалительной и иммуносупрессивной терапии высокую активность заболевания и формирование гормонозависимой его формы, пациентке была назначена антицитокиновая терапия инфликсимабом (Ремикейд®) в дозе 5 мг/кг/сут.
После первых инфузий отмечено улучшение клинико-лабораторных данных, достигнута ремиссия, однако через 4 недели после 5-й инфузии (ноябрь 2009 г.) вновь наступило ухудшение: появилась слабость, через несколько дней – жидкий стул до 3–4 раз в сутки с примесью крови, рвота после приема пищи. Добавление в терапию микроклизм с гидрокортизоном, Смекты и метронидазола, а также снижение дозы преднизолона до 5 мг/сут не дало положительной динамики. Пациентка была госпитализирована в НЦЗД РАМН, где она получила антицитокиновую терапию инфликсимабом в увеличенной дозе – 10 мг/кг (400 мг) по прежней схеме (1 инфузия в 8 недель).
Через 2 недели (декабрь 2009 г.) отмечено еще одно обострение заболевания на фоне катаральных явлений: лихорадка до фебрильных значений, стул жидкий с примесью большого количества крови 2–3 раза в сутки, тошнота, многократная рвота желудочным содержимым. Ребенок был госпитализирован в НЦЗД РАМН. Эзофагогастродуоденоскопия показала распространенный эрозивный гастрит, эрозивный бульбит, дуоденит, еюнит, недостаточность привратника, терминальный эзофагит, кардиоэзофагеальный пролапс. По данным колоноскопии – распространенный колит, левосторонний афтозный колит, эрозивно-язвенный проктосигмоидит. Видеокапсульное исследование показало распространенный гастрит, бульбит, дуоденит, колит. Назначена терапия: месалазин 3 г/сут, преднизолон 5 мг/сут, азатиоприн 50 мг/сут, микроклизмы с гидрокортизоном 125 мг, а также симптоматическая и антибактериальная терапия (цефтриаксон, амикацин, метронидазол). После нормализации состояния было решено продолжить антицитокиновую терапию инфликсимабом с сокращением интервала между инфузиями до 6 недель. Проведена 7-я инфузия Ремикейда 400 мг (10 мг/кг). В течение всего 2010 г. пациентка получала Ремикейд® по указанной схеме, что позволило добиться состояния устойчивой клинико-лабораторной и эндоскопической ремиссии.
Учитывая длительное (в течение 2 лет) проведение антицитокиновой терапии с положительным эффектом в виде клинико-эндоскопической ремиссии (2 года), решено снизить дозу Ремикейда до 7 мг/кг (300 мг) и увеличить интервалы между введениями до 8 недель (с 21.02.2012), а впоследствии (с 13.08.2012) доза препарата была уменьшена до 4,5 мг/кг (200 мг) с соблюдением интервала между инфузиями 8 недель. В настоящее время курс атицитокиновой терапии прекращен, поскольку пациентка находится в длительной ремиссии (2,5 года), что отражено, в частности, в снижении индекса PUCAI (рис. 3).
Препараты биологической терапии способны уменьшить потребность в колэктомии даже среди пациентов, у которых уже развились осложнения ЯК, что видно из клинического наблюдения, описанного А.А. САРЫЧЕВОЙ в соавторстве с профессором Э.И. АЛИЕВОЙ (Измайловская детская городская клиническая больница (ИДГКБ), г. Москва). Пациентка, 14 лет, в январе 2009 г. обратилась к участковому педиатру с жалобами на лихорадку, боли в животе, частый стул, вялость, кровь в стуле, сонливость и бледность. Участковым педиатром диагностирована дизентерия, назначен антибактериальный препарат, ферменты и лактобактерии, однако состояние ребенка на фоне проводимого лечения ухудшалось.
Пациентка была госпитализирована в инфекционную больницу с выраженными явлениями колита. Проведенная в больнице колоноскопия показала выраженный отек слизистой оболочки с множественными язвенными дефектами на разных стадиях развития, покрытыми фибрином и окруженными геморрагиями. Пациентке был поставлен диагноз неспецифического язвенного колита с осложнением в виде кишечного кровотечения и проведена инфузионная, антибактериальная и гемостатическая терапия. Кроме того, пациентке были назначены системные ГКС: преднизолон в дозировке 30 мг/сут.
После стабилизации состояния ребенок был переведен в ИДГКБ. При поступлении в клинику состояние пациентки оценивалось как тяжелое: жалобы на боли в животе и слабость, субфебрильная лихорадка, стул до 10 раз в сутки, жидкий, без каловых масс, с большим количеством крови. Тяжелое состояние сохранялось даже на фоне массивной инфузионной терапии (эритроцитарная масса, свежезамороженная плазма, гемостатическая, гормональная, антибактериальная терапия), девочка была переведена на парентеральное питание. Резистентность к проводимой терапии, активное кишечное кровотечение и потребность в ежедневном переливании компонентов крови стали основанием для постановки вопроса о колэктомии, однако родители пациентки отказались от проведения операции.
По жизненным показаниям пациентке был назначен Ремикейд в дозировке 5 мг/кг. После первой инфузии препарата (1 апреля 2009 г.) состояние ребенка улучшилось, что выразилось в уменьшении эндотоксикоза, исчезновении лихорадки, сокращении частоты стула (до 3–4 раз в сутки), в изменении калового характера стула (умеренная примесь крови). После второй инфузии Ремикейда (15 апреля 2009 г.) исчезла видимая кровь в каловых массах. Контрольная ректосигмоскопия (осмотрено 50 см от ануса) показала минимальную активность воспалительного процесса: слизистая оболочка прямой кишки сигмовидной кишки пестрая, умеренно отечная, сосудистый рисунок четкий до 1-го порядка, местами – до 2-го, видны единичные эрозии до 2 мм и единичные псевдополипы до 3 мм; контактной кровоточивости выделено не было; в просвете – оформленные каловые массы и пристеночная слизь.
После третьей инфузии (27 мая 2009 г.) пациентка была выписана домой в удовлетворительном состоянии. В январе 2010 г. пациентка самостоятельно отменила назначенную терапию (месалазин, азатиоприн, преднизолон внутрь, инфликсимаб по схеме). В марте 2010 г. ее состояние ухудшилось, а 1 апреля 2010 г. пациентка была доставлена бригадой скорой медицинской помощи в тяжелом состоянии в ближайший стационар. Спустя сутки пациентка была переведена в ИДГКБ. Уровень гемоглобина при поступлении – 26 г/л (произведена гемотрансфузия эритроцитарной массы). Ректоскопия показала наличие множественных эрозий до 3 мм, слизистая сигмовидной и прямой кишки алого цвета, складки сглажены, морфологическое исследование продемонстрировало выраженную воспалительную инфильтрацию собственной пластинки слизистой оболочки. Однако возобновление инфузий Ремикейда (4 апреля 2010 г.) в дозе 5 мг/кг в сочетании с препаратами 5-аминосалициловой кислоты (5-АСК) 2 г/сут, ноотропными препаратами, гемостатиками, ГКС 30 мл 3 раза в день и антибактериальными средствами (рифаксимин, метронидазол) позволило улучшить состояние больной и выписать ее домой 24 апреля 2010 г. Сейчас, спустя почти 3 года, состояние пациентки остается стабильным, она продолжает получать комбинированную терапию месалазином и азатиоприном в сочетании с инфузиями Ремикейда 1 раз в 8 недель. Клинико-лабораторных симптомов обострения заболевания зарегистрировано не было, что подтверждено в том числе результатами колоноскопии. Описанный клинический случай представляет интерес, поскольку демонстрирует положительный опыт повторного применения инфликсимаба при обострении ЯК после длительного перерыва в антицитокиновой терапии.
Эффективность лечения инфликсимабом ребенка с язвенным колитом
Опытом применения инфликсимаба у подростка с ЯК поделилась к.м.н. Эльвира Николаевна ФЕДУЛОВА (Нижегородский НИИ детской гастроэнтерологии (ННИИДГ), г. Нижний Новгород). Пациенка Н., 16 лет, частый жидкий стул впервые был выявлен в августе 2006 г. На фоне стационарного лечения с диагнозом «острая кишечная инфекция неуточненная» было достигнуто временное улучшение, однако по окончании курса лечения состояние ребенка вновь ухудшилось: пациентка предъявляла жалобы на нарастающую слабость, кроме того, у нее участился стул, а каловые массы стали жидкими с примесью слизи. В декабре 2006 г. пациентка была вновь госпитализирована в стационар по месту жительства. После выявления на ректороманоскопии признаков дистального ЯК пациентка была направлена в ННИИДГ на дообследование и лечение, куда и поступила в феврале 2007 г. в тяжелом состоянии, с жалобами на боли в животе (перед дефекацией) и голеностопных суставах, стул до 10 раз в сутки, жидкий с примесью слизи и крови. В анализах крови были выявлены палочкоядерный сдвиг (до 39%), лейкоцитоз (20 × 109/л), ускоренная СОЭ (40 мм/ч) и анемия легкой степени (Hb 108 г/л). Морфологическое исследование показало деформацию крипт, наличие крипт-абсцессов, диффузную лимфо-плазмоцитарную инфильтрацию собственной пластинки слизистой оболочки нисходящего отдела толстой кишки и фокус эозинофильных гранулоцитов в собственной пластинке слизистой сигмовидного отдела. По результатам исследований пациентке был поставлен диагноз «язвенный колит, тотальный, тяжелый, 3-й степени активности; реактивный олигоартрит, абактериальная лейкоцитурия».
Была назначена строгая безмолочная диета, месалазин 100 мг/кг/сут, преднизолон 1 мг/кг/сут, кишечные антисептики, ферменты, сорбенты. На фоне гормонотерапии состояние пациентки улучшилось, однако после попытки снизить дозу вновь ухудшилось, что привело к повторной госпитализации. Назначение азатиоприна для преодоления гормонозависимости привело к обострению панкреатита, и препарат пришлось отменить. Проведенная в ходе очередной госпитализации (апрель 2009 г.) фиброколоноскопия показала полное отсутствие сосудистого рисунка, трубкообразный просвет кишки, множественные подслизистые геморрагии и выраженную контактную кровоточивость. Также было отмечено изменение рельефа слизистой оболочки подвздошной кишки по типу толстокишечного.
Несмотря на назначение максимальных доз месалазина и максимально переносимых доз азатиоприна, а также постоянной терапии системными ГКС, добиться состояния ремиссии не удалось, и в связи с неэффективностью проводимой терапии хирургами были выставлены показания к оперативному лечению – проведению тотальной колэктомии. Однако врачебный консилиум принял решение (одобренное родителями и локальным этическим комитетом) предпринять еще одну попытку консервативного лечения препаратом Ремикейд в дозировке 5 мг/кг сначала на 0, 2 и 6-й неделе, а затем – каждые 8 недель.
Через 6 месяцев биологической терапии системные ГКС были полностью отменены, а доза месалазина снижена до 50 мг/кг/сут. Для предотвращения выработки антител к инфликсимабу пациентка постоянно получает азатиоприн в дозе 1,2 мг/кг/сут. Состояние пациентки улучшилось, ребенок стал посещать школу, физическое и половое развитие нормализовалось. Проведенное морфологическое исследование выраженных изменений не выявило. Через 3 года проводимой терапии состояние пациентки стабильное, клиники гемоколита не отмечается; в гемограмме анемии нет, лейкоцитарная формула без воспалительных изменений; СОЭ на фоне регулярных инфузий в норме; уровень кальпротектина остается повышенным, но в динамике снижается. Для повышения не только эффективности, но и безопасности антицитокиновой терапии на базе ННИИДГ был открыт Центр антицитокиновой терапии, где инфузии Ремикейда и других биологических препаратов проводятся в палатах интенсивной терапии. «Таким образом, даже если серьезные нежелательные реакции возникнут, вероятность, что их удастся купировать, очень велика», – подчеркнула Э.Н. Федулова.
Биологическая терапия у детей с язвенным колитом: взгляд хирурга
В зарубежных детских клиниках, где Ремикейд успешно применяется давно, уже с 2007–2008 гг. используется алгоритм ведения детей, страдающих тяжелым язвенным колитом (рис. 4). Как отметила детский хирург к.м.н. Ольга Вячеславовна ЩЕРБАКОВА (отделение колопроктологии Российской детской клинической больницы (РДКБ), г. Москва), в нашей стране такого согласительного документа нет, и биологическая терапия зачастую назначается слишком поздно, несмотря на то что эффективность инфликсимаба в отношении снижения потребности в колэктомии или как минимум в переносе операции на более поздний срок доказана, равно как и то, что прием инфликсимаба не влияет на частоту инфекционных осложнений в послеоперационном периоде8.
Немаловажной с точки зрения хирурга является также способность биологической терапии снижать потребность в терапии ГКС, поскольку именно последняя нередко является причиной серьезных операционных осложнений – от раневой инфекции и грибкового перитонита до несостоятельности швов. К настоящему времени на базе РДКБ было прооперировано 7 детей в возрасте от 6 до 15 лет, ранее получавших Ремикейд®, при этом различалось как количество инфузий до операции (от 2 до 12), так и время, прошедшее с момента последней инфузии (от 30 дней до 2 лет).
Возникшие показания к проведению колэктомии не следует считать признаком полной неэффективности биологической терапии: назначение Ремикейда в ряде случаев помогло не только снизить дозу ГКС в предоперационном периоде, но и отсрочить время операции, дав родителям и ребенку возможность свыкнуться с мыслью о необходимости оперативного лечения. У врачей РДКБ уже есть опыт послеоперационного применения Ремикейда. О.В. Щербакова привела пример пациентки с язвенным колитом, перенесшей колэктомию с наложением илеостомы в возрасте 6 лет и реконструктивную операцию (мукозэктомию прямой кишки с наложением илео-анального анастомоза) в 7 лет. После второго хирургического вмешательства у ребенка наблюдался частый (10–15 р/сут) стул с примесью алой крови. Назначение местной терапии (месалазин в виде пены и свечей, будесонид в форме пены, преднизолон в форме свечей и микроклизмы с гидрокортизоном) к улучшению не привело, напротив, частота дефекаций увеличилась до 15–20 р/сут, отмечалось ночное недержание кала, ректальные кровотечения.
Пациентке была назначена терапия инфликсимабом в сочетании с будесонидом в форме пены, признаки клинического улучшения появились уже через сутки после первой инфузии. Вскоре частота дефекаций уменьшилась до 4–7 раз в сутки, ночная дефекация отсутствовала, уменьшилась интенсивность кровотечений. Этот и другие клинические случаи свидетельствуют о целесообразности назначения инфликсимаба с целью как отсрочить операцию, так и улучшить состояние пациента в пред- и послеоперационном периоде.
Российские рекомендации по диагностике и лечению язвенного колита у детей
В ходе XVII съезда педиатров России были приняты рекомендации по диагностике и лечению язвенного колита у детей. С основными положениями документа слушателей ознакомил д.м.н., профессор Александр Сергеевич ПОТАПОВ (заведующий отделением гастроэнтерологии НИИ педиатрии НЦЗД РАМН). Согласно документу, язвенный колит – хроническое рецидивирующее воспалительное поражение толстой кишки, распространяющееся непрерывно в проксимальном направлении от прямой кишки. По протяженности воспалительного процесса ЯК подразделяют на проктит, левосторонний колит (включая проктосигмоидит, до селезеночного изгиба), тотальный колит (распространенный колит или панколит с ретроградным илеитом или без него); по характеру течения выделяют рецидивирующий (часто, редко) и непрерывный ЯК; по тяжести атаки – легкий, средний и тяжелый ЯК; по ответу на стероидную терапию – стероидорезистентный и стероидозависимый ЯК.
Рецидивом считается появление симптомов заболевания у больных ЯК в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой. При этом клинической ремиссией называют отсутствие клинических симптомов заболевания и воспалительной активности в анализах крови (PUCAI < 10 баллов). Клинико-эндоскопическая (полная) ремиссия – это наличие клинической ремиссии и полное заживление слизистой оболочки. Стероидорезистентность (стероидорефрактерность) определяют как сохранение активности заболевания, несмотря на внутривенное введение или пероральный прием адекватной дозы ГКС в течение 7–14 дней. Стероидозависимость – достижение клинической ремиссии на фоне терапии ГКС и возобновление симптомов при снижении дозы или в течение 3 месяцев после полной отмены ГКС, а также в случаях если терапию ГКС не удается прекратить в течение 14–16 недель.
Диагноз ЯК у детей должен устанавливаться на основании сочетания данных анамнеза, физикального осмотра и илеоколоноскопии с множественной биопсией, выполненной гастроэнтерологом с педиатрической специализацией. Первоначальные лабораторные исследования должны включать развернутый общий анализ крови, определение уровня печеночных ферментов, альбумина, СОЭ, уровня С-реактивного белка и оценку обмена железа. Во всех случаях рекомендуется выполнение эндоскопического исследования верхних отделов ЖКТ для исключения болезни Крона. Для исключения инфекционной диареи обязателен посев стула; определение токсина Clostridium difficile рекомендуется проводить не менее чем в 3 отдельных порциях стула.
Эндоскопическая оценка рекомендуется при постановке диагноза, при существенных изменениях лечения и при затруднениях в оценке клинических симптомов. Эндоскопическое исследование у детей не рекомендуется проводить рутинно при нетяжелых обострениях или в период ремиссии, при отсутствии подозрений на развитие колоректального рака. Особое внимание при диагностике и оценке активности процесса уделяется педиатрическому индексу активности язвенного колита – PUCAI – у пациентов с ЯК, находящихся в клинической ремиссии, спонтанной или медикаментозно поддерживаемой. Значение этого индекса должно составлять 10 или менее баллов (табл. 2)9.
В качестве терапии первой линии для индукции и поддержания ремиссии у детей с легкой и среднетяжелой активностью ЯК рекомендованы пероральные препараты 5-АСК. Монотерапия местными препаратами 5-АСК может быть эффективной у отдельных групп детей с легким и среднетяжелым проктитом (однако подобный фенотип редко встречается в педиатрической практике). Рекомендованы следующие дозы препаратов 5-АСК у детей: месалазин: орально 60–80 мг/кг/сут (максимально 4,8 г/сут) в 2 приема, ректально 25 мг/кг (до 1 г однократно), максимальная комбинированная оральная и ректальная доза не должна превышать стандартную оральную дозу более чем на 50% или 6,4 г/сут у взрослых;
- сульфасалазин: орально 40–70 мг/кг/сут в 2 приема (максимум 4 г/сут);
- поддерживающие дозы такие же, как при индукционной терапии.
Антибактериальная терапия при ЯК у детей не показана для индукции или поддержания ремиссии и применяется в случае развития осложнений. Тиопурины (азатиоприн и меркаптопурин) рекомендуются для поддержания ремиссии у детей с непереносимостью 5-АСК или у пациентов с часто рецидивирующим течением (2–3 обострения в год) или развитием гормонозависимой формы заболевания на фоне проведения терапии 5-АСК в максимальных дозах. Иммуномодуляторы неэффективны для индукции ремиссии. Тиопурины рекомендуются для поддерживающей терапии при остром тяжелом колите после индукции ремиссии при помощи ГКС, поскольку вероятность агрессивного течения заболевания у таких пациентов выше. При этом у детей с острым тяжелым колитом, ранее не получавших 5-АСК, при условии быстрого ответа на ГКС может рассматриваться поддерживающая монотерапия 5-АСК.
С практической точки зрения важно помнить, что терапевтический эффект тиопуринов достигается в период до 10–14 недель от начала лечения. Доза может достигать приблизительно от 1 до 2,5 мг/кг азатиоприна или 1–1,5 мг/кг меркаптопурина и приниматься однократно. Терапию тиопуринами следует прекратить при клинически значимой миелосупрессии или панкреатите. Назначать тиопурины повторно после лейкопении следует в меньшей дозе после тщательной оценки риска и пользы от терапии. Переход от азатиоприна на меркаптопурин может быть эффективным при острых гриппоподобных и желудочно-кишечных нежелательных явлениях. Продолжение терапии 5-АСК после назначения тиопуринов может иметь ряд преимуществ. Метотрексат может применяться только в ограниченной подгруппе пациентов с ЯК, характеризующихся отсутствием ответа на тиопурины или их непереносимостью, если недоступны альтернативные способы лечения. У всех детей следует оценить график вакцинаций. Вакцинацию живыми вакцинами следует проводить не позднее чем за 6 недель до начала приема иммуносупрессоров, однако проведение вакцинаций не должно приводить к задержке в назначении препаратов, необходимых для контроля заболевания.
Важную роль в индукции и поддержании ремиссии ЯК у детей играет антицитокиновая терапия инфликсимабом, по эффективности сравнимая с аналогичным показателем для взрослых пациентов. На основании результатов имеющихся клинических исследований инфликсимаба было решено включить его в российские клинические рекомендации по лечению ЯК у детей в качестве препарата, возможность назначения которого должна рассматриваться у пациентов с хроническим, непрерывным или гормонозависимым течением ЯК, не контролируемым 5-АСК или тиопуринами. Инфликсимаб следует назначить при гормонорезистентной форме заболевания (устойчивости как к пероральным, так и к внутривенным ГКС). Если инфликсимаб был назначен при острой атаке у пациента, ранее не получавшего тиопурины, биологическая терапия инфликсимабом может использоваться как вспомогательная для перехода на терапию тиопуринами, в этом случае применение инфликсимаба может быть прекращено через 4–8 месяцев. Адалимумаб может применяться только у пациентов с потерей ответа на инфликсимаб или непереносимостью последнего.
Таким образом, сегодня инфликсимаб является препаратом первой линии биологической терапии у детей с ЯК и назначается в дозе 5 мг/кг по следующей схеме: 3 индукционных дозы в течение 6 недель, далее – каждые 8 недель в качестве поддерживающей терапии. В некоторых случаях необходим индивидуальный подбор дозы. Комбинированное применение препаратов 5-АСК и биологических препаратов на сегодняшний день считается рациональным. Подбирая лечение для детей, страдающих ЯК, следует помнить, что терапевтическая стратегия при данном диагнозе в педиатрии должна основываться преимущественно на оценке активности болезни. Эффективность и безопасность инфликсимаба подтверждена не только клиническими испытаниями, но и повседневной практикой – этот препарат успешно применяется в ведущих российских педиатрических ЛПУ, а теперь инфликсимаб включен в Российские рекомендации по диагностике и лечению язвенного колита у детей.
1. Rutgeerts P., Sandborn W.J., Feagan B.G. et al. Infliximab for induction and maintenance therapy for ulcerative colitis // N. Engl. J. Med. 2005. Vol. 353. № 23. P. 2462–2476.
2. Sandborn W.J., Rutgeerts P., Feagan B.G. et al. Colectomy rate comparison after treatment of ulcerative colitis with placebo or infliximab // Gastroenterology. 2009. Vol. 137. № 4. P. 1250–1260.
3. Hyams J., Damaraju L., Blank M. et al. Induction and maintenance therapy with infliximab for children with moderate to severe ulcerative colitis // Clin. Gastroenterol. Hepatol. 2012. Vol. 10. № 4. P. 391–399.
4. Hyams J., Walters T.D., Crandall W. et al. Safety and efficacy of maintenance infliximab therapy for moderate-to-severe Crohn's disease in children: REACH open-label extension // Curr. Med. Res. Opin. 2011. Vol. 27. № 3. P. 651–662.
5. Turner D., Levine A., Escher J.C. et al. Management of pediatric ulcerative colitis: joint ECCO and ESPGHAN evidence-based consensus guidelines // J. Pediatr. Gastroenterol. Nutr. 2012. Vol. 55. № 3. P. 340–361.
6. Turner D. Severe acute ulcerative colitis: the pediatric perspective // Dig. Dis. 2009. Vol. 27. № 3. P. 322–326.
7. Turner D., Travis S.P., Griffiths A.M. et al. Consensus for managing acute severe ulcerative colitis in children: a systematic review and joint statement from ECCO, ESPGHAN, and the Porto IBD Working Group of ESPGHAN // Am. J. Gastroenterol. 2011. Vol. 106. № 4. P. 574–588.
8. Bordeianou L., Kunitake H., Shellito P., Hodin R. Preoperative infliximab treatment in patients with ulcerative and indeterminate colitis does not increase rate of conversion to emergent and multistep abdominal surgery // Int. J. Colorectal Dis. 2010. Vol. 25. № 3. P. 401–404.
9. Turner D., Otley A.R., Mack D. et al. Development, validation, and evaluation of a pediatric ulcerative colitis activity index: a prospective multicenter study // Gastroenterology. 2007. Vol. 133. № 2. P. 423–432.
Новости на тему
СТАТЬИ по теме
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
