Меланогенез – это процесс образования меланина из тирозина с помощью ферментов тирозиназы и ДОФА-оксидазы. Меланосомы, гранулы, заполненные меланином, транспортируются в кератиноциты через ветвящиеся отростки путем фагоцитоза. Меланоциты располагаются среди клеток базального слоя и имеют несколько отростков, которые могут удаляться на расстояние до 100 мкм от тела клетки до мембран отдельных кератиноцитов. Распределение меланоцитов и способ их ветвления в норме таковы, что почти каждая клетка базального слоя контактирует с их концевыми отделами. Имеет место и контакт отростков меланоцитов между собой. Образование меланосом и синтез в них меланинового пигмента – процессы независимые, поскольку у альбиносов, а также у больных витилиго в эпидермисе присутствуют меланоциты с меланосомами, не содержащие премеланин и меланин. Биосинтез меланина начинается на внутренних мембранах меланосом. Под действием тирозиназы (тирозингидролазы) тирозин превращается в L-ДОФА-хинон (L-диоксифенилаланин). Кроме того, тирозиназа очень чувствительна к ультрафиолету и ионам меди и кислорода. В дальнейшем последовательно протекают такие этапы:
1. ДОФА-хинон преобразуется в содержащий индольное кольцо ДОФА-хром.
2. Ферменты ДОФА-хром-таутомераза и DHICA-оксидаза превращают ДОФА-хром в 5,6-дигидроксииндол-2-карбоновую кислоту (5,6-dihidroxyindole-2-carboxylic acid – DHICA).
3. Заключительный этап синтеза – полимеризация 5,6-дигидроксииндол-2-карбоновой кислоты (DHICA) с образованием коричневого DHICA-меланина, содержащего от 100 до 1000 мономеров DHICA. Для этой реакции необходимо присутствие цинка и кислорода.
4. ДОФА-хром может также превращаться в 5,6-дигидроксииндол (5,6-dihidroxyindole, DHI). Продуктом окислительной полимеризации DHI является черный или коричневый DHI-меланин (эумеланин), содержащийся в коже и волосах. Он нерастворим в органических растворителях и устойчив к химической обработке. Таким образом, физиологический меланогенез невозможен без тирозина, молекулярного кислорода, ионов меди и цинка [1].
Регуляция меланогенеза
Медиаторы нервной системы – катехоламины влияют на гипоталамус, который в свою очередь стимулирует промежуточную долю гипофиза к выработке меланостимулирующего гормона (МСГ). Установлено, что МСГ могут продуцировать сами кератиноциты под воздействием ультрафиолета и других факторов (воспаление, травмы). На меланогенез оказывают влияние гормоны надпочечников, щитовидной и половых желез, а также стресс, химические и физические факторы (нервные окончания вырабатывают нейропептиды, стимулирующие меланогенез).
Функции меланина
Классическая структура меланина – длинноцепочечный полимер. Это определяет его барьерную защитную функцию. В литературе упоминается о том, что меланины, синтезируемые в организме человека, участвуют в ликвидации любого стрессового воздействия и являются составной частью иммунной системы организма. Меланин дезактивирует свободные радикалы, возникающие после облучения организма ультрафиолетом и ионизирующим излучением, а также в результате ряда ферментативных процессов и реакций аутоокисления; катализирует многие биохимические процессы; обладает ионообменными свойствами.
Основная функция меланина заключается в том, чтобы регулировать количество ультрафиолетового (УФ) излучения, проникающего в кожу. Спектр поглощения меланина перекрывает весь диапазон видимого света и УФ-диапазона. При поглощении квантов света часть энергии меланин превращает в тепло, а часть расходует на фотохимические реакции. Меланин и его предшественники могут окисляться, полимеризоваться, а также продуцировать свободные радикалы кислорода, которые повреждают клетку. Из-за способности меланина генерировать активные формы кислорода его называют обоюдоострым мечом кожи [2].
Дефицит меланина и оксидантный стресс
В данном обзоре мы решили сделать акцент на пациентах с гипохромиями, в частности с витилиго. Больные витилиго составляют 0,5–4% всего населения земного шара. Это около 40 млн человек [3]. Существуют различные классификации витилиго. В большинстве из них в качестве критериев используются распространенность и локализация очагов депигментации. Согласно классификации J.P. Ortonne витилиго подразделяется на локализованное, генерализованное и универсальное.
Локализованные формы:
- фокальная (одно или несколько пятен на отдельном участке кожного покрова, не составляющем сегмента);
- сегментарная (одно пятно или более в пределах сегмента);
- витилиго слизистых оболочек.
Генерализованные формы:
- акрофациальная (с поражением дистальных отделов конечностей и лица);
- вульгарная (с появлением симметричных множественных депигментированных пятен на различных участках кожи);
- смешанная.
Универсальная форма имеет место, когда пигмент отсутствует на площади, превышающей 80% общей площади кожного покрова.
В настоящее время нет четких критериев активности витилиго. Согласно оценке по шкале VIDA (Vitiligo disease activity), предложенной D. Njoo и соавт. (1999) [4], за прогрессирование витилиго принимается увеличение существующих очагов депигментации или возникновение новых в течение последнего года. Отсутствие роста и появления пятен в течение более 1 года – характерные признаки стабильного течения витилиго.
В патогенезе заболевания особое значение имеют генетические факторы. Установлен аутосомно-рецессивный тип наследования, обусловленный отсутствием в меланоцитах и меланосомах фермента тирозиназы.
Существует множество теорий этиологии витилиго. В исследованиях показано, что общим для всех групп пациентов с витилиго является повышение активности перекисного окисления липидов, что приводит к накоплению гидроперекисей липидов, диеновых конъюгатов и малонового диальдегида в крови. Выявлены изменения и среди ферментов антиокислительной системы, контролирующих уровень активных форм кислорода. У пациентов с витилиго установлено также снижение активности супероксиддисмутазы (СОД) и каталазы [5]. Ряд авторов подтверждают снижение активности этих экзогенных ферментов при различных патологических процессах [6, 7].
Коррекция активности супероксиддисмутазы
Применение препаратов на основе СОД апробировано многими авторами. В лечении пигментной ксеродермы такие препараты оказывали восстанавливающее действие на структуру кератиноцитов [8], in vitro стимулировали метаболизм фибробластов и действовали на свободные радикалы, оказывая нейтрализующее действие на супероксид-ион. In vivo препараты способствуют детоксикации и стимулируют общий метаболизм в клетках [9]. DISMUTIN BT защищает от свободных радикалов, обладает противовоспалительным действием и замедляет перекисное окисление липидов, устраняет из цепи супероксидные радикалы, не повреждается в ходе реакции и в комплексной терапии показал хорошие результаты в лечении пациентов с витилиго [8].
В 2009 г. было объявлено о выделении новой модификации СОД, получившей название DISMUTIN-J PF, признанной одним из самых быстродействующих и наиболее стабильных природных ферментов. DISMUTIN-J PF был разработан для снижения числа кислородных радикалов в коже при УФ-излучении и других стрессовых воздействиях. Высокая эффективность фермента была продемонстрирована в исследованиях in vitro и ex vivo. Препарат DISMUTIN-J PF представляет собой водный раствор высокоочищенного фермента, полученного биотехнологическим путем из природного штамма дрожжей Saccharomyces cerevisiae [10].
Материалы и методы исследования
УФ-излучение и частый контакт с химическими загрязнителями, такими как озон, приводят к избыточному образованию свободных кислородных радикалов в коже. Они разрушают мембраны путем окисления ненасыщенных жирных кислот и белков, а также вызывают деполяризацию и образование перекрестных связей биополимеров. Это провоцирует возникновение острых состояний, таких как эритема, гиперпролиферация, шелушение и хроническое раздражение кожи с общим повреждением коллагена, что вместе с депонированием эластина в дерме приводит к преждевременному старению кожи.
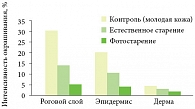
Собственная защитная система кожи основана на действии СОД. Эндогенные СОД в большом количестве обнаружены в роговом слое. Присутствуют они и в дерме. При фотостарении кожи значительно снижается содержание эндогенного фермента в роговом слое и эпидермисе (D. Sanders и соавт., 2002) (рис. 1) [10].
В данных ситуациях считается обязательной заместительная терапия экзогенным СОД с помощью косметических препаратов. При нанесении на кожу супероксиддисмутаза способна проникать в неповрежденный роговой слой и достигать верхних слоев эпидермиса, что было показано с помощью флуоресцентных меток FITC (I. Emerit и соавт., 1997). Данные литературы, как и информация разработчиков, подтверждают защитный эффект DISMUTIN-J PF при местном применении против УФ-индуцированного повреждения кожных покровов, что проявляется в способности компенсировать отсутствие эндогенной СОД и восстанавливать антиоксидантный гомеостаз кожи. Антиокислительный эффект DISMUTIN-J PF изучали при воздействии свободного кислорода на раствор гиалуроновой кислоты. Защитный эффект DISMUTIN-J PF против перекисного окисления липидов был испытан при УФ-облучении кожи предплечья добровольцев [10].
Результаты и обсуждение
Защита гиалуроновой кислоты от свободных кислородных радикалов
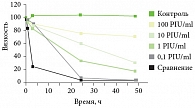
Защитный эффект DISMUTIN-J PF изучали при экспозиции гиалуроновой кислоты в системе, генерировавшей свободный кислород (гипоксантин/ксантиноксидазы). Последствия атаки свободных радикалов определяли путем измерения снижения вязкости раствора гиалуроновой кислоты. DISMUTIN-J PF показал дозозависимую способность защищать данный биополимер от деполимеризации. Концентрация 100 ЕД/мл на протяжении 50 часов сохраняла вязкость раствора гиалуроновой кислоты на уровне, близком к уровню контрольной группы (без обработки активным кислородом) (рис. 2) [10].
Защита кожи от УФ-индуцированной липопероксидации
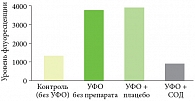
Защитный эффект препарата DISMUTIN-J PF против перекисного окисления липидов в коже был испытан при ультрафиолетовом облучении (УФО) кожи предплечья добровольцев. Образование липидного пероксида измерялось с помощью хемилюминесценции. В отличие от группы плацебо и группы без нанесения препарата в группе, где применяли DISMUTIN-J PF, наблюдалось существенное ингибирование дополнительного перекисного окисления на фоне УФ-излучения. В группах без нанесения препарата и с нанесением нейтрального геля имел место высокий уровень хемилюминесценции. Группа с защитой экзогенным СОД показала после УФО такой же низкий уровень люминесценции, как и группа добровольцев, не получавших местного средства и УФО (рис. 3) [10].
DISMUTIN-J PF защищает кожу от вредного воздействия свободных радикалов кислорода, образующихся под воздействием УФ-излучения или других факторов окружающей среды, таких как озон. Экзогенный фермент помогает отсрочить преждевременное старение кожи, вызванное воздействием солнечного излучения. Проявлениями такого фотостарения становятся сухость, образование морщин и пигментных пятен, потеря эластичности. DISMUTIN-J PF также облегчает симптомы раздражения кожи, то есть обладает как защитной, так и профилактической активностью. В связи с этим DISMUTIN-J PF должен быть рассмотрен для включения в новые формулы продуктов защиты от солнца, неблагоприятного воздействия факторов внешней среды, в состав продуктов для восстановления кожи после пребывания на солнце и в состав средств, стабилизирующих окислительные процессы в коже [10].
Лечение витилиго на основе коррекции перекисного окисления липидов
Ускорения окисления L-ДОФА для усиления синтеза меланина достигают путем воздействия фотосенсибилизаторов совместно с УФ-А-облучением (ПУВА-терапия) или специфических альфа-липопротеинов плацентарного экстракта, а также за счет восполнения недостатка в коже микроэлементов – ионов меди и кальция; требуется уменьшение содержания в коже пероксид-ионов – нанесение на поврежденные участки дополнительного количества каталазы и антиоксидантов; стимуляция пролиферации и миграции меланоцитов – нанесение экстракта плаценты, содержащего гликосфинголипиды и эндотелин, экстракта плодов черного перца, содержащего пиперин, гиалуронатов. Особенность витилиго заключается в том, что течение заболевания зависит от психоэмоционального состояния больных. Поэтому среднестатистическая эффективность медикаментозного лечения витилиго составляет 30–40% [11]. Описано применение витаминов (РР, В6, В12), фурокумариновых соединений, седативных и пероральных антиоксидантных препаратов [3] в комплексе с УФО. Часто рекомендуются маскирующие декоративные средства.
Сочетание указанных принципов местной терапии было апробировано на основе гидрополимерного геля Витискин (Vitiskin, ISIS, Швейцария) в университетской клинике г. Безансон, Франция, в 2007 г. [8]. В состав геля для наружного применения входят СОД, цинк, медь, пантотенат кальция и витамин В12. Применение экзогенной дисмутазы защищает кожу больных витилиго от свободных радикалов, подавляет избыточное перекисное окисление липидов и оказывает противовоспалительное действие. Микроэлементы цинк и медь защищают кожу от окислительных повреждений. Кроме того, медь является важным кофактором тирозиназы и способствует синтезу нового меланина. Пантотенат кальция необходим для усвоения меди и совместно с витамином В12 участвует в синтезе меланина. Назначенное лечение в комбинации с УФО-терапией в 83% случаев привело к умеренному улучшению течения витилиго – прогрессированию равномерной репигментации. У 17% пациентов исследование было завершено со значительным улучшением (курс лечения 10 недель в сочетании с УФО-терапией) [7].
Сейчас выдвигаются новые требования к составу косметических средств. В частности, в связи с онкологической настороженностью рекомендуется не включать в них такие компоненты, как парабены [12, 13]. С учетом этой тенденции удалось стабилизировать фермент супероксиддисмутазу без использования парабенов. Новая молекула была классифицирована как DISMUTIN-J PF и рекомендована для включения в состав лечебных косметических средств как экстракт дрожжей (yeast extract) [10].
Заключение
Несмотря на сохранение клинического интереса к нарушениям обмена меланина и достаточно глубокую изученность этих процессов на биохимическом и молекулярном уровнях, эффективных способов коррекции гипохромии, в частности витилиго, не существует. Теория оксидантного стресса и изучение процессов перекисного окисления липидов заставляют внимательно относиться к местным методам терапии, стабилизирующим окислительные процессы в коже. Высокая клиническая эффективность фермента супероксиддисмутазы, выделенного из экстракта дрожжей Saccharomyces cerevisiae, позволяет рекомендовать его вместе с микроэлементами медью и цинком, витамином В12 и пантотенатом кальция в составе препаратов для лечения пациентов с витилиго.