Современные представления об аллергическом рините у детей
- Аннотация
- Статья
- Ссылки


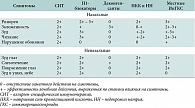
![Таблица 4. Некоторые дифференциально-диагностические признаки аллергических и инфекционных поражений респираторного тракта [12]](/upload/resize_cache/iblock/1b5/195_350_1/nazonex4.jpg)
![Таблица 5. Уровни доказательства пользы различных вмешательств при АР [17]](/upload/resize_cache/iblock/459/195_350_1/nazonex5.jpg)
![Таблица 6. Ступенчатый подход к терапии АР [4]](/upload/resize_cache/iblock/dd1/195_350_1/nazonex6.jpg)

Терминология и классификация
Все еще используемый иногда термин «респираторный аллергоз» нельзя признать корректным в связи с необходимостью уточнения у конкретного больного локализации аллергического воспаления (АР, аллергический фарингит, бронхит, бронхиальная астма) для назначения адекватной терапевтической программы.
До недавнего времени было принято делить АР на две основные формы – сезонный (САР) и круглогодичный (КАР), которые провоцируются соответственно пыльцевыми/грибковыми и бытовыми аллергенами. В 2001 г. международной группой экспертов ARIA (Allergic Rhinitis and its Impact on Asthma – Аллергический ринит и его влияние на астму) данная классификация была пересмотрена. Основанием для пересмотра явились следующие факты:
- в некоторых регионах пыльца и плесень являются круглогодичными аллергенами;
- симптомы КАР не во всех случаях сохраняются на протяжении всего года;
- большинство пациентов сенсибилизированы к различным аллергенам;
- изменения климата сопровождаются изменением сроков длительности пыльцевого сезона, которые трудно прогнозировать;
- пациенты путешествуют;
- у части пациентов, сенсибилизированных только к одному виду пыльцы, симптомы сохраняются на протяжении всего года;
- в результате персистенции минимального аллергического воспаления и развития назальной гиперреактивности у пациентов с бессимптомным АР клинические проявления не всегда возникают в сезон аллергии, либо персистируют на протяжении 2–3 недель после окончания сезона цветения у больных САР, когда вещества, обладающие неспе-цифическим раздражающим действием (такие как воздушные поллютанты), способны индуцировать симптомы (примирующий эффект).
В связи с этим предлагается классифицировать АР следующим образом [1]:
- Интермиттирующий АР – симп-томы сохраняются менее 4 дней в неделю или менее 4 недель подряд.
- Персистирующий АР – симп-томы сохраняются более 4 дней в неделю и более 4 недель подряд.
Легкий АР – симптомы не причиняют беспокойства, отсутствуют следующие проблемы:
- нарушение сна;
- нарушение повседневной активности, отдыха и/или занятий спортом;
- нарушение учебной или трудовой деятельности.
Среднетяжелый/тяжелый АР – симптомы вызывают беспокойство, присутствует по крайней мере одна из следующих проблем:
- нарушение сна;
- нарушение повседневной активности, отдыха и/или занятий спортом;
- нарушение учебной или трудовой деятельности.
Эпидемиология
Аллергический ринит – одно из наиболее распространенных заболеваний человека. Эпидемиологические исследования, проведенные в последние годы, свидетельствуют о существенном увеличении распространенности АР. В России в результате исследований, проводившихся в рамках международной программы ISAAC (International Study of Asthma and Allergies in Childhood – Международное исследование астмы и аллергий в детском возрасте) в 1993–2000 гг., выявлена высокая распространенность симптомов АР у детей. Так, в Москве и Зеленограде распространенность АР составляет 9,8–10,4%, в Новосибирске – 22,5–29,6%, в Иркутской области – 14,8–28,6%, в Ижевске – 23%. Однако, по данным статистической отчетности лечебно-профилактических учреждений, в этих регионах на диспансерном учете находилось менее 0,3% детей с этим заболеванием. Таким образом, очевидна существенная гиподиагностика АР [2]. По некоторым данным, средний срок установления диагноза АР составляет 3 года от начала первых проявлений заболевания (с колебаниями от 1 года до 8 лет).
Распространенность респираторной аллергии у детей первых четырех лет жизни составляет 6%, их них 66% приходится на АР [3]. Заболевание обычно начинается в дошкольном возрасте. Для возникновения клинических проявлений АР необходимо воздействие аллергена в течение двух-трех сезонов, хотя отмечены случаи заболевания у детей первого полугодия жизни. АР распространен больше среди городских жителей, чем среди сельских. В детском возрасте чаще болеют мальчики.
АР не относится к числу тяжелых заболеваний, однако он является причиной существенного снижения качества жизни больных, сопоставимого со снижением качества жизни больных бронхиальной астмой, нарушений сна и способности к обучению. Плохо контролируемые симптомы АР вызывают бессонницу в результате нарушения всех фаз сна. Седация у больных АР, связанная с заболеванием, может еще более усугубляться приемом седативных лекарственных средств, в частности, по-прежнему назначаемых в нашей стране антигистаминных препаратов I поколения, которые уже в течение нескольких лет не рекомендуются международными экспертами (ARIA, 2008) [4]. Более того, в связи с воздействием этих препаратов на ЦНС рассматривается вопрос об исключении их из группы безрецептурного отпуска [5]. САР вызывает усиление сонливости в дневное время. Дети с неконтролируемым АР хуже учатся в школе. Проблемы с обучением могут быть результатом как самого ринита, так и ночной бессонницы и – как следствие – утомляемости в дневное время. САР ассоциируется с ухудшением способности к обучению и результатов экзаменов. Лечение антигистаминными препаратами с седативной активностью усугубляет эти проблемы, в то время как неседативные антигистаминные препараты частично уменьшают их. Другой причиной снижения успеваемости могут быть пропуски школьных занятий. Так, в США из-за АР дети пропускают до 1,5 млн школьных часов ежегодно [6]. С учетом этих данных становится понятно, какое драматическое значение для развития ребенка может иметь позднее, как говорилось ранее, с задержкой в среднем на 3 года, установление диагноза и неполучение адекватного лечения.
Важность проблемы АР обусловлена его тесной связью с такими заболеваниями, как бронхиальная астма, острый и хронический риносинусит, аллергический конъюнктивит. Установлено, что у 24% детей АР явился предрасполагающим фактором для развития острого и хронического среднего отита, а в 28% случаев – хронического риносинусита [7].
Этиология и патогенез
Аллергия, или гиперчувствительность, – это собирательное название типовых иммунопатологических процессов, развивающихся в сенсибилизированном организме генетически предрасположенных лиц в режиме вторичного иммунного ответа при контакте с антигеном, вызвавшим сенсибилизацию. Антигены, провоцирующие аллергию, получили название аллергенов. Основные аллергены, вызывающие развитие АР, это [6]:
Внешние (причина САР):
Пыльца:
- деревьев (береза, ольха, лещина, дуб, вяз, клен) – апрель–июнь;
- злаковых (луговых) трав (тимофеевка, овсяница, костер, ежа, райграс, лихохвост, рожь) – июнь–июль;
- сорняков (лебеда, полынь, амброзия) – август–сентябрь;
Плесневые грибы (Aspergillus, Cladosporium) – сентябрь–октябрь.
Внутридомашние (причина КАР):
- клещи домашней пыли (Dermatophagoides farinae, pteronyssinus);
- теплокровные домашние животные (кошки, собаки и др.);
- синантропные виды (мыши, крысы, тараканы);
- плесневые грибы (Aspergillus, Penicillium);
- сухой корм для аквариумных рыбок (рачки циклопы, дафнии).
В соответствии с классической классификацией R. Gell и P. Coombs (1964) выделяют четыре типа реакций гиперчувствительности. Тип I (атопия) характеризуется связыванием IgE с Fc-рецепторами тучных клеток. При контакте с аллергеном происходит перекрестное связывание IgE, что приводит к дегрануляции тучных клеток и высвобождению медиаторов аллергических реакций. АР является классическим атопическим заболеванием.
Аллергический процесс последовательно проходит иммунологическую, патохимическую и патофизиологическую стадии. Данная периодизация была предложена основоположником отечественной аллергологии А. Д. Адо. Результаты современных исследований позволили детализировать события аллергического ответа, происходящие на данных стадиях.
Иммунологическая стадия охватывает все изменения в иммунной системе с момента первого поступления аллергена в организм до соединения эффекторов иммунного ответа (антител) с повторно поступившим в организм аллергеном. Дихотомию дифференцировки CD4+ Т-лимфоцитов в процессе развития иммунного ответа с возникновением либо Tх1-, либо Tх2‑лимфоцитов называют иммунным отклонением, или девиацией иммунного ответа в сторону той или иной субпопуляции – Tх1 или Tх2 типа. Тх2‑девиация иммунного ответа является основной причиной атопии. Тх1‑ и Тх2‑клетки находятся во взаимно антагонистических отношениях, регулируют активность друг друга по механизму реципрокной регуляции.
Соотношение субпопуляций Тх1 и Тх2 в разные возрастные периоды имеет определенные различия. Если у здоровых взрослых отмечается относительное преобладание Тх1, а отношение Тх2 : Тх1 составляет в периферической крови 3 : 4, то в пуповинной крови это отношение 10–100 : 1, следовательно, для плода и новорожденного ребенка характерна Тх2‑поляризация. Она чрезвычайно важна для физиологического течения беременности. Доминирование в конце внутриутробной жизни выработки Тх2‑клеток носит адаптивный характер и направлено на защиту плаценты от потенциальной токсичности Тх1. Было установлено, что у женщин, страдающих АР, быстрее наступает беременность по сравнению с женщинами, не имеющими данного заболевания. Однако, с учетом существования генетической предрасположенности, у этих женщин чаще будут рождаться дети с АР.
Суть патохимической стадии заключается в образовании и выделении биологически активных медиаторов воспаления. В настоящее время в развитии аллергического ответа выделяют раннюю и позднюю фазы, различия клинических проявлений которых связывают с действием разных медиаторов (табл. 1).
Патофизиологическая стадия, или стадия клинических проявлений, характеризуется патогенным действием медиаторов на клетки, ткани и органы. При АР это слизистая оболочка носа. Связь некоторых клинических симптомов АР с действием медиаторов представлена в табл. 2 [9].
Клиническая картина и диагностика
АР у детей, в особенности раннего и дошкольного возраста, диагностировать трудно.
Большое значение в диагностике АР имеет сбор анамнеза. Следует определить длительность сохранения симптомов, связь времени их начала или прекращения с сезонностью, сменой места жительства или жилища, появлением в доме домашних животных, сыростью в квартире (плесневые грибы), провоцирующими факторами (действующие сезонно или круглогодично аллергены), неспецифическими раздражителями (сигаретный дым, холодный воздух, химические пары, резкие запахи).
Важно установить наличие симптомов в момент обращения к врачу, включая зуд, чихание, ринорею, боль в области пазух, определить степень заложенности носа. Чрезвычайно характерны и специфичны для АР у детей симптомы-эквиваленты зуда: «аллергический салют» (утирание носа движением руки вверх и кнаружи), гримасы, появление поперечной складки на спинке носа.
Для определения терапевтической тактики чрезвычайно важно выявить один из двух фенотипов болезни:
- ведущими симптомами являются чихание и зуд в полости носа;
- доминирует заложенность носа (у детей этот синдром усугубляет узкий просвет носовых ходов).
Здесь просматривается связь с различной эффективностью подавления симптомов аллергического ринита разными методами лечения (табл. 3) [10, 11].
Необходимо уточнить наличие симптомов со стороны глаз (зуд, слезотечение, отечность), со стороны глотки (першение, болезненность при глотании, зуд в области неба и горла) и сопутствующих общих симптомов в виде недомогания, слабости, нарушения сна, аллергических заболеваний (атопический дерматит, бронхиальная астма), отягощенности семейного аллергологического анамнеза, эффективность применяемых лекарственных препаратов.
Кроме чихания, зуда в носу, выделений и заложенности носа, у детей со среднетяжелым/тяжелым АР могут наблюдаться шумное дыхание, храп и нарушение обоняния или вкуса, рецидивирующие носовые кровотечения (результат форсированного сморкания и ковыряния в носу). Могут также отмечаться изменения лица, слизистых оболочек ротовой полости и признаки обструкции дыхательных путей: открытый рот, растрескавшиеся губы, гипертрофия слизистой оболочки десен и фолликулов задней стенки глотки, удлинение лица (аденоидное лицо), готическое небо, аномалии прикуса. Профузная или периодическая ринорея с выделением большого количества водянистого секрета приводит к раздражению кожи над верхней губой и крыльев носа, вызывая их отечность и гиперемию, при осмотре зева определяются прозрачные или белые выделения на задней стенке глотки. У больных АР могут выявляться также периорбитальный цианоз, дополнительные суборбитальные складки Денни-Моргана (типично для больных с сопутствующим атопическим дерматитом). Появление гнойных выделений, нехарактерных для неосложненного АР, свидетельствует о присоединении вторичной инфекции. Могут быть увеличены передние шейные лимфатические узлы. Раздражающее действие подтекающего из носа секрета, а также персистирующее воспаление верхних дыхательных путей вызывают хронический непродуктивный кашель. Кашель может сопровождаться жалобами на затруднение дыхания. Проглатывание большого количества слизи может вызывать боли в животе.
Характерной особенностью САР является периодичность обострений. Симптомы рецидивируют из года в год, в одно и то же время, четко связаны с периодом цветения определенных растений. Клинические симптомы САР, вызванного пыльцой растений, ослабевают вплоть до полного прекращения во время дождя, когда концентрация пыльцы в воздухе уменьшается.
Симптомы АР часто путают с проявлениями острых респираторных инфекций. При сохранении респираторных симптомов более двух недель на фоне нормальной температуры тела, а также при наличии других признаков аллергического характера заболевания (табл. 4) необходимо исключать АР.
Подтверждают диагноз АР результаты риноскопии (бледная или голубоватая окраска слизистой оболочки носа, увеличенная нижняя носовая раковина), назоцитограммы (эозинофилия), аллергодиагностика. Последняя осуществляется с помощью постановки кожных проб или сопоставимого по информативности определения специфических IgE-антител к причинно значимым аллергенам. В связи с тем, что при обострении заболевания IgE фиксируются в тканях, оптимально проводить их определение в фазе ремиссии АР. Спектр тестируемых аллергенов определяется на основании сбора анамнеза. При оценке результатов определения специфических IgE необходимо учитывать возможность латентной сенсибилизации. Повышенный уровень в сыворотке крови общего IgE не является критерием диагностики АР (также как и бронхиальной астмы) и надежным предиктором атопии, поскольку показатели общего IgE значительно варьируют у детей в зависимости от возраста, увеличиваются на фоне инфекционных заболеваний [13, 14].
Дифференциальная диагностика АР у детей дошкольного возраста проводится, помимо инфекционного ринита (обычно вирусного), с инородным телом, анатомическими дефектами носа, включая одностороннюю атрезию хоан, доброкачественными опухолями, в том числе дермоидными кистами, менингоэнцефалоцеле, муковисцидозом, мукоцилиарной дискинезией и синдромом Картагенера, обструкцией носа вследствие гипертрофии аденоидов.
У детей старшего возраста АР необходимо дифференцировать от последствий травмы (гематома перегородки, перелом костей носа и синехии), цереброспинальной ринореи, глиомы носа и медикаментозного ринита при злоупотреблении местными деконгенсантами. При наличии полипоза носа требуется исключение муковисцидоза [4].
Аллергический ринит и бронхиальная астма
На основании анализа эпидемиологических, клинических наблюдений и изучения патогенеза АР и бронхиальной астмы установлена тесная взаимосвязь данных заболеваний.
Носовые ходы являются интегративной частью респираторного тракта. Слизистая оболочка носа сходна со слизистой оболочкой бронхов. В АRIA 2008 г. отмечено, что около 80% астматиков имеют АР и 10–40% больных АР имеют бронхиальную астму. Соответственно была предложена концепция «одни дыхательные пути, одна болезнь».
АР способствует развитию обострений астмы, увеличению частоты приступов удушья, обращений за неотложной медицинской помощью, госпитализаций по поводу астмы. Вероятность заболеть бронхиальной астмой у пациентов, страдающих АР, в три раза выше, чем у здоровых людей, кроме того, формированию астмы, как правило, предшествует ринит (у 32–49% пациентов). Многие больные АР имеют повышенную бронхиальную реактивность. Эта взаимосвязь обусловлена единством триггерных факторов и патогенетических механизмов развития обоих заболеваний. Таким образом, когда речь идет о диагностике АР или бронхиальной астмы, необходимо проводить обследование как верхних, так и нижних дыхательных путей. Эксперты АRIA 2008 г. рекомендуют обязательное обследование пациентов с персистирующим АР для исключения астмы (исследование функции внешнего дыхания на наличие бронхиальной обструкции и ее обратимости), пациентов с астмой для исключения АР (риноскопия, аллергодиагностика). Установлено, что раннее энергичное лечение АР может помочь предотвратить развитие бронхиальной астмы и уменьшить ее тяжесть. Несколько исследований показали улучшение симптомов астмы на фоне интраназального применения кортикостероидов при астме [14, 15]. Существование системной связи между АР и бронхиальной астмой обусловливает рациональность применения единой системной терапии этих заболеваний. Средствами системной терапии пациентов, страдающих одновременно АР и астмой, являются антагонисты лейкотриеновых рецепторов (монтелукаст натрия), специфическая иммунотерапия, при тяжелых формах заболевания – моноклональные антитела к IgE, системные кортикостероиды.
Лечение
При составлении терапевтической программы у ребенка, страдающего АР, необходимо учитывать следующие аспекты:
- эффективность тех или иных терапевтических/профилакти-ческих вмешательств. Оценивается с точки зрения патофизиологической обоснованности и воздействия на различные проявления заболевания (табл. 1, 3) и на основании контролируемых исследований с позиций доказательной медицины (табл. 5);
- очень важно оценивать побочные эффекты терапии, уникальные для детей, особенно при сочетании АР и астмы (задержка роста, влияние на когнитивную функцию);
- особое внимание следует уделять когнитивной функции у детей дошкольного и школьного возраста, которая может ухудшаться под влиянием АР и/или терапии антигистаминными препаратами I поколения;
- многие лекарственные препараты, назначаемые детям с АР, не зарегистрированы для применения в педиатрии;
- при лечении АР необходимо учитывать тяжесть и длительность болезни, предпочтения пациента, а также эффективность и доступность для пациента лекарственных препаратов;
- фармакотерапию подбирают индивидуально. Следует избегать полипрагмазии и стремиться к достижению контроля заболевания минимально достаточным объемом терапии, используя ступенчатый подход в зависимости от степени тяжести АР, рекомендованный согласительными документами ARIA 2001 и 2008 гг. (табл. 6).
Ниже представлены новые данные об эффективности и рекомендации использования различных терапевтических вмешательств при АР у детей на основании согласительного документа ARIA 2008 г. Антигистаминные препараты. Большое значение в лечении АР у детей имеют антигистаминные препараты. Маленькие дети предпочитают пероральные препараты интраназальным. Антигистаминные препараты I поколения вызывают серьезные побочные эффекты у детей, усугубляя влияние самого заболевания на состояние нервной системы (седация, усталость, снижение концентрации внимания, бессонница, раздражительность), поэтому назначаться при АР не должны. Напротив, новые антигистаминные препараты уменьшают недомогание, вызванное АР, и могут даже улучшить способность к обучению пациентов с АР. В длительных исследованиях АР у детей подтверждена эффективность и безопасность лоратадина, цетиризина, левоцетиризина и дезлоратадина [18–20].
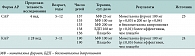
Глюкокортикостероиды. Интраназальные кортикостероиды (ИнГКС) – это самые эффектив-ные средства лечения АР. В настоящее время в России зарегистрирован ряд препаратов ИнГКС в виде назальных спреев, дозированных аэрозолей, назальных капель (табл. 7) [7].
Современные препараты ИнГКС хорошо переносятся больными и могут использоваться в качестве базисной терапии среднетяжелого/тяжелого АР без риска угнетения мукоцилиарного клиренса и атрофии слизистой оболочки носа длительное время. Вместе с тем при их назначении всегда необходимо учитывать страх родителей перед системными побочными эффектами, которые в действительности встречаются не часто. Предполагается, что ИнГКС не влияют на гипо-таламо-гипофизарно-надпочеч-никовую систему у детей и могут назначаться длительно. В 12‑месячных исследованиях у детей, получавших флутиказона пропионат, мометазона фуроат, не была отмечена задержка роста [21, 22]. В то же время у детей, регулярно пользовавшихся интраназальным беклометазоном, в течение года было выявлено небольшое снижение скорости роста [23]. У флутиказона пропионата биодоступность составляет 1–2%, а у мометазона фуроата – всего 0,1%, чем объясняется благоприятный профиль безопасности мометазона фуроата и делает данный ИнГКС препаратом выбора у детей начиная с двухлетнего возраста. Эффективность мометазона фуроата подтверждена в рандомизированных плацебо-контролируемых исследованиях как при САР, так и при КАР у детей на основании шкал оценки общих назальных симптомов (табл. 8).
При лечении АР у детей следует избегать применения пероральных кортикостероидов.
Кромоны. Кромогликат натрия был одним из самых популярных препаратов в лечении АР у детей, однако он менее эффективен, чем ИнГКС или антигистаминные средства. У детей этот препарат не вызывает побочных эффектов. Однако кромогликат необходимо использовать 4–6 раз в сутки, что определяет низкую комплаентность при его назначении.
Антагонисты лейкотриеновых рецепторов. Монтелукаст рекомендуется применять для лечения САР у пациентов старше 6 лет, он является препаратом выбора при сочетании АР с персистирующей бронхиальной астмой.
Деконгенсанты. Интраназальные деконгенсанты (сосудосуживающие препараты) могут быть назначены на короткий срок (до 7 дней) пациентам с тяжелой обструкцией носа. Препараты этой группы следует применять с осторожностью у детей грудного возраста, так как интервал между терапевтической и токсической концентрацией препарата небольшой.
Специфическая иммунотерапия. Экспертами ARIA 2008 г. были сформулированы следующие положения о применении специфической иммунотерапии (СИТ) при АР:
- в настоящее время возможно местное применение СИТ;
- СИТ возможна только при подтвержденном диагнозе IgE-опосредованной аллергии;
- подкожная СИТ эффективна у взрослых и детей с аллергией на пыльцу и клещей домашней пыли, но она несет в себе риск побочных реакций, в том числе жизнеугрожающих;
- сублингвальная СИТ рекомендуется для лечения пыльцевой аллергии у взрослых, возможна у пациентов с аллергией на клещей, ее безопасность была установлена у детей дошкольного возраста, однако эффективность нуждается в дополнительном изучении;
- СИТ у больных ринитом предотвращает развитие бронхиальной астмы (вторичная профилактика астмы), снижает риск сенсибилизации к новым аллергенам, может изменить естественное течение аллергических заболеваний;
- долгосрочный эффект СИТ сохраняется в течение нескольких лет после ее отмены;
- СИТ обычно не рекомендуется в возрасте до 5 лет из-за риска побочных эффектов, а также сложности выполнения повторных инъекций на протяжении нескольких месяцев/лет.
Таким образом, АР у детей является распространенным атопическим заболеванием с назальными и неназальными симптомами, тесно связанным с бронхиальной астмой. Международные рекомендации ARIA 2008 г. содержат важнейшую информацию о современных методах диагностики и лечения АР у детей. Фармакотерапией первой линии у пациентов со среднетяжелым/тяжелым течением ринита являются интраназальные глюкокортикостероиды. Препаратом выбора, рекомендуемым для детей раннего возраста (от 2 лет и старше), является мометазона фуроат (Назонекс) в связи с самой низкой среди известных интраназальных ГКС биодоступностью (< 0,1%), высоким профилем безопасности и эффективности.
