Терапия респираторных обструктивных заболеваний: стандарты и реальность. XIV Международный конгресс «Современные проблемы иммунологии, аллергологии и иммунофармакологии». Сателлитный симпозиум компании «Натива»
- Аннотация
- Статья
- Ссылки




GINA-2016 и GINA-2017. Федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы: практические вопросы терапии
В 2016 г. были опубликованы два обновленных документа – руководство по лечению и профилактике бронхиальной астмы GINA (Global Initiative for Asthma), в некоторой степени обновленное и дополненное в 2017 г., и федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы Российского респираторного общества. Как отметил главный специалист по аллергологии и иммунологии Приволжского федерального округа и Министерства здравоохранения Республики Татарстан, д.м.н., профессор Рустэм Салахович ФАССАХОВ, существенных отличий между двумя руководствами нет. Но для отечественных специалистов основополагающими являются российские федеральные клинические рекомендации, подготовку которых Минздрав России поручил профессиональному медицинскому сообществу.
В руководствах дано новое определение бронхиальной астмы (БА). Это гетерогенное заболевание, обычно характеризующееся хроническим воспалением дыхательных путей. Основные изменения касаются также контроля БА и практического всестороннего подхода к ведению пациентов. Выделены две важные составляющие – контроль симптомов и оценка факторов риска неблагоприятных исходов. Что касается подхода к ведению больных БА, в отличие от GINA в федеральных клинических рекомендациях приведены примеры формулировок диагноза.
В новых рекомендациях предусмотрен четкий диагностический алгоритм для врача. Выявление вариабельной обструкции – важный этап диагностики БА. Для ее подтверждения изучают функцию внешнего дыхания. По словам профессора Р.С. Фассахова, без функциональной диагностики, исследования проходимости бронхов говорить о БА нецелесообразно. Если первоначальное исследование дало отрицательный результат, необходимо провести повторное при появлении симптомов или после отмены бронхолитических средств.
Анализ контроля БА предусматривает оценку симптомов в течение последних четырех недель и факторов риска неблагоприятных исходов. На контроль астмы влияют:
- техника выполнения ингаляций;
- побочные эффекты терапии;
- приверженность пациента назначенному врачом лечению;
- отношение пациента к своему заболеванию.
Факторы риска неблагоприятных исходов включают в том числе наличие сопутствующей патологии (риносинусита, гастроэзофагеальной рефлюксной болезни, ожирения, обструктивного апноэ во сне) и депрессию. Лечение сопутствующих заболеваний приводит к улучшению контроля БА и в конечном итоге к снижению объема терапии.
К факторам риска обострений относятся неконтролируемые симптомы БА, наличие более одного обострения за предыдущий год, низкий объем форсированного выдоха за первую секунду (ОФВ1), а также развитие необратимой обструкции и побочного действия лекарственных средств. Еще в GINA-2015 отмечалось, что фактором риска обострений может быть передозировка бета-2-агонистов короткого действия (КДБА), а причиной летального исхода – очень частое (более 200 доз в месяц) их использование.
Тяжесть БА у больных с установленным диагнозом, получающих лечение, оценивается ретроспективно по уровню терапии, необходимой для контроля симптомов и обострений. Астма легкой степени характеризуется хорошим контролем на первой-второй ступени терапии (КДБА или низкие дозы ингаляционных глюкокортикостероидов (ИГКС)). Среднетяжелая БА хорошо контролируется на третьей ступени (низкие дозы ИГКС + бета-2-агонисты длительного действия (ДДБА)). Тяжелая БА предполагает проведение терапии четвертого-пятого уровня (средние или высокие дозы ИГКС + ДДБА и проч.).
Тяжесть астмы со временем может меняться. Не случайно ведение пациента с БА – это непрерывный цикл, предполагающий оценку симптомов, коррекцию терапии, обучение пациента технике ингаляции и проверку необходимых навыков.
Как известно, вариабельность течения астмы подразумевает ступенчатый подход к лечению. Поскольку роль воспаления в патогенезе БА очевидна, ИГКС признаны основными препаратами в лечении данного заболевания. Терапия ИГКС на начальных ступенях предполагает применение низких доз. Показанием для назначения ИГКС являются симптомы чаще двух раз в месяц, ночные пробуждения из-за БА чаще одного раза в месяц или любые симптомы астмы при наличии хотя бы одного из рисков обострения.
Если на первой ступени предпочтительны КДБА по требованию или комбинация КДБА и ипратропия бромида, то на второй ступени обязателен прием низких доз ИГКС, а также КДБА по требованию. Кроме того, на второй ступени показан периодический прием ИГКС и КДБА по требованию у пациентов с пыльцевой БА в отсутствие симптомов вне сезона. Таким больным следует назначать ИГКС сразу после появления симптомов и продолжать терапию в течение четырех недель после завершения сезона.
На третьей ступени обычно используют низкие дозы ИГКС в комбинации c ДДБА, КДБА или низкие дозы ИГКС/формотерола по требованию. На четвертой ступени больным старше 18 лет с обострениями в анамнезе к комбинации средних или высоких доз ИГКС/ДДБА можно добавлять тиотропия бромид (только в форме раствора для ингаляций). На пятой ступени предусмотрены направление больных на обследование к специалисту и назначение омализумаба в случае подтвержденной аллергической астмы.
Состояние пациента первоначально оценивают через 1–3 месяца после лечения и впоследствии каждые 3–12 месяцев. После обострения в течение первой недели пациента необходимо проконсультировать. Если БА плохо контролируется, можно увеличить продолжительность терапии (на два-три месяца). При вирусной инфекции или контакте с аллергенами возможно кратковременное (одна-две недели) повышение дозы. При хорошем контроле астмы в течение трех месяцев рассматривают вопрос о снижении дозы препаратов.
В целом последние международные и федеральные клинические рекомендации по астме являются для специалистов практическим руководством при выборе оптимальной тактики ведения больных БА.
Что касается лекарственной терапии пациентов с БА, в настоящее время преимущественно все препараты поставляются в страну иностранными производителями. В рамках государственной программы импортозамещения, утвержденной Президентом РФ еще в 2009 г., проводится ряд мероприятий по выпуску в стране до 90% препаратов, используемых для терапии БА и хронической обструктивной болезни легких (ХОБЛ). Однако единственным примером реализации данной стратегии фактически служит только производственная деятельность российской фармацевтической компании «Натива». Компания является исполнителем 43 государственных контрактов в области разработки и полного цикла производства лекарственных средств (из Перечня жизненно необходимых и важнейших лекарственных препаратов, утвержденного Правительством РФ), а также фармацевтических субстанций. Производство лекарственных препаратов организовано в соответствии с европейскими правилами GMP (компанией получены европейский и российский сертификаты GMP), что позволяет осуществлять контроль качества выпускаемых препаратов на всех этапах.
Перечень лекарственных средств компании, применяемых в пульмонологии, включает фактически весь спектр препаратов базисной терапии и препаратов экстренной терапии для больных БА и ХОБЛ.
Свойства воспроизводимых ингаляционных препаратов компании «Натива», как односоставных, так и в виде фиксированных комбинаций, а также их эффективность и безопасность сравнивали с таковыми оригинальных лекарственных средств в лабораторных, рандомизированных многоцентровых клинических исследованиях и в рамках наблюдательных исследований.
Результаты открытых рандомизированных многоцентровых клинических исследований сравнительной эффективности (ОФВ1, л, ОФВ1, % прироста, ФЖЕЛ (форсированная жизненная емкость легких), % прироста, ПСВ (пиковая скорость выдоха), CAT (COPD Assessment Test), ACQ (Asthma Control Questionnaire) и др.) и безопасности препаратов в виде растворов, аэрозолей и порошков для ингаляций продемонстрировали полную терапевтическую эквивалентность: препарата Ипратерол-натив и оригинального комбинированного препарата «фенотерол + ипратропия бромид», Фенотерол-натив и оригинального препарата фенотерола, Ипратропиум-натив и оригинального препарата ипратропия бромида, Ипратропиум-аэронатив и оригинального препарата ипратропия бромида в виде дозированного аэрозоля, Формисонид-натив и оригинального препарата «формотерол + будесонид», Салтиказон-натив и оригинального препарата «салметерол + флутиказон».
При сравнительных исследованиях аэродинамических свойств (респирабельная фракция) препараты Ипратерол-натив, Ипратропиум-натив, Ипратропиум-аэронатив, Формотерол-натив, Беклометазон-аэронатив и другие продемонстрировали полную идентичность иностранным аналогам по величине респирабельной фракции и профилям распределения частиц по размерам1.
Таким образом, отечественные воспроизведенные препараты, применяемые в терапии БА, ХОБЛ и бронхообструктивного синдрома, сопоставимы по качественному и количественному составу, показателям респирабельной фракции, клинической эффективности и безопасности, при этом на 20–30% экономически более выгодны. В современных экономических и политических условиях это принципиально важно для страны.
Профессор Р.С. Фассахов подчеркнул, что появление на рынке новых производителей, особенно отечественных, способствует повышению конкурентоспособности, возможной локализации производства иностранных препаратов в стране и в конечном итоге повышению качества лекарственных препаратов и их доступности для большего числа пациентов (лишь немногие имеют возможность получать лекарственные препараты бесплатно в рамках государственной программы льготного лекарственного обеспечения). У пациентов появляется возможность применять более доступные и качественные лекарственные средства. Современная фармакотерапия позволяет успешно контролировать течение БА, а основу терапии у подавляющего большинства пациентов с БА составляют препараты ИГКС, в том числе в комбинации с ДДБА.
Бронхиальная астма: научные дискуссии или реалии и практика
По словам заместителя директора по клинической работе – главного врача Института иммунологии ФМБА России, главного аллерголога ФМБА России, д.м.н., профессора Натальи Ивановны ИЛЬИНОЙ, сегодня ни у кого не вызывает сомнения, что бронхиальная астма – хроническое, воспалительное, неизлечимое заболевание, гетерогенное по этиологии и патогенезу. Тяжесть БА, степень которой у каждого пациента может меняться в течение нескольких месяцев и лет, зависит не только от выраженности симптомов, но и от ответа на терапию.
С позиции современной медицины БА имеет ряд хорошо очерченных фенотипов. Выделяют аллергическую (атопическую), неаллергическую, БА с поздним дебютом, с фиксированной обструкцией дыхательных путей и БА у пациентов с ожирением.
В исследовании P. Haldar и соавт. были определены клинические фенотипы, такие как ранняя астма с преобладанием симптомов, неэозинофильная астма с ожирением, атопическая астма с ранним началом, доброкачественная астма и астма с преобладанием воспаления2.
Описаны различные фенотипы БА при распределении больных по кластерам. Био- или воспалительные фенотипы БА характеризуют тип воспаления дыхательных путей: эозинофильный (> 3% эозинофилов в мокроте), нейтрофильный (> 61% нейтрофилов в мокроте), смешанный гранулоцитарный (> 3% эозинофилов и > 61% нейтрофилов) и малогранулоцитарный (эозинофилы и нейтрофилы в пределах нормы).
В 2010 г. итальянские ученые описали менопаузальную астму как новый биологический фенотип, отличающийся прежде всего нейтрофильным респираторным воспалением3. По мнению исследователей, такая форма астмы невосприимчива к ГКС, характеризуется слабым контролем симптомов и повышенным уровнем лейкотриенов.
Вместе с тем не утратила актуальности сформулированная в 1969 г. профессорами А.Д. Адо и П.К. Булатовым классификация, согласно которой БА подразделяют на инфекционно-аллергическую и неинфекционно-аллергическую (атопическую). Кроме того, в рутинной клинической практике широко применяют клинико-патогенетические варианты БА, разработанные в 1982 г. профессором Г.Б. Федосеевым.
Индикатором патофизиологического процесса или ответа на терапевтическое воздействие служит биомаркер – физикальный или лабораторный параметр. Биомаркер должен отличаться чувствительностью, специфичностью, возможностью измерения, своевременностью, воспроизводимостью и доступной ценой.
Профессор Н.И. Ильина отметила, что современные лабораторные биомаркеры, такие как оксид азота (FeNO), остеопонтин, периостин, как правило, не отвечают перечисленным выше требованиям и не могут использоваться в ежедневной практике. Единственным лабораторным биомаркером, используемым в реальной клинической практике, остается уровень эозинофилии (кровь, мокрота, назальный секрет).
Разработка иммунобиологических препаратов привела к появлению таргетной терапии БА. Один из таргетных препаратов (омализумаб) включен в клинические рекомендации как препарат пятой ступени терапии атопической БА, хотя, по мнению докладчика, при атопической астме по-прежнему эффективна известная базисная комбинированная терапия ИГКС и ДДБА. Тяжелая форма БА обычно ассоциируется с сопутствующей патологией, требующей диагностического поиска. Иммунобиологические препараты по сравнению с известной базисной терапией отличаются высокой стоимостью и на практике не всегда доходят до пациентов.
Астма слишком сложное заболевание, и мишенизирование одного рецептора или медиатора не может быть эффективным. Основу терапии БА по-прежнему составляют ИГКС, полностью подавляющие воспаление4. Выбор наилучшего препарата затруднителен. Дело в том, что все ИГКС имеют достаточную для клинического эффекта противовоспалительную активность. Эффективность в конечном итоге выходит на плато, и дальнейшее увеличение дозы на нее не влияет.
Современным направлением в лечении БА (кроме легкой степени астмы) считается использование в качестве стартовой терапии комбинированных препаратов, обеспечивающих максимальный контроль над болезнью. Добавление к ИГКС препаратов ДДБА существенно повышает эффективность и безопасность противоастматической терапии. Систематический обзор и метаанализ пяти исследований показали, что отмена ДДБА у пациентов с астмой, контролируемой на фоне применения комбинации ДДБА и ИГКС, приводит к ухудшению контроля и качества жизни пациентов.
Согласно GINA, снижая объем терапии, необходимо уменьшать на 50% дозу ИГКС, не отменяя ДДБА. FDA (Food and Drug Administration – Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) рекомендует использовать ДДБА в комбинации с ИГКС в течение непродолжительного периода до достижения контроля.
К сожалению, достичь идеального контроля над симптомами заболевания удается не всегда. Этому мешает, в частности, низкая приверженность пациентов лечению (в клинической практике явление далеко не редкое): по оценкам, около половины пациентов с БА при длительной терапии не принимают назначенных врачом препаратов (нарушаются кратность приема, дозировка, постоянство терапии)5. Причин несколько: недооценка пациентом тяжести своего заболевания, недовольство врачом, неудобный режим приема лекарственного средства, сложное для применения дозирующее ингаляционное устройство и неадекватная техника использования ингалятора, побочные эффекты, удаленность аптек, стероидофобия, прекращение назначенной врачом терапии после достижения контроля астмы в течение определенного периода. Кроме того, существенным препятствием на пути лечения бронхиальной астмы является низкая доступность профильной медицинской помощи (нехватка специалистов в регионах) и необходимых лекарственных препаратов (как правило, комбинированных препаратов базисной терапии).
Как показал опрос пациентов с БА об удобстве пользования системой льготного лекарственного обеспечения, проведенный методом анкетирования в 2014 г. специалистами Института иммунологии ФМБА России:
- каждый второй пациент приобретает препараты самостоятельно;
- 45% считают действующую систему обеспечения лекарственными средствами неудобной.
Таким образом, становится очевидной необходимость, с одной стороны, оптимизации системы льготного лекарственного обеспечения, с другой – обеспеченности эффективными, безопасными и экономически доступными отечественными лекарственными средствами. Не случайно в 2015 г. вышло постановление Правительства РФ об ограничении допуска происходящих из иностранных государств лекарственных средств, относящихся к важнейшим и жизненно необходимым, для муниципальных и региональных программ льготного лекарственного обеспечения и закупок стационарами.
Итоги опроса пациентов в аптеках, организованного Общероссийским народным фронтом, о существующем лекарственном обеспечении показали, что в 70% случаев сами пациенты оценивали качество купленных ими отечественных препаратов как идентичное качеству импортных аналогов (по мнению 9% респондентов, качество отечественных препаратов по сравнению с иностранными аналогами выше).
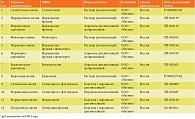
По словам профессора Н.И. Ильиной, выпускаемые в настоящее время российской компанией «Натива» воспроизведенные лекарственные средства являются де-факто единственными российскими препаратами для ступенчатой терапии БА. Компания производит практически весь спектр противоастматических лекарственных средств, рекомендованных как GINA, так и федеральными клиническими рекомендациями (таблица). При этом порошковые формы снабжены оригинальным простым, удобным, надежным ингалятором Инхалер CDM.
Институт иммунологии был главной клинической базой при проведении целого ряда многоцентровых рандомизированных сравнительных клинических исследований эффективности и безопасности лекарственных препаратов «Натива» (в одинаковой дозе у пациентов с неконтролируемой и частично контролируемой персистирующей БА). Анализ полученных данных позволил сделать вывод, что по эффективности, безопасности и переносимости исследуемые отечественные препараты не уступали препаратам сравнения:
- Салтиказон-натив и Серетид Мультидиск (GSK, Великобритания)6;
- Салтиказон-аэронатив и Серетид (GSK, Польша);
- Формисонид-натив и Симбикорт Турбухалер (AstraZeneca, Швеция);
- Формотерол-натив и Форадил (Novartis, Швейцария).
Важны также результаты фармакокинетических исследований препаратов компании «Натива». Клинические фармакологи Российского национального исследовательского медицинского университета им. Н.И. Пирогова сравнивали аэродинамические характеристики препаратов Беклометазон-аэронатив и Беклазон (Teva, Израиль) и Кленил (Chiesi pharmaceuticals, Италия), Ипратерол-натив и Беродуал (Boehringer Ingelheim, Германия) и др. Показатели однородности дозирования и респирабельности фракции у отечественных и иностранных препаратов были одинаковы7.
С учетом возрастающей доступности лекарственных средств экономическая выгода от применения препаратов Салтиказон-натив в сравнении с препаратом Серетид Мультидиск и Формисонид-натив в сравнении с препаратом Симбикорт Турбухалер составляет 20–25%.
В заключение профессор Н.И. Ильина перечислила способы повышения эффективности терапии астмы:
- проведение биомаркер-ориентированной терапии (например, титрование ИГКС в зависимости от эозинофилии мокроты или FeNO);
- выделение клинических фенотипов с разным ответом на терапию;
- выявление биомаркеров и фармакогенетических параметров, позволяющих прогнозировать ответ на терапию;
- повышение приверженности пациентов назначенной врачом терапии за счет создания ингаляционных препаратов, применяемых один раз в день;
- повышение доступности лекарственных препаратов базисной терапии БА, особенно отечественных;
- повышение приверженности пациентов назначенной врачом терапии за счет внедрения в практику лекарственных препаратов с простыми и надежными средствами доставки;
- повышение доступности медицинской помощи, оказываемой специалистами респираторной медицины, увеличение штата таких специалистов, а также времени, уделяемого ими для обучения и работы с каждым пациентом.
Бронхиальная астма и ХОБЛ: фармакоэкономика внедрения клинических рекомендаций
Экономическая оценка в системе здравоохранения представляет собой определение денежной стоимости применяемых технологий. Евгений Кронидович БЕЛЬТЮКОВ, главный аллерголог Уральского федерального округа и Свердловской области, д.м.н., профессор кафедры терапии Уральского государственного медицинского университета, отметил, что, например, в США ежегодные прямые и непрямые затраты на лечение БА достигают 12 млрд долл., на лечение ХОБЛ – 32 млрд долл.8 Согласно подсчету благотворительного фонда «Качество жизни», в России общие и косвенные затраты, экономические потери, связанные с отсутствием на рабочем месте (для работающих), в 2013 г. для БА превысили 13 млрд руб., для ХОБЛ – 24 млрд руб.
Как известно, международным руководством по диагностике и лечению БА признаны рекомендации GINA, по диагностике, лечению и профилактике ХОБЛ – рекомендации GOLD (Global Initiative for Chronic Obstructive Lung). Однако для российских врачей приоритетными должны оставаться федеральные клинические рекомендации по диагностике и лечению БА и ХОБЛ.
Профессор Е.К. Бельтюков представил результаты собственных исследований фармакоэкономической эффективности внедрения GINA и GOLD.
В ходе исследования были проанализированы общепринятые медико-экономические показатели:
- число вызовов скорой медицинской помощи (СМП) и госпитализаций на 1000 населения;
- частота первичной инвалидизации, в том числе лиц трудоспособного возраста, на 10 тыс. населения;
- смертность на 100 тыс. населения.
Анализ стоимости болезни включал оценку прямых (визиты к врачу, вызовы СМП, госпитализация, амбулаторная лекарственная терапия) и непрямых затрат (временная нетрудоспособность, стойкая нетрудоспособность, потери производства из-за отсутствия сотрудника на рабочем месте, неуплата налогов).
Экономический ущерб от болезни оценивали как стоимость болезни, экстраполированную на изучаемую популяцию пациентов. Предотвращенный экономический ущерб рассчитывали как разницу между экономическим ущербом от болезни до внедрения технологий и экономическим ущербом в результате внедрения технологий.
Для проведения стартового исследования в Свердловской области был выбран г. Лесной, где смертность от БА в 1999 г. составила 15 случаев на 100 тыс. населения, что в 2,5 раза превысило средние показатели смертности от астмы в Свердловской области. Чтобы внедрить технологию GINA, в этом городе была инициирована специальная локальная программа помощи больным астмой, включавшая создание регистра больных БА и ведение пациентов в соответствии с рекомендациями GINA.
Обучение проходили не только пациенты, но и врачи, фармацевты, организаторы здравоохранения. Одновременно осуществлялось информирование населения об астме и аллергии. В рамках исследования было организовано необходимое лекарственное и материально-техническое обеспечение.
При проведении ступенчатой фармакотерапии и оказании неотложной помощи больным БА применяли преимущественно отечественные препараты в соотношении 4:1. Рекомендации GINA специалисты внедряли экспедиционным методом. Эффективность внедрения рекомендаций оценивали исходя из динамики медико-экономических показателей, стоимости астмы, предотвращенного экономического ущерба и экономической эффективности.
В течение двух лет функционирования программы по внедрению рекомендаций GINA в г. Лесной (центральная медико-санитарная часть № 91 ФМБА России) число вызовов СМП удалось снизить в 1,5 раза, число госпитализаций – в 1,2 раза. При этом отмечался пролонгированный эффект внедренной технологии, поскольку в 2004–2006 гг. число вызовов СМП сократилось в 3,2 раза, число госпитализаций – в 1,7 раза. Случаев первичной инвалидизации лиц трудоспособного возраста отмечалось в 2,5 раза меньше. Значительно снизился и показатель смертности – с 8,5 на 100 тыс. населения в 1998–1999 гг. до 0,7 на 100 тыс. населения в 2004–2006 гг.
Анализ распределения суммы прямых и непрямых расходов на одного больного в зависимости от степени тяжести БА показал, что внедрение рекомендаций GINA позволило сократить затраты на лечение легкой интермиттирующей астмы в 13 раз, легкой персистирующей – в 2,2 раза, среднетяжелой – в 1,5 раза, тяжелой – в 1,3 раза. Прямые затраты сократились в 2,3 раза, непрямые – в 1,8 раза. В целом затраты уменьшились в 2 раза: если до внедрения клинических рекомендаций стоимость одного случая БА составляла 9461 руб., то после внедрения рекомендаций она снизилась до 4670 руб.
Динамика затрат на амбулаторное лечение продемонстрировала незначительный прирост (20%), при этом затраты на стационарное лечение одного больного уменьшились в 7 раз. Сумма прямых и непрямых затрат до внедрения технологии составляла 3 млн 200 тыс. руб. на 353 пациентов с БА, через год после внедрения – 1 млн 970 тыс. руб. на 439 больных БА. Таким образом, предотвращенный экономический ущерб только за год превысил 1 млн 240 тыс. руб. Разделив эту сумму на сумму дополнительных затрат на внедрение программы (50 700 руб.), исследователи установили, что экономическая эффективность программы в 25 раз превысила затраты на ее внедрение.
Исследование фармакоэкономической эффективности внедрения клинических рекомендаций по диагностике и лечению БА было проведено в г. Новоуральске (центральная медико-санитарная часть № 31 ФМБА России). В этом городе при проведении ступенчатой фармакотерапии астмы обычно использовались импортные противоастматические средства, которые назначались пациентам более чем в 2 раза чаще отечественных. Эффективность внедрения рекомендаций оценивали по динамике медико-экономических показателей, прямых затрат, предотвращенному экономическому ущербу и уровню контроля над астмой.
В результате внедрения клинических рекомендаций GINA количество пациентов с контролируемой астмой возросло в 2,1 раза, с частично контролируемой – в 1,9 раза, количество пациентов с неконтролируемой БА уменьшилось в 2 раза. Число вызовов СМП снизилось в 2 раза, число госпитализаций – в 1,3 раза. Частота первичной инвалидизации сократилась в 2,5 раза, в частности лиц трудоспособного возраста – в 7 раз. Смертность уменьшилась в 3,6 раза.
До внедрения технологии в г. Новоуральске среди прямых затрат на ведение больных астмой преобладали затраты на госпитализацию (53%) и амбулаторную лекарственную терапию (34%). После внедрения клинических рекомендаций прямые затраты на амбулаторную лекарственную терапию одного больного астмой в год в связи с преобладанием импортных препаратов возросли в 1,7 раза, затраты на госпитализацию снизились в 3,7 раза. В целом предотвращенный экономический ущерб составил 905 тыс. руб. (-21%).
По словам профессора Е.К. Бельтюкова, внедрение клинических рекомендаций в Лесном способствовало более значимому снижению прямых затрат (в 2,3 раза), чем в Новоуральске (в 1,3 раза), на одного больного БА в год из-за преобладания в структуре назначаемых противоастматических средств отечественных, а не импортных препаратов.
Для проведения исследования по внедрению клинических рекомендаций по диагностике и лечению ХОБЛ (GOLD) был выбран г. Березовский, где смертность от ХОБЛ в среднем составляла 30 случаев на 100 тыс. населения. В данном исследовании (2008–2010 гг.) внедрением клинических рекомендаций у больных ХОБЛ (n = 336) занимались терапевты и пульмонологи. В структуре фармакотерапии ХОБЛ преобладали импортные препараты. Эффективность внедрения рекомендаций GOLD оценивали по числу обострений ХОБЛ, степени толерантности к физическим нагрузкам, динамике прямых затрат, предотвращенному экономическому ущербу и смертности.
Внедрение клинических рекомендаций GOLD позволило повысить толерантность пациентов к физической нагрузке на 21%, снизить количество обострений ХОБЛ в 1,4 раза, частоту госпитализаций – в 3,2 раза, смертность – до 20 на 100 тыс. населения, смертность от ХОБЛ трудоспособного населения свести к нулю.
Между тем динамика уменьшения прямых затрат была не такой очевидной, как в предыдущих исследованиях: прямые затраты на одного больного ХОБЛ в год сократились в 1,1 раза (на 10%). Предотвращенный экономический ущерб при экстраполировании на 336 больных ХОБЛ составил 391 тыс. 440 руб.
Доля затрат на амбулаторную лекарственную терапию в структуре прямых затрат на лечение больных ХОБЛ была выше, чем у больных БА, – 64–84%. Подобные результаты, по мнению профессора Е.К. Бельтюкова, заставляют искать новые возможности для уменьшения затрат на фармакотерапию ХОБЛ и БА. Решение проблемы – в использовании отечественных эффективных и качественных, экономически выгодных, воспроизведенных ингаляционных препаратов, которые сегодня выпускает российская компания «Натива». Производство отечественных лекарственных препаратов для лечения БА вписывается в государственную стратегию лекарственной безопасности страны и развития фармацевтической промышленности РФ, которые утверждены Президентом РФ.
Препарат Салтиказон-натив (салметерол + флутиказон), разработанный и выпускаемый компанией «Натива», эквивалентен иностранному препарату Серетид Мультидиск. Подтверждение тому – опубликованные результаты клинических многоцентровых исследований, проведенных под руководством профессора Н.И. Ильиной. Салтиказон-натив выпускается в комплекте с оригинальным ингалятором Инхалер CDM во всех необходимых дозировках и разрешен к применению у детей с четырех лет. Важно, что при сопоставимой эффективности и безопасности отечественного и импортного препаратов стоимость препаратов Салтиказон-натив, порошок для ингаляций, и Салтиказон-аэронатив, аэрозоль для ингаляций, на 20% ниже стоимости иностранного препарата Серетид Мультидиск и Серетид, аналогичных по формам выпуска и дозировкам.
Такие же положительные результаты были получены и в отношении препарата Формисонид-натив (формотерол + будесонид). Согласно результатам опубликованного клинического исследования (главный исследователь профессор С.В. Недогода), воспроизведенный лекарственный препарат Формисонид-натив сопоставим с оригинальным препаратом Симбикорт Турбухалер (формотерол + будесонид) по показателям эффективности и безопасности. При этом препарат Формисонид-натив более доступен для пациентов и государственных учреждений здравоохранения, поскольку его стоимость на 22–26% ниже стоимости импортного аналога.
Формотерол-натив (формотерол) успешно применяется для профилактики и лечения нарушений бронхиальной проходимости у больных БА и ХОБЛ. При эквивалентных клинических показателях стоимость препарата Формотерол-натив на 34% ниже таковой иностранного препарата Форадил.
Препарат Тиотропиум-натив (тиотропия бромид), как и иностранный препарат Спирива, уменьшает одышку и повышает работоспособность пациентов с ХОБЛ. Стоит отметить, что современные эластичные капсулы препарата Тиотропиум-натив из гипромелозы устойчивы к хранению при низких и высоких температурных режимах. Этим они отличаются от желатиновых капсул с красителями, которые более хрупкие и хранятся в строго определенных условиях. При этом стоимость препарата Тиотропиум-натив на 14% ниже стоимости импортного аналога.
Важно, что для всех препаратов компании «Натива» для ингаляционного применения используется один тип оригинального ингалятора – Инхалер CDM, что упрощает врачам процесс обучения пациентов и сокращает время приема.
Эквивалентными по эффективности и безопасности являются также комбинированные бронхолитики: Ипратерол-натив и Ипратерол-аэронатив (ипратропия бромид + фенотерол) в сравнении с иностранными аналогами Беродуал и Беродуал Н соответственно. При этом стоимость российского препарата на 13–25% ниже стоимости иностранных, что делает его более доступным для пациентов.
Таким образом, воспроизведенные препараты компании «Натива» с подтвержденными в клинических исследованиях эффективностью и безопасностью, эквивалентными таковым иностранных аналогов, более доступны по цене, что экономически выгодно для пациента, врача и организаторов здравоохранения. Все порошки для ингаляций снабжены простым надежным одинаковым ингалятором Инхалер CDM. Это удобно и для врача, и для пациента. Препараты компании «Натива» являются предпочтительным выбором в терапии БА и ХОБЛ.
Резюмируя сказанное, профессор Е.К. Бельтюков отметил, что внедрение в практику клинических рекомендаций по ведению больных БА и ХОБЛ с точки зрения фармакоэкономики позволяет:
- уменьшить прямые и непрямые затраты на ведение пациентов;
- предотвратить экономический ущерб от заболеваний;
- уделить должное внимание пациентам, работа с которыми дает ощутимый эффект при минимальных затратах;
- снизить затраты государства на дорогостоящие стационарные технологии за счет увеличения доли на амбулаторное лекарственное обеспечение.
Возможности импортозаместительной терапии при социально значимых заболеваниях органов дыхания
В продолжение темы импортозамещения в медицине и ее целесообразности Александр Андреевич ВИЗЕЛЬ, главный внештатный специалист-пульмонолог Республики Татарстан, заведующий кафедрой фтизиопульмонологии Казанского государственного медицинского университета, профессор, д.м.н., констатировал, что, например, за период 2012–2015 гг. в кардиологии и антибиотикотерапии доля отечественных лекарственных средств превышала или соответствовала таковой импортных аналогов в натуральном и денежном выражении. Между тем в пульмонологии к 2015 г. доля импортных препаратов постоянно увеличивалась, с максимальным расходованием на них финансовых средств как государственными органами здравоохранения, так и самими пациентами.
Социально-экономические потери от БА и ХОБЛ не снижаются и в совокупности превышают ежегодно 37 млрд руб. Практические врачи отмечают выраженную тенденцию к приобретению пациентами более доступных лекарственных препаратов-аналогов. Конечно, государство постепенно увеличивает норматив финансовых затрат: в 2017 г. сумма, выделяемая из бюджета на одного льготника в месяц, составила 807,2 руб. Но этого явно недостаточно для обеспечения необходимыми лекарственными средствами пациентов с ХОБЛ и БА.
Долгое время разработки ряда отечественных компаний не обеспечивали широкого выбора лекарственных средств для лечения бронхообструктивных заболеваний. Сегодня, благодаря появлению на рынке целого перечня ингаляционных лекарственных препаратов российской фармацевтической компании полного цикла «Натива», ситуация начала меняться к лучшему.
Пульмонологический портфель компании представлен коротко- и длительнодействующими бронхолитиками разных групп, ИГКС и их комбинациями. В перечне препаратов компании – аэрозоли для ингаляций (Салтиказон-аэронатив, Ипратерол-аэронатив, Беклометазон-аэронатив, Ипратропиум-аэронатив), порошки для ингаляций (Салтиказон-натив, Тиотропиум-натив, Формисонид-натив, Формотерол-натив) и растворы для применения через небулайзер (Ипратерол-натив, Ипратропиум-натив, Сальбутамол-натив, Будесонид-натив, Фенотерол-натив). Такое разнообразие форм выпуска чрезвычайно важно при выборе индивидуальной терапии для пациентов с БА и ХОБЛ.
Салтиказон-аэронатив (салметерол + флутиказон) в виде аэрозоля для ингаляций – единственный российский комбинированный препарат для базисной терапии БА и ХОБЛ, разрешенный к применению у детей с четырех лет. При его использовании бронходилатирующее действие отмечается в течение 1–3 минут и сохраняется в течение не менее 12 часов после ингаляции. Как уже отмечалось, его стоимость на 20% ниже стоимости Серетида при эквивалентных показателях клинической эффективности и переносимости пациентами.
Первый российский комбинированный бронхолитик Ипратерол-аэронатив (ипратропия бромид + фенотерол) также характеризуется сопоставимой с Беродуалом Н эффективностью и безопасностью при более доступной цене (стоимость меньше на 20%). На фоне применения препарата Ипратерол-аэронатив бронхоспазм купируется уже в течение первых 15 минут после ингаляции.
Салтиказон-натив (салметерол + флутиказон), Формотерол-натив (формотерол), Формисонид-натив (будесонид + формотерол) и Тиотропиум-натив выпускаются в виде капсул с порошком для ингаляций. Оригинальный однодозовый ингалятор Инхалер CDM, разработанный и запатентованный в 2007 г. английским и немецким инженерами, позволяет удобно дозировать и вдыхать препарат в очень малых дозах. Ингалятор позволяет пациентам надежно контролировать прием препарата: при вдохе слышится звук вибрирующей капсулы, пациент ощущает слабо-сладкий вкус во рту (за счет лактозы, применяемой в качестве носителя, в том числе во всех иностранных порошковых препаратах для ингаляционного введения). Кроме того, прозрачность капсулы помогает контролировать наличие или отсутствие в ней препарата после произведенного пациентом вдоха. Доказанные в клинических исследованиях сопоставимые эффективность и безопасность всех воспроизведенных порошковых препаратов, а также их более низкая стоимость свидетельствуют о том, что импортным аналогам действительно найдена достойная замена.
Аналогичные качества присущи воспроизведенным растворам для небулайзеров. Уже накоплен достаточный положительный клинический опыт применения препарата Ипратерол-натив у пациентов с бронхообструктивным синдромом, при обострении ХОБЛ и БА. Кроме того, доказана идентичность аэродинамических свойств и показателей респирабельной фракции1 препаратов Ипратерол-натив и Беродуал.
Профессор А.А. Визель поделился собственным исследовательским опытом применения препарата Ипратерол-натив у пациентов в условиях стационара. На момент проведения исследования ФЖЕЛ составляла 66,5 ± 4,9% от должной, ПСВ – 47,2 ± 5,3% от должной. Через 30 минут после ингаляции 20 капель препарата Ипратерол-натив прирост ФЖЕЛ составил 0,304 ± 0,093 л, ОФВ1 – 0,368 ± 0,059 л, ПСВ – 0,860 ± 0,146 л/с, средняя объемная скорость выдоха на уровне 25–75% – 0,500 ± 0,168 л/с9.
В многоцентровом исследовании участвовали более 200 пациентов (80 – с ХОБЛ, 82 – с БА, 39 – с сочетанием БА и ХОБЛ) из клиник Казани, Москвы и Санкт-Петербурга. У пациентов, применявших препараты Ипратерол-натив, Сальбутамол-натив и Беродуал, оценивали показатели функции легких. Согласно предварительным данным, максимальную эффективность при ХОБЛ достоверно (р < 0,001) продемонстрировал Ипратерол-натив, при БА – Сальбутамол-натив. При БА и ХОБЛ Беродуал несколько превосходил остальные препараты.
Профессор А.А. Визель подчеркнул, что все пульмонологические препараты компании «Натива» отличаются оптимальным соотношением «цена – качество» и включены в стандарты оказания медицинской помощи, федеральные клинические рекомендации и Перечень жизненно необходимых и важнейших лекарственных препаратов.
Заключение
Чтобы удовлетворить потребность всех пациентов с социально значимыми бронхообструктивными заболеваниями легких в лекарственных препаратах, соответствующих требованиям современных клинических рекомендаций, необходимо наладить их производство в России. В настоящее время разработки российской компании «Натива» позволили обеспечить пациентов с БА и ХОБЛ качественными и недорогими воспроизведенными отечественными препаратами, иностранные аналоги которых с одинаковыми действующими веществами являются востребованными. Пульмонологический портфель компании представлен коротко- и длительнодействующими бронхолитиками разных групп, ИГКС и их комбинациями.
Доказанные качественные и количественные характеристики, а также данные клинических исследований пульмонологических воспроизведенных препаратов компании «Натива», сопоставимые с таковыми оригинальных препаратов, с учетом существенно более низкой стоимости и наличия оригинального простого надежного дозирующего устройства (порошки для ингаляций – ингалятор Инхалер CDM), позволяющего достоверно контролировать прием дозы препарата, свидетельствуют о том, что в России появилась достойная замена дорогостоящим импортным лекарственным средствам для лечения пациентов с социально значимыми обструктивными заболеваниями легких.
