«Квартет здоровья» против «смертельного квартета». Часть первая: метаболическая невропатия – легко диагностировать, трудно лечить
- Аннотация
- Статья
- Ссылки


С конца XIX – начала XX века заболеваниям, связанным с эндокринно-метаболическими нарушениями в организме, в медицинском сообществе стало уделяться все больше внимания. Так, A. Bouchardat в 1875 г. описал взаимосвязь между ожирением и сахарным диабетом, E. Neubauer в 1910 г. обнаружил взаимозависимость артериальной гипертензии и гипергликемии. В 1922 г. Г.Ф. Ланг обратил внимание на коморбидность таких патологий, как гипертоническая болезнь, сахарный диабет, ишемическая болезнь сердца, ожирение, нарушения липидного и пуринового обмена [1]. Впервые предположение о роли инсулинорезистентности в патогенезе сахарного диабета и артериальной гипертензии было высказано в 1988 г., когда G. Reaven предложил термин «синдром X» или «синдром инсулинорезистентности», включавший в себя:
- инсулинорезистентность;
- нарушение толерантности к глюкозе и гиперинсулинемию;
- повышение холестерина липопротеидов низкой плотности и триглицеридов, снижение липопротеидов высокой плотности;
- артериальную гипертензию.
Стоит отметить, что G. Reaven выделил среди симптомов, составляющих метаболический синдром, именно инсулинорезистентность как ведущее звено в патогенезе сахарного диабета, артериальной гипертензии и, как выяснилось со временем, многих других патологических состояний. В 1989 г. N. Kaplan ввел, на наш взгляд, более точно отражающий суть проблемы термин «смертельный квартет», или «метаболический синдром», объединив:
- андроидное ожирение;
- нарушение толерантности к глюкозе;
- гиперинсулинемию;
- артериальную гипертензию.
Основываясь на понимании патогенетических механизмов клеточного старения и развития основных болезней цивилизации: ожирения, атеросклероза, артериальной гипертонии и сахарного диабета 2 типа, мы сформулировали концепцию «квартета здоровья» – комплексной метаболической терапии. Понятие «метаболическая терапия» подразумевает лечение, направленное в первую очередь на поддержание или восстановление клетки как наименьшей единицы живого, ее физиологических функций, структуры тканей и организма в целом. Термин «метаболическая» подчеркивает характер терапии, направленной на восстановление гормонально-биохимического фона, соответствующего 30–35-летнему возрасту пациента.
«Квартет здоровья» включает в себя гормональную терапию (прежде всего заместительную гормональную терапию половыми гормонами при гипогонадизме), поддержание физиологического уровня витамина D и терапию незаменимыми жирными кислотами: омега-3 полиненасыщенными жирными кислотами (ПНЖК) и тиоктовой (альфа-липоевой) кислотой. Каждый компонент «квартета здоровья» обоснован и одинаково важен. В настоящее время в современной литературе активно обсуждается заместительная гормональная терапия, терапия андрогенами, препаратами омега-3 ПНЖК, растет интерес к коррекции дефицита (гиповитаминоза) витамина D. Между тем антиоксидантная терапия препаратами тиоктовой кислоты или вообще не рассматривается, или обсуждается только в связи с назначением при алкогольной или диабетической невропатиях. Именно поэтому начать рассмотрение «квартета здоровья» мы решили с тиоктовой кислоты как одной из составляющих метаболической терапии.
Тиоктовая кислота как составляющая «квартета здоровья»
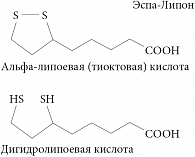
Тиоктовая кислота состоит из 8 атомов углерода и двух атомов серы (рис. 1) [2]. Тиоктовая кислота была выделена в клетках аэробов и изначально носила название «витамин N», что подчеркивало ее незаменимость и важность для функции нервной ткани (витамины – незаменимые вещества, поступающие с пищей, N – «невро»). Однако витамином она не является по химической структуре, к тому же в небольшом количестве образуется в организме (показана способность E. coli к синтезу этой кислоты), что не позволяет отнести ее к «абсолютно» незаменимым жирным кислотам. Тем не менее стоит отметить крайне низкое ее содержание в продуктах питания (табл. 1) [3]. Следует подчеркнуть, что тиоктовая кислота является:
- Коферментом как минимум двух дегидрогеназных комплексов цикла трикарбоновых кислот (цикла Кребса).
- Необходимым компонентом в рецикле основных антиоксидантов, таких как витамин Е, глутатион, убихинон (коэнзим Q10).
- Веществом, непосредственно обладающим собственной антиоксидантной активностью.
- Веществом, обладающим липотропной активностью: способствует образованию коэнзима А, облегчает перенос ацетата и жирных кислот из цитозоля в митохондриальный матрикс, ускоряя окисление жирных кислот и способствуя снижению липидов в плазме крови.
Ключевое значение дефицита именно тиоктовой кислоты как кофермента доказано экспериментально в проведенных исследованиях и теоретически обосновано [2–4]. Дефицит возникает из-за того, что актуальный для других коферментов (витамины группы B, пантотеновая кислота) алиментарный способ поступления необходимых доз тиоктовой кислоты невозможен: содержание этой кислоты в продуктах питания крайне мало (табл. 1). Так, больше всего тиоктовой кислоты содержится в гепатоцитах млекопитающих – концентрация в говяжьей печени составляет 10 мг/30 т. В то же время в условиях окислительного стресса отмечается повышенный расход тиоктовой кислоты, и ее суточная потребность для взрослого человека достигает 200–300 мг/сут.
Тиоктовая кислота – самый эффективный из всех известных антиоксидантов, но ее терапевтическая ценность недооценена, а показания к назначению необоснованно сужены. «Классическими» показаниями к назначению препаратов тиоктовой кислоты считаются диабетическая полиневропатия и, отчасти, хроническая неврологическая боль различной локализации и патогенеза, широко освещенные в опубликованных данных нескольких крупных и фундаментальных рандомизированных клинических исследований [5, 6]. Между тем, исходя из представлений о биохимических свойствах тиоктовой кислоты (табл. 2), истории ее изучения и доказанной эффективности в лечении, в том числе невропатии любой этиологии, показания к ее применению должны быть значительно расширены. Кроме того, тиоктовая кислота является не только универсальным антиоксидантом, но и повышает эффективность любой другой терапии.
Роль окислительного стресса в старении организма
Многие тысячелетия человечество задается одними и теми же вопросами. Почему человек стареет? Можно ли замедлить этот процесс? Почему одни люди уже в 40 лет больны и некрасивы, а другие здоровы и привлекательны даже в 70? На сегодняшний день предложено множество теорий старения, выявлены различные пагубные процессы, со временем развивающиеся в организме, и разработаны методы их торможения. Одной из основных гипотез старения является теория свободных радикалов [7].
Свободные радикалы – нестабильные атомы и соединения, действующие как агрессивные окислители и в результате повреждающие жизненно важные структуры организма, – образуются при воздействии неблагоприятных факторов окружающей среды (экология, курение, токсины). Кроме того, выработка свободных радикалов растет при инсулинорезистентности, повышении уровня сахара в крови, ожирении, возрастном снижении половых гормонов как у мужчин, так и у женщин. Окислительный стресс – несостоятельность антиоксидантной системы организма – неизбежно возникает при нарастающем поступлении и/или нарастающем образовании in vivo свободных радикалов и преобладании окислительных реакций над восстановительными.
Образование свободных радикалов и свободнорадикальные реакции – физиологический процесс, неизбежно приобретающий патофизиологические черты с течением жизни человека. Физиологичность заключается в том, что некоторые свободные радикалы (активные формы кислорода, перекиси) закономерно образуются при окислении жирных кислот как энергетического субстрата и в норме нейтрализуются антиоксидантной системой; при перекисном окислении липидов – необходимом процессе в обновлении фосфолипидных клеточных мембран; при индуцированном локальном окислительном стрессе (при контакте иммунокомпетентных клеток с антигеном с целью его разрушения). Физиологичность прекращается при лавинообразном нарастании окислительных процессов. Рассмотрим лишь несколько классических примеров «патофизиологического перехода»:
- Инсулинорезистентность. Невозможность использования глюкозы как субстрата для выработки аденозинтрифосфата (АТФ) в инсулинзависимых тканях (печень, мышцы), переход исключительно на окисление жирных кислот (увеличение образования свободных радикалов), неминуемое ожирение, нарастание инсулинорезистентности, концентрации свободных жирных кислот (тоже имеющих свободнорадикальную активность) – истощение антиоксидантной системы.
- Гипергликемия, так называемая «глюкозотоксичность». Усиленное гликирование не что иное, как окисление субстратов глюкозой (выступает как свободный радикал плюс инактивация ферментов).
- Физиологическое старение. Неизбежная кумуляция (накопление) свободных радикалов и эффект накопления мутаций в течение жизни наряду с «дисфункцией транскрипции генов» на фоне гипогонадизма (андрогенный дефицит у мужчин и женщин, постменопауза) – прогрессивное нарастание окислительного стресса.
Таким образом, окислительный стресс следует рассматривать как неизбежный для каждого человека процесс – основную причину старения и возраст-ассоциированных заболеваний, в том числе доброкачественных и злокачественных опухолей.
Окислительный стресс как причина невропатии
Невропатия – это дистрофически-дегенеративные изменения нервной ткани, развивающиеся вследствие различных процессов, в том числе старения, приводящие к нарушению функции центральной, периферической чувствительной, двигательной и вегетативной нервной системы и гармоничной работы всех органов и систем. Это связано с тем, что невропатия затрагивает всю нервную ткань, включая репепторы – сложные образования нервной ткани, обеспечивающие взаимодействие всех органов и систем [4]. Несмотря на причину, патогенез невропатии всегда обусловлен двумя процессами: нарушением энергетического обмена и окислительным стрессом [2]. Можно выделить несколько характерных особенностей нервной ткани. Во-первых, обновление нервных волокон невозможно, несмотря на то что возможность деления у нервных клеток существует. В противном случае неизбежны прерывания в проведении импульса во время апоптоза и паузы, до возникновения новой дифференцированной клетки. Во-вторых, нервная ткань инсулиннезависима. Глюкоза (единственный субстрат для синтеза АТФ в нервной ткани) проникает в клетки по градиенту концентраций без участия инсулина и включается в цикл Кребса. В ферментных системах последнего выделяют два «слабых звена»: пируватдегидрогеназный и кетоглутаратдегидрогеназный комплексы, нарушение работы которых может привести к остановке работы цикла Кребса. Оба они очень схожи между собой и состоят из трех ферментов, пяти коферментов (коэнзимы) и одного кофактора (Mg+). Коферментами катализируемых реакций являются витамины В1, В6, пантотеновая кислота, никотинамид и тиоктовая кислота. Дефицит коферментов может привести к указанной остановке работы цикла трикарбоновых кислот, которая губительна для нервной клетки: прекращение выработки АТФ (энергетический голод), накопление конечных продуктов окисления глюкозы, активация гликирования внутриклеточных ферментов (глюкоза постоянно поступает в клетку – простая диффузия, тем более катастрофическая при гипергликемии), накопление осмотически активных компонентов – глюкоза в отсутствие переработки трансформируется в сорбитол. Начинается гидратация клеток, которая вкупе с энергетическим голодом и окислительным стрессом приводит к гибели нервной клетки.
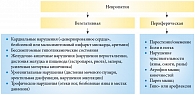
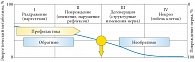
Учитывая «тропность» окислительного стресса к нервной ткани, роль которой переоценить невозможно, в задачи врача любой специальности должна входить не только тщательная дигностика проявлений невропатии (рис. 2), но и активное лечение невропатии препаратами тиоктовой кислоты. В связи с тем что профилактика невропатии наиболее эффективна до развития симптомов, терапия препаратами тиоктовой кислоты, как одним из компонентов «квартета здоровья», должна начинаться как можно раньше (рис. 3). Особое внимание следует уделять выявлению и профилактике вегетативной невропатии, которая проявляется клинически значительно раньше периферической и которую, исходя из вышесказанного, можно рассматривать как метаболическую невропатию. Вегетативная невропатия развивается неизбежно (так как она всегда имеет место при физиологическом старении) и парадоксально игнорируется во врачебной практике.
Заключение
Противостояние «смертельному квартету» необходимо начинать до появления первых клинических проявлений – в этом заключается идеология профилактической медицины. Особенно это актуально для профилактики невропатии, которая наиболее эффективна до развития симптомов. Известно, что невропатия развивается в результате двух процессов: нарушения энергетического обмена и окислительного стресса. В этой связи следует не только тщательно диагностировать проявления невропатии, но и активно лечить невропатию препаратами тиоктовой кислоты – самым эффективным из всех известных антиоксидантов.
