количество статей
6372
Загрузка...
Пожалуйста, авторизуйтесь:
Исследования
Влияние глибенкламида, таурина и их совместного применения на основные показатели углеводного обмена
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Эндокринология" №4 (35)
- Аннотация
- Статья
- Ссылки
- English
Терапия сахарного диабета 2 типа является одной из важнейших проблем современной медицины. Экспериментальные и клинические данные, свидетельствующие о важной роли аминокислоты таурина в физиологии и патофизиологии углеводного обмена, создали предпосылки для более широкого его внедрения в практику лечения. Однако в литературе нет достоверных сведений о характере влияния этого вещества и созданного на его основе отечественного препарата Дибикор® на показатели метаболизма глюкозы при монотерапии, а также о взаимодействии его с пероральными сахароснижающими средствами.
В настоящем исследовании сравнивали эффекты таурина и глибенкламида при однократном приеме и курсовой 2- и 4-недельной терапии. Показано, что комбинированная терапия глибенкламидом и таурином в течение 1 месяца более эффективно снижает базальную и постпрандиальную гликемию и глюкозурию, чем монотерапия каждым из этих препаратов.
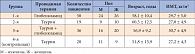
Таблица. Характеристика групп исследования
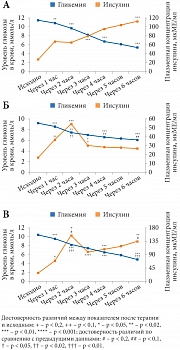
Рис. 1. Влияние однократного приема глибенкламида (А), таурина (Б) и сочетания глибенкламида с таурином (В) на уровень глюкозы в капиллярной крови и плазменную концентрацию инсулина у лиц с СД 2 типа
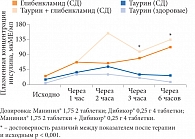
Рис. 2. Влияние глибенкламида и таурина на уровень инсулина крови в ходе острой фармакологической пробы

Рис. 3. Влияние однократного приема таурина в дозе 1,0 г (4 таблетки Дибикора 0,25 г) на уровень глюкозы в капиллярной крови и плазменную концентрацию инсулина у здоровых лиц
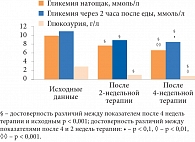
Рис. 4. Влияние монотерапии глибенкламидом на показатели углеводного обмена у лиц с СД 2 типа
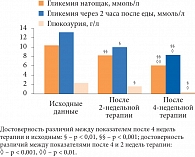
Рис. 5. Влияние монотерапии таурином на показатели углеводного обмена у лиц с СД 2 типа
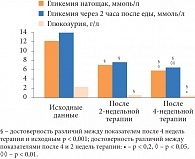
Рис. 6. Влияние комбинированной терапии глибенкламидом и таурином на показатели углеводного обмена у лиц с СД 2 типа

Рис. 7. Сравнительное действие 4-недельной терапии у пациентов с СД (в % к исходным значениям до лечения)
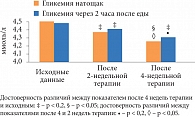
Рис. 8. Влияние монотерапии таурином на показатели углеводного обмена у здоровых лиц
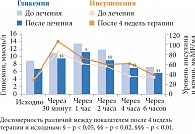
Рис. 9. Влияние монотерапии таурином на уровень глюкозы в капиллярной крови и плазменную концентрацию инсулина у лиц с СД 2 типа в ходе ПТТГ до и после лечения
Введение
Сахарный диабет 2 типа представляет собой серьезную медико-социальную проблему, что обусловлено его высокой распространенностью, тенденцией к росту числа больных, хроническим течением, определяющим кумулятивный характер заболевания, и высокой инвалидизацией [1]. Большая социальная значимость СД 2 типа состоит в том, что его течение осложняется сосудистыми заболеваниями, в числе которых микроангиопатии (ретино- и нефропатия) и макроангиопатии (инфаркт миокарда, инсульт, гангрена нижних конечностей). Продолжительность жизни у больных СД на 7–10 лет меньше, чем у лиц без диабета [2, 3]. Основные причины смерти больных СД 2 типа – ишемическая болезнь сердца (50%), инсульт (15%), хроническая почечная недостаточность (8%) [2, 4].
Терапия СД является одной из важнейших проблем в клинической фармакологии. Проблема комплексного лечения СД актуальна, так как практически на всех стадиях болезни для компенсации углеводного обмена трудно обойтись монотерапией. При этом в последние годы существенно повысились требования к критериям компенсации СД 2 типа [5], а активную сахароснижающую терапию рекомендуется начинать на ранних стадиях (всем больным, у которых гликемия превышает норму) [6].
В то же время применяемые для лечения СД 2 типа пероральные препараты (бигуаниды, глитазоны) имеют большое количество противопоказаний и сами могут вызывать серьезные побочные эффекты. С середины 1970-х гг. обсуждается вопрос о повышении риска смерти от сердечно-сосудистых заболеваний вследствие приема производных сульфонилмочевины (ПСМ), но данные до сих пор достаточно противоречивы.
Таким образом, вырисовываются две основные проблемы:
- увеличение количества поздних осложнений СД 2 типа, необходимость их ранней профилактики, а при возникновении – своевременного лечения;
- сведение к минимуму побочных эффектов проводимой терапии.
Исходя из вышесказанного, для оценки терапевтической эффективности пероральных гипогликемизирующих веществ используют три основных критерия: гипо- или нормогликемизирующая активность, предупреждение дегенеративных ангиопатических осложнений, безопасность применения [7]. Особую актуальность приобретает создание новых пероральных гипогликемических средств, обладающих вышеперечисленными признаками [8, 9].
Накопленные экспериментальные и клинические данные, свидетельствующие о важной роли аминокислоты таурина в физиологии и патофизиологии углеводного обмена, создали предпосылки для более широкого внедрения таурина в практику лечения СД 2 типа [10, 11]. Однако в литературе нет достоверных сведений о характере влияния этого вещества и созданного на его основе отечественного препарата Дибикор® при монотерапии на показатели метаболизма глюкозы и жирового обмена, реологические свойства крови у больных СД, а также о взаимодействии его с другими пероральными сахароснижающими средствами.
Все вышесказанное послужило предпосылкой к проведению настоящего исследования.
Работа выполнена на кафедре клинической фармакологии и интенсивной терапии Волгоградского государственного медицинского университета в дизайне открытого простого рандомизированного исследования в параллельных группах.
Исследование являлось клинико-инструментальным и проводилось на базе терапевтического отделения областной клинической больницы ст. Волгоград-1 ФГУП «Приволжская железная дорога МПС России» и эндокринологического отделения (областной диабетологический центр) Волгоградской областной клинической больницы № 3.
Цель исследования – повысить эффективность лечения пациентов, страдающих СД 2 типа, с помощью препарата таурина, предварительно изучив его фармакодинамику.
Материалы и методы
Для данной работы были обследованы и в дальнейшем пролечены 125 испытуемых, в том числе 20 практически здоровых лиц без нарушений углеводного обмена и 105 больных СД 2 типа, у 64 из которых СД 2 типа выявлен впервые. Исследованием было охвачено 49 мужчин и 56 женщин с СД 2 типа в возрасте от 37 до 76 лет включительно (в среднем 58,2 ± 10,3 года), средний индекс массы тела (ИМТ) составил 29,8 ± 4,9 кг/м2. Диагноз был установлен на основании клинико-анамнестических и лабораторных данных, согласно классификации и диагностическим критериям СД и других нарушений углеводного обмена, опубликованным ВОЗ в 1999 г. [12]. Исследуемые и контрольная группы находились на амбулаторном и стационарном лечении.
Все пациенты в течение как минимум двух месяцев, предшествовавших исследованию, не получали пероральных сахароснижающих препаратов, находясь на диетотерапии.
Из исследования были исключены пациенты, находившиеся в состоянии кетоацидоза; применявшие регулярно нестероидные противовоспалительные средства (кроме мазей); нуждающиеся в назначении инсулина по клиническим показаниям; имевшие повышенную чувствительность к какой-либо из применяемых нами групп препаратов, а также следующие сопутствующие заболевания и нарушения:
- сердечную недостаточность (II–IV функциональный класс по классификации NYHA (New-York Heart Association – Нью-Йоркская ассоциация кардиологов)), тяжелую или злокачественную артериальную гипертонию (артериальное давление > 180/114 мм рт. ст.);
- хроническую почечную недостаточность (уровень креатинина сыворотки > 130 мкмоль/л);
- онкологические заболевания;
- ожирение тяжелой степени (ИМТ > 45 кг/м2);
- острое инфекционное заболевание или обострение хронического;
- психические заболевания (или недееспособность);
- зависимость от алкоголя или наркотиков;
- иные клинически значимые заболевания внутренних органов в стадии обострения, которые могли значимо повлиять на оценку исследуемых параметров.
Обязательным условием включения больных в исследование являлось добровольное согласие на его проведение.
Из исследования исключались пациенты при гликемии натощак > 16,5 ммоль/л или выше исходного уровня; возникновении побочных эффектов, требующих отмены препарата.
Все пациенты были разделены на 3 группы в зависимости от проводимого им лечения. Больные 1-й группы получали традиционную монотерапию СД 2 типа пероральным сахароснижающим ПСМ – микронизированной формой глибенкламида (Манинил® 1,75, “Berlin-Chemie AG/Menarini Group” (Германия)); 2-й – таурин (Дибикор®, «ПИК-ФАРМА» (Россия)) в монотерапии, а 3-й – комплексную терапию (Дибикор® в сочетании с Манинилом 1,75). Четвертую (контрольную) группу составили практически здоровые лица, получавшие Дибикор®. Характеристика групп исследования дана в таблице.
На этапе курсовой терапии (4 недели) дозировку таурина определяли на основании результатов, полученных при исследовании препарата М.Ю. Фроловым [13], И.М. Кахновским и соавт. [14]. Начальная доза составила 1,0 г/сут. В случае недостижения целевых значений гликемии в течение 2 недель суточную дозу удваивали.
Дозировку глибенкламида определяли исходя из общепринятых рекомендаций по лечению СД 2 типа [6]. Начальная доза составляла 3,5 мг/сут. При недостижении целевых значений гликемии в течение 2 недель суточную дозу удваивали, а при достижении – уменьшали вдвое.
При комбинированной терапии глибенкламидом и таурином начальная суточная доза глибенкламида составила 3,5 мг, а таурина – 1,0 г. При недостижении целевых значений гликемии в течение 2 недель суточную дозу глибенкламида удваивали, а при достижении – уменьшали вдвое. Суточная доза таурина оставалась постоянной на протяжении всего курса терапии.
В группе практически здоровых лиц суточная доза таурина оставалась постоянной на протяжении всего курса терапии и составляла 1,0 г. Основной задачей данного этапа нашей работы было оценить эффективность проводимой терапии в отношении нормализации углеводного обмена и доказать целесообразность включения таурина в схемы лечения больных СД 2 типа.
Статистическая обработка полученных результатов проводилась на персональном компьютере IBM PC/AT 486 с использованием пакетов программ BioStat и Excel, для каждого признака вычислялись среднее и среднее квадратическое отклонение. Достоверность различий между группами определялась с использованием критерия Вилкоксона – Уитни – Манна или Т-критерия Стьюдента. Корреляционный анализ проводился с помощью корреляционных матриц в статистическом пакете Statistica 6.0.
Различия между исследуемыми группами считались достоверными при р < 0,05, в то время как при 0,1 ≤ р < 0,2 изменения характеризовались как тенденция, а при 0,05 ≤ р < 0,1 – как выраженная тенденция.
Пероральный тест на толерантность к глюкозе
В течение 3 суток перед пробой обследуемые получали по 150–200 г/сут углеводов. Пробу проводили утром натощак. Последний прием пищи допускался не позже, чем за 10 часов до начала пробы, но общая продолжительность голодания не должна была превышать 16 часов. Пациентам давали глюкозу перорально в виде раствора, доза для взрослых: 75 г на 250–300 мл воды. Концентрацию глюкозы в крови измеряли перед приемом глюкозы и спустя 2 часа после него.
У обследованных иногда отмечались тошнота, рвота, головокружение, сердцебиение. Считается, что одномоментный прием большого количества глюкозы вызывает перегрузку бета-клеток и может провоцировать развитие СД 2 типа у лиц из группы риска. Данные, подтверждающие это мнение, в литературе отсутствуют. Однако многие эндокринологи с осторожностью назначают пероральный тест на толерантность к глюкозе (ПТТГ) детям и подросткам и стараются, чтобы интервал между повторными пробами был не менее месяца.
Учитывая, что у больных СД 2 типа уровень глюкозы, как правило, не восстанавливается до исходного спустя 2 часа после нагрузки глюкозой при проведении ПТТГ, мы определяли уровень гликемии также через 4 и 6 часов. Параллельно определяли уровень инсулина сыворотки крови натощак и через 1, 2, 3 и 6 часов после нагрузки глюкозой.
Острый фармакологический тест
При проведении острого фармакологического теста оценивали изменение уровня гликемии и инсулина сыворотки крови перед началом теста, а также на протяжении 6 часов после приема препарата. За основу острого фармакологического теста взята методика нагрузки сульфаниламидными препаратами, принятыми внутрь [15]. Проба проводится с целью установить возможность успешного применения сульфаниламидных препаратов для лечения СД 2 типа.
Больной СД 2 типа принимал натощак суточную дозу любого ПСМ. До приема и в течение 5 часов после этого каждые 1/2–1 час исследовали уровень сахара в крови. Если гликемия понижалась на 30% по отношению к исходному уровню, то чувствительность к ПСМ трактовали как хорошую. При инсулинорезистентных формах гликемия в конце пробы превышала 6,6 ммоль/л. Считается, что терапевтический эффект можно получить в тех случаях, когда во время исследования сахар в крови больных снижается до уровня менее 6,6 ммоль/л.
Уровень глюкозы в крови определялся в лабораторных условиях унифицированным глюкозооксидазным методом с использованием анализатора «Экзан-Г». Уровень инсулина в сыворотке крови определяли иммунологическим методом с помощью набора Enzymun-Test® Insulin (“Boehringer Mannheim”, Германия).
Специфичность метода: возможны перекрестные реакции с человеческим проинсулином (40%), С-пептидом (0%), бычьим инсулином (35%), свиным инсулином (85%). Нормальным является уровень инсулина натощак в диапазоне от 3 до 17 мкМЕ/мл.
Тощаковый и постпрандиальный уровень глюкозы крови, а также выраженность глюкозурии определяли исходно и контролировали через 2 и 4 недели терапии.
Результаты исследования и обсуждение
Влияние глибенкламида, таурина и их совместного применения на основные показатели углеводного обмена при однократном пероральном приеме
После однократного приема глибенкламида у больных СД 2 типа (n = 9) уровень сахара крови достоверно снижался: через 1 час – на 4,9 ± 4,4% (р = 0,01), через 2 часа – на 14,9 ± 6,0% (р < 0,01), через 4 часа – на 39,4 ± 7,4% (р < 0,01) и через 6 часов – на 52 ± 7,4% от исходного (р < 0,01) (рис. 1, A). После приема глибенкламида у пациентов с СД 2 типа (n = 4) наблюдался рост плазменной концентрации инсулина от исходной 28,1 ± 8,6 мкМЕ/мл до 67,0 ± 33,4 мкМЕ/мл через 1 час, 64,8 ± 41,5 мкМЕ/мл через 2 часа (различия недостоверны), 79,3 ± 8,5 мкМЕ/мл через 3 часа (р < 0,01) с достижением максимальных значений (112,33 ± 24,66 мкМЕ/мл) через 6 часов, что достоверно превышало как исходный уровень инсулина, так и этот показатель через 3 часа после приема препарата (р < 0,05) (рис. 1, А). Таким образом, прием глибенкламида сопровождается длительной гиперинсулинемией, что в клинических условиях может приводить к явным или скрытым гипогликемическим состояниям.
После однократного приема таурина у больных СД 2 типа (n = 12) снижение уровня глюкозы крови от исходного соответственно составило через 1 час 8,48 ± 12,62%, через 2 часа – 21,3 ± 13,2%, через 4 часа – 29,6 ± 9,45%, через 6 часов – 33,9 ± 7,3% (во всех случаях р < 0,005) (рис. 1, Б). Однако различие в снижении уровня глюкозы крови между 4-м и 6-м часом после приема препарата не было статистически достоверно (р = 0,075). Прием таурина пациентами с СД 2 типа (n = 10) стимулировал секрецию инсулина умеренно, уже через 1 час содержание инсулина в крови было достоверно выше исходного 16,6 ± 13,5 мкМЕ/мл и составляло 36,6 ± 21,8 мкМЕ/мл (р < 0,05), максимальный уровень (54,19 ± 28,36 мкМЕ/мл) достигался через 2 часа (р < 0,01), а затем постепенно снижался. К 3-му часу уровень инсулина составил 30,2 ± 15,9 мкМЕ/мл, что было достоверно ниже аналогичного показателя через 2 часа после приема препарата (р < 0,05), а к 6-му часу достигал 27,08 ± 16,99 мкМЕ/мл (рис. 1, Б).
Однократный прием одновременно глибенкламида и таурина у части больных СД 2 типа (n = 10) сопровождался снижением уровня гликемии от исходного на 7,85 ± 7,7, 21,6 ± 10,5, 38,1 ± 6,8 и 51,7 ± 8,6% соответственно (во всех случаях р < 0,01) через те же временные интервалы (рис. 1, В). У некоторых пациентов (n = 3) действие глибенкламида и таурина на секрецию инсулина суммировалось: уже через 1 час после их приема уровень инсулина был выше исходного (27,75 ± 12,7 мкМЕ/мл) и составлял 68,3 ± 30,7 мкМЕ/мл (р = 0,1), максимальный уровень 153,74 ± 43,91 мкМЕ/мл достигался через 2 часа (р = 0,1), затем несколько снижался до 98,83 ± 15,90 мкМЕ/мл (р < 0,001), после чего вновь увеличивался к 6-му часу до 134,76 ± 9,15 мкМЕ/мл (р < 0,02) (рис. 1, В).
Проведенный дисперсионный анализ показал, что достоверные различия между группами наблюдались к 4-му и 6-му часу. Более выраженное снижение гликемии к этому времени отмечалось в группе пациентов, получающих глибенкламид или глибенкламид в сочетании с таурином, хотя сначала (через 1 час) тенденция к снижению гликемии была более выражена в группах больных, получивших таурин и таурин в сочетании с глибенкламидом.
Полученные результаты можно объяснить, сравнив влияние препаратов на уровень инсулина в крови после их перорального применения (рис. 2).
По данным дисперсионного анализа, достоверные различия между группами наблюдались уже через 2 часа после приема препаратов (р < 0,005), наибольшее стимулирующее действие на секрецию инсулина оказывал совместный прием глибенкламида и таурина, наименьшее – одного таурина; через 3 и 6 часов различия были еще больше выражены (р < 0,001). Ни в одном случае у больных СД 2 типа эпизодов гипогликемии не зафиксировано.
Прием таурина лицами без СД (n = 8) сопровождался снижением уровня гликемии через 1, 2, 4 и 6 часов на 0,16% (р > 0,2), 4,8% (р < 0,05), 9,47% (р < 0,02), 14,98% (р < 0,02) соответственно (рис. 3).
Сахароснижающий эффект и в этом случае может быть объяснен стимулирующим влиянием таурина на секрецию инсулина. Уровень инсулина натощак у здоровых лиц (n = 3) составлял 19,4 ± 2,4 мкМЕ/мл, после приема таурина повышался через 1 час до 30,9 ± 26,3 мкМЕ/мл, через 2 часа – до 31,9 ± 23,2 мкМЕ/мл, после чего несколько снижался к 3-му часу до 21,2 ± 14,2 мкМЕ/мл и 7,9 ± 3,7 мкМЕ/мл к 6-му часу (во всех случаях p = 0,1) (рис. 3). Эпизодов гипогликемии не зафиксировано.
При однократном приеме здоровыми добровольцами (n = 5) двух таблеток глибенкламида 1,75 мг снижение уровня сахара крови отмечалось через 1 час – на 18,9%, через 2 часа – на 39,7% (максимальное), что в двух случаях сопровождалось субъективными и клиническими признаками легкой гипогликемии. К 4-му и 6-му часу уровень сахара крови был ниже исходного на 26,2 и 25,3% соответственно (во всех случаях p < 0,001).
Влияние глибенкламида, таурина и их совместного применения на основные показатели углеводного обмена при курсовой терапии
В 1-й группе больных, получавших глибенкламид, средние показатели гликемии натощак снизились по сравнению с исходными на 27,2% (р < 0,0001) через 2 недели лечения. При продолжении приема препарата в последующие 2 недели наблюдалось дальнейшее снижение данного показателя на 13,4% (р < 0,001), или на 36,9% (р < 0,0001) от исходного. Уровень постпрандиальной гликемии снизился через 2 недели на 25,0% (р < 0,0001) от исходного. Наблюдалась выраженная тенденция к снижению данного показателя и при продолжении терапии. В последующие 2 недели он снизился на 5,6% (р = 0,053), или на 29,2% (р < 0,0001) от исходных цифр. Уровень сахара в моче снизился от исходного за первые 2 недели на 72,5% (р < 0,001) и на 78,1% (р < 0,0001) за весь период наблюдения (рис. 4).
Во 2-й группе больных, получавших таурин, средние показатели гликемии натощак снизились по сравнению с исходными на 24,9% (р < 0,001) через 2 недели после начала лечения. При продолжении приема препарата наблюдалось дальнейшее снижение данного показателя на 18,7% (р < 0,001) в последующие 2 недели, или на 38,9% (р < 0,001) от исходных цифр. Уровень постпрандиальной гликемии снизился через 2 недели на 26,7% (р < 0,01) от исходного. Наблюдалось снижение данного показателя и при продолжении терапии. В последующие 2 недели он снизился на 9,6% (р < 0,01), или на 33,7% (р < 0,0001) от исходных цифр. Уровень сахара в моче снизился от исходного за первые 2 недели на 41,8% (р < 0,01) и на 84,0% (р < 0,0001) за весь период наблюдения (рис. 5).
В 3-й группе пациентов, получавших глибенкламид вместе с таурином, средние уровни гликемии натощак снизились по сравнению с исходными на 40,9% (р < 0,0001) через 2 недели после начала лечения. При продолжении приема препарата наблюдалось дальнейшее снижение данного показателя на 14,5% (р < 0,05) в последующие 2 недели, или на 49,5% (р < 0,0001) от исходного. Уровень постпрандиальной гликемии снизился через 2 недели на 39,1% (р < 0,0001) от исходного. Наблюдалось снижение данного показателя и при продолжении терапии: в последующие 2 недели он снизился на 15,1% (р < 0,05), или на 48,3% (р < 0,0001) от исходных цифр. Уровень сахара в моче снизился от исходного за первые 2 недели на 91,5% (р < 0,001) и на 97,8% (р < 0,0001) за весь период наблюдения (рис. 6).
Таким образом, курсовое лечение больных СД 2 типа глибенкламидом, таурином или комбинацией этих препаратов сопровождалось снижением тощаковой, постпрандиальной гликемии и глюкозурии.
По данным дисперсионного анализа, через 2 недели терапии наибольшее снижение гликемии натощак отмечалось в группе больных СД 2 типа, принимавших глибенкламид в сочетании с таурином (p < 0,05). В этой же группе наблюдалась тенденция к более выраженному снижению глюкозурии (p = 0,068). Различие в снижении постпрандиальной гликемии от вида терапии было недостоверно (p = 0,22).
Через 4 недели у пациентов с СД 2 типа, принимавших глибенкламид в сочетании с таурином, наблюдалось наибольшее снижение как тощаковой (p < 0,01), так и постпрандиальной гликемии (p < 0,05). И в этой же группе отмечалось наибольшее уменьшение глюкозурии (p < 0,05).
Сравнительный эффект монотерапии и сочетанной терапии показан на рис. 7.
Данные свидетельствуют о том, что на начальном этапе лечения больных СД 2 типа таурин не уступает по влиянию на углеводный обмен одному из самых распространенных сахароснижающих препаратов – глибенкламиду. Сочетанное применение глибенкламида и таурина способствует более выраженной компенсации болезни.
У здоровых добровольцев длительный прием таурина (4 недели) тоже сопровождался улучшением показателей углеводного обмена. Через 2 недели после начала лечения наблюдалась тенденция к снижению как тощаковой гликемии – на 3,1% (р = 0,14), так и постпрандиальной – на 1,5% (р = 0,07). Через 4 недели данные показатели снизились на 4,2% (р < 0,05) и 4,1% (р = 0,07) соответственно (рис. 8).
Учитывая отсутствие в литературе данных о механизмах положительного влияния монотерапии таурином на углеводный обмен при длительной (4 недели и более) терапии, мы исследовали динамику уровня гликемии и инсулинемии после пероральной нагрузки глюкозой в группе больных СД 2 типа до лечения и через 4 недели монотерапии таурином.
По окончании курсовой терапии, хотя средние уровни инсулина в крови через 1/2, 1, 2, 4 и 6 часов после нагрузки глюкозой и были несколько выше, чем до лечения, но данные изменения не были статистически достоверны (р > 0,2). В то же время уровни сахара крови как натощак, так и через 1/2, 1, 2, 4 и 6 часов после нагрузки глюкозой были ниже, чем до лечения, на 24,2% (р < 0,01), 13,6% (р < 0,02), 16,8% (р < 0,05), 23,9% (р < 0,02), 13,8% (р < 0,02) и 21,9% (р < 0,02) соответственно (рис. 9), что свидетельствует об уменьшении инсулинорезистентности. Косвенным подтверждением этого утверждения служит и тенденция к уменьшению в данной группе индекса НОМА-IR (Homeostasis Model Assessment of Insulin Resistance – Гомеостатическая модель для оценки резистентности к инсулину) с 11,4 ± 5,7 до 7,1 ± 4,9% (p = 0,1).
Заключение
Изучив влияние таурина, глибенкламида и их сочетания на углеводный обмен, мы установили, что:
- таурин при однократном приеме оказывает сахароснижающее действие за счет стимуляции бета-клеток, не сопровождающееся длительной гиперинсулинемией и риском гипогликемии;
- после однократного приема сахароснижающее действие глибенкламида сопровождается длительной гиперинсулинемией и у больных СД 2 типа начинается позднее, чем у здоровых лиц;
- применение глибенкламида потенциально опасно в отношении развития гипогликемии;
- 4-недельная терапия таурином сопровождается снижением гликемии натощак, постпрандиальной гликемии и глюкозурии, сопоставимым с таковым при лечении глибенкламидом;
- длительная (4 недели и более) терапия таурином способствует уменьшению инсулинорезистентности;
- комбинированная терапия глибенкламидом и таурином в течение 1 месяца более эффективно снижает базальную и постпрандиальную гликемию и глюкозурию, чем монотерапия каждым из этих препаратов.
1. Аметов А.С. Терапевтические задачи и возможности их реализации при сахарном диабете типа 2 // Consilium medicum. 2003. Т. 5. № 9. С. 484–486.
2. Gu K., Cowie C.C., Harris M.I. Mortality in adults with and without diabetes in a national cohort of the U.S. population, 1971–1993 // Diabetes Care. 1998. Vol. 21. № 7. P. 1138–1145.
3. Roman S.H., Harris M.I. Management of diabetes mellitus from a public health perspective // Endocrin. Metabol. Clinics. 1997. Vol. 26. P. 443–460.
4. Сахарный диабет: доклад комитета экспертов ВОЗ. М., 1987. 68 с.
5. Дедов И.И., Шестакова М.В., Максимова М.А. Федеральная целевая программа «Сахарный диабет» (Методические рекомендации). М.: Медиа Сфера, 2002. 88 с.
6. Древаль А.В., Мисникова И.В., Зайчикова О.С. Микронизированный манинил как препарат первого выбора при неэффективности диетотерапии ИНСД // Сахарный диабет. 1999. № 2. С. 35–36.
7. Друэн П. Клинические испытания и использование пероральных гипогликемизирующих веществ при диабете: Статья из Франции // Фармация. 1981. Т. 30. № 3. С. 54–55.
8. Ефимов А.С. Некоторые итоги и перспективы развития диабетологии // Проблемы эндокринологии. 1988. Т. 34. № 3. С. 8–14.
9. Панков Ю.А. Пептидные гормоны и современные вопросы биотехнологии // Проблемы эндокринологии. 1996. Т. 42. № 2. С. 3–8.
10. De la Puerta C., Arrieta F.J., Balsa J.A. Taurine and glucose metabolism: a review // Nutr. Hosp. 2010. Vol. 25. № 6. P. 910–919.
11. Аметов А.С., Кочергина И.И., Елизарова Е.П. Роль таурина в эксперименте и в клинике сахарного диабета // Consilium medicum. Т. 15. № 4. С. 49–53.
12. Definition, diagnosis and classification of diabetes mellitus and its complications: Report of a WHO Consultation: Part 1: Diagnosis and classification of diabetes mellitus. Geneva, 1999. 60 с.
13. Фролов М.Ю. Фармакодинамика антагонистов кальция, бета-адреноблокаторов и таурина у больных с хроническими диффузными заболеваниями печени: автореф. дис. … канд. мед. наук. Волгоград, 1994. 19 с.
14. Кахновский И.М., Королева Т.В., Захарченко В.Н., Ларионов С.М. Таурин в лечении сахарного диабета // Клиническая фармакология и терапия. 1997. Т. 6. № 3. С. 57.
15. Цюхно З.И., Славнов В.Н., Панченко Н.И. и др. Функциональные методы исследования в эндокринологии. Киев: Здоровье, 1981. 240 с.
Effect of glibenclamide, taurine and combination on carbohydrate metabolism parameters
V.V. Naumov
State Health Care Institution ‘Clinical Hospital N.4’, Volgograd
Contact person: Vladimir Vladimirovich Naumov, vovochka1@yandex.ru
Treatment of diabetes is an important medical problem nowadays. Experimental and clinical studies have established the role of amino acid taurine in normal and impaired carbohydrate metabolism giving a rationale for the extensive use of taurine in clinical practice. However, only limited data is available concerning the effects of taurin and domestic taurin preparation Dibicor® on glucose metabolism and taurine interaction with oral hypoglycemic drugs.
In this study, we compared effects of taurine and glibenclamide after single use and 2- or 4-week therapy. 1-month treatment with glibenclamide and taurine combination was more effective in reducing basal and postprandial glycemia and glucosuria than treatment with single components.
Новости на тему
02.02.2024
01.02.2023
23.08.2022 01:00:00
01.07.2022 11:00:00
СТАТЬИ по теме
25.12.2023
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
