Влияние остеопороза на профилактику рецидива мочекаменной болезни
- Аннотация
- Статья
- Ссылки
- English
Кроме того, детализированы факторы риска остеопороза и выполнено исследование минеральной плотности костной ткани путем рентгеновской денситометрии. 69 (80,2%) пациентов не имели показаний к профилактике рецидива камнеобразования, а 17 (19,8%) больным назначено лечение. С учетом данных рентгенофазового анализа конкремента и показателей суточной экскреции кальция и мочевой кислоты десять пациентов принимали тиазиды, а семь – аллопуринол. Тиазиды способствовали уменьшению экскреции кальция, не влияя на экскрецию мочевой кислоты и диурез, а аллопуринол приводил к уменьшению концентрации мочевой кислоты, не влияя на экскрецию кальция и диурез. Отмечено, что фактором, воздействующим на частоту и скорость развития рецидива у пациентов с мочекаменной болезнью, может быть снижение минеральной плотности костной ткани. Так, рецидив мочекаменной болезни произошел у девяти пациентов со сниженной минеральной плотностью костной ткани и только у одного пациента с нормальным состоянием костной ткани. Уточнение факторов риска остеопороза позволит прогнозировать течение мочекаменной болезни, а также вероятность ее рецидива.
Кроме того, детализированы факторы риска остеопороза и выполнено исследование минеральной плотности костной ткани путем рентгеновской денситометрии. 69 (80,2%) пациентов не имели показаний к профилактике рецидива камнеобразования, а 17 (19,8%) больным назначено лечение. С учетом данных рентгенофазового анализа конкремента и показателей суточной экскреции кальция и мочевой кислоты десять пациентов принимали тиазиды, а семь – аллопуринол. Тиазиды способствовали уменьшению экскреции кальция, не влияя на экскрецию мочевой кислоты и диурез, а аллопуринол приводил к уменьшению концентрации мочевой кислоты, не влияя на экскрецию кальция и диурез. Отмечено, что фактором, воздействующим на частоту и скорость развития рецидива у пациентов с мочекаменной болезнью, может быть снижение минеральной плотности костной ткани. Так, рецидив мочекаменной болезни произошел у девяти пациентов со сниженной минеральной плотностью костной ткани и только у одного пациента с нормальным состоянием костной ткани. Уточнение факторов риска остеопороза позволит прогнозировать течение мочекаменной болезни, а также вероятность ее рецидива.


Введение
Цель послеоперационного обследования, лечения и наблюдения пациентов с мочекаменной болезнью (МКБ) – предотвращение рецидива камнеобразования. К настоящему времени разработаны практические рекомендации для выявления факторов риска первичного и рецидивного образования мочевых камней, а также клинические рекомендации по профилактике повторного камнеобразования [1, 2].
Один из факторов риска развития и рецидива МКБ – остеопороз. Это состояние характеризуется снижением минеральной плотности костной ткани (МПКТ), связанным со снижением уровня кальция в сыворотке крови и его повышенным выведением с мочой (гиперкальциурией). Результатом нарушения кальциевого обмена становится образование кальциевых камней в почках, поэтому у больных остеопорозом повышена частота уролитиаза [3, 4]. А у больных нефролитиазом в свою очередь отмечаются снижение МПКТ и гиперкальциурия [5]. Применение средств, препятствующих патологическому обмену костной ткани, и повышение физической нагрузки позволяют предотвратить отрицательный баланс кальция и снизить вероятность образования камней в почках [6, 7].
Для коррекции биохимических изменений в крови и моче назначают ряд лекарственных препаратов. Так, тиазидные диуретики снижают уровень кальция в моче. Увеличение выделения кальция с мочой обусловлено прямым и непрямым влиянием тиазидных диуретиков на почки, а также их внепочечным эффектом.
В проксимальном отделе нефрона тиазидные диуретики оказывают слабое и однонаправленное действие, снижая реабсорбцию натрия и кальция. Однако в дистальном отделе нефрона действие тиазидных диуретиков разнонаправлено: реабсорбция натрия снижается, а кальция – повышается или не меняется. Выраженность гипокальциурического эффекта тиазидных диуретиков зависит от количества потребляемой поваренной соли и объема внеклеточной жидкости. Так, при ограничении поступления натрия и уменьшении объема внутриклеточной жидкости реабсорбция кальция в проксимальных канальцах повышается и его выделение уменьшается, а при увеличении введения натрия выделение кальция повышается.
Следует отметить, что на фоне приема тиазидных диуретиков выделение кальция с мочой в первые дни лечения не меняется, а к концу первой недели уменьшается, оставаясь на таком уровне в течение всего периода лечения [8]. При прекращении приема тиазидных диуретиков может наблюдаться преходящий рикошетный эффект с увеличением выделения кальция с мочой.
Внепочечный эффект тиазидных диуретиков проявляется прямым и опосредованным через паратиреоидный гормон действием на костную ткань. Тиазидные диуретики стимулируют высвобождение и активность паратиреоидного гормона, что может иметь серьезное клиническое значение при гиперпаратиреоидизме.
Уровень кальция в крови определяется также всасываемостью в кишечнике: тиазидные диуретики не меняют или, по данным ряда исследований, снижают всасывание, что может компенсировать задержку кальция почками. Возможно, последнее объясняет отсутствие осложнений (например, отложения кальция в тканях), обусловленного влиянием тиазидных диуретиков на выделение кальция почками [9, 10].
Таким образом, тиазидные диуретики уменьшают почечную экскрецию кальция посредством следующих механизмов:
- прямо, повышая реабсорбцию кальция в дистальных отделах нефрона;
- опосредованно, уменьшая объем внутриклеточной жидкости и повышая в проксимальных канальцах реабсорбцию не только натрия и воды, но и связанную с этим пассивную реабсорбцию кальция;
- экстраренально, усиливая секрецию паратиреоидного гормона, повышая всасывание из кишечника и мобилизуя кальций из костных депо.
Способность тиазидных диуретиков влиять на обмен кальция позволяет использовать его у больных с гиперпаратиреоидизмом, гиперкальциурией и кальциевыми камнями в почках, получающих лечение витамином D или его аналогами. Благоприятный эффект тиазидных диуретиков при МКБ обусловлен также повышением выделения с мочой магния, цинка пирофосфата и тенденцией к снижению выделения оксалатов и цитратов [10].
Назначение тиазидных диуретиков имеет положительный эффект не только при профилактике камнеобразования, но и в случае снижения МПКТ. Прием тиазидных диуретиков снижает вероятность перелома шейки бедра у женщин в постменопаузальном и предклимактерическом периоде, этот эффект наблюдается и у мужчин. Тиазидные диуретики не только уменьшают кальциурию, но также стимулируют образование и активность остеобластов, ингибируют экспрессию остеокальцина и создают условия для формирования кости и ее минерализации.
При образовании смешанных кальциево-оксалатных конкрементов на фоне гиперурикозурии применяют аллопуринол, ингибитор ксантиноксидазы [11]. Препарат может снижать риск образования конкрементов из оксалата кальция за счет уменьшения вероятности кристаллизации мочевой кислоты и уратов, способствующих выпадению в осадок оксалата кальция, образования комплекса между коллоидным уратом и макромолекулярными ингибиторами, а также снижения экскреции оксалатов [2].
Цель исследования
Уточнить влияние остеопороза на течение мочекаменной болезни.
Материал и методы
С 2016 по 2018 г. обследовано 86 пациентов с МКБ, из них 47 (54,7%) мужчин и 39 (45,3%) женщин, средний возраст 48,0 ± 14,2 года. Всем пациентам выполнено оперативное лечение: в 42 (48,8%) случаях – чрескожная нефролитотрипсия, в 22 (25,6%) случаях – дистанционная ударно-волновая литотрипсия, в 21 (24,4%) случае – контактная уретеролитотрипсия и в 1 (1,2%) случае – лапароскопическая пиелолитотомия.
Пациенты заполнили анкету факторов риска остеопороза, разработанную Международным обществом по остеопорозу (рис. 1) [12, 13]. Анализ результатов анкетирования показал, что у 44 (51,2%) пациентов с МКБ имели место факторы риска остеопороза, а у 42 (48,8%) их не было.
Состояние костной ткани у пациентов оценивали с помощью двухэнергетической рентгеновской абсорбциометрии как наиболее широко используемого метода определения плотности костной ткани [14]. С его помощью получают изображение костей в области сканирования и вычисляемые показатели костной плотности, выраженные в граммах на 1 см² площади исследованного участка кости. Проводится сканирование поясничного отдела позвоночника, шейки бедра, предплечья или всего тела целиком. МПКТ определяют путем измерения степени проницаемости кости для рентгеновских лучей. Чем больше гасится излучение при прохождении через кость, тем выше ее плотность. При этом используют два пучка фотонов – высокой и низкой энергии, что позволяет исключить влияние структуры мягких тканей на измерение костной массы и плотности. На основании многочисленных методов оценки показано, что распространенность переломов коррелирует с МПКТ поясничного отдела позвоночника и проксимальных отделов бедренных костей (уровень доказательности А).
Индивидуальная МПКТ сравнивается с референсной базой данных. Из-за различных методов измерения (в зависимости от аппаратуры) наиболее приемлемым способом оценки МПКТ считается применение Т- и Z-критериев. Т-критерий отражает разницу между плотностью кости обследуемого человека и стандартом, который соответствует плотности кости здоровых людей при достижении ее максимальных значений – пика костной массы. Z-критерий – количество стандартных отклонений выше или ниже среднего показателя минеральной плотности кости для лиц аналогичного возраста.
Определение остеопороза разработано Всемирной организацией здравоохранения для женщин европеоидной расы и основано на определении МПКТ в любой точке осевого скелета по Т-критерию:
- норма – показатели Т-критерия от -1 и выше стандартных отклонений от пиковой костной массы;
- остеопения – показатели Т-критерия от -1 до -2,5 стандартных отклонений включительно;
- остеопороз – показатели Т-критерия от -2,5 стандартных отклонений и ниже;
- тяжелый остеопороз – показатели Т-критерия от -2,5 стандартных отклонений и ниже с одним и более переломов в анамнезе.
У мужчин в возрасте 65 лет и старше тоже применяют Т-критерий и диагноз остеопороза устанавливается при Т-критерии, равном -2,5 стандартных отклонений и ниже. В возрасте 50–65 лет может использоваться Т-критерий, но диагноз остеопороза подтверждается при сочетании Т-критерия, равного -2,5 стандартных отклонений и ниже, и других факторов риска. У мужчин любого возраста с вторичными причинами низкой МПКТ (например, лечение глюкокортикоидами, гипогонадизм, гиперпаратиреоз) диагноз ставится на основании клинических данных и подтверждается низкой МПКТ.
Из 35 больных, которые прошли двухэнергетическую рентгеновскую абсорбциометрию, у 17 (48,6%) было выявлено снижение МПКТ, а у 18 (51,4%) МПКТ была в пределах нормальных значений.
У 29 пациентов выполнен рентгенофазовый анализ мочевых камней и их фрагментов (таблица). Чаще удаленные камни состояли из гидроксилапатита и ведделлита (44,8%), вевеллита (17,2%) и мочевой кислоты (10,3%).
Через месяц после выписки из стационара при нормализации показателей общего анализа мочи, отрицательных результатах бактериологического посева мочи у пациентов определяли суточную экскрецию кальция и мочевой кислоты. Никто из больных не принимал диуретических препаратов. Все пациенты получили письменные инструкции относительно сбора суточной мочи. Первая утренняя порция мочи не учитывалась, все остальные порции мочи в течение дня и ночи, включая первую утреннюю порцию на следующий день, пациент должен был собирать в одну емкость. После завершения сбора мочи пациент измерял ее объем, перемешивал и отливал в контейнер. Уровень суточной экскреции кальция определяли О-крезолфталеиновым методом (референсные значения – от 2,5 до 7,5 ммоль/сут). Показатели суточной экскреции мочевой кислоты устанавливали энзиматическим (уриказным) методом (референсные значения – от 1,48 до 4,43 ммоль/сут).
Выбор метода лечения, направленного на предотвращение рецидива камнеобразования, основывался на результатах исследования состава камня и суточной экскреции кальция и мочевой кислоты.
У 69 (80,2%) пациентов изменений суточной экскреции мочевой кислоты и кальция не выявлено, и они оставались под наблюдением. Семи (8,1%) пациентам был назначен аллопуринол в дозе 100 мг в сутки три раза в день на основании повышения экскреции мочевой кислоты, десяти (11,6%) больным – тиазидные диуретики в дозе 25 мг/сут на основании повышения экскреции кальция.
Контрольное клиническое обследование и определение суточной экскреции кальция и мочевой кислоты выполняли через три месяца.
Результаты обработаны с применением статистической программы MedCalc. Данные представлены в виде среднего и стандартного отклонения. Сравнение данных выполняли с применением критерия Краскелла – Уоллиса, критерия χ2 и регрессионного анализа, а уровень значимости p принят равным 0,05.
Результаты
Значимых различий по возрасту между группами не выявлено (р = 0,136).
У пациентов, находившихся под наблюдением, преобладали кальций-оксалатные камни (р = 0,0254).
Частота факторов риска остеопороза была одинаковой во всех группах (р = 0,2156).
Частота снижения МПКТ в группах не имела значимых различий (р = 0,64).
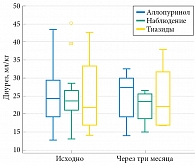
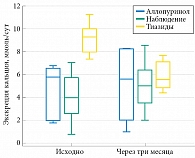
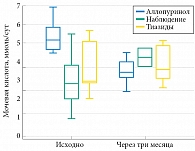
Динамика диуреза, суточной экскреции кальция и уратов представлена на рис. 2–4. Значимых изменений диуреза при контрольном исследовании у всех пациентов не выявлено (р = 0,487). На фоне приема тиазидов отмечено значимое снижение суточной экскреции кальция (р = 0,0054). В процессе лечения аллопуринолом произошло значимое снижение экскреции мочевой кислоты (р = 0,021), без изменений суточной экскреции кальция и диуреза. У пациентов, которым не проводилось лечение ввиду отсутствия объективных показаний, значимых изменений кальция и мочевой кислоты не обнаружено.
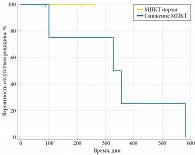
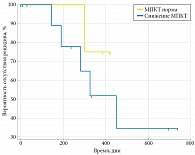
Результаты наблюдения за пациентами с МКБ после оперативного лечения и результаты исследования МПКТ представлены на рис. 5 и 6. Рецидив МКБ на фоне лечения произошел у четырех пациентов со сниженной МПКТ. Среди пациентов, которые лечения не получали, рецидив имел место у пяти пациентов со сниженной МПКТ и одного пациента с нормальной МПКТ. Таким образом, рецидив камнеобразования на фоне лечения выявлен у четырех пациентов при среднем сроке наблюдения 381 ± 61 дня, а в контрольной группе – у шести пациентов при сроке наблюдения 836 ± 64 дня.
Обсуждение
Высокая частота распространения факторов риска остеопороза среди пациентов с МКБ, а также выявление сниженной МПКТ может быть одним из условий возникновения, прогрессирования и рецидивирования камнеобразования. Лечение, направленное на предотвращение рецидива МКБ, проводится при установлении нарушения экскреции кальция и мочевой кислоты. Современные методы коррекции суточной экскреции кальция и мочевой кислоты позволяют контролировать эти показатели. Однако даже на фоне профилактического лечения рецидив камнеобразования произошел у четырех (4,6%) пациентов.
При сравнении частоты и динамики рецидива камнеобразования у пациентов со снижением МПКТ повторное образование камней после оперативного лечения происходит быстрее. Такая тенденция наблюдалась и у пациентов на фоне лечения, и у пациентов, не получавших терапии ввиду отсутствия показаний для ее назначения. Данный факт может указывать на связь снижения МПКТ и камнеобразования за счет повышения экскреции кальция, причем воздействие этого фактора происходит неравномерно во времени и не отражается на показателях суточной экскреции кальция. Диагностировать процесс снижения МПКТ можно только по результатам денситометрии.
Заключение
Лечение, направленное на предотвращение рецидива камнеобразования, основано на результатах послеоперационного обследования. При повышении экскреции кальция были назначены тиазидные диуретики, а при повышении экскреции мочевой кислоты – аллопуринол. Проводимое лечение позволило контролировать измененные параметры. Прием тиазидов способствовал уменьшению экскреции кальция, а аллопуринола – мочевой кислоты. Однако на частоту и скорость рецидива у больных МКБ может оказывать снижение МПКТ за счет увеличения экскреции кальция. У 51,2% обследованных пациентов выявлены факторы риска остеопороза, а у 48,6% – снижение МПКТ. При нормальной МПКТ рецидив выявлен у одного пациента, а при сниженной МПКТ – у девяти. По нашему мнению, диагностика остеопороза и его факторов позволяет прогнозировать течение МКБ, эффективность метафилактики, а также вероятность рецидива.
V.I. Rudenko, MD, PhD, Prof., Yu.L. Demidko, MD, PhD, L.S. Demidko, G.M. Kuzmicheva, D.Chem.Sci., PhD, Prof.
I.M. Sechenov First Moscow State Medical University
MIREA – Russian Technological University, Moscow
Contact person: Yury L. Demidko, demidko1@mail.ru
The results of examination of 86 patients with urolithiasis who underwent surgical treatment are presented. For all the patients it was made the physical and chemical examination of urinary stones and their fragments and as well determined the excretion of calcium, uric acid and oxalates. In patients, risk factors for osteoporosis were also detailed and bone mineral density was studied by x-ray densitometry. 69 (80.2%) patients had no indications for the prevention of stone formation recurrence, and 17 (19.8%) patients were prescribed treatment. Taking into account the data of x-ray phase analysis of the concretion and daily excretion of calcium and uric acid, ten patients took thiazides, and seven patients took allopurinol. Thiazides reduced calcium excretion without affecting uric acid excretion and diuresis, and allopurinol reduced uric acid without affecting calcium excretion and diuresis. It is noted that the factor affecting the frequency and speed of recurrence in patients with urolithiasis may be the decrease in bone mineral density. Thus, recurrence of urolithiasis occurred in nine patients with reduced bone mineral density and only in one patient with normal bone tissue. Refinement of risk factors for osteoporosis will allow predicting the course of urolithiasis, as well as the probability of its recurrence.
