Вторичная профилактика ишемического инсульта: антиагрегантная терапия у пациентов с высоким сосудистым риском
- Аннотация
- Статья
- Ссылки
Достижения современной медицины позволили снизить уровень смертности после первого инсульта. Однако среди пациентов, ранее перенесших ИИ, риск развития повторного инсульта увеличивается в 6–9 раз [11, 30]. Риск повторного цереброваскулярного события, независимо от патогенетического типа первого инсульта, наиболее высок в течение первого месяца после приступа – 4%, в течение 3 месяцев – от 1,2% до 9%, и 12% в течение первого года [29, 32, 40, 47]. Начиная со второго года, средний ежегодный риск равен 4% [30]. Кумулятивный риск первого повтора инсульта в течение 5 лет составляет около 16,6%, в течение 10 лет – 43% [30, 31].
В зависимости от патогенетического типа первого инсульта, наиболее высокий риск рецидива в течение 30 дней имеют пациенты, перенесшие (по критериям National Institute of Neurological Diseases and Stroke Data Bank) инсульт в результате атеросклероза крупных артерий – 18,5%, лакунарный инсульт – 1,4%, инсульт при кардиоэмболии – 5,3%, инсульт неустановленного генеза – 3,3% [45].
Повторный инсульт становится причиной смерти большинства пациентов с цереброваскулярными заболеваниями: комбинированный риск повторного инсульта и смерти составляет 65,3% в течение 10 лет [31]. Тридцатидневная смертность после повторного инсульта значительно выше, чем в этот же период у пациентов с первым инсультом (41% и 22% соответственно) [34]. Повторный инсульт ведет к тяжелой инвалидизации вследствие двигательного дефицита и когнитивных нарушений, что в свою очередь в несколько раз увеличивает риск развития внемозговых осложнений, таких как гипостатическая пневмония, тромбозы и тромбоэмболии, уроинфекция и т. п. [33, 35]. В связи с этим одной из основных задач при ведении больных после инсульта является снижение высокого риска раннего повторного инсульта, а в долгосрочной перспективе – риска всех серьезных сосудистых событий, как фатальных, так и нефатальных [26, 42].
Атеротромбоз является наиболее частой причиной возникновения острых сосудистых событий, которые в большинстве случаев манифестирует цереброваскулярными (инсульт, транзиторная ишемическая атака ТИА), кардиоваскулярными событиями (инфаркт миокарда) и поражением артерий нижних конечностей (перемежающаяся хромота, ишемия конечностей). Факторы риска этих синдромов схожи: сахарный диабет, дислипидемия, артериальная гипертензия, курение [48, 50]. Общность факторов подчеркивает системную природу атеросклероза. Однако эпидемиологические исследования показывают некоторые отличия в патогенетических процессах и особенностях реализации факторов риска. Так дислипидемия играет существенную роль в реализации коронарных событий, но степень ее участия в развитии инсульта до конца не установлена [50]. Если в большинстве случаев инфаркт обусловлен атеросклеротической бляшкой, то инсульт вызывается атеросклерозом крупных артерий только в 20–25%.
Исследования среди больных с симптоматическим атеросклерозом показали, что повторным сосудистым событием в группе пациентов с ИИ в 77–79% случаев был инсульт, а у пациентов с инфарктом миокарда (ИМ) в 76–84% развивался повторный ИМ [36]. Эта же тенденция была отмечена и в исследовании CAPRIE (1996) [20]. Таким образом, можно сделать вывод, что большинство пациентов с инсультом должны получать антиагреганты с доказанной эффективностью при острых цереброваскулярных событиях. Новые методы ультразвуковой диагностики позволяют мониторировать степень атеротромбоза и определять эмбологенность бляшек [13]. Однако арсенал медикаментозных средств воздействия на патогенетические звенья инсульта и вторичной профилактики не претерпел существенных изменений в течение последнего десятилетия.
Основными принципами проведения вторичной профилактики инсульта являются: индивидуальный выбор программы профилактических мероприятий; дифференцированный подход в зависимости от типа и клинического варианта перенесенного инсульта; комбинированный характер проводимых терапевтических воздействий; использование антигипертензивной, антитромботической, гиполипидемической терапии и возможностей хирургического лечения [11]. Достаточно условно мероприятия по вторичной профилактике можно разделить на две категории: снижение риска кардиоэмболии и предотвращение тромботических ишемических событий.
Кардиоэмболия является причиной 15–20% ишемических инсультов [23, 52]. Для предупреждения повторных кардиоэмболий используются варфарин и аспирин, выбор зависит от степени риска кардиоэмболии и характера патологии сердца. На основании этого разработаны рекомендации по выбору препарата (Тhe Trial of ORG 10172 in Acute Stroke Treatment) у больных с фибрилляцией предсердий (ФП). Высокий риск (8% в год) развития кардиоэмболий характерен для женщин старше 75 лет, страдающих повышенным САД (выше 160 мм рт. ст.), имеющих гипертрофию левого желудочка и перенесших транзиторную ишемическую атаку или инсульт. Для этой группы предпочтительным является назначение варфарина. Варфарин также показан больным с дилатационной кардиомиопатией, перенесшим ИМ и/или имеющим тромбоз левого желудочка, а также пациентам с искусственными клапанами [48]. Для больных с низким риском (1%) повторной кардиоэмболии (пациенты только с ФП) возможно назначать аспирин.
Поскольку доказана роль активации тромбоцитарно-сосудистого звена гемостаза в тромбо- и атерогенезе, для профилактики ишемических инсультов, особенно при атеротромботическом их варианте, необходимо применение антиагрегантных препаратов. Систематизированный обзор результатов клинических исследований выявил доказательства преимуществ антитромбоцитарной терапии, использование которой позволяет уменьшить риск серьезных сосудистых эпизодов примерно на 25%. Наиболее изученными среди антитромботических средств являются антиагрегантные препараты – ацетилсалициловая кислота (АСК), дипиридамол, клопидогрел, тиклопедин, которые имеют разные механизмы действия и оказывают влияние на различные звенья тромбообразования [4, 5, 8, 11, 12, 14].
Аспирин остается наиболее распространенным антитромбоцитарным средством, действие препарата обусловлено влиянием на каскад арахидоновой кислоты: ингибируя преимущественно тромбоцитарную циклооксигеназу-1, препарат снижает синтез и высвобождение тромбоцитарного тромбоксана А2 [38]. Анализ результатов исследований (Antithrombotic Trialists’ Collaboration, 2002) выявил приблизительно одинаковую эффективность ацетилсалициловой кислоты в дозах от 75 до 1500 мг/сут: снижение частоты сердечно-сосудистых заболеваний на 19% при приеме больших доз (500–1500 мг/сут), на 26% – при приеме средних доз (160–325 мг/сут), на 32% – при приеме небольших доз (75–150 мг/сут). Использование малых доз ацетилсалициловой кислоты (менее 75 мг/сут) менее эффективно: частота сердечно-сосудистых заболеваний снижается всего на 13%. Учитывая меньший риск осложнений со стороны желудочно-кишечного тракта при использовании средних и небольших доз ацетилсалициловой кислоты, для профилактики сердечно-сосудистых заболеваний оптимален прием ацетилсалициловой кислоты в дозах от 75 до 325 мг/сутки [6, 18].
Второй группой препаратов являются производные тиенопиридонов – клопидогрел и тиклопедин, которые селективно и необратимо блокируют связывание АДФ с его тромбоцитарным рецептором P2 Y12 и последующую АДФ-индуцированную активацию комплекса гликопротеина IIb/IIIа в тромбоцитах. Первым из препаратов стал применяться тиклопедин, который показал свою эффективность в снижении риска повторного инсульта у больных, ранее перенесших ТИА или малый инсульт, а также риска смерти и ИМ у больных с нестабильной стенокардией. Сравнительные исследования эффективности применения аспирина и тиклопедина показали высокую эффективность последнего – 17% и 25% соответственно. Однако ряд побочных эффектов (нейтропения, тромбоцитопения, апластическая анемия, тромботическая тромбоцитопеническая пурпура) ограничивают применение данного препарата [4].
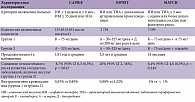
Клопидогрел (Плавикс®) – наиболее распространенный препарат из группы тиенопиридинов, его получают более 40 млн людей во всем мире [44]. Эффективность препарата изучалась в ряде крупных исследований (табл. 1) [57].
В исследовании CAPRIE [20, 56] в 1996 году приняли участие 19 185 больных, в том числе 6400 пациентов с недавно перенесенным инсультом, ИМ и с клиническими проявлениями атеросклеротического поражения периферических сосудов. Сравнивалась эффективность приема 325 мг аспирина с 75 мг клопидогрела, период лечения составил от 1 до 3 лет. Результаты исследования показали более высокую эффективность монотерапии клопидогрелем в снижении риска развития ИМ, инсульта и смерти от сосудистых событий, чем у аспирина. Совокупный риск был ниже на 8,7%. Более детальный анализ выявил наибольшую эффективность клопидогрела (снижение риска на 23,8%) в предотвращении сосудистых событий у пациентов с атеросклеротическим поражением периферических артерий и в подгруппах пациентов с высоким риском (ранее переносивших инсульт или инфаркт миокарда).
Пациенты с симптоматическими проявлениями атеросклероза имели более высокий риск развития инфаркта миокарда, инсульта или смерти от сосудистой причины. Трехлетнее наблюдение за данной субпопуляцией показало, что в группе пациентов, принимавших клопидогрел, данные конечные точки регистрировались в 20,4% случаях, в то время как в группе принимавших ацетилсалициловую кислоту – в 23,8%. Таким образом, абсолютный риск снижался на 3,4%, относительный – на 14,9%. Исследование также показало, что прием аспирина повышает риск желудочно-кишечного кровотечения, а для клопидогрела свойственно более частое появление кожной сыпи и диареи. Частота развития симптоматического внутримозгового кровотечения была сопоставима в обеих группах. Данное исследование интересно еще и тем, что продемонстрировало возможность длительного приема клопидогрела.
Если в исследовании CAPRIE включались пациенты, перенесшие инсульт в течение 3 месяцев, то пилотное исследование FASTER было посвящено изучению эффективности комбинации клопидогрела с аспирином в начальном периоде терапии в течение суток после развития ТИА или инсульта [34]. Клопидогрел назначался в дозе 300 мг однократно, затем по 75 мг, одновременно с антиагрегантами больные получали 40 мг/сутки симвастатина. Исследование было прекращено досрочно в связи с медленным набором пациентов, однако оно показало сравнимую эффективность аспирина и клопидогрела за 90 дней наблюдения. В настоящее время в ранний период инсульта вторичная профилактика осуществляется аспирином, в то время как клопидогрел назначается только с 7 дня.
Эффективность совместного приема клопидогрела и аспирина с целью вторичной профилактики изучалась и в ряде других исследований. Комбинация клопидогрела (75 мг/сутки) и аспирина (75–160 мг/сутки) и монотерапия аспирином проводилась у 15 603 пациентов с кардиоваскулярной патологией, из них 4320 пациентов перенесли инсульт или ТИА в течение предшествующих 5 лет [21]. По результатам исследования в подгруппе пациентов с предшествующим ишемическим инсультом, комбинированная терапия снижала риск серьезных сосудистых событий на 22%, по всей популяции частота развития серьезных сосудистых явлений сопоставима в обеих группах. Касательно нежелательных явлений: при комбинированной терапии не было выявлено повышения риска тяжелых кровотечений.
Исследование MATCH, напротив, сравнивало эффективность комбинированной терапии (клопидогрел – 75 мг/сутки, аспирин 75–160 мг/сутки) и монотерапии клопидогрелем [24]. В исследование вошли 7 599 больных, перенесших ТИА или инсульт по типу малого в предшествующие 3 месяца. Добавление аспирина не привело к снижению риска серьезных сосудистых событий. Было зафиксировано увеличение риска кровотечения у пациентов при комбинированной терапии: данный побочный эффект был кумулятивным и начинал нарастать спустя 4 месяца после начала лечения. Полученные данные интересны тем, что показали эффективность монотерапии клопидогрелем в предотвращении повторных сосудистых событий, таких как осложнения атеросклероза, в долгосрочной перспективе.
Исследование CARESS (Clopidogrel and Aspirin for reduction of Emboli in Symptomatic Carotid Stenosis) показало эффективность комбинированной терапии в снижении риска появления асимптомных микроэмболов у пациентов с симптоматическим стенозом каротидных артерий с высоким риском повторной эмболии [37]. Исследование является оригинальным, потому что впервые для оценки влияния антиагрегантов на атеросклеротический процесс были использованы инструментальные методы. С помощью транскраниального дуплексного ультразвукового сканирования сравнивалась эффективность клопидогрела в дозе 74 мг/сутки с АСК (75 мг/сутки) и монотерапия АСК. Наблюдение выявило, что комбинированная терапия снижает относительный риск асимптомных микроэболов на 39,8%, почасовая частота микроэмболии снижалась на 61,6% ко 2‑му и 7‑му дню терапии. Полученные данные согласуются с результатами исследования, которое изучало возможность предотвращения послеоперационного эмболического инсульта (регистрируется в 2–3% случаев) комбинированной терапией клопидогрелем и аспирином у больных с планируемой каротидной эндартерэктомией. В это исследование вошли 100 больных, 44 человека накануне операции принимали 150 мг аспирина и 75 мг клопидогрела, у остальных были отменены антиагрегантные препараты. Частота микроэмболов регистрировалась в послеоперационном периоде с помощью ультразвукового мониторинга. Данное исследование первым продемонстрировало снижение риска потенциальных тромбоэмболических осложнений на фоне приема антиагрегантов без увеличения риска кровотечения [43]. В связи с полученными данными пациентам, которым показана каротидная эндартерэктомия, не рекомендуется отменять прием аспирина [54].
В настоящее время активно изучается дозозависимый эффект препарата. Анализ повторных ишемических событий на фоне приема клопидогрела показал вероятность возникновения резистентности к клопидогрелу. Однако это предположение пересматривается в связи с методологической неопределенностью термина «резистентность». Проведенные фармакокинетические исследования позволили предположить, что в получении терапевтического эффекта имеет значение доза препарата. Недостаточность дозы и нарушение режима приема может являться модифицируемым фактором риска повторного инсульта [44, 53]. Таким образом, проведенные клинические исследования клопидогрела показали его более высокую эффективность в предотвращении повторных инсультов по сравнению другими антиагрегантами у пациентов высокого сосудистого риска. Это нашло отражение в Европейских рекомендациях ESO.
Еще одним представителем группы антитромботических препаратов является дипиридамол, который представляет собой умеренный антиагрегантный препарат, применяющийся в комбинации с АСК во вторичной профилактике некардиоэмболического инсульта на протяжении последних 30 лет [16]. Механизм действия основан на конкурентном ингибиторовании аденозиндезаминазы и адениловой фосфодиэстеразы. Препарат повышает содержание аденозина и цАМФ в тромбоцитах и гладкомышечных клетках сосудистой стенки, предотвращая их активацию. Установлено влияние на метаболизм арахидоновой кислоты вследствие увеличения продукции простациклина в сосудистой стенке и торможения биосинтеза тромбоксана А2 в тромбоцитах путем подавления тромбоксансинтетазы [38, 44]. В сравнительных исследованиях препарат показал эффективность в снижении относительного риска серьезных сосудистых событий на 18% по сравнению с аспирином, однако эффективность в предотвращении повторных инсультов была сопоставима с аспирином [42]. В исследовании ESPS-2 было показано, что сочетанное применение 50 мг АСК и 400 мг дипиридамола позволило увеличить количество предотвращенных повторных ишемических инсультов до 37%, что значительно выше, чем при лечении только АСК (снижение ОР на 23,1%) или только дипиридамолом (снижение ОР на 24,7%). Комбинированная терапия оказалась более эффективной, чем каждый препарат в отдельности, что подтверждает синергизм их действия [11]. В настоящее время применяется дипиридамол с замедленным высвобождением в сочетании с небольшими дозами аспирина. Учитывая тот факт, что наиболее частым осложнением является головная боль, рекомендуется постепенное увеличение дозы [55]. Вышеуказанная комбинация препаратов в сравнении с монотерапией клопидогрелем не показала своей эффективности в предотвращении повторного инсульта в исследовании PRоFESS [27]. Высок риск нефатальных геморрагических инсультов (относительный риск развития внутричерепных кровотечений достоверно увеличился на 42% в группе больных, получавших аспирин в комбинации с дипиридамолом МВ, по сравнению с группой клопидогрела). Побочные явления в группе пациентов, принимавших комбинированную терапию АСК и дипиридамолом, стали причиной досрочного прекращения лечения. Головокружения, обмороки, головная боль были наиболее частыми побочными эффектами, приводящими к отмене лечения, и достоверно чаще отмечались в группе лечения комбинацией аспирина с дипиридамолом МВ (16,4%), чем в группе лечения клопидогрелем (10,6%).
К настоящему времени сформированы показания к каротидной эндартерэктомии, при которых эффект оперативного лечения превышает консервативную тактику ведения. Открытым остается вопрос о целесообразности оперативного лечения с целью предотвращения ишемических инсультов у больных с асимптомными стенозами, так как не доказаны преимущества ни хирургических, ни консервативных методов лечения [54].
Таким образом, на сегодняшний день неоспоримым фактом остается эффективность антитромбоцитарных препаратов в снижении риска развития повторных инсультов, в особенности у пациентов, входящих в группу высокого сосудистого риска (пациенты, перенесшие ранее инфаркт или/и инсульт, имеющие симптоматические проявления периферического атеросклероза).