Основные вопросы наиболее эффективных и безопасных методов комплексной терапии ВПЧ-ассоциированных заболеваний шейки матки и лечения кандидозного вульвовагинита обсуждались ведущими российскими специалистами на круглом столе «Урогенитальные инфекции: современный взгляд на проблему», организованном компанией «Гедеон Рихтер» 29 сентября 2011 г. в рамках ХII Всероссийского научного форума «Мать и дитя».

профессор С.А. Леваков

«Урогенитальные инфекции: современный взгляд на проблему»
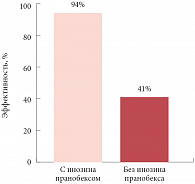
Рис. 1. Сравнительная эффективность традиционной терапии генитальных кондилом с применением и без применения инозина пранобекса* * Mohanty K.C

профессор А.Л. Тихомиров

Рис. 2. Скорость исчезновения симптомов кандидозного вульвовагинита при лечении бутоконазолом

профессор Т.А. Обоскалова
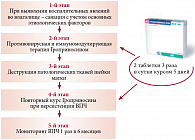
Рис. 3. Клинический алгоритм ведения пациенток с CIN I–III степени
Доброкачественные и злокачественные заболевания шейки матки, ассоциированные с вирусными инфекциями
Рак шейки матки (РШМ) по-прежнему остается актуальной медицинской проблемой – по частоте встречаемости он занимает одну из лидирующих позиций среди гинекологических видов рака с тенденцией роста заболеваемости среди женщин 20–30 лет, сообщил в начале своего доклада профессор Сергей Александрович ЛЕВАКОВ (зав. кафедрой акушерства и гинекологии ФГОУ ДПО ИПК ФМБА России, зав. отделением гинекологии ФГУЗ КБ № 83 ФМБА РФ, д. м. н.).
Доказано, что вирус папилломы человека (ВПЧ) является основной причиной предрака и рака шейки матки, а 90% случаев рака шейки матки обусловлено ВПЧ онкогенных типов (16, 18, 45, 31, 33). Скрининговые программы выявляют только 7% рака шейки матки и около 20% цервикальной интраэпителиальной неоплазии (CIN). Цитологический результат с выявленной клеточной атипией требует проведения биопсии шейки матки под контролем кольпоскопии. До сих пор не существует единого клинического мнения о выборе метода деструкции и роли иммунотерапии в лечении ВПЧ-ассоциированных заболеваний шейки матки. «Известно, что развитию рака шейки матки предшествуют длительные предраковые процессы в виде цервикальной интраэпителиальной неоплазии, которая в течение 10 лет переходит из первой во вторую, а затем в третью степень. Однако и после органосохраняющего лечения этих предраковых процессов впоследствии может развиваться цервикальная интраэпителиальная неоплазия первой степени. Вероятнее всего, это связано с сохранением персистенции ВПЧ в эпителии, что приводит к прогрессированию процесса», – уточнил докладчик.
В морфологической структуре патологии шейки матки большинство изменений – около 70% – представлены доброкачественными и предраковыми процессами и только 30% – раком. Следовательно, у врача есть значительный запас времени для того, чтобы верифицировать диагноз, спрогнозировать и провести лечение.
Цитологическое исследование является первым методом скрининга патологических изменений шейки матки. По данным профессора С.А. Левакова, при CIN II–III в первичном цитологическом мазке высокая степень плоскоклеточной неоплазии обнаруживается у 31% больных, низкая – у 39% и атипичные клетки – у 30% больных. При циркулярной биопсии шейки матки диагноз меняется с частотой от 0,5 до 9% случаев. При проведении цитологического контроля необходимо учитывать, что более 95% всех CIN возникают внутри зоны трансформации шейки матки, особое внимание нужно уделять переходным зонам между эпителиями.
Следующий метод диагностики – морфологическая верификация, которая проводится после расширенной кольпоскопии, позволяющей выявить измененный эпителий. Результаты цитологического контроля и кольпоскопического исследования могут различаться. Чувствительность цитологического контроля при выявлении CIN II–III составляет 67–76%. Ошибки прицельной биопсии выявляются в 15% случаев. «По данным цитологического контроля и кольпоскопического исследования мы можем лишь заподозрить наличие патологического процесса в области шейки матки, но диагноз должен быть поставлен только после морфологической верификации», – пояснил докладчик.
Таким образом, к основным методам исследования, необходимым для постановки диагноза, относятся: цитологическое исследование мазков, взятых из
экто- и эндоцервикса; кольпоскопическое исследование; исследование урогенитальной инфекции; биопсия шейки матки; выскабливание цервикального канала. Диагностическое выскабливание цервикального канала позволяет избежать ошибок в диагностике РШМ при наличии железистого рака. По словам докладчика, риск диагностической ошибки при раке цервикального канала составляет около 1% наблюдений. Например, при соскобе из цервикального канала и резекции измененного участка эктоцервикса, размерами 3–5 мм х 7 мм, аденокарцинома выявлялась в одном случае из 141 наблюдения больных с CIN (0,73%).
Предраковые заболевания шейки матки лечатся амбулаторно и стационарно. Амбулаторное лечение включает в себя проведение радиоволновой хирургической петлевой эксцизии, которая должна выполняться всем пациенткам при наличии атипичной кольпоскопической картины, применение криотерапии и лазеровапоризации. Стационарный метод лечения предполагает проведение конизации шейки матки, ампутацию шейки матки и гистерэктомию. На сегодняшний день среди физических методов воздействия наиболее актуальными считаются радиоволновая и лазерная хирургия, которые позволяют разрушать практически любые образования.
Лечение, помимо деструкции зоны трансформации, предполагает также стимуляцию местного иммунитета и устранение факторов риска развития рецидива. Современный подход к лечению папилломавирусных поражений шейки матки предполагает применение противовирусной и иммуномодулирующей терапии, так как именно нарушения системы местного иммунитета обусловливают высокую частоту рецидивов папилломавирусных поражений шейки матки после проведенного стандартного лечения. Отличительным свойством препарата инозина пранобекс (Гроприносин®) является то, что он обладает как противовирусным, так и иммуномодулирующим действием. «Доказана высокая эффективность инозина пранобекса в отношении всех форм и типов папилломавирусной инфекции, в том числе и высокого онкогенного риска. Препарат способствует элиминации ВПЧ, снижает частоту рецидивов и восстанавливает иммунитет. Включение инозина пранобекса в комбинированную терапию генитальных кондилом существенно увеличивает эффективность лечения – с 41% до 94%», – отметил профессор С.А. Леваков (рис. 1).
Он кратко остановился на характеристике инвазивных методов лечения ВПЧ, к которым относятся: электрокоагуляция, лазеротерапия, радиоволновая хирургия, криотерапия, химиодеструкция, салицилово-резорциновый коллодий. Все методы имеют свои преимущества и недостатки, однако наиболее безопасным среди них считается метод радиоволновой хирургии, поскольку он не изменяет архитектонику шейки матки. Процедура электрохирургической петлевой эксцизии поражения внешней части шейки матки является как диагностической, так и лечебной. Пациентам с CIN II–III, а также с раком нулевой стадии первоначально проводят иммуномодулирующую терапию с санацией влагалища, затем – конизацию шейки матки или ампутацию влагалищной части шейки матки с последующим курсом иммунотерапии для профилактики рецидива заболевания. Современная тактика лечения пациентов с CIN I–II предусматривает проведение противовоспалительного лечения и иммунокорректирующую терапию. Циркулярная биопсия с помощью радиохирургического метода производится при персистенции онкогенных типов ВПЧ, наличии атипичной кольпоскопической картины. Критериями чувствительности CIN I–II степени к лечению считаются иммунологические критерии, когда снижение степени диспластических изменений коррелирует с достоверными позитивными сдвигами показателей местного иммунитета и биоценоза влагалища, и морфологические, а именно: отсутствие признаков дисплазии, снижение плоидности ядер эпителиоцитов до 2 с, снижение пролиферативной активности – экспрессии Ki-67 до 30%.
В заключение профессор С.А. Леваков подчеркнул, что лечение ВПЧ-ассоциированных заболеваний шейки матки должно быть комплексным и индивидуальным, состоящим из иммунокорригирующей терапии, терапии сопутствующих воспалительных процессов, радио- и лазерной деструкции, профилактики рецидивов и реинфекции. А решить проблему заболеваемости раком шейки матки поможет создание государственных стандартов, экспертного совета по пересмотру существующих стандартов, а также приверженность принципам доказательной медицины.
Кандидозный вульвовагинит: грани проблемы, современная терапия
Кандидозный вульвовагинит (КВВ) – это инфекционное поражение нижнего отдела гениталий, вызванное дрожжеподобными грибами рода Candida. В начале своего выступления профессор Александр Леонидович ТИХОМИРОВ (кафедра акушерства и гинекологии лечебного факультета Московского государственного медико-стоматологического университета, д. м. н.) остановился на современных проблемах КВВ, к которым относятся: значительный рост хронических форм заболевания, увеличение доли Candida non-albicans в этиологической структуре, высокая частота сопутствующего КВВ уретрита и уретроцистита (УТК), частота регистрации восходящей инфекции, угроза гематогенной диссеминации, возможность развития аутоиммунного процесса; кроме того, осложнения беременности, родов и послеродового периода. «Это самопроизвольные выкидыши на ранних сроках, угроза прерывания беременности, хориоамнионит, плацентит, преждевременное излитие околоплодных вод, преждевременные роды, послеродовый эндометрит, сепсис, внутриутробное инфицирование плода, а в 70–85% – интранатальное инфицирование плода и возможное развитие неонатального кандидоза», – уточнил докладчик.
Грибы рода Candida являются условно-патогенными аэробными микроорганизмами, лишенными половой стадии жизненного цикла, которые растут преимущественно в дрожжевой фазе. В мицелиальной или тканевой стадии развития Candida имеют гифоподобную форму, в дрожжевой стадии – округлую, эллипсоидную, овальную или цилиндрическую форму. Истинного мицелия не образуют, а за счет соприкосновения удлиненных клеток формируют псевдомицелий и митоспоры. В слабокислой среде влагалища при нормальной температуре тела создаются наиболее благоприятные условия для роста и размножения грибов рода Candida. В настоящее время описано около 200 биологических видов дрожжеподобных грибов. Самыми частыми возбудителями вульвовагинального кандидоза являются C. albicans. Но в последнее время лидирующие позиции стали занимать виды Candida non-albicans, которые ассоциируются с хроническим КВВ.
При кандидозном вульвовагините инфекционный процесс затрагивает чаще только поверхностные слои эпителия влагалища. На поверхности слизистой оболочки грибы рода Candida вступают во взаимодействие с различными представителями микрофлоры. Процесс инвазии осуществляется благодаря сочетанному действию механических и ферментных факторов и сопровождается трансформацией гриба. К факторам агрессии, способствующим проникновению возбудителя в ткань, можно отнести большой набор ферментов (протеолитические, липолитические, карбогидразы), которые продуцирует Candida. В диагностических исследованиях обнаружение инвазии грибов в морфологическом материале служит единственным неоспоримым критерием микотического процесса, отличающим его от носительства, для которого характерно нахождение грибов на поверхности эпителия. «У женщин, страдающих кандидозным вульвовагинитом, в образцах, полученных из влагалища, содержится большое количество иммуносупрессивного микотоксина – глиотоксина. У здоровых женщин глиотоксин не обнаружен», – пояснил профессор А.Л. Тихомиров.
Круглый стол компании «Гедеон Рихтер»
Существуют эндогенные и экзогенные факторы риска развития КВВ, а точнее: физиологические (беременность), механические (внутриматочная спираль, первый половой контакт, тесная синтетическая одежда), химические (спермициды, частые спринцевания), эндокринные (сахарный диабет, патология щитовидной железы), ятрогенные (прием антибиотиков, кортикостероидов, иммуносупрессоров, высокодозированных оральных контрацептивов) и иммунные (иммунодефицит). Достоверно известно, что кандидозный вульвовагинит занимает второе место среди всех вагинальных инфекций, являясь самой распространенной причиной обращения женщин к гинекологу и венерологу. Согласно официальным статистическим данным, 75% женщин детородного возраста имели один эпизод КВВ, 50% – повторный эпизод, у 40% беременных отмечался КВВ, 5% женщин страдают хроническим рецидивирующим кандидозом. Данные интернет-опроса 2108 респондентов (женщин, больных кандидозом) показали, что у 36,2% из них продолжительность КВВ составляла менее 1 года, у 44,2% – от года до 5 лет, у 19,6% – более 5 лет. Продолжительность заболевания положительно коррелировала с частотой обострения КВВ.
Различают три клинические формы генитального кандидоза: истинный кандидоз, хронический кандидоз (15–25%) и бессимптомное кандидоносительство (15–20%). Ведущая роль в диагностике кандидозного вульвовагинита принадлежит микробиологическим методам исследования. Микроскопия является одним из наиболее доступных и простых методов выявления гриба, его мицелия, спор, а также количества лейкоцитов. Исследование проводят на нативных и окрашенных по Граму препаратах. Для видовой идентификации гриба необходимо проводить культуральное исследование. В настоящее время продолжаются разработки методов полимеразной цепной реакции с праймерами, специфичными для определенных видов. Если ранее выделение грибов в диагностической концентрации при отсутствии симптомов воспалительного процесса не считалось патологией, то в настоящее время многие авторы считают целесообразным рассматривать Candida как патогенную микрофлору даже при отсутствии клинических проявлений местного воспаления. Кандидоносители инфицируют партнеров, а также новорожденных при родоразрешении. Острая форма КВВ характеризуется ярко выраженной воспалительной картиной. У пациенток с хроническим рецидивирующим КВВ на коже, слизистых оболочках вульвы и влагалища преобладают вторичные элементы в виде инфильтрации, лихенизации и атрофии тканей. Истинный хронический КВВ часто осложняется или сочетается с хроническим дерматитом кожи вульвы и промежности.
Лечение кандидозного вульвовагинита направлено на эрадикацию возбудителя. Для лечения в настоящее время используются препараты полиенового, имидазолового, триазолового ряда и пр. Согласно общим рекомендациям по лечению кандидозного вульвовагинита, при остром КВВ рекомендуется местное лечение, при хроническом КВВ – сочетание системного лечения с местной терапией, для лечения КВВ у беременных – только местная терапия. По словам докладчика, наблюдается тенденция снижения эффективности ряда противогрибковых препаратов на грибы рода Candida: так, например, некоторые исследователи (Е.Т. Мальбахова и соавт., 2009) показали снижение за последние 10 лет чувствительности грибов рода Candida к флуконазолу в 2,2 раза, к клотримазолу – в 1,9 раза, к кетоконазолу – в 2,7 раза, к итраконазолу – в 1,7 раза, к нитрофунгину – в 3 раза.
Препарат последнего поколения бутоконазол (Гинофорт®) имеет самые низкие подавляющие концентрации в отношении трех видов грибов: C. albicans, C. glabrata, C. parapsilosis – по сравнению с другими препаратами имидазолового ряда. При лечении кандидозного вульвовагинита бутоконазолом симптомы КВВ исчезают на 6–7-й день (рис. 2). Препараты для локального введения всегда пользовались популярностью и у врачей, и у пациенток благодаря высокой комплаентности, относительно низкой стоимости курса лечения в сочетании с достаточной клинической и микробиологической эффективностью. Однако у некоторых местных препаратов есть определенные недостатки, например, необходимость многократного введения при неосложненном вагинальном кандидозе, неудобства, связанные с вытеканием препарата. В отличие от них препарат Гинофорт® (бутоконазол), предназначенный для лечения КВВ, имеет более удобный режим дозирования в виде однократной интравагинальной аппликации крема. «Уникальная запатентованная биоадгезивная технология VagiSite™ (эмульсия типа “вода в масле”) позволяет бутоконазолу длительно удерживаться на влажной слизистой влагалища, медленно высвобождаться, минимизируя вытекание препарата. Гинофорт® не вытекает, в то время как на вытекание обычного крема жалуются 29% пациентов», – подчеркнул профессор А.Л. Тихомиров. Поскольку Гинофорт® содержит минеральное масло, повреждающее изделия из латекса или резины (презервативы, влагалищные диафрагмы), то в течение 72 часов после применения препарата не рекомендуется использовать данные средства контрацепции.
Профессор А.Л. Тихомиров представил следующую схему лечения острого и рецидивирующего кандидозного вульвовагинита с использованием препарата Гинофорт®: при остром КВВ препарат Гинофорт® назначается однократно; при рецидивирующем – Микосист® 150 мг двукратно + Гинофорт® однократно; поддерживающая терапия – Гинофорт® однократно после менструаций в течение 3–6 месяцев. Эффективность лечения с использованием данного метода терапии при остром КВВ достигает 95%, а при рецидивирующем – 89%. В целом же тактика ведения пациенток с хроническим рецидивирующим кандидозным вульвовагинитом включает определение вида Candida и чувствительности к антимикотическим препаратам, назначение системных препаратов с широким спектром действия; особенно перспективным является сочетание системной и местной терапии. Существуют данные, что при рецидивирующем кандидозном вульвовагините резервуаром для грибов и источником реинфекции может являться кишечник. В этой связи, по мнению докладчика, важно помнить: лечение и профилактика кандидоза слизистых оболочек половых органов могут быть неудачными без адекватного подавления грибов в кишечнике.
Алгоритмы лечения пациенток с неопластическими процессами шейки матки, ассоциированными с вирусом папилломы человека
Профессор Т.А. ОБОСКАЛОВА (зав. кафедрой ГБОУ ВПО «Уральская государственная медицинская академия», д. м. н.) познакомила участников семинара с результатами проведенного группой авторов исследования, цель которого заключалась в выявлении факторов, характеризующих локальный иммунитет вагинальной среды у пациенток с цервикальной интраэпителиальной неоплазией, и в оценке влияния инозина пранобекса на иммунитет влагалища.
Участницы исследования в возрасте 15–40 лет были разделены на две группы – основную и контрольную. В основную группу вошли 28 пациенток с установленным диагнозом «цервикальная интраэпителиальная неоплазия» (CIN) I, II, III степени, которым проводили комплексное лечение препаратом инозина пранобекс (Гроприносин®) до проведения деструкции патологических очагов шейки матки по схеме: 1000 мг 3 раза в сутки в течение 5 дней; терапевтический эффект оценивался через 30 дней после окончания терапии. Группу контроля составили 24 женщины, считавшие себя здоровыми, у которых не была выявлена патология шейки матки.
Клинические исследования включали в себя изучение гинекологического анамнеза; ПЦР-диагностику инфекций половых путей, включая ВПЧ; кольпоскопию; морфологические исследования биоптатов шейки матки. Для определения количественного содержания цитокинов в вагинальном секрете собирался определенным образом стандартный материал и исследовался уровень интерлейкинов и интерферонов. Татьяна Анатольевна Обоскалова отметила наиболее значимые свойства исследуемого препарата: «Мы применяли инозина пранобекс (Гроприносин®), который представляет собой комплекс инозина и N,N-диметиламино-2-пропанола в соотношении 1:3. Эффективность определяется инозином, диметиламинопропанол обеспечивает проникновение препарата в клетки. Препарат стимулирует функции макрофагов, регулирует продукцию интерлейкинов, повышает синтез антител, подавляет репликацию ДНК и РНК вирусов, тем самым проявляя иммуномодулирующий и противовирусный эффекты».
Клинический алгоритм ведения пациенток состоял из 5 этапов. На первом этапе при выявлении воспалительных явлений во влагалище выполнялась санация с учетом основных этиологических факторов; второй этап включал терапию Гроприносином; на третьем этапе проводилась деструкция патологических тканей шейки матки; на четвертом этапе при персистенции ВПЧ – повторный курс терапии Гроприносином; на пятом этапе проводился мониторинг ВПЧ 1 раз в 6 месяцев (рис. 3).
Гинекологический анамнез пациенток показал, что пациентки основной группы имели значительно больше инфекционных заболеваний половых органов (ВЗОМТ, вагинит, цервицит), нежели женщины контрольной группы. В структуре типов ВПЧ преобладал ВПЧ 16 типа (53%). В основной группе ВПЧ был выявлен у 26 пациенток (92,8%), в контрольной ВПЧ 16 типа был выявлен у 3 женщин (12,5%), считавшихся условно здоровыми. Морфологическое исследование биоптата шейки матки у женщин основной группы выявило преобладание цервикальной интраэпителиальной неоплазии I степени (53,1%), вторую позицию заняла CIN II степени (35,7%).
«Что нам продемонстрировали параметры вагинального иммунитета? Уровни интерферона-альфа (IFN-α) и интерферона-гамма (IFN-γ) соответствовали параметрам контрольной группы, что свидетельствует о защитной функции интерферонов при ВПЧ. Уровень иммуноглобулина А у пациенток был снижен и не достиг нормальных значений после лечения. Однако влияние инозина пранобекса было эффективным в отношении интерлейкинов. Все интерлейкины, уровень которых был повышен до начала лечения, достигали нормы после терапии Гроприносином», – констатировала профессор Т.А. Обоскалова.
Деструктивные методы лечения, применяемые у пациенток основной группы, включали аргоноплазменную аблацию шейки матки, электроэксцизию, электроконизацию. Аргоноплазменная аблация проводилась у 42,8% пациенток, электроэксцизия – у 39,2%, электроконизация – у 14,2%; в лечении 4,6% пациенток основной группы не использовались деструктивные методы. На основании результатов исследования было определено, что для женщин, больных цервикальной интраэпителиальной неоплазией шейки матки, являются характерными высокая частота воспалительных заболеваний половых путей, высокая частота заселения влагалища условно-патогенной флорой и персистенция вирусной инфекции, а в структуре типов ВПЧ преобладает 16 тип. «Мы пришли к выводу, что достоверное снижение интерлейкинов у всей исследованной группы свидетельствует о ликвидации воспалительного ответа тканей на фоне лечения Гроприносином. Иммуномодулирующий и противовирусный препарат Гроприносин® может использоваться в комплексном лечении или в монотерапии ВПЧ-инфекции у женщин», – подчеркнула профессор Т.А. Обоскалова. В заключение она отметила, что лечение интраэпителиальных поражений шейки матки должно состоять из нескольких этапов: ликвидация воспалительных процессов, противовирусная терапия, применение деструктивных методов лечения, реабилитация и последующий мониторинг.







