Доброкачественная гиперплазия простаты – новые аспекты терапии
- Аннотация
- Статья
- Ссылки




Основываясь на результатах новейших исследований патогенеза заболевания и механизмах действия лекарственных препаратов, можно сделать вывод, что медикаментозная терапия занимает важное место в лечении пациентов, страдающих ДГПЖ. На различных моделях in-vitro и in-vivo было доказано возникающее под действием индол-3-карбинола угнетение активности андрогеновых (1, 2) и эстрогеновых рецепторов (3, 4), играющих важную роль в патогенезе ДГПЖ. Также неоднократно отмечалось, что молекулы индол-3-карбинола и эпигаллокатехин-3-галлата обладают способностью ингибировать пролиферативные каскады, запускаемые ростовыми факторами и цитокинами (5, 6, 7), что приводит к торможению процессов гиперплазии предстательной железы. Индол-3-карбинол в чистом виде и стандартизированный экстракт катехинов зеленого чая содержатся в препарате Индигал, выпускаемом фармацевтической фирмой ЗАО «МираксБиоФарма». Индигал – средство нового поколения, в основе которого лежит комплексное воздействие на широкий спектр биологических процессов. Кроме блокирования андроген- и эстрогензависимого путей активации пролиферации, препарат ингибирует гормон-независимую пролиферацию, индуцирует апоптоз трансформированных клеток, снижает уровень сосудистого фактора роста и активность его рецептора. Индигал на клеточном уровне воздействует на процессы, приводящие к ДГПЖ, таким образом, предотвращая развитие заболевания на разной стадии.
Материалы и методы
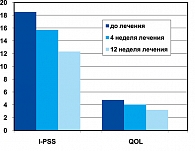
В Центре простатологии РАЕН под наблюдением находилось 35 пациентов, страдающих ДГПЖ, которым проводилась консервативная терапия доброкачественной гиперплазии предстательной железы препаратом Индигал. Распределение по стадиям было следующим: у 22 больных – 1 стадия, у 13 больных – 2 стадия ДГПЖ. У всех пациентов имелись в той или иной мере выраженные симптомы заболевания. Критериями включения в исследование были: сумма баллов по шкале I-PSS > 8, показатель индекса качества жизни QOL > 3, максимальная скорость потока мочи Qmax < 15мл/сек, объем выделенной мочи > 120 мл. Критерии исключения: наличие абсолютных показаний к хирургическому лечению ДГПЖ, наличие сахарного диабета, диабетической нейропатии, карциномы предстательной железы, присутствие в анамнезе травм или любых хирургических вмешательств в области таза, пациенты, которые во время исследования нуждаются в операции на нижних мочевых путях (за исключением единичной катетеризации), подозрение на рак предстательной железы, камни и дивертикулы мочевого пузыря, симптомы инфекции мочевых путей или хронический простатит в фазе обострения, хроническая почечная недостаточность, возможная дисфункция мочевого пузыря нейрогенного происхождения, наличие стриктуры уретры или склероза шейки мочевого пузыря в анамнезе. Средний возраст пациентов составил 65,56 ± 6,72 лет. Средние показатели оценки субъективных симптомов и индекса качества жизни до начала лечения составили: I-PSS – 18,5 ± 6,8 баллов, QOL – 4,76 ± 0,93 баллов. Средний показатель максимальной объемной скорости мочеиспускания составил
13 мл/сек (8,9 мл/сек – 15,0 мл/сек). Показатель средней скорости потока мочи Qcp до начала лечения составил 9,08 мл/сек.
По количеству остаточной мочи в мочевом пузыре (УЗИ) больные были разделены на 2 группы. В первой группе (Vres < 100мл), у 24 пациентов, среднее значение Vres составило 59,4 ± 25,08мл. Во второй группе (Vres > 100мл), у 11 пациентов, среднее значение Vres составило 124,73 мл ± 34,5.
Исследуемый препарат назначался по 2 капсулы 2 раза в день. Длительность наблюдения – 12 недель с момента начала исследования. Для оценки эффективности действия Индигала пациенты не получали других препаратов во время исследования. Всем больным до начала лечения, через 4 и 12 недель лечения проводили оценку субъективных симптомов по опроснику I-PSS с определением индекса качества жизни QOL, физикальное обследование, пальцевое ректальное исследование, ультразвуковое исследование предстательной железы при помощи трансабдоминального датчика с определением объема простаты, количества остаточной мочи, а также урофлоуметрию с определением Qmax, Qcp. Также выполнялись общие анализы мочи, крови, определялся уровень креатинина, мочевины, общего билирубина, АлТ, АсТ глюкозы, протромбиновый индекс.
Результаты
В исследование были включены 35 пациентов, страдающих ДГПЖ. Полный курс лечения на момент написания работы завершили все пациенты. Через 4 недели после начала лечения средние показатели составили: IPSS – 15,07 ± 4,91 баллов (-18,54%), QOL – 4,03 ±1,1 баллов (-15,33%). Через 12 недель лечения (n = 35) средние показатели составили: I-PSS – 12,3 ± 4,7 баллов (- 33%), QOL – 3,2 ± 1,45 баллов (-32,7%) (рисунок 1). Максимальная объемная скорость потока мочи оказалась равна 14,7 мл/сек, средняя объемная скорость мочеиспускания Qcp = 11 мл/сек. Таким образом, средние показатели I-PSS через 4 недели лечения уменьшились на 18,54% (с 18,5 до 15,07 баллов), а через 12 недель уменьшились на 33% (до 12,3 баллов) по сравнению с исходными данными. Динамика субъективных параметров мочеиспускания представлена в таблице 1.
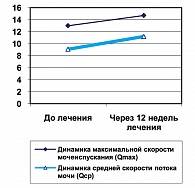
Прирост максимальной скорости мочеиспускания через 12 недель после начала лечения составил 13% (рисунок 2). Динамика среднего показателя Qmax представлена в таблице 2.
Прирост средней скорости мочеиспускания через 12 недель лечения составил 23% (рисунок 2). Динамика средней скорости потока мочи Qcp представлена в таблице 3.
Изменение объема остаточной мочи у пациентов отражено в таблице 4.
В предыдущих исследованиях отмечена прекрасная переносимость препарата Индигал, редкие побочные явления были представлены преимущественно легкими расстройствами со стороны желудочно-кишечного тракта, которые, как правило, не приводили к необходимости отмены лечения. Так и в нашем исследовании большинством больных препарат переносился хорошо, нежелательные явления были отмечены у 2 пациентов. Один пациент отмечал возникновение дискомфорта в эпигастральной области после приема препарата. Легкий кожный зуд спустя 1 неделю приема наблюдался у 1 пациента (связь явления с приемом препарата возможна). Выраженность явлений была слабой, то есть все они достаточно удовлетворительно переносились. Все нежелательные явления проходили самостоятельно и не требовали отмены препарата.
Выводы
Полученные данные свидетельствуют о том, что на фоне терапии Индигалом происходит уменьшение выраженности субъективных симптомов заболевания, уменьшение объема остаточной мочи, увеличение максимальной и средней скорости мочеиспускания, а также улучшение качества жизни пациентов. Индигал был эффективен у большинства исследуемых больных, было зарегистрировано улучшение всех параметров акта мочеиспускания. Препарат хорошо переносился больными, побочные эффекты наблюдались в 5,7% случаев, все явления были слабо выражены, не потребовали отмены препарата и исчезли самостоятельно.

