Эхографические признаки диабетической фетопатии
- Аннотация
- Статья
- Ссылки





Cогласно рекомендациям ВОЗ, в акушерской практике выделяют следующие типы СД: прегестационный инсулинозависимый СД – СД типа 1 (код по МКБ-10 – Е10); прегестационный инсулинонезависимый СД – СД типа 2 (код по МКБ-10 – Е11); гестационный СД (код по МКБ-10 – О24,4); другие типы СД, связанного с определенными состояниями и синдромами. По степени компенсации заболевания различают компенсированный и декомпенсированный СД. Из перечисленных типов СД наибольшее значение при беременности имеют – СД типа 1 и гестационный СД (ГСД). СД типа 2 играет меньшую роль, так как встречается реже и чаще развивается у женщин старше 40 лет [1, 2].
Распространенность СД среди беременных, по данным различных авторов, составляет 3–12% [1, 3]. Крайне неблагоприятное влияние диабета матери на внутриутробное развитие плода приводит к высокой перинатальной смертности – 3–15% [3, 4]. В ряде регионов России она достигает 40% [1].
В зависимости от сроков возникновения внутриутробной патологии при СД матери выделяют диабетическую гаметопатию, бластопатию, эмбриопатию и фетопатию. Диабетическая фетопатия (ДФ) – это изменения плода, возникающие с 4-го лунного месяца внутриутробной жизни. К внешним проявлениям ДФ относят такие признаки, как: одутловатое, лунообразное лицо, заплывшие глаза, короткая шея, широкий плечевой пояс, общая пастозность и ожирение туловища, гипертрихоз, короткие конечности [1]. Характерной особенностью потомства больных СД матерей является макросомия, которая отчетливо может быть выявлена после 28 недель беременности. Например, при СД типа 1 она отмечается в 25–45% случаев по сравнению с 8–14% в общей популяции [5–7]. В то же время у матерей с диабетической микроангиопатией, длительным и лабильным течением СД, беременность у которых нередко осложняется присоединением позднего гестоза, отмечается, как правило, рождение маловесных детей.
Вероятность возникновения ДФ зависит от типа СД, а также от особенностей его течения. Чаще поражение плода отмечается при тяжелом течении основного заболевания, реже – при легком его течении. Однако даже удовлетворительная коррекция углеводного обмена, отсутствие осложнений СД и беременности не гарантируют рождение ребенка без ДФ. Возможно, это обусловлено тем, что не все изменения в организме матери, приводящие к возникновению ДФ, могут быть диагностированы, в том числе с помощью лабораторных методов исследования. Так, по данным P. Greco и соавт. [8], плодам беременных с СД свойственно ожирение даже при компенсированном его течении. Признаки ДФ могут быть выявлены независимо от массы тела новорожденного, в том числе и у маловесных детей.
Выявляемые при ультразвуковом исследовании особенности роста плода у беременной с CД могут рассматриваться как проявления ДФ. Ее наличие и выраженность зависят от особенностей течения диабета матери. Одним из эхографических признаков ДФ является диспропорциональное увеличение размеров туловища плода, особенно его живота. Его лабильный рост, прежде всего, обусловлен динамикой увеличения размеров печени плода, которая напрямую зависит от уровня гликемии у беременной с СД [9]. При декомпенсированном течении СД увеличение размеров печени плода может быть отмечено уже во II триместре беременности, а в III триместре беременности при СД матери они достоверно превышают таковые у плодов здоровых беременных.
Диагностировать гепатомегалию можно по результатам определения продольного, вертикального и поперечного размеров печени плода. Полученные данные сравнивают с нормативными значениями в зависимости от гестационного возраста плода. Однако непосредственное измерение печени плода во время ультразвукового исследования, подтверждающее ее увеличение при СД, может вызывать определенные трудности, обусловленные особенностями положения плода. Косвенной характеристикой гепатомегалии могут служить размеры живота плода, определяемые на уровне пупочной вены, так как именно печень у плода занимает основной объем брюшной полости [10], а увеличение других внутренних органов и толщины его мягких тканей выражено не до такой степени, чтобы этими изменениями можно было бы объяснить столь интенсивное увеличение диаметра его живота. К тому же, печень является одним из основных органов, депонирующих гликоген, необходимость в чем у плодов беременных, больных СД, значительно выше, чем в норме. Напротив, при строгом соблюдении диабетического контроля и, соответственно, компенсированном течении сахарного диабета различий в росте плода у больной диабетом беременной, по сравнению с таковым в общей популяции, не выявляется [11].
С.С. Феоктистова и соавт. [12] считают патогномоничными эхографическими признаками ДФ – макросомию и висцеромегалию, выявляемые с 32 недель, и к 35–36 неделям беременности отмечаемые у 20% плодов больных диабетом беременных. В свою очередь, E. Koukkou и соавт. [13] считают характерным для потомства больных СД матерей – маленьких размеров голову и ожирение, даже у детей с нормальным весом. A. Weissman и P. Jakobi [14] установлено, что при ДФ отмечается увеличение диаметра пупочного канатика. В этой связи авторы предлагают использовать этот показатель как маркер ДФ. Еще одним способом диагностики ДФ является определение отношения расстояния между щеками плода к его бипариетальному размеру (БПР). У плодов здоровых беременных это отношение находится в пределах 0,6 (в 20 недель) – 0,7 (в 41 неделю), то есть практически не зависит от гестационного возраста плода. При ДФ оно больше нормы, а при макросомии, не связанной с диабетом, оно соответствует нормативным показателям [15].
Щечная область плода является одним из основных мест локализации его жировых клеток. В этой связи, а также исходя из того, что для плодов с ДФ характерно ожирение, М.С. Валид и соавт. [16] предложили оценивать так называемый букальный коэффициент, позволяющий судить о толщине подкожно-жировой клетчатки в проекции щек плода. Для этого проводится измерение расстояния от наружного уголка рта до наружной поверхности щеки плода параллельно нижней границы орбиты. У плодов без признаков ДФ данный коэффициент в 34–36 недель составляет 10–20 мм. При ДФ даже у плодов с нормотрофией и гипотрофией этот показатель больше 20 мм. Диагностическая точность теста, по данным авторов, составляет 94% (чувствительность – 92,5%; специфичность 86,7%).
Эти же авторы предложили еще ряд эхо-признаков ДФ, а именно:
- незернистая эхогенность печени плода, обусловленная отеком гепатоцитов и межклеточного пространства; диагностическая точность теста – 78%; чувствительность – 80,7%; специфичность – 75,8%. Выявление этого признака в сочетании с гепатомегалией повышает точность диагностики ДФ до 98% (чувствительность – 100%; специфичность – 89%);
- смещение эхо-тени желудка плода к его позвоночнику, что обусловлено увеличением в размерах левой доли печени плода; диагностическая точность теста – 66%; чувствительность – 72%; специфичность – 65%.
Уместно отметить, что из предложенных М.С. Валид. и соавт. [16] диагностических тестов ДФ лишь букальный коэффициент является объективным, так как может быть охарактеризован метрической величиной. При этом его определение может быть затруднено ввиду особенностей положения головы плода. Выявление же других признаков ДФ базируется на субъективных оценках эхографической картины специалистом, выполняющим ультразвуковое исследование, что, безусловно, снижает их диагностическую ценность.
Наиболее простым для регистрации объективным признаком ДФ является диспропорциональный рост туловища плода. Наглядным его подтверждением может служить динамика отношений средних диаметров его груди и живота к БПР. Если при физиологически протекающей беременности рост плода характеризуется небольшими колебаниями показателей этих отношений, то при СД матери они претерпевают значительные изменения. Диспропорциональный рост туловища плода у беременной с СД типа 1, оцениваемый по отношению среднего диаметра груди (СДГ) к величине БПР, может отмечаться с 26 недель беременности (рис. 1), а по отношению среднего диаметра живота (СДЖ) к БПР – уже с 24 недель беременности (рис. 2). Наиболее он выражен, как правило, в период с 30 до 35 недель. Так, если у плодов здоровых беременных отношение СДГ/БПР с 0,98 в 30–31 неделю увеличивается до 1,01 в 34–35 недель беременности, то у плодов беременных с СД оно возрастает соответственно с 1,09 до 1,16. В свою очередь, отношение СДЖ/БПР у плодов здоровых беременных с 1,04 в 30–31 неделю увеличивается до 1,08 в 34–35 недель беременности, а у плодов беременных с СД оно возрастает в эти сроки с 1,18 до 1,25. При ГСД диспропорциональный рост туловища плода носит менее выраженный характер, но если при этом интенсивный рост груди отмечается с 28 недель беременности, то живота – так же как и при СД типа 1 с 24 недель (рис. 1, 2).
Другим демонстративным эхографическим признаком ДФ является двойной контур плода, обусловленный увеличением у него подкожно-жирового слоя и/или его отеком. Объективная оценка выраженности жирового слоя плода позволяет судить об особенностях течения СД у беременной [17]. При компенсированном течении СД такой признак ДФ, как двойной контур головы плода, не определяется. Напротив, его наличие является следствием метаболических нарушений, обусловленных декомпенсированным течением СД матери. Подтверждением этому является установленная нами прямая связь между НbА1с у беременных с СД в III триместре беременности и толщиной мягких тканей теменной области головы плода: r = 0,39 (р < 0,01). Нормализация уровня гликемии у беременной и, соответственно, у ее плода может привести к его уменьшению. Ожирение и отек плода – факторы, определяющие наличие и выраженность эхографически выявляемого «двойного контура» плода. Вот почему его регистрация при ультразвуковом исследовании свидетельствует о декомпенсированном течении диабета у беременной, даже если на это не указывают результаты лабораторного контроля, и является поводом для более детального проведения последнего.
С целью выяснения возможностей ультразвуковой диагностики ДФ по результатам фетометрии был проведен анализ связи между биометрическими данными, полученными накануне родов, и состоянием новорожденного, включающего в себя выявление и оценку выраженности ДФ. При фетометрии определяли такие величины, как: бипариетальный и лобно-затылочный размеры головы плода с последующим определением среднего диаметра головы (СДГол) плода, межполушарный размер мозжечка (МРМ), СДЖ, длину бедра (ДБ), а также толщину мягких тканей теменной области головы плода. В результате достоверно установлено, что наиболее информативными эхографическими признакам ДФ являются: утолщение мягких тканей теменной области головы плода, увеличение отношения СДЖ/МРМ и увеличение отношения СДЖ/ДБ (табл. 1). Предпочтение из указанных отношений может быть отдано последнему как показателю, который основан на биометрии, проводимой при скрининговом исследовании. К тому же, дифференцирование контуров мозжечка и, соответственно, определение его размеров может быть затруднено, особенно в сроки доношенной беременности.
Таким образом, проведение ультразвукового исследования во второй половине III триместра беременности позволяет диагностировать ДФ, объективно оценивать степень ее выраженности, что может способствовать рациональному ведению беременных с СД.
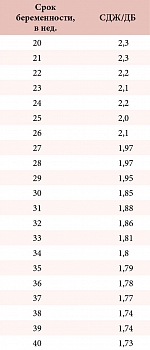
Выраженность ДФ у потомства больных СД матерей связана со сроками ее возникновения, а также с динамикой ее развития в период их внутриутробного роста. Чем раньше у плода беременной с СД выявлены признаки ДФ и чем активнее они нарастают, тем больше они будут выражены при его рождении. Такое положение указывает на неблагоприятное течение диабета у беременной и сложности с его компенсацией. Например, при рассмотрении связи между началом регистрации диспропорционального роста туловища плода и выраженностью ДФ у новорожденного коэффициент корреляции (r) составил – 0,34. Диспропорциональность плода оценивалась по отношению СДЖ/ДБ. Для этого на основании процентильных таблиц, отражающих рост СДЖ и ДБ у плодов в общей популяции [18], была определена условная верхняя граница нормы для отношения СДЖ/ДБ (табл. 3).
Коэффициент корреляции, характеризующий связь между динамикой развития диспропорциональности плода и выраженностью ДФ у новорожденных, составил 0,57. В свою очередь, связь между началом появления признака «двойной контур» плода, а также его динамикой – с одной стороны, и выраженностью ДФ – с другой, была охарактеризована, соответственно, как r = -0,76 и r = 0,82.
Типичным клиническим признаком неблагоприятного влияния СД на течение беременности (декомпенсированного течения СД во время беременности) является многоводие. Его своевременное выявление способствует выбору рациональной тактики ведения беременных и рожениц и, соответственно, снижению перинатальной патологии и смертности их потомства. При этом ультразвуковая диагностика зарекомендовала себя как простой и достаточно надежный метод его определения. Вместе с тем при ультразвуковом исследовании визуально может быть установлено только выраженное многоводие, тогда как незначительное увеличение количества околоплодных вод установить практически невозможно. Связано это с тем, что современная ультразвуковая диагностическая аппаратура не позволяет достаточно точно определить объем амниотической жидкости.
Традиционно при ультразвуковом исследовании многоводие диагностируется в случае увеличения свободных от эхо-структур пространств, оцениваемых проводящим исследование специалистом субъективно на основании имеющегося у него опыта работы. С целью повышения точности оценки количества околоплодных вод рекомендуется проводить измерение зон, не занятых частями плода и пуповиной. У здоровых беременных вертикальный размер любой из выбранных для оценки зон не должен превышать 8 см [19]. Согласно предложению L.M. Hill и соавт. [20], глубина кармана вод 8–12 см свидетельствует об умеренном многоводии, 12–16 см – о многоводии средней степени выраженности, 16 см и более – о выраженном. C.J. Sivit и соавт. [21] разработали свою классификацию многоводия. В ней выделено многоводие средней степени тяжести – когда выявляются один или два кармана вод глубиной более 7,0 см; и тяжелое – когда визуализируется множество карманов глубиной более 7,0 см.
Наиболее распространенным способом оценки количества околоплодных вод в настоящее время является определение индекса амниотической жидкости. Он основан на определении суммы вертикальных размеров зон, выделенных в четырех квадрантах беременной матки. При физиологическом течении беременности, согласно разным источникам, она не должна превышать либо 18, либо 20, либо 24 см. При этом индекс амниотической жидкости, превышающий последнее значение, рассматривается как наиболее достоверный признак многоводия [22–25].
Однако даже такой подход не лишен, на наш взгляд, существенных недостатков. Во-первых, не исключена зависимость регистрируемых данных от особенностей расположения плода и его двигательной активности. Во-вторых, не исключен субъективизм в выборе измеряемых зон. Следует подчеркнуть, что при оценке количества амниотической жидкости большое значение имеет расположение плода в полости матки. При поперечном положении плода, а также при его расположении в непосредственной близости к стенке матки может создаваться впечатление многоводия. Кроме того, выбор и измерение оцениваемых зон могут быть затруднены ввиду совершаемых плодом движений.
С целью более объективной оценки количества околоплодных вод и динамического за ними наблюдения может быть использована разница между переднезадним размером полости матки (ПЗРПМ) как наименее вариабельным по сравнению с ее длиной и шириной [26] и СДЖ плода как самой крупной его частью. К тому же выбор параметров продиктован возможностями современной ультразвуковой диагностической аппаратуры и стремлением к минимальной затрате времени для их определения. Измерение ПЗРПМ проводится приблизительно на границе верхней и средней трети тела матки в месте, неэкранированном туловищем плода. Обязательным условием является получение четких контуров передней и задней стенок, между внутренними поверхностями которых и осуществлялось измерение независимо от локализации плаценты (рис. 3).
Установлено, что при физиологическом течении беременности происходит постепенное уменьшение разницы между ПЗРПМ и СДЖ плода (рис. 4), причем в III триместре этот показатель чаще всего не превышает 1,5 см [27]. При доношенной беременности отмечается его некоторое увеличение. Так, если до 37 недель включительно он находится в пределах 1,6–2,5 см только у 11,3% обследованных, то в 38–41 недель – у 19,1%. Вероятно, это обусловлено перераспределением накануне родов тонуса матки с изменением формы ее полости.
В свою очередь, анализ результатов исследований беременных с СД показал, что на протяжении всего II и III триместров беременности разница между ПЗРПМ и СДЖ плода превышает таковую у здоровых беременных (рис. 4). При СД типа 1 с 26–27 недель отмечается значительное и статистически достоверное ее увеличение, наиболее выраженное с 30 недель. При ГСД достоверное увеличение разницы между ПЗРПМ и СДЖ плода отмечается с 30–31 недель беременности.
В III триместре беременности может использоваться следующая упрощенная классификация количества околоплодных вод: положительные значения разницы между ПЗРПМ и СДЖ плода, не превышающие 1,5 см, расцениваются как отражающие физиологическое количество амниотической жидкости; находящиеся в пределах 1,6–2,0 см – как намечающееся многоводие (состояние пограничное между нормой и патологией); находящиеся в пределах 2,1–3,0 см – как умеренное; и превышающие 3,0 см – как выраженное многоводие. В ряде случаев при ультразвуковом исследовании могут быть зарегистрированы отрицательные значения разницы между ПЗРПМ и СДЖ плода. Их трактовка требует уточнения, которое, не исключено, позволит выработать критерии оценки степени выраженности маловодия.
Выявление многоводия является поводом для проведения детального исследования, направленного на диагностику СД, так как не всегда слепой отбор проб на глюкозу, взятых как натощак, так и после еды, может выявить нарушение углеводного обмена. Однако при этом увеличение объема амниотической жидкости не является весомым признаком ДФ.
Следует иметь в виду, что ряд диагностируемых при ультразвуковом исследовании признаков ДФ может отмечаться и при других патологических состояниях плода, например, при гемолитической болезни и неиммунной водянке плода. При гемолитической болезни средней степени отмечается увеличение размеров живота плода (вследствие гепатоспленомегалии) и увеличение размеров плаценты. При СД матери также нередко регистрируется интенсивный рост плаценты. Наблюдаемый эффект является следствием протекающих в плаценте при СД матери гиперпластических процессов, обусловленных реализацией компенсаторно-приспособительных реакций, вызванных, в свою очередь, хронической внутриутробной гипоксией плода – патологией, характерной для течения беременности при СД матери.
При гемолитической болезни тяжелой степени, наряду с вышеуказанными признаками, может отмечаться отек плода (симптом «двойного контура»), выпот в полостях (асцит, гидроторакс, гидроперикард) и многоводие. Одним из способов дифференциальной диагностики является уточнение резус-принадлежнос-ти крови у обследуемой беременной с определением титра антител, увеличение которого при отечной форме ГБ особенно выражено.
При неиммунной водянке отмечаются: отек плода (симптом «двойного контура»), выпот в полостях плода (асцит, гидроторакс, гидроперикард), аномалии развития плода (пороки сердечно-сосудистой системы – почти в 50% случаев), увеличение размеров плаценты, многоводие [28, 29].
Таким образом, наиболее значимым отличительным признаком гемолитической болезни тяжелой степени и неиммунной водянки плода является выпот в полостях плода, что не характерно для ДФ.

