Клинический опыт применения алендроната для лечения остеопороза
- Аннотация
- Статья
- Ссылки
Первичный остеопороз условно делится на постменопаузальный и сенильный. Постменопаузальный ОП связан с ускоренной потерей костной массы у женщин после прекращения менструаций, причина его развития – дефицит эстрогенов. Наиболее выраженные изменения на фоне дефицита эстрогенов происходят в трабекулярной кости. Активация костного обмена на тканевом уровне характеризуется увеличением количества активированных единиц костного ремоделирования, наряду с увеличением резорбции возрастает и формирование костной ткани, однако оно не может полностью компенсировать резорбцию, вследствие чего увеличивается нестабильность костной трабекулярной архитектоники, что приводит к повышенному риску развития переломов трабекулярных костей.
Сенильный ОП характеризуется пропорциональными потерями трабекулярной и кортикальной кости. Основными причинами развития сенильного ОП у лиц обоего пола являются снижение потребления кальция, нарушение его всасывания в кишечнике и дефицит витамина D, что может приводить к вторичному гиперпаратиреозу и вследствие этого ускорению костного ремоделирования. Одним из факторов, влияющих на развитие сенильного ОП, считают снижение физической активности в пожилом возрасте. Необходимо подчеркнуть, что в процессе старения организма взаимодействие гормонов с факторами роста и другими цитокинами, влияющими на процесс остеобластогенеза, подвергается существенным изменениям, а активность многих локальных факторов снижается. Гистоморфометрические исследования показали значительное уменьшение количества остеобластов у данных больных, а также замедление процессов ремоделирования (снижение остеобластогенеза и остеокластогенеза, уменьшение продолжительности жизни остеоцитов).
ОП развивается постепенно и клинически нередко выявляется уже после переломов, что послужило основанием называть его «скрытой эпидемией». Так, в московской популяции частота ОП в возрасте 50 лет и старше у женщин составила 33,8%, а у мужчин – 26,9%. Следует отметить, что частота ОП повышается с возрастом, поэтому наблюдаемое в последние десятилетия увеличение продолжительности жизни в развитых странах и связанный с ним быстрый рост числа пожилых людей, особенно женщин, ведет к нарастанию частоты этого заболевания, делая его одной из важнейших проблем здравоохранения во всем мире.
Лечение ОП представляет непростую задачу, так как он диагностируется достаточно поздно, когда уже имеются переломы различной локализации, часто выявленные случайно. Лечение должно быть длительным, поскольку эффект может проявиться спустя много месяцев. Целью лечения является замедление, а если это возможно, прекращение потери костной массы, предотвращение переломов костей, улучшение состояния больного, уменьшение болевого синдрома, улучшение качества жизни.
В настоящее время препаратами выбора для лечения и профилактики ОП являются лекарственные средства класса бисфосфонатов (БФ). Их действие основано на снижении скорости костного обмена при сохранении костной микроархитектоники и повышении минеральной плотности кости (МПК).
Одним из препаратов класса БФ является алендронат, который в течение уже почти 15 лет широко применяется в клинической практике во всем мире. При лечении алендронатом происходит подавление процессов резорбции остеокластами и восстановление процессов метаболизма костной ткани до пременопаузального уровня, в результате он предотвращает микроархитектурные нарушения и потерю костной ткани. Процессы костного метаболизма остаются стабильными при длительном лечении алендронатом в течение 10 лет, при этом накопление препарата в кости не приводит к излишней суппрессии костного обмена, а напротив, было показано, что костный обмен остается на пременопаузальном уровне, а качество кости остается нормальным в течение всего периода лечения.
Данные фармакокинетических исследований подтвердили, что эффективность действия БФ на массу и силу кости зависит от кумулятивной дозы этих препаратов. Так, одно и то же количество алендроната абсорбируется при однократном приеме 70 мг 1 раз в неделю или 10 мг 7 раз в неделю.
Эффективность применения алендроната у больных ОП была доказана в ходе проведения нескольких рандомизированных клинических двойных слепых плацебо-контролируемых исследований (РКИ). Наиболее крупные из них: FOSIT – многоцентровое (34 страны) РКИ, включавшее 1908 постменопаузальных женщин с ОП, получавших ежедневно в течение 12 месяцев 10 мг алендроната (2), и исследование FIT – многоцентровое (11 центров в США) РКИ, включавшее 2027 постменопаузальных женщин, получавших 5 мг и 10 мг алендроната в течение трех лет (3), а также длительное 10-летнее наблюдение пациентов, продолжавших получать 5 мг либо 10 мг алендроната или плацебо (4). Прием алендроната показал высокую эффективность: повышая МПК во всех областях измерения от 5,4% в шейке бедра до 13,7% в позвоночнике, достоверно снижал частоту переломов в позвоночнике (на 47%), бедре (на 51-56%) и предплечье (на 48%), а у 64% больных уменьшилось прогрессирование деформаций позвонков (3, 5).
При приеме пероральных БФ большое внимание уделяется нежелательным явлениям (НЯ), связанным с поражением желудочно-кишечного тракта. Следует отметить, что в ходе проведенных исследований частота всех НЯ при приеме 10 мг алендроната в день не превышала таковую в группе плацебо (3).
Как продолжение исследования FIT, было проведено исследование FLEX, оценившее динамику МПК через 10 лет в группах больных, принимавших алендронат в течение всего этого периода или переведенных на плацебо спустя первые пять лет активной терапии. У женщин, продолжавших получать 10 мг/сут. алендроната, происходило постепенное повышение МПК позвоночника до 13,7% (p < 0,001), а МПК бедра до 6,7% (p < 0,001) относительно исходного уровня. В результате приема алендроната снижался уровень маркеров костного метаболизма до пременопаузального уровня, который оставался стабильным в течение всего 10-летнего периода без признаков сверхсупрессии. По сравнению с основной группой у лиц, принимавших плацебо в течение последних 5 лет, было отмечено снижение МПК в общем показателе бедра (–2,4%; 95% ДИ 2,9%; –1,8%; р < 0,001) и поясничном отделе позвоночника (–3,7%; 95% ДИ 4,5%; –3,0%; р < 0,001), однако средние значения МПК оставались выше исходного уровня при включении в исследование. Через 5 лет общий риск периферических переломов не различался достоверно между группами (ОР 1,00; 95%; ДИ 0,76; 1,32). У продолживших терапию алендронатом был значительно меньше риск клинически выраженных переломов позвонков: так, в группе плацебо они встречались у 5,3% пациенток, а в группе алендроната – у 2,4% (ОР 0,45; 95%; ДИ 0,24; 0,85). Для переломов, выявляемых при рентгеноморфометрии позвоночника, такой закономерности обнаружено не было (11,3% и 9,8% соответственно; ОР 0,86; 95%; ДИ 0,60; 1,22). Небольшое число биопсий подвздошной кости не выявило никакой качественной патологии костной ткани. Таким образом, данное исследование показало, что прекращение лечения через 5 лет значимо не повышает риск переломов, однако женщины с высоким риском клинических переломов позвонков должны продолжить лечение свыше 5 лет (4).
В 2008 г. опубликован систематический обзор Кокрановской электронной библиотеки (Cochrane Database…), который включил 11 РКИ (12068 женщин), опубликованных в период 1966-2007 гг. Оценивался эффект приема алендроната в дозе 10 мг/сут. на протяжении года и более по сравнению с плацебо на фоне приема кальция и витамина D. При вторичной профилактике значимое снижение относительного риска переломов доказано для позвонков на 45% (ОР 0,55, 95%; ДИ 0,43; 0,69) с уменьшением абсолютного риска на 6%, периферических переломов на 23% (ОР 0,77; 95%; ДИ 0,64; 0,92) со снижением абсолютного риска на 2%, переломов бедра на 53% (ОР 0,47; 95%; ДИ 0,26; 0,85) с уменьшением абсолютного риска на 1%, переломов предплечья на 50% (ОР 0,50; 95%; ДИ 0,34; 0,73) с уменьшением абсолютного риска на 2%. При первичной профилактике показано только снижение риска переломов позвонков на 45% (ОР 0,55; 95%; ДИ 0,38; 0,80) (6).
В крупномасштабном РКИ было показано, что прием 70 мг алендроната один раз в неделю обеспечивает терапевтическую эквивалентность ежедневной дозе препарата 10 мг, одновременно лучшую переносимость и удобство применения (7-10). Так, прирост МПК составил 6,8% и 7,4% соответственно в позвоночнике, 4,1-4,3% в бедре. Двухлетнее наблюдение за пациентами, получавшими различные дозы алендроната, показало, что частота переломов в группе 70 мг 1 раз в неделю была 7,3%, а в группе 10 мг/сут. – 7,0% (p < 0,05). Имеются бесспорные доказательства снижения риска переломов при приеме 10 мг алендроната ежедневно, а отсутствие различий в частоте возникновения переломов на обеих дозах, сопоставимое повышение МПК, и аналогичные изменения уровней маркеров костного обмена наводят на мысль о схожем влиянии данных дозировок на риск переломов. На биопсийном материале не было выявлено признаков остеомаляции при приеме обеих доз препарата.
В сравнительном исследовании было показано, что частота желудочно-кишечных НЯ (эзофагит, эрозии, геморрагии, рефлюкс, гастрит, язва желудка и др.) в группах, получавших различные дозы алендроната, была схожей, т. е. увеличение однократно принятой дозы в 7 раз не увеличивало риск развития НЯ (7, 10).
В НИИР РАМН проведено изучение эффективности и безопасности алендроната (ФосамаксÒ) 70 мг в неделю в ходе открытого одногодичного контролируемого исследования, в которое были включены 90 амбулаторных пациенток (средний возраст 64,8 ± 7,6 лет): 58 человек принимали алендронат (ФосамаксÒ) 70 мг 1 раз в неделю в сочетании с 500-1000 мг кальция и 400-800 МЕ витамина Д3; 32 женщины наблюдались в качестве контрольной группы и принимали только 1000 мг кальция и 400-800 МЕ витамина D3 (11). Группы были сопоставимы по возрасту, росту и весу, индексу массы тела (ИМТ), продолжительности менопаузы. Все пациентки имели остеопороз в одной из областей измерения (поясничный отдел позвоночника L1-L4 и/или шейка бедра). Оценка эффективности лечения велась по динамике МПК, болевого синдрома и влиянию его на активность пациента, регистрации переломов. При проведении оценки эффективности и безопасности препарата статистический анализ проводился как на всей популяции, включенной в исследование (Intent-to-treat – ITT), так и на группе, закончившей лечение или наблюдение по протоколу (per protocol – PP).
Через 12 месяцев после окончания исследования пациенты, не получавшие активного антирезорбтивного лечения, повторно были приглашены в клинику для оценки последействия алендроната. Всего в изучении последействия приняли участие 49 человек: 35 – из основной группы, кто закончил исследование по протоколу, и 14 – из контрольной (средний возраст 64,0 ± 7,3 лет и 65,2 ± 6,8 лет соответственно, р = 0,63).
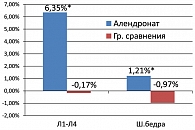
При сравнении динамики МПК между группами был получен достоверный прирост в L1-L4 и в области шейки бедра у больных, получавших алендронат относительно группы сравнения (р = 0,00001 и р = 0,030 соответственно). В других областях достоверных различий между группами не было выявлено (рисунок 1).
При проведении IIT-анализа прирост МПК в группе лечения составил 5,31% в L1-L4, что было достоверно выше, чем в группе сравнения (р = 0,00001), в проксимальном отделе бедра значимых различий между группами получено не было.
При оценке количества пациентов со значимым приростом или снижением МПК в позвоночнике и проксимальном отделе бедра было выявлено, что в группе, получавшей лечение алендронатом, 85,7% пациентов имели прирост более 2% в L1-L4 и 42,8% лиц – в области шейки бедра, а 38,8% имели значимый прирост в обеих областях измерения, что было достоверно выше, чем в группе сравнения (р = 0,01). При этом прирост МПКТ более 6% в позвоночнике встречался у 53% женщин, получавших алендронат, и у 6,3% лиц в группе сравнения (р = 0,00004), а в шейке бедра – прирост более 3% у 30,6% и 12,5% женщин соответственно (р = 0,06). Кроме того, при приеме алендроната было достоверно больше женщин, положительно ответивших на лечение, чем женщин, у которых эффект отсутствовал (р < 0,001).
Основной конечной точкой, определяющей эффективность антирезорбтивного препарата, является влияние его на снижение риска переломов. В ходе проведения исследования у двух пациенток из группы лечения алендронатом возникли переломы: у одной – перелом двух ребер при автомобильной аварии, у второй – перелом костей таза вследствие падения с дерева. В группе контроля также произошли два перелома – оба перелома предплечья в результате падения с высоты своего роста, т. е. в результате минимальной травмы. Не было выявлено новых деформаций позвонков через 12 месяцев лечения ни в одной из групп при повторном морфометрическом анализе рентгенограмм позвоночника. Полученные в нашем исследовании данные не позволяют сделать вывод о влиянии алендроната на риск переломов вследствие небольшого количества как переломов, так и срока наблюдения за пациентами. Однако мета-анализ, проведенный M.C. Hochberg с соавт. (12), продемонстрировал, что увеличение МПК L1-L4 на 6% и более в год на фоне приема антирезорбтивных препаратов снижал риск периферических переломов на 39%, а прирост МПК в шейке бедра на 3% и более снижал риск данных переломов на 46%.
Эффективность лечения алендронатом также оценивалась по влиянию его на болевой синдром и ограничение физической активности (ОФА). Снижение болевого и ОФА индексов отмечалось уже через 3 месяца лечения и продолжало уменьшаться в течение всего периода наблюдения (р = 0,04 и р = 0,008, соответственно). В группе сравнения статистически значимых различий по данным показателям получено не было (р > 0,05).
Побочные эффекты регистрировались как в основной группе, так и группе сравнения на фоне приема только препаратов кальция и витамина D. Нами не было получено значимых различий по частоте побочных эффектов между группами. В группе, получавшей алендронат, метеоризм и запоры были связаны не с приемом основного препарата, а с сопутствующим приемом карбоната кальция, после отмены которого данные нежелательные явления проходили.
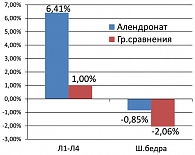
Через год после окончания исследования 49 пациенток, которые не получали в течение этого времени антирезорбтивной терапии, кроме препаратов кальция и витамина D3, вновь посетили клинику для контроля. При оценке МПК в поясничном отделе позвоночника и проксимальном отделе бедра было выявлено, что в группе, получавшей лечение алендронатом, сохранялся достоверный прирост МПК в L1-L4 относительно показателей при включении в исследование и по сравнению с группой контроля (р = 0,000062), а в проксимальном отделе бедра различия между группами были статистически не достоверными (p > 0,05) (рисунок 2).
При анализе рентгеноморфометрий у 1 пациентки (2,9%) основной группы, имевшей в анамнезе уже 2 остеопоротических перелома позвонков, была выявлена новая деформация позвонка 1 степени; в группе сравнения у 1 пациентки (7,1%) произошел перелом хирургической шейки плечевой кости, возникший при падении с высоты роста. В результате за весь период наблюдения в основной группе было диагностировано 3 перелома: 2 травматических периферических перелома и 1 деформация позвонка, а в группе сравнения 3 периферических перелома при минимальной травме (р > 0,05).
Таким образом, наше исследование показало высокую эффективность алендроната в дозе 70 мг 1 раз в неделю при лечении первичного остеопороза у женщин в постменопаузе: он оказывал положительный эффект на МПК, снижал болевой синдром и вследствие этого снижал ограничение физической активности пациенток. Отмечена достаточно хорошая переносимость препарата, побочные эффекты в группе лечения были сопоставимы с таковыми в группе сравнения. Анализ действия алендроната показал, что он обладает последействием в течение 12-месячного периода после окончания лечения в отношении МПК позвоночника.
Алендронат эффективен и у мужчин, как и у женщин, для профилактики и лечения глюкокортикоидного (ГК) остеопороза как в отношении увеличения МПК, так и снижения риска переломов (13). Принципиальные доказательства эффективности алендроната получены в рандомизированном клиническом исследовании с плацебо-контролем, в котором мужчины и женщины (n = 477) с вновь назначенными ГК (34% пациентов) либо с ГК-терапией, продолжавшейся более 4 месяцев (66% пациентов), находились под наблюдением более 48 недель. Положительные эффекты лечения в течение 12 месяцев на МПК были статистически достоверны в поясничном отделе позвоночника и шейке бедра. Отмечено, что в группе алендроната новых переломов позвонков за период наблюдения возникло меньше, чем в группе плацебо (2,3% и 3,7% соответственно, p > 0,05). В последующем наблюдении за 208 пациентами была продемонстрирована эффективность терапии алендронатом в течение второго года и доказано значительное уменьшение числа новых переломов позвонков в группе алендроната (0,7%) по сравнению с группой плацебо (6,8%; p = 0,026) (10).
Согласно многочисленным данным, среди лиц, страдающих остеопорозом, выявляется большой процент пациентов с низкими показателями уровня витамина D. Учитывая низкую приверженность потреблению таблетированных форм витамина D, был разработан комбинированный препарат алендроната 70 мг и витамина D 2800 МЕ (Фосаванс). В РКИ продолжительностью 15 недель было показано, что совместное применение этих компонентов в одной таблетке не снижает антирезорбтивную эффективность алендроната и позволяет поддерживать достаточный уровень витамина D в сыворотке крови у больных остеопорозом. В ходе исследования не отмечено развития гиперкальциемии, а гиперкальциурия встречалась с одинаковой частотой (3,9%) как в группе, получавшей комбинированный препарат, так и монотерапию алендронатом. Таким образом, добавление в таблетированную форму витамина D в дозе 2800 МЕ не увеличивало риск данных осложнений. Переносимость комбинированного препарата была сопоставима с монотерапией алендронатом (14).
Следует помнить, что алендронат необходимо принимать натощак сразу после подъема с постели, таблетку нужно запивать 1 стаканом (180-240 мл) чистой воды, а после приема следует находиться в вертикальном положении (сидя или стоя), в течение как минимум 30 минут. БФ могут вызывать побочные эффекты, связанные с поражением ЖКТ, а также головную боль, боли в мышцах и костях, снижение уровня кальция и фосфора в сыворотке крови, в редких случаях – сыпь и эритему. При передозировке БФ – гипокальциемия и гипофосфатемия, расстройства ЖКТ. Однако соблюдение рекомендаций по приему препарата значительно снижает риск возникновения желудочно-кишечных НЯ. Противопоказания к назначению: гиперчувствительность к препарату, стриктура и ахалазия пищевода, тяжелая почечная недостаточность (клиренс креатинина ниже 35 мл/мин), гипокальциемия, беременность и грудное вскармливание, детский возраст, тяжелый гипопаратиреоз, мальабсорбция кальция.

