Место гепатопротекторов в сопровождающей терапии онкологических заболеваний. XXI Российский онкологический конгресс. Сателлитный симпозиум компании «Полисан»
- Аннотация
- Статья
- Ссылки





Поддерживающее лечение при проведении полихимиотерапии. Опыт применения Ремаксола
Профессор кафедры факультетской хирургии и онкологии Саратовского государственного медицинского университета (СГМУ) им. В.И. Разумовского Минздрава России, хирург-онколог, профессор, д.м.н. Ольга Михайловна КОНОПАЦКОВА поделилась собственным опытом применения гепатопротекторов в качестве препаратов поддерживающей терапии.
Как известно, при распространенных новообразованиях у больных на фоне заболевания, а также при использовании агрессивных режимов противоопухолевой терапии развивается интоксикация. Поиск гепатопротекторов, способных защитить печень от токсического воздействия и усилить детоксикацию организма, в онкологической практике особенно актуален.
Сегодня на российском фармацевтическом рынке представлен широкий спектр лекарственных средств с гепатопротективными свойствами. Однако выбрать препарат с минимальными нежелательными явлениями и максимальной эффективностью трудно. В идеале препарат должен способствовать не только регенерации митохондриальной мембраны (липидный бислой мембраны клетки), но и восстановлению клеточного, энергетического и пластического обмена в печени.
Идеальный гепатопротектор соответствует следующим критериям:
- полная абсорбция;
- наличие эффекта «первого прохождения» через печень;
- связывание высокоактивных повреждающих соединений;
- уменьшение воспаления;
- подавление фиброгенеза;
- стимуляция регенерации печени;
- отсутствие токсичности.
При выборе препарата не последнюю роль играет его экономическая доступность. Важно также, чтобы препарат в короткий срок обеспечивал максимальный эффект. В связи с этим особый интерес представляет отечественный препарат Ремаксол®, в состав которого входят янтарная кислота, N-метилглюкамин, рибоксин, метионин, никотинамид. Это первый готовый к применению нормоосмолярный инфузионный раствор со сбалансированным ионным составом, с несколькими синергичными механизмами гепатопротективного действия. Препарат восстанавливает энергетический, пигментный и белковый баланс гепатоцитов. Ремаксол® безопасен и хорошо переносится пациентами. Основным показанием к его применению являются заболевания, сопровождающиеся поражением печени, а также интоксикация организма различной степени.
Целью исследования, проведенного профессором О.М. Конопацковой и ее коллегами, была оценка клинической эффективности препарата Ремаксол® в схеме терапии больных раком молочной железы (РМЖ) стадий IIB и IIIA. Клинические результаты и динамику биохимических показателей крови в процессе полихимиотерапии сравнивали у пациенток, получавших Ремаксол®, и у больных, не принимавших его. Кроме того, исследователи анализировали параметры качества жизни.
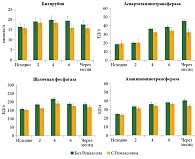
На первом этапе оценивали результаты при адъювантной полихимиотерапии (АПХТ) у 400 больных РМЖ стадий IIB и IIIA. Пациенток разделили на две равные группы. На первом этапе всем больным была проведена ПХТ по схеме FAC с повторением курса каждые три недели – всего шесть курсов. Пациентки основной группы получали после каждого курса АПХТ Ремаксол® 400 мл один раз в сутки (внутривенно, медленно), пациентки группы сравнения – АПХТ и препарат Эссенциале Н. Установлено, что стандартные биохимические показатели билирубина, трансаминаз, щелочной фосфатазы в группе Ремаксола восстанавливались быстрее и фактически приблизились к исходным (рис. 1).
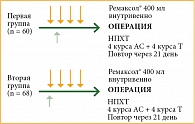
Далее у 128 пациенток с РМЖ стадий IIB и IIIA оценивали эффективность Ремаксола 400 мл один раз в сутки в качестве поддерживающего препарата на фоне неоадъювантной полихимиотерапии (НПХТ) с использованием таксанов (рис. 2). Результаты показали, что более выраженная нормализация показателей печеночной активности отмечалась в группе пациенток, получавших Ремаксол® в качестве поддерживающего препарата при НПХТ.
При включении Ремаксола в комплексную терапию больных РМЖ как при АПХТ, так и НПХТ значительно улучшалось качество жизни. До лечения снижение интегральных показателей и астеновегетативный синдром зафиксированы у 67,6% больных, получавших АПХТ, и у 59,9%, получавших НПХТ. Оценка психологического статуса больных по завершении лечения продемонстрировала улучшение качества жизни. Так, 58,2% пациенток группы АПХТ и 49,8% больных группы НПХТ отметили удовлетворенность лечением. Качество жизни по всем параметрам при НПХТ оказалось значительно выше, чем при АПХТ.
В другом исследовании больные колоректальным раком (КРР) получали ПХТ. Исследователи анализировали две группы – без метастазов в печени (110 больных) и с множественными метастазами в печени (80 больных). Схема лечения пациентов основной группы была следующей: АПХТ проводили в режимах FOLFIRI, FOLFOX, шесть курсов с повторением через две недели, в качестве поддерживающей терапии применяли Ремаксол® 400 мл внутривенно. В группе сравнения использовали препарат Эссенциале Н, внутривенно, струйно, в течение четырех дней. Согласно полученным результатам, даже у пациентов с метастазами в печени на фоне применения Ремаксола биохимические показатели печеночных проб приближались к норме быстрее, чем в группе сравнения. В группе Ремаксола пациенты с множественными метастазами в печени легче переносили ПХТ и быстрее восстанавливались. Кроме того, если до лечения с учетом множественного метастатического поражения у 71,4% пациентов были снижены практически все параметры качества жизни, то после лечения 47% больных при оценке психосоциального статуса отметили удовлетворенность им.
Профессор О.М. Конопацкова также представила данные исследования эффективности Ремаксола, включенного в схему лечения больных раком предстательной железы с костными метастазами. У 42 пациентов была проанализирована терапия бисфосфонатами с добавлением гепатопротекторов. Срок появления метастазов – от восьми месяцев до пяти лет, локализация в костях таза – 41,8%, поясничном отделе – 32%, ребрах – 26,2%. 26 пациентам основной группы вводили золедроновую кислоту и Ремаксол® в течение трех дней. 16 пациентов группы сравнения использовали Эссенциале Н. Результаты биохимических тестов продемонстрировали положительное влияние препарата Ремаксол® на биохимические показатели, в том числе простатический специфический антиген (ПСА). В группе пациентов с метастатическим раком предстательной железы, получавших в комплексной терапии Ремаксол®, биохимические показатели приближались к норме быстрее, чем в группе Эссенциале Н. Если исходно ПСА составлял около 150 нг/мл, то по окончании курса терапии – 0,2–13,6 нг/мл. У пациентов группы Ремаксола улучшилось качество жизни. У больных, получавших препарат Ремаксол® в качестве сопроводительной терапии, интенсивность боли была меньше по сравнению с теми, кто этот препарат не получал.
Итак, Ремаксол® комплексно решает проблему гепатопротекции. На фоне его применения наблюдается более выраженное снижение метаболических расстройств:
- увеличивается кратность снижения цитолитических ферментов и холестатических факторов;
- улучшаются белок-синтезирующая функция печени, липидный обмен;
- повышается качество жизни.
Кроме того, препарат оказывает антиоксидантное действие.
Что касается распределения по типам адаптационных реакций, до лечения реакция активации имела место у 11,1% больных, реакция стресса – у 41,7%. По окончании терапии Ремаксолом эти показатели составили 51,5 и 27,3% соответственно.
В ходе исследования не зафиксировано ни одного случая отмены препарата из-за побочных эффектов. Нежелательные явления в виде гиперемии кожи лица и туловища, чувства жара, скорее всего обусловленные нарушением скорости введения препарата, отмечались у 3,8% больных. Серьезных нежелательных реакций не зарегистрировано. Препарат хорошо переносился пациентами и не требовал особых условий введения.
Как известно, на фоне химиотерапии снижается чувствительность опухоли к дальнейшему лечению. Ремаксол® нивелирует подобный факт. Это обусловлено составом препарата (четыре активных компонента, обладающие синергичным механизмом действия), наличием нескольких точек приложения и возможностью применения коротким курсом.
Применение препарата Ремаксол® в качестве сопроводительной терапии уменьшает гепатотоксичность химиотерапии, что проявляется более быстрой и выраженной нормализацией показателей печеночной активности, и улучшает качество жизни пациентов за счет повышения социальной, эмоциональной и физической активности. Исходя из сказанного препарат Ремаксол® можно рекомендовать для широкого применения.
Эффективность Ремаксола при радиочастотной аблации у больных с метастазами колоректального рака в печени
По словам заведующего кафедрой факультетской хирургии и онкологии СГМУ им. В.И. Разумовского, д.м.н., профессора Сергея Викторовича ВЕРТЯНКИНА, ежегодно число заболевших КРР в мире превышает миллион человек. Из них у 40–50% диагностируются метастазы в печени. Общая пятилетняя выживаемость при метастатическом КРР составляет около 13%1. Метастазы в печени считаются наиболее распространенной причиной смерти пациентов с КРР2.
В настоящее время стандартом лечения опухолевых заболеваний печени признано резекционное вмешательство. Правда, в ряде случаев резекция печени исключена, в частности из-за наличия сопутствующих заболеваний.
Метод радиочастотной аблации (РЧА) прочно удерживает одну из лидирующих позиций среди малоинвазивных технологий локальной деструкции в борьбе с вторичными заболеваниями. Внедрение радиочастотной термоаблации позволило существенно расширить контингент больных, подлежащих радикальному лечению. Почти всем пациентам, получившим отказ в резекционном вмешательстве, можно выполнять радиочастотную термоаблацию.
РЧА – альтернатива классическому хирургическому лечению операбельных больных с очаговыми новообразованиями печени с высокой степенью операционного риска3–5.
Следует отметить, что РЧА вызывает термическое повреждение, в том числе неопухолевой ткани печени, что приводит к острому нарушению функции гепатоцитов разной степени выраженности. Обширная и мультифокальная аблация при больших и множественных очагах печени может вызывать постаблационный синдром (ПАС). В мировой литературе представлены результаты множества исследований, касающихся мониторинга функции гепатоцитов по биохимическим и гематологическим профилям как до, так и после процедуры РЧА6, 7.
По данным исследований, чаще основные отклонения показателей от исходных значений наблюдаются с первых суток до недели и возвращаются к исходным уровням в течение одного – трех месяцев. Наиболее заметно на проведение РЧА реагируют уровни аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), билирубина, альбумина, протромбинового времени8.
Докладчик представил результаты проспективного наблюдательного исследования эффективности гепатопротективных препаратов при РЧА у пациентов с метастазами КРР в печени, проведенного на базе СГМУ им. В.И. Разумовского, клинической больницы им. С.Р. Миротворцева. Перед исследователями стояли задачи:
- определить характер изменений и динамику восстановления лабораторных биохимических показателей функции печени после РЧА метастазов КРР в печени;
- оценить эффективность различных гепатопротективных препаратов в профилактике постаблационных нарушений биохимических показателей функции печени после РЧА метастазов КРР в печени;
- проанализировать влияние различных гепатопротективных препаратов на сроки нормализации постаблационных нарушений биохимических показателей функции печени после РЧА.
В исследование были включены 30 больных КРР с метастазами в печени (20 мужчин и десять женщин) в возрасте от 58 до 78 лет (средний возраст – 66,1 года). Период наблюдения составил три года (2013–2017 гг.).
Всего выполнено 40 сеансов РЧА, из них 32 – однократно, восемь – повторно. Шестеро больных проходили процедуру дважды, двое – трижды. Причины разные: множественные метастазы, оставшиеся неохваченными в ходе первой процедуры, рецидив на новом месте, рост в зоне предыдущей аблации.
У восьми пациентов за один сеанс выполнена РЧА двух метастазов одновременно. Девять процедур проведены под видеолапароскопическим контролем, 31 – под контролем ультразвукового исследования (УЗИ). Обратите внимание: выполнение аблации под лапароскопическим контролем следует минимизировать. Даже в случае проведения аблации под лапароскопическим или визуальным контролем на открытой операции качество аблации всей опухолевой ткани необходимо контролировать интраоперационным УЗИ. Метод позволяет контролировать весь процесс аблации.
Стандартное предоперационное обследование пациентов включало УЗИ органов брюшной полости, магнитно-резонансную томографию или компьютерную томографию брюшной полости, ирригоскопию или колоноскопию для исключения местного рецидива, рентгенографию грудной клетки, а также другие стандартные исследования.
При распределении пациентов по группам учитывались различия в медикаментозной профилактике и коррекции постаблационных нарушений функции печени в послеоперационном периоде.
Первую группу (группа контроля) составили 17 пациентов. С первых до пятых – седьмых суток они находились в стационаре и получали:
- инфузионную терапию в объеме до 1200–1800 мл;
- нестероидные противовоспалительные препараты (метамизол натрия, кеторолак);
- антибактериальные препараты (цефалоспорины) в целях профилактики.
Во вторую группу вошли 12 пациентов, которые в дополнение к стандартной терапии получали гепатопротектор Гептрал 400 мг внутривенно капельно (адеметионина 1,4-бутандисульфонат) два раза в сутки в течение пяти дней с момента операции.
11 пациентов третьей группы помимо стандартной терапии получали препарат Ремаксол® 400 мл внутривенно капельно (янтарная кислота, N-метилглюкамин (меглюмин), рибоксин (инозин), метионин, никотинамид) в виде инфузии по 400 мл дважды в сутки в течение трех дней.
Следует отметить, что при выполнении РЧА возможны осложнения, как правило обусловленные нарушением методики проведения процедуры. В литературе описаны случаи развития абсцессов печени, гемобилии, внутрибрюшных кровотечений, коагуляционной травмы желудка. В исследовании, проведенном профессором С.В. Вертянкиным и его коллегами, подобных осложнений не зарегистрировано.
В послеоперационном периоде у больных метастатическим КРР токсические компоненты из очага асептического некроза попадают в кровяное русло. Возникающие при этом патологические симптомы, объединенные в ПАС, связаны со слабостью, вялостью, адинамичностью, гипертермией. Доказана четкая взаимосвязь между зоной постаблационного некроза и риском возникновения и продолжительностью ПАС9.
В указанном исследовании ПАС зафиксирован у четырех (10%) пациентов. Зона аблационного некроза у данных пациентов составила 26–100 см3. Изменения лекарственной терапии не потребовалось, симптомы ПАС были купированы.
В предоперационном периоде статистически достоверных отклонений уровней биохимических показателей функции печени от нормы у участников исследования не отмечалось. Поэтому дополнительного включения в схему терапии гепатопротекторов в дооперационном периоде не потребовалось.
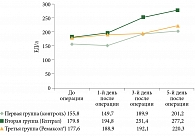
Наиболее показательную постаблационную динамику продемонстрировали уровни АЛТ, АСТ, общего билирубина, щелочной фосфатазы, общего белка, активированного частичного тромбопластинового времени. В большинстве случаев показатели достигали пиковых уровней отклонения через 24 часа после РЧА и приближались к базовым значениям на седьмой день после операции (рис. 3 и 4).
Таким образом, в ходе исследования подтверждены преимущества периоперационного применения гепатопротекторов в целях коррекции постаблационных нарушений функции печени в послеоперационном периоде при РЧА по поводу колоректальных метастазов в печени. По сравнению с Гептралом Ремаксол®, добавленный к стандартной терапии, обеспечивал нормализацию большинства лабораторных биохимических показателей в более сжатые сроки при более коротком курсе.
Некоторые аспекты диагностики, профилактики и лечения неопухолевых поражений печени у пациентов со злокачественными новообразованиями
Симпозиум продолжила к.м.н., доцент кафедры госпитальной хирургии Северо-Западного государственного медицинского университета им. И.И. Мечникова Елена Ивановна ДРОГОМИРЕЦКАЯ. Она отметила, что за последние 15 лет возрос удельный вес низкодифференцированных форм абдоминального рака, характеризующихся агрессивным течением, инфильтративным типом роста, ранним метастазированием. Увеличился процент пациентов, получавших или получающих на момент поступления в стационар этапное хирургическое лечение, химиотерапию, таргетную, лучевую терапию, комбинированное лечение, при этом находящихся на длительной нутритивной поддержке и симптоматической терапии. Значительно возрос удельный вес пациентов пожилого и старческого возраста с распространенным раком, подвергающихся и хирургическому, и лекарственному лечению. Увеличилось число пациентов с несколькими сопутствующими заболеваниями, в том числе заболеваниями и состояниями, обусловленными нарушением обменных процессов. Это привело к изменению профиля, частоты и тяжести осложнений противоопухолевого лечения, в частности характера поражения печени и длительности его проявлений.
В ряде случаев снижение дозы цитостатиков, длительные перерывы, прекращение лечения из-за развившейся токсичности или иного осложнения, в том числе хирургического, считаются причинами прогрессирования онкологического заболевания.
Прямое токсическое повреждение ткани печени (гепатоцитов, эндотелия) представляет собой патологические процессы, развивающиеся в печени при использовании лекарственных средств в терапевтических дозах. Это прежде всего истинная гепатотоксичность противоопухолевых лекарственных средств и истинная гепатотоксичность препаратов сопроводительной терапии (обезболивающие, анестезиологические, антибактериальные, кардиологические и т.д.).
Риск возникновения гепатотоксичности связан:
- с характером действия противоопухолевого препарата (токсическое влияние на структуру гепатоцитов, стромальные структуры печени, желчные протоки, сосуды; генетически детерминированные метаболизм и системы детоксикации);
- исходным состоянием паренхимы печени (стеатоз, гепатит, цирроз, нодулярная гиперплазия, метастазы и т.д.);
- исходным состоянием протоковой системы (холангиты, стриктуры желчного пузыря);
- тромбозами и эмболиями в портальной системе и печеночных венах и артериях (операции на печени и соседних органах, предыдущая химиотерапия);
- фоновыми заболеваниями и состояниями (эндокринные, аутоиммунные и т.д.).
Среди видов гепатотоксичности выделяют:
- острые транзиторные (функциональные) нарушения работы печени;
- острое поражение печени (гепатит, стеатоз, стеатогепатит);
- синдром синусоидальной обструкции, тромбоз портальной вены (вено-окклюзионная болезнь);
- хронизацию процесса (жировая дистрофия, дегенеративно-воспалительные явления – гепатиты, некротические изменения с исходом в фиброз и цирроз, опухоли).
В клинической практике для установления степени гепатотоксичности используется ряд показателей, в частности уровни щелочной фосфатазы, билирубина, гамма-глутамилтранспептидазы, АСТ, АЛТ и альбумина. В дополненной версии шкалы критериев гепатотоксичности CTCAE v. 4.03 (Common Terminology Criteria for Adverse Events), подготовленной и выпущенной в 2010 г. Национальным институтом рака, приведены объективные и субъективные проявления различных видов токсичности по пяти градациям: 0 – нет токсичности, 1 – слабая токсичность, 2 – умеренная, 3 – сильная, 4 – угрожающая жизни токсичность.
Распространенные проявления гепатотоксичности – повышение активности внутриклеточных ферментов, уровня билирубина, стеатозы, гепатиты. При этом конкретный класс препаратов характеризуется присущими только ему признаками лекарственной гепатотоксичности. Так, использование цитостатиков сопровождается повышением активности внутриклеточных ферментов, на фоне терапии таргетными препаратами могут развиться гепатиты.
Гепатотоксическая реакция при противоопухолевом лекарственном лечении метастатического КРР имеет свои особенности. Так, при использовании оксалиплатина нередко повышаются уровни щелочной фосфатазы, билирубина, лактатдегидрогеназы, АСТ, АЛТ. При этом виде терапии предсказуемая гепатотоксичность достигает 80%. В свою очередь препарат иринотекан вызывает повышение уровня трансаминаз, щелочной фосфатазы, билирубина и креатинина в сыворотке крови, а фторпиримидины – нарушение функции печени. В случае противоопухолевой терапии предсказуемая гепатотоксичность составляет 47%.
Лекарственные средства или токсины с истинной прямой гепатотоксичностью – вещества, которые имеют предсказуемую кривую зависимости «доза – эффект» (более высокие дозы или концентрации вещества вызывают больший гепатотоксический эффект) и обладают известными механизмами гепатотоксического действия (прямое повреждение гепатоцитов или блокада метаболических процессов в печени).
Типичным примером препарата с истинной прямой гепатотоксичностью служит ацетаминофен (парацетамол) при передозировке. Это связано с насыщением его обычного пути метаболизма, имеющего ограниченную пропускную способность, и включением альтернативного пути биотрансформации ацетаминофена, при котором образуется токсический высокореактивный нуклеофильный метаболит.
Прямая гепатотоксичность обычно проявляется вскоре после достижения определенного порогового уровня концентрации токсического вещества в крови.
В качестве компонентов сопроводительной терапии при гепатотоксичности назначают препараты, стимулирующие клеточное дыхание, способствующие детоксикации, «разгону» метаболизма, обеспечивающие доставку субстратов в клетку, легкую стимуляцию диуреза при сохранении объема циркулирующей крови. Не последнюю роль при выборе препарата играет и такой показатель, как удобство использования.
В клинической практике для названных целей широко применяют гепатопротекторы, восстанавливающие структуры и функции печени. Среди них Ремаксол®, в состав которого входят несколько компонентов, нормализующих работу печени, в том числе янтарная кислота и метионин. Препарат применяют при нарушениях функции печени вследствие ее острого или хронического повреждения (токсические, алкогольные, лекарственные гепатиты и др.).
По словам Е.И. Дрогомирецкой, предпочтительна комбинация инфузионных и таблетированных препаратов с дезинтоксикационным, метаболическим и холеретическим эффектами. Речь идет о Ремаксоле, Гептрале, Реамберине, их комбинациях. В реальной клинической практике активно используют комбинацию Ремаксола и Реамбирина как средство премедикации. Гептрал в таблетированной форме применяют между циклами.
Курсовое введение препаратов предпочтительно и привязано к схеме ПХТ. В случае развития энцефалопатии к терапии добавляют Цитофлавин или Гептрал.
При холестатическом типе поражения печени на фоне противоопухолевого лечения, так называемом внутрипротоковом холестазе, тактика ведения пациентов зависит от типа поражения. При сегментарном блоке имеет место внутрипротоковый холестаз, но паренхима печени поражена не полностью. При подпеченочном блоке паренхима печени поражена полностью.
При холестазе на выраженность поражения печени влияют:
- характер и длительность холестаза, степень поражения паренхимы печени вследствие внутрипротоковой гипертензии;
- контрастные препараты, которые используются при эндобилиарных вмешательствах (лечебных и диагностических);
- фоновое поражение печени (например, до 1/3 пациентов имеют стеатоз, фиброзные изменения паренхимы до начала химиотерапии);
- катетерная инфекция – холангит, инфицирование затеков желчи и гематом с вовлечением паренхимы печени, так называемый реактивный гепатит;
- послеоперационная гемобилия и тромбозы, внутрибрюшные кровотечения.
Таким образом, наличие холестатического поражения печени влияет на выбор противоопухолевой терапии, сроки ее начала, дозу препарата (исходные значения критериев токсичности). Пациентам с холестатическим поражением печени рекомендованы инфузионные препараты с дезинтоксикационным эффектом (но без холеретического) до дренирующей операции (Реамберин, Цитофлавин).
При адекватном дренировании в отсутствие сегментарного блока показано введение препаратов с холеретическим эффектом (Ремаксол®).
В случае проведения стандартной ПХТ гепатопротекторы применяют в составе премедикации и в таблетированном виде между циклами.
Поражения паренхимы печени могут быть обусловлены прямым механическим и физическим воздействием. Например, незначительное уменьшение объема функционирующей паренхимы печени развивается после сегментарной или атипичной резекции. Значительное уменьшение объема функционирующей паренхимы печени может быть следствием гемигепатэктомии. Физические факторы воздействия, вызывающие поражения паренхимы печени, – РЧА, криодеструкция, эмболизация.
Докладчик подчеркнула, что использование Ремаксола 400 мл/сут в составе премедикации у пациентов с локальным метастатическим поражением печени после радикального оперативного вмешательства на фоне ПХТ позволяет сохранить структуру и функцию паренхимы печени, снижает риск развития гепатотоксичности (рис. 5). В этой группе пациентов предпочтительно применение инфузионных препаратов с дезинтоксикационными свойствами в ранние сроки после оперативного вмешательства. В целях ускорения репарации поврежденной паренхимы печени обоснованно применение препаратов с метаболическим и антигипоксическим эффектом, сочетающимся с холеретическими свойствами (Ремаксол®).
При проведении стандартной ПХТ гепатопротекторы используют в составе премедикации, далее – по гибкому графику.
В случае развития в послеоперационном периоде тромбоза венозной системы применяют инфузионные препараты, усиливающие метаболизм печени и устраняющие гепатотоксический эффект. Речь прежде всего идет о Реамберине и Ремаксоле, а также антиагрегантах.
У пациентов со злокачественными новообразованиями вследствие замещения паренхимы опухолевой тканью может развиться локальное или распространенное поражение.
Факторами, влияющими на функционирование внутрипеченочных систем детоксикации оставшейся (не замещенной опухолью) паренхимы, считаются синдром лизиса опухоли, некроз опухоли с исходом в фиброз или абсцедирование, скорость прогрессирования метастатического процесса, паранеопластический синдром.
В группе больных с поражением печени вследствие замещения паренхимы опухолевой тканью также предпочтительно применение инфузионных препаратов с дезинтоксикационными свойствами без холеретического эффекта до начала противоопухолевого лечения. При регрессии применяют препараты с метаболическим и антигипоксическим действием (Реамберин, Мафусол). Холеретики (Ремаксол®, Гептрал) следует использовать при исключении сегментарного блока. Тогда дезинтоксикационный эффект значительно усиливается и дополняется метаболическим. При проведении стандартной ПХТ используют инфузионные гепатопротекторы в составе премедикации, а таблетированные формы – на протяжении всего периода химиотерапии.
Таким образом, особенности повреждения печени у онкологических больных связаны с непосредственным лекарственным повреждением паренхимы печени (гепатоцитов, эндотелия) – гепатотоксичностью, поражением печени вследствие внутрипротоковой желчной гипертензии, замещения паренхимы печени опухолевой тканью, а также развитием внепеченочной интоксикации, гипоксии печени.
Подводя итог, Е.И. Дрогомирецкая отметила, что дифференциальный диагноз характера поражения печени важен при выборе лечебной тактики, но крайне затруднен при сочетании этапного хирургического и лекарственного противоопухолевого лечения. Что касается профилактики и лечения поражений печени, предпочтительны препараты с дезинтоксикационными и метаболическими свойствами, сочетающимися с холеретическим действием (Ремаксол®).
Заключение
Комбинированный метаболический препарат Ремаксол® (компания «Полисан», Россия) – современный гепатопротектор с доказанной эффективностью и безопасностью. В состав раствора для инфузий Ремаксол® входят активные компоненты, обладающие выраженным сбалансированным гепатотропным действием, – янтарная кислота, меглюмин (N-метилглюкамин), инозин (рибоксин), метионин, никотинамид.
Под действием препарата улучшается энергетическое обеспечение гепатоцитов, увеличивается синтез макроэргических соединений, повышается устойчивость мембран гепатоцитов к перекисному окислению липидов, восстанавливается активность ферментов антиоксидантной защиты. При использовании Ремаксола реологические свойства крови не меняются, показатели, характеризующие степень поражения гепатоцитов и функциональное состояние печени, нормализуются.
Показаниями к применению Ремаксола являются нарушения функции печени вследствие острого или хронического ее повреждения (токсические, алкогольные, лекарственные гепатиты), а также как дополнение к этиотропной терапии в комплексном лечении вирусных гепатитов.
Кроме того, применение препарата Ремаксол® в качестве сопроводительной терапии у онкологических больных при лекарственном поражении печени улучшает качество их жизни и повышает эффективность химиотерапии.

