Проведение организационных мероприятий при внедрении метода реперфузионной терапии у пациентов с ишемическим инсультом
- Аннотация
- Статья
- Ссылки
- English



Введение
Сосудистые заболевания головного мозга – проблема чрезвычайной медицинской и социальной значимости вследствие высоких показателей заболеваемости, смертности и инвалидизации [1]. Внутривенный (системный) тромболизис с использованием рекомбинантного тканевого активатора плазминогена (rt-PA) является наиболее эффективным медикаментозным методом терапии ишемического инсульта в первые 4,5 часа от начала развития симптоматики в соответствии с Российскими национальными клиническими рекомендациями, рекомендациями Европейской организации по борьбе с инсультом (European Stroke Organisation), Американской кардиологической ассоциации и Американской ассоциации по лечению инсульта (AHA/ASA) (уровень доказательности 1, степень рекомендации А) [2–5]. В настоящее время в связи с большей эффективностью тромболитической терапии (ТЛТ) по сравнению с другими методами лечения в острейшем периоде инсульта, а также исходя из фармакоэкономических данных во всем мире прилагаются значительные усилия, чтобы как можно чаще использовать тот или иной метод реперфузии [6–8].
Цель
Оценка влияния организационно-методических мероприятий, проводимых в условиях первичного сосудистого отделения на базе городской клинической больницы № 2 «Сосновая роща» г. Калуги, на безопасность и эффективность реперфузионной терапии у пациентов с ишемическим инсультом.
Материал и методы
В исследование были включены все пациенты, которые проходили стационарное лечение и которым проводилась системная ТЛТ с 2011 по 2015 г. в неврологическом отделении для больных с острыми нарушениями мозгового кровообращения (ОНМК) на базе городской клинической больницы № 2 «Сосновая роща» г. Калуги. Для системной ТЛТ использовалась rt-PA в дозе 0,9 мг/кг массы тела, максимальная доза 90 мг, 10% в виде болюса внутривенно в течение одной минуты, оставшаяся доза вводилась в течение часа. Схема ТЛТ соответствовала международным рекомендациям, методическим рекомендациям Научно-исследовательского института цереброваскулярной патологии и инсульта Российского национального исследовательского медицинского университета им. Н.И. Пирогова и Национальным клиническим рекомендациям по проведению ТЛТ [3–5, 9]. Диагноз ишемического инсульта устанавливали на основании жалоб, данных анамнеза и объективного исследования больных, результатов компьютерной томографии при поступлении в клинику. Для объективизации тяжести состояния пациентов и оценки выраженности неврологического дефицита использовали шкалу инсульта Национального института здоровья США (National Institutes of Health Stroke Scale – NIHSS) при поступлении и далее в соответствии с протоколом ТЛТ [10]. Степень функционального восстановления нарушенных неврологических функций у выживших больных при выписке определяли по модифицированной шкале Рэнкина [11]. Удовлетворительный функциональный исход соответствовал 0–2 баллам.
Пациентам при поступлении в стационар, а также через 24 часа после ТЛТ выполняли компьютерную томографию головного мозга на 64-срезовом компьютерном томографе с определением ранних признаков ишемического повреждения (гиподенсивность размером менее 1/3 бассейна васкуляризации средней мозговой артерии, отсутствие контраста между серым и белым веществом, утрата ребристой структуры островка, сглаженность рисунка борозд и извилин) и в случае развития геморрагической трансформации (ГТ) ее тип в соответствии с критериями ECASS [12]. Всем пациентам проводили ультразвуковое исследование брахиоцефальных артерий и сердца, электрокардиографию, рентгенографию органов грудной полости, лабораторные исследования крови и мочи по стандартным методикам. На основании данных клинической картины, результатов компьютерной томографии, ультразвуковых методов исследования устанавливали патогенетический вариант инсульта в соответствии с критериями TOAST [13].
В качестве временных критериев при проведении ТЛТ анализировались следующие показатели (в минутах): время от начала заболевания до ТЛТ, время от поступления до выполнения лабораторных исследований, время от поступления до проведения компьютерной томографии и время «от двери до иглы».
Безопасность ТЛТ оценивалась по показателям госпитальной летальности, частоте развития ГТ очага поражения головного мозга, включая симптомную. Симптомную ГТ определяли в соответствии с критериями исследования ECASS как любое кровоизлияние, сопровождающееся увеличением на 4 балла или выше по шкале NIHSS от исходного уровня или наименьшего уровня в первые семь дней, либо любое кровоизлияние, закончившееся смертельным исходом. Кроме того, кровоизлияние должно быть идентифицировано как основная причина неврологического ухудшения [14].
Организационно-методические мероприятия, внедренные в неврологическом отделении для больных с ОНМК в 2014–2015 гг., включали в себя:
- четыре образовательных мероприятия для врачей (мастер-классы по реперфузионной терапии, использованию шкалы NIHSS, в том числе в рамках клинико-образовательного комплекса STROKE);
- образовательные мероприятия для среднего и младшего медицинского персонала с целью повышения мотивации, в рамках которых приводились примеры эффективности ТЛТ и объяснялось, чем обусловлен приоритет работы с данными пациентами;
- повышение частоты выполнения ТЛТ пациентам с 5–7 баллами по шкале NIHSS, что соответствует протоколу реперфузионной терапии (в 2011–2013 гг. ТЛТ в таких случаях проводилась крайне редко);
- постоянный административный контроль тактики ведения больных, госпитализированных в период терапевтического окна, с разбором каждого случая, если ТЛТ не выполнялась. При этом каждый пациент, поступивший в первые 4,5 часа от начала инсульта, рассматривался как потенциальный кандидат для проведения ТЛТ.
Статистическую обработку полученных данных проводили с использованием программного обеспечения SPSS 8.0. Категориальные переменные сравнивали с помощью теста хи-квадрат и знакового критерия Уилкоксона, а для непрерывных переменных использовали t-тест или критерий суммы рангов Уилкоксона (Манна – Уитни) в зависимости от нормальности распределения. Значение вероятности менее 0,05 (двусторонняя проверка значимости) демонстрировало статистическую значимость.
Результаты
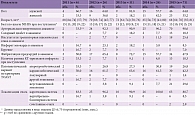
С 2011 по 2015 г. было выполнено 140 процедур системной ТЛТ, базисные характеристики пациентов представлены в табл. 1. Среди факторов риска инсульта выявлена более низкая представленность артериальной гипертензии у больных в 2011 г. (33,3%, p < 0,05) по сравнению с пациентами, пролеченными в другие годы. При сравнении других базисных показателей (пол, возраст и т.д.) между группами больных достоверных различий выявлено не было.
Среди пациентов преобладали мужчины (от 57,7% в 2014 г. до 81,8% в 2013 г.), медиана возраста колебалась от 65 лет в 2014 г. до 72 лет в 2013 г. Несмотря на отсутствие достоверных различий между группами больных по возрасту, отмечалось расширение возрастного диапазона в 2014 и 2015 гг. по сравнению с предшествующим периодом (минимальные и максимальные значения составили 41 год и 80 лет в 2014 г. и 35 лет и 81 год в 2015 г.).
Степень выраженности неврологического дефицита по шкале NIHSS была сопоставимой (12 баллов в 2012 г., в остальные годы – 15 баллов). Преобладали пациенты с каротидной локализацией очага поражения (от 83,3 до 100%) и кардиоэмболическим патогенетическим вариантом инсульта (от 42,3 до 63,6%).
Сравнительный анализ частоты выполнения ТЛТ среди пациентов, госпитализированных в стационар в период терапевтического окна, выявил значительное увеличение доли лиц, которым проводилась ТЛТ, в 2015 г. – 26,3% (р < 0,001) по сравнению с показателями в другие годы (табл. 2). При этом максимальное количество пациентов, поступивших в первые часы от начала инсульта, отмечалось в 2011 г. (n = 459), однако в том году доля ТЛТ составила всего 1,3%. В последующем удельный вес выполненных процедур ТЛТ колебался от 6,1% в 2013 г. до 12,3% в 2014 г., достигнув максимального показателя в 2015 г. Доля больных, которым проводилась ТЛТ, среди всех пациентов с ишемическим инсультом в 2015 г. составила 6,6%.
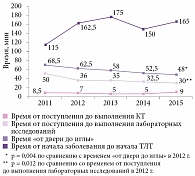
При анализе временных критериев качества оказания помощи при проведении системного тромболизиса выявлено значительное уменьшение (на 20,5 минут) времени «от двери до иглы» в течение анализируемого периода (с 68,5 минут в 2011 г. до 48 минут в 2015 г.). При этом различия между 2012 и 2015 гг. были достоверно значимыми (р = 0,004, рис. 1). Показатель времени от поступления пациента до выполнения лабораторных анализов, предписанных протоколом ТЛТ, также имел тенденцию к снижению в течение всего периода, достигая значимых различий при сравнении данных 2012 и 2015 гг. (р = 0,012). Данные о времени от поступления до выполнения компьютерной томографии существенно не различались и колебались в диапазоне от пяти до девяти минут. Наблюдалась тенденция к увеличению времени от начала заболевания до выполнения ТЛТ (без достоверных различий), свидетельствующая о более поздней обращаемости за медицинской помощью.
Показатель частоты ГТ очага поражения головного мозга (как симптомной, так и асимптомной, табл. 3) варьировал от 11,3% в 2015 г. до 26,9% в 2012 г. (без достоверных различий). При этом частота симптомной ГТ составила 3,8% в 2012 г., 18,2% в 2013 г., 3,8% в 2014 г., 4,2% в 2015 г. также без достоверных различий между годами. В целом, в течение анализируемого периода частота симптомной ГТ составила 4,3% (n = 6), и в четырех случаях ГТ послужила причиной летального исхода (у двух больных в 2013 г. и у двух в 2015 г.).
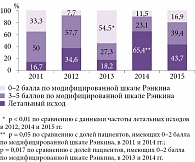
Анализ частоты летальных исходов выявил значительное преобладание умерших пациентов в 2013 г. (n = 6, 54,5%, р < 0,01) по сравнению с данными 2012, 2014 и 2015 гг. (рис. 2). Причиной летального исхода у двух больных послужила симптомная ГТ, у четырех пациентов с обширными ишемическими очагами смерть наступила при явлениях нарастающего отека головного мозга. В течение анализируемого периода летальность у пациентов с ишемическим инсультом, которым проводилась ТЛТ, составила 17,9% (n = 25).
Имела место тенденция к увеличению количества пациентов с удовлетворительным функциональным восстановлением нарушенных неврологических функций (от 0 до 2 баллов по модифицированной шкале Рэнкина) в течение 2011–2015 гг. с максимальным уровнем в 2014 г. – 65,4% (р = 0,05 по сравнению с данными 2011 г. и р = 0,017 по сравнению с данными 2013 г.). В 2015 г., когда было выполнено наибольшее количество процедур ТЛТ, данный показатель составил 43,7% (n = 31).
Было проанализировано влияние показателя времени «от двери до иглы» менее (n = 39, 27,9%) или более (n = 101, 72,1%) 40 минут (табл. 4). Несмотря на более выраженную неврологическую симптоматику при поступлении (медиана суммы баллов по NIHSS 16 и 13 соответственно, р = 0,015) и большую продолжительность времени от начала заболевания до поступления в стационар (медиана времени 99 и 90 минут соответственно, р = 0,048), для группы пациентов, ТЛТ которым была начата в течение 40 минут от поступления в стационар, был характерен более низкий показатель времени от двери до выполнения лабораторных исследований (медиана времени 20 и 36 минут соответственно, р < 0,01). Несмотря на более высокий исходный балл при поступлении по шкале NIHSS, у больных со временем «от двери до иглы» менее 40 минут отмечалась тенденция к более частому удовлетворительному восстановлению неврологических функций (на 13,7%) и меньшей частоте развития симптомной ГТ (на 2,4%) по сравнению с пациентами, выполнение ТЛТ которым было начато позднее 40 минут от поступления.
Обсуждение
Исследование показало значимость проводимых организационно-методических мероприятий при внедрении метода ТЛТ в клиническую практику. В течение пятилетнего периода работы отделения для больных с ОНМК увеличилось количество процедур системного тромболизиса с шести в 2011 г. до 71 в 2015 г. Доля больных, которым проводился тромболизис в 2015 г., составила 26,3% среди всех пациентов с ишемическим инсультом, госпитализированных в периоде терапевтического окна, и 6,6% среди всех больных с ишемическим инсультом. Это значение превысило минимальный целевой показатель (5%), установленный Министерством здравоохранения Российской Федерации. При этом абсолютное количество больных, поступивших в стационар, было максимальным в 2011 г. (n = 459) и в последующие годы значительно уменьшилось (см. табл. 2).
По нашим данным, результаты настоящего исследования – первые результаты, опубликованные в Российской Федерации, по максимальному количеству пациентов, которым выполнялась ТЛТ в условиях одной медицинской организации, а также по доле таковых среди всех больных ишемическим инсультом. Согласно проведенным ранее исследованиям, частота ТЛТ до 2015 г. в России не превышала 2% среди больных с ишемическим инсультом [15], тогда как в ряде стран данный показатель достигает 5–10% [16, 17].
В отношении безопасности при проведении ТЛТ наиболее значима частота развития симптомной ГТ. В ряде рандомизированных исследований данный показатель варьировал от 2,4 до 6,4% [12, 14, 18–20], в ранее опубликованных данных в Российской Федерации – от 4 до 6,2% [21–23], в нашем исследовании составил 4,3%. Следует отметить, что увеличение количества процедур ТЛТ в течение анализируемого периода времени не сопровождалось увеличением частоты развития данного осложнения. Это свидетельствует о правильном отборе пациентов для ТЛТ с учетом противопоказаний и о соблюдении протокола по проведению ТЛТ.
В соответствии с зарубежными рекомендациями показатель времени «от двери до иглы» не должен превышать 60 минут (чем меньше, тем лучше) [5]. В настоящем исследовании было показано, что по мере внедрения метода реперфузии и реализации организационных мероприятий отмечалось существенное уменьшение времени «от двери до иглы» (с 68,5 до 48 минут). Сравнение результатов лечения показало, что при времени «от двери до иглы» менее 40 минут увеличивалось количество больных с удовлетворительным функциональным восстановлением и уменьшалась частота симптомной ГТ, несмотря на более выраженную неврологическую симптоматику при поступлении в стационар. Таким образом, уменьшение возможных задержек при поступлении в стационар (внутрибольничная маршрутизация, время от поступления до выполнения диагностических исследований, скорость работы бригады специалистов) – чрезвычайно значимый фактор, влияющий на исход заболевания у пациентов с ишемическим инсультом.
Уровень летальности среди больных, которым была проведена ТЛТ (17,9%), соответствовал таковому в ранее проведенном исследовании в Российской Федерации (18,2%) и был несколько выше, чем в исследовании ECASS III и регистре SITS-MOST (11,3 и 7,7% соответственно) [14, 22, 24]. Возможно, подобные различия объясняются исходно более тяжелым неврологическим дефицитом у больных в нашем исследовании, что не могло не отразиться на уровне летальности (15 баллов по шкале NIHSS по сравнению с 10,7 балла в исследовании ECASS III и 12 баллами в SITS-MOST). Косвенным образом это подтверждается сходными данными исследования NINDS, в котором летальность через три месяца была зарегистрирована на уровне 17%, а суммарный балл по шкале NIHSS при поступлении составил 14 [18].
Выводы
Результаты настоящего исследования подтвердили значимость проведения комплекса организационно-методических мероприятий. Удалось повысить частоту проведения ТЛТ в условиях первичного сосудистого центра, что способствовало улучшению качества оказания медицинской помощи больным ишемическим инсультом и увеличению количества пациентов с хорошим функциональным восстановлением нарушенных неврологических функций.
A.N. Lazukin, M.A. Holopov, N.N. Rogova, K.N. Rogov, K.N. Kozlova, Ye.V. Koshelkova, U.T. Magomedov, A.N. Baglikov, L.V. Dmitriyeva, V.K. Andriyanova, A.P. Tolmachev, N.A. Shamalov
City Clinical Hospital No 2 ‘Sosnovaya Roshcha’, Kaluga
N.I. Pirogov Russian National Research Medical University, Moscow
Contact person: Nikolay Anatolyevich Shamalov, shamalovn@gmail.com
A set of organizational and methodical activities conducted at the primary vascular department allowed to increase amount of thrombolysis procedures. It facilitated improved quality of medical care provided to patients with ischemic stroke and increased number of patients with good functional recovery of impaired neurological functions.

