Смешанная форма недержания мочи: патогенез, диагностика и методы лечения
- Аннотация
- Статья
- Ссылки



Международным комитетом по недержанию мочи данное заболевание определяется как «непроизвольное выделение мочи, являющееся социальной или гигиенической проблемой, при наличии объективных проявлений неконтролируемого мочеиспускания».
В настоящее время выделяют три основные формы заболевания: стрессовое, ургентное (императивное) и смешанное недержание мочи. Стрессовое недержание мочи характеризуется непроизвольными потерями мочи, связанными с превышением внутрипузырного давления над максимальным уретральным в отсутствие сокращений детрузора, т.е. при физической нагрузке: кашле, чихании, смехе и т.д. Ургентное недержание мочи характеризуется наличием императивных позывов к мочеиспусканию и связанных с ними непроизвольных потерь мочи. Наиболее трудным в плане диагностики и лечения является смешанное недержание мочи, встречающееся примерно у 34% женщин в возрасте от 30 до 70 лет, причем частота заболевания увеличивается с возрастом. Смешанное недержание мочи (СНМ) – заболевание, в котором комбинируются в различных сочетаниях и с различной степенью выраженности симптомы стрессового и императивного недержания мочи (таблица 1).
Говоря о причинах развития СНМ, следует отметить, что данное заболевание – многофакторное. Одним из ведущих этиологических факторов развития недержания мочи у женщин в менопаузе является прогрессирующий эстрогенный дефицит. По мнению ряда авторов, при возрастном эстрогенном дефиците возникают атрофические процессы в уротелии, уменьшается васкуляризация стенки мочеиспускательного канала, а также снижается содержание и эластичность коллагена соединительной ткани урогенитального тракта и мышечно-связочного аппарата органов малого таза (4, 18, 24).
Неоспоримым является тот факт, что в большинстве случаев болеют рожавшие женщины. Согласно последним данным, в развитии заболевания основную роль играет не количество, а характер родов. НМ чаще возникает после родов, носивших травматичный характер, сопровождающихся разрывами мышц тазового дна, промежности, мочеполовой диафрагмы, акушерскими операциями, что приводит к расхождению мышц тазовой диафрагмы, замещению мышечной ткани соединительно-тканными рубцами (6, 18, 22).
Однако НМ встречается и у пациентов, не имевших в анамнезе причин, нарушающих функцию сфинктеров мочевого пузыря. В таких случаях заболевание может быть связано с врожденной системной недостаточностью соединительной ткани (9, 20). Причинами СНМ являются различные гинекологические операции: экстирпация матки, гистерэктомия, а также эндоуретральные операции. Развитие нарушений мочеиспускания и НМ у женщин после радикальных операций на матке связаны с парасимпатической и соматической денервацией мочевого пузыря, уретры и мышц тазового дна, нарушением анатомических взаимоотношений органов малого таза; если при операции удаляются яичники, то дополнительно возникает гипоэстрогения (6, 14, 26).
Кроме того, возникновению НМ способствуют курение, хронические заболевания органов дыхания, сопровождающиеся сильным кашлем, хронические запоры и ожирение. По мнению ряда авторов, кашель и натуживание провоцируют резкое и длительное повышение внутрибрюшного давления (например, во время приступов), способствующее нарушению механизмов передачи давления на мочевой пузырь и уретру, что приводит к перерастяжению и перенапряжению нервно-мышечных структур тазового дна, сопровождающимся их микроповреждением и развитием в дальнейшем денервации и дистрофических изменений в сфинктерном аппарате мочевого тракта (14). Причинами императивного НМ являются хронические воспалительные заболевания мочевыводящих путей и патология ЦНС (опухоли, кисты, травмы, воспалительные заболевания).
В патогенезе стрессового компонента СНМ выделяют два основных механизма: гипермобильность мочевого пузыря и уретры и недостаточность внутреннего сфинктера уретры. В основе гипермобильности уретры лежит слабость поддержки ее мышечно-связочными структурами тазового дна, вследствие чего происходит ротационное опущение шейки мочевого пузыря и проксимального отдела уретры в периоды возрастания внутрибрюшного давления (9, 10, 14). При сопутствующем раскрытии уретры происходит недержание мочи при физическом напряжении.
Недостаточность внутреннего сфинктера уретры определяется как снижение или отсутствие замыкательной функции шейки мочевого пузыря и проксимального отдела уретры. Эта форма стресс-инконтиненции характеризуется открытой шейкой мочевого пузыря в покое и низким абдоминальным давлением, вызывающим истечение мочи (Valsalva leak point pressure).
Существуют две основные точки зрения на патогенез синдрома императивных нарушений мочеиспускания. Старое представление базируется на нарушении иннервации мочевого пузыря и уретры: воздействие таких факторов, как воспаление, ишемия, травмы, эстроген-дефицит могут вызывать повреждение холинэргических нервных волокон, иннервирующих детрузор. В неизмененных холинэргических волокнах развивается повышенная чувствительность к холинэргической нервной стимуляции, что проявляется нестабильными сокращениями детрузора (5, 8).
Современный взгляд на патогенез данной патологии заключается в том, что в основе дисфункции детрузора лежит недостаточность его энергетического метаболизма, обусловленная многими факторами, в том числе расстройствами кровообращения.
Указанное звено патогенеза схематически можно представить следующим образом: повышение активности симпатического отдела вегетативной нервной системы → спазм артериальных сосудов мочевого пузыря → нарушение поступления и утилизации кислорода в гладкомышечных клетках детрузора → энергетическая гипоксия → чрезмембранные нарушения транспорта кальция → гиперактивность детрузора → уменьшение резервуарной функции мочевого пузыря → синдром императивного мочеиспускания (2).
Установление диагноза смешанного недержания мочи осуществляется на основании тщательно собранного анамнеза, анкетирования, осмотра больной в гинекологическом кресле, определении функциональных проб (кашлевой пробы, пробы Вальсальвы).
Е.Л. Вишневский и соавт. предложили специальный опросник для женщин с комбинированной формой недержания мочи с целью определения степени выраженности симптомов в баллах. При сумме баллов более 6 следует заподозрить у пациентки смешанную форму недержания мочи (таблица 2).
Основным методом для диагностики недержания мочи является комплексное уродинамическое исследование, которое при помощи ряда тестов позволяет определить нарушения функции мочевого пузыря, сфинктерной системы и мочевыводящих путей и осуществить выбор метода лечения данных нарушений (3, 10, 24). В последнее время фирма Johnson and Johnson выпускает новый уродинамический прибор для диагностики стрессового недержания мочи Monitorr Gynecare, с помощью которого определяется такой важный параметр, как давление обратного сопротивления уретры (URP). URP – это минимальное давление, которое требуется для открытия внутреннего сфинктера мочевого пузыря и поддержания его в раскрытом состоянии.
Уродинамическими критериями для смешанной формы недержания мочи являются:
- повышение чувствительности уротелия;
- некоординированные колебания детрузорного давления (более 10-15 см водн. ст.);
- снижение функционального и максимального цистометрических объемов мочевого пузыря;
- снижение показателей максимального внутриуретрального давления на 30% и более;
- снижение показателей давления обратного сопротивления уретры (URP) от 44 до 68 см водн. ст.
В настоящее время развитие компьютерных технологий предоставляет новые возможности в ультразвуковом исследовании нижних мочевых путей. Одним из перспективных направлений в УЗИ является трехмерная эхография. При трехмерной реконструкции оценивается объем, толщина стенок в разных отделах мочевого пузыря, состояние слизистой оболочки мочеполового тракта, состояние внутреннего сфинктера уретры, наличие или отсутствие гипермобильности уретры, а также возможно определить кровоток в области шейки мочевого пузыря и уретры (5, 11).
В лечении смешанного недержания мочи выделяют 2 этапа:
- консервативная терапия, направленная на устранение императивных нарушений мочеиспускания;
- оперативная коррекция стрессового недержания мочи – различные виды уретропексий, слинговые операции (TVT, TVT-O, TOT), парауретральное введение объемообразующих средств.
Консервативное лечение включает в себя медикаментозную терапию; тренировку мышц тазового дна с помощью метода обратной биологической связи; физиолечение (электрическая стимуляция мышц тазового дна с помощью ректальных, влагалищных, уретральных датчиков) и т.д.
Большое значение в лечении императивных нарушений мочеиспускания имеет правильный выбор селективного модулятора негормональных рецепторов мочеполового тракта, что возможно только на основании результатов комплексного уродинамического исследования.
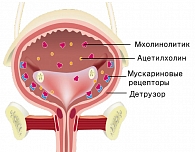
Одним из современных и эффективных лекарственных препаратов, используемых для лечения императивного и смешанного недержания мочи, является солифенацин (Везикар) – селективный антагонист мускариновых рецепторов. Императивные позывы на мочеиспускание связаны с повышением активности холинэргических рецепторов. Как видно на рисунке, ацетилхолин, связываясь с мускариновыми рецепторами, вызывает нестабильные сокращения мышцы мочевого пузыря – детрузора. Солифенацин блокирует мускариновые рецепторы, тем самым предотвращает связывание с ними ацетилхолина.
Таким образом, солифенацин (Везикар), применяемый в дозе 5-10 мг/ сут в течение 3 месяцев, позволяет:
- ингибировать сокращения миоцитов детрузора;
- снизить частоту мочеиспусканий в сутки;
- повысить функциональную и максимальную емкости мочевого пузыря;
- снизить количество эпизодов недержания мочи;
- значительно повысить качество жизни.
Одним из положительных качеств Везикара является его избирательность действия на мочевой пузырь (селективность) (таблица 3).
Благодаря высокой селективности Везикар превосходит по эффективности все существующие на сегодняшний день М-холинолиттики, редко вызывает побочные эффекты, связанные с антимускариновым действием на другие органы: сухость во рту, сухость кожи, запор, диспепсия, сонливость.
Поскольку лечение императивных позывов мочеиспускания предполагает постоянный прием антимускариновых препаратов, переносимость назначенного лечения приобретает решающее значение.
По данным F. Haab (2005), 81% пациентов, принимавших солифенацин (Везикар), успешно продолжали лечение в течение года, в то время как 80% пациентов, принимавших оксибутинин, отказались от лечения в течение первых 6 месяцев (Keller C.J et al, 1997) (27, 28).
Для коррекции стрессового недержания мочи применяются различные оперативные методики. В настоящее время разработано и модифицировано более 200 различных методов хирургической коррекции стресс-инконтиненции, среди которых можно выделить несколько групп:
- операции, восстанавливающие нормальную пузырно-уретральную анатомию влагалищным доступом;
- операции, относящиеся к так называемым позадилонным уретроцистоцервикопексиям в различных модификациях;
- операции, корригирующие пузырно-уретральную анатомию и фиксирующие мышечно-связочный аппарат;
- слинговые (петлевые) операции в различных модификациях;
- парауретральное введение объемообразующих средств.
Выбор того или иного метода хирургического лечения должен осуществляться с учетом типа и степени тяжести НМПН, а также с учетом наличия и степени цистоцеле (4).
Наиболее распространенными операциями при I и II типах стрессового недержания мочи являются различные варианты уретроцистоцервикопексий; при III типе показано парауретральное введение объемообразующих средств (при легкой, среднетяжелой форме стресс-инконтиненции), слинговые операции (при тяжелой форме заболевания) (6).
Эффективность современных подвешивающих операций, по данным разных авторов, колеблется от 70 до 80%; эффективность различных слинговых операций несколько выше и составляет от 80 до 90% (4, 12, 18).
Вопрос этапности в лечении больных со смешанной инконтиненцией по-прежнему вызывает много споров. По данным одних авторов (Пушкарь Д.Ю., Мазо Е. Б., Iosif C.S.), оперативное лечение недержания мочи при напряжении при наличии гиперактивности детрузора является вполне обоснованным. Однако по мнению других авторов (Петрова В.Д., Shandera K.C., Blaivas J.G.) и на наш взгляд, императивные нарушения мочеиспускания являются противопоказанием к хирургической коррекции нарушений мочеиспускания при напряжении, так как после проведения антистрессовых операций возможно усугубление императивных нарушений мочеиспускания и переход их в более тяжелую форму.
Материалы и методы исследования
За период с 2003 по 2008 гг. в отделении гинекологической эндокринологии НЦАГиП им. академика В.И. Кулакова Росмедтехнологий пролечено 220 пациенток со смешанной формой недержания мочи. Все больные были разделены на две группы: 1 группа – 120 пациенток, к которым применена двухэтапная система лечения: консервативная терапия императивного недержания мочи в течение 1-3 месяцев, затем антистрессовая операция; 2 группа – 100 женщин, которым антистрессовая операция проводилась на фоне императивных нарушений мочеиспускания без предварительной коррекции. Возраст пациенток колебался от 36 до 68 лет (средний возраст – 52 года). Для коррекции императивных симптомов у больных 1 группы применялось комбинированное лечение, которое включало медикаментозную терапию (ЗГТ по показаниям, Везикар в дозе 5-10 мг/сут), тренировку мышц тазового дна с помощью метода биологической обратной связи.
Антистрессовые операции пациенткам 1 группы выполнялись при достижении суточного ритма мочеиспусканий 6-8 раз в сутки, а также при отсутствии у них по данным уродинамических исследований некоординированных колебаний детрузорного давления (более 15 см водн. ст.) и при увеличении физиологического и максимального цистометрического объемов мочевого пузыря.
Перед началом терапии всем пациенткам проводилось анкетирование, комплексное уродинамическое исследование (КУДИ), а также ультразвуковое исследование с применением трехмерной реконструкции изображения. По результатам уродинамического исследования у женщин определялось снижение функционального и максимального цистометрического объемов, а у 57,4% женщин отмечались признаки нестабильности детрузора, у остальных определялись подпороговые колебания детрузорного давления. Кроме того, у всех пациенток отмечались уродинамические признаки стрессового недержания мочи разной степени выраженности. По данным трехмерной эхографии у 87,2% определялось снижение объемных показателей парауретрального кровотока, что свидетельствовало о нарушении трофических процессов в этой области.
В качестве антистрессовых операций у 76 пациенток 1 группы и 54 пациенток 2 группы применялись слинговые операции (TVT, TVT-O при тяжелой форме стрессового НМ), а у 44 пациенток 1 группы и 46 женщин 2 группы с легкой и среднетяжелой формой стресс-инконтиненции применялся метод парауретрального введения объемообразующих средств.
Результаты
Результаты, оцененные после оперативного вмешательства, показали, что у пациенток 1 группы императивные нарушения в послеоперационном периоде отмечались у 10 женщин (8,3%), которые быстро купировались назначением М-холинолитиков в течение 1-3 месяцев и курсом терапии методом биологической обратной связи (10-15 процедур). Во 2 группе у 54% женщин императивные нарушения мочеиспускания отмечались в той же степени, что и до оперативного лечения; у 46% женщин императивные нарушения мочеиспускания возникли в более сильной степени (учащение симптомов мочеиспускания, возникновение императивного недержания мочи у больных, у которых данного симптома не отмечалось до операции) и потребовали применения М-холинолитиков, иногда в сочетании с a-блокаторами в течение длительного времени (до 6-8 месяцев) и повторных курсов БОС-терапии и физиолечения. Однако у 7% женщин 2 группы данное лечение оказалось недостаточно эффективным и симптомы императивности оставались.
Заключение
СНМ в настоящее время остается самым трудоемким в плане диагностики и лечения. Учитывая данные многочисленных исследований и накопленный нами опыт, полагаем, что соблюдение этапности в лечении больных со смешанной формой недержания мочи является необходимым: I этап – консервативная терапия императивного компонента до купирования симптомов, II этап – антистрессовая операция, после которой продолжение консервативной терапии императивного компонента. Это позволит снизить частоту усиления симптомов ургентности в послеоперационном периоде у женщин со смешанной формой недержания мочи.

