Авторы провели сравнительное исследование эффективности прамипексола и пирибедила на ранних стадиях болезни Паркинсона. Через шесть месяцев у пациентов, получавших прамипексол, наблюдались менее выраженные неврологические нарушения по шкале UPDRS по сравнению с больными, принимавшими пирибедил. Была отмечена хорошая переносимость прамипексола.
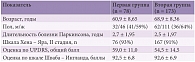
Таблица 1. Характеристики групп пациентов, получавших прамипексол (первая группа) и пирибедил (вторая группа)
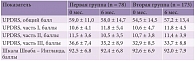
Таблица 2. Динамика показателей неврологических шкал пациентов, получавших прамипексол (первая группа) и пирибедил (вторая группа)
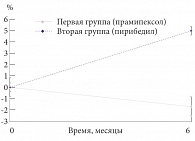
Рисунок. Динамика величины шкалы UPDRS в течение шести месяцев наблюдения (общий балл UPDRS на первом осмотре (месяц 0) принят за 100%)
Введение
Болезнь Паркинсона относится к группе нейродегенеративных заболеваний [1, 2]. Основным патофизиологическим звеном болезни Паркинсона является гибель дофаминергических нейронов в компактной части черной субстанции. Потеря более 50% дофаминергических нейронов в данной структуре головного мозга приводит к возникновению основных моторных симптомов заболевания. В настоящее время существуют различные средства терапии, позволяющие компенсировать нехватку дофамина в головном мозге при болезни Паркинсона. После восполнения дефицита дофамина уменьшается выраженность неврологических нарушений, однако доказанных методов замедления гибели дофаминергических нейронов (нейропротективной терапии) или их восстановления (нейрорепаративной терапии) не существует [3]. В этой связи разработка методов лечения, обеспечивающих уменьшение скорости нейродегенеративного процесса при болезни Паркинсона, остается одной из первоочередных задач, стоящих перед исследователями [3].
Основным наиболее эффективным симптоматическим средством лечения болезни Паркинсона считаются препараты леводопы, которые рано или поздно приходится назначать всем пациентам. Однако эти препараты обладают общим недостатком. На фоне их приема практически неизбежно развиваются флуктуации и дискинезии, которые, с одной стороны, обусловлены коротким периодом полужизни леводопы в крови, а с другой – текущим процессом нейродегенерации и критическим падением численности нигростриарных нейронов, что инициирует пульсирующую стимуляцию дофаминовых рецепторов в стриатуме [2]. По этой причине более длительная и избирательная стимуляция дофаминовых рецепторов, обеспечиваемая агонистами дофаминовых рецепторов, противодействует кратковременной пульсирующей стимуляции, осуществляемой препаратами леводопы [2, 3, 4].
Использование на ранней стадии агонистов дофаминовых рецепторов в качестве монотерапии позволяет отсрочить назначение леводопы и тем самым развитие флуктуаций и дискинезий, практически не жертвуя противопаркинсоническим эффектом. На развернутой стадии заболевания агонисты дофаминовых рецепторов дают возможность ограничить необходимую дозу леводопы, а позднее – обеспечить коррекцию развившихся флуктуаций и дискинезий. При этом агонисты дофаминовых рецепторов уступают по эффективности только леводопе. Более того, согласно экспериментальным данным, агонисты дофаминовых рецепторов имеют нейропротективный потенциал, влияя на активацию пресинаптических дофаминовых ауторецепторов с уменьшением кругооборота дофамина, оказывая (через D2-рецепторы) антиоксидантный эффект. Агонисты дофаминовых рецепторов также обеспечивают торможение апоптоза и эксайтотоксичности, вызванной гиперактивностью субталамического ядра [4, 5].
Больше всего экспериментальных данных накоплено в отношении прамипексола. Однако в клинических испытаниях его нейропротективный эффект доказать не удалось (исследование PROUD [4]), возможно, это было связано с относительно высокой симптоматической активностью препарата, перекрывающей нейропротективный потенциал. Особое значение терапия агонистами дофаминовых рецепторов имеет у пациентов моложе 65–70 лет на начальной стадии болезни Паркинсона, поскольку у них риск флуктуаций и дискинезий проявляется особенно рано [6, 7].
В настоящее время в РФ зарегистрированы шесть агонистов дофаминовых рецепторов, применяемых для лечения болезни Паркинсона (прамипексол, ропинирол, пирибедил, ротиготин, бромокриптин, каберголин). Первые четыре препарата относятся к числу неэрголиновых и имеют преимущество в связи с более высокой безопасностью. Наиболее широко в РФ применяются прамипексол и пирибедил (агонисты D2/D3 дофаминовых рецепторов). В целом ряде клинических исследований доказана эффективность терапии прамипексолом и пирибедилом как на ранних, так и на поздних стадиях болезни Паркинсона. Однако сравнительных исследований, которые бы позволили обоснованно выбирать между прамипексолом и пирибедилом исходя из их эффекта, особенно на ранних стадиях, проведено недостаточно. В этой связи нами выполнено натуралистическое открытое сравнительное исследование эффективности и безопасности прамипексола и пирибедила на базе данных регистра болезни Паркинсона в кабинете паркинсонизма Восточного административного округа г. Москвы.
Материал и методы
По данным регистра болезни Паркинсона, на июль 2014 г. в кабинете паркинсонизма Восточ-
ного административного округа г. Москвы наблюдалось 738 пациентов с болезнью Паркинсона, в том числе 251 больной (34%) на I–II стадии по Хену – Яру. Диагноз болезни Паркинсона установлен на основании наличия в неврологическом статусе асимметричных признаков гипокинезии в сочетании с тремором покоя и/или мышечной ригидностью. Пациенты были разделены на две группы: в первой (n = 78) пациенты принимали прамипексол в индивидуально подбираемой дозе от 1,5 до 3 мг в сутки, во второй (n = 173) – пирибедил в дозе от 200 до 400 мг в сутки.
В качестве коллектора данных использовалась информационная система «Прогресс», предназначенная для анализа клинико-эпидемиологических данных болезни Паркинсона. С помощью информационной системы «Прогресс» сформирована централизованная электронная база высокоформализованных данных по болезни Паркинсона. В информационной системе созданы удобный интерактивный интерфейс, оптимизированный под последовательность действий специалиста, а также автоматизированный расчет и заполнение пунктов унифицированной шкалы оценки проявлений болезни Паркинсона (Unified Parkinson's Disease Rating Scale – UPDRS), исходя из введенных формализованных данных неврологического статуса пациента [8–10].
Данные регистра были взяты за шесть месяцев (с февраля по июль 2014 г.). За это время проведено не менее двух осмотров каждого пациента, обязательные из которых были в феврале и июле 2014 г. На каждом осмотре состояние пациентов оценивалось по шкалам UPDRS и Шваба – Ингланда. Рассчитывались отдельно субшкалы UPDRS: часть I
(психические нарушения), часть II (повседневная активность), часть III (двигательные нарушения) и суммарный балл UPDRS. Оценивались также безопасность и переносимость прамипексола и пирибедила.
Статистический анализ проводили с помощью критерия t Стьюдента и критерия U с использованием функции Фишера в программе SPSS 11.
Результаты
В момент начала наблюдения первая и вторая группы статистически значимо не различались по половозрастным характеристикам, тяжести неврологических нарушений, суммарному баллу UPDRS (табл. 1). В обеих группах число пациентов на I стадии болезни Паркинсона было незначительным (3 и 9% соответственно).
Как в первой, так и во второй группе у двух третей (65 и 68%) больных отмечались сходные побочные эффекты от приема препаратов: тошнота, головокружение, сонливость, боли в спине. Данные явления носили временный характер, имели легкую степень выраженности и не приводили к отмене препарата. Нарушения сна в первую очередь выражались в затруднениях засыпания, прерывистом сне, а также дневной сонливости.
Через шесть месяцев в группе пациентов, принимавших прамипексол, общий балл по шкале UPDRS оставался на стабильном уровне со снижением оценки только на один балл (p > 0,05; табл. 2). В то же время в группе пациентов, получавших терапию пирибедилом, сумма баллов по шкале UPDRS увеличилась на 2,7 балла (p > 0,05). Сравнение результатов по I–III частям шкалы UPDRS в первой группе продемонстрировало наибольшее уменьшение по части III, которое составило 1,4 балла. Во второй группе отмечено относительно равномерное увеличение на 0,9 балла по каждой из трех частей шкалы UPDRS.
Степень нарастания неврологических нарушений, оцененных по сумме баллов по шкале UPDRS, во второй группе составила 4,9% относительно первоначального уровня по сравнению со снижением степени неврологических нарушений в первой группе на 1,7% относительно первоначального уровня (p < 0,05; рисунок).
Через шесть месяцев как в первой, так и во второй группе отсутствовали изменения в функциональной оценке по шкале Шваба – Ингланда.
Обсуждение
Регистр болезни Паркинсона в кабинетах паркинсонизма административных округов г. Москвы начал вестись с 2012 г. [10]. Процесс накопления первичной информации, когда стало возможным выделять статистически значимые группы больных, завершился к 2014 г. Данные регистра позволили провести отбор, оценить динамику неврологических нарушений, определить долю назначения агонистов дофаминовых рецепторов больным на ранних стадиях болезни Паркинсона. При этом врачи кабинетов паркинсонизма вносили в регистр результаты неврологического осмотра в максимально формализованном виде, а информационная система выполняла автоматизированный расчет неврологических шкал, включая шкалу UPDRS. Именно поэтому данные регистра позволяют оценить непосредственно «живой» прием пациентов специалистом по болезни Паркинсона, выявить реальную картину динамического наблюдения пациентов с болезнью Паркинсона, структуру терапии, в том числе и долю больных, получающих агонисты дофаминовых рецепторов, включая прамипексол и пирибедил.
Препараты леводопы больным на ранних (I–II) стадиях по Хену – Яру назначались достаточно часто: по данным регистра, доля таких пациентов составляла около 40%. В то же время число пациентов, принимающих агонисты дофаминовых рецепторов, составляло более двух третей от всех пациентов на ранних стадиях болезни Паркинсона. Почти треть (31%) больных с болезнью Паркинсона на I–II стадиях по Хену – Яру получали прамипексол.
Следует отметить хорошую переносимость прамипексола: основными побочными эффектами были тошнота (27%) и сонливость или нарушения сна (36%). В регистре отсутствуют данные о прекращении приема прамипексола в связи с развитием побочных эффектов. У пациентов на ранней стадии болезни Паркинсона, по данным регистра, через шесть месяцев после приема прамипексола отмечались менее выраженные неврологические нарушения по шкале UPDRS по сравнению с больными, не принимавшими прамипексол.
Полученные результаты соответствуют данным четырех плацебоконтролируемых исследований у пациентов на ранних стадиях болезни Паркинсона. Было установлено, что монотерапия прамипексолом дозозависимым образом уменьшает симптомы паркинсонизма (согласно сумме баллов по шкале UPDRS). В исследовании СALM-PD [11] снизилась частота моторных флуктуаций и дискинезий по сравнению с начальной терапией леводопой. Исследование включало нейровизуализационный метод – SPECT с радиолигандом [123]iodine2-b-carboxymethoxy-3-b-(4-iodophenyl)tropane (123I-b-CIT), связывающимся с пресинаптическим дофаминовым транспортером и служащим суррогатным маркером прогрессирования заболевания. Хотя в исследовании на фоне приема прамипексола скорость связывания с ДАТ-лигандом была ниже, чем на фоне приема леводопы, интерпретация этих результатов не могла быть однозначной.
Тем не менее полученные нами данные при всей их неоднозначности также косвенно подтверждают наличие нейропротективного потенциала прамипексола. Еще одним обоснованием раннего применения прамипексола может быть способность препарата уменьшать симптомы депрессии и повышенной утомляемости.
Заключение
Проведенное исследование продемонстрировало эффективность и безопасность прамипексола у пациентов с болезнью Паркинсона на I–II стадии по Хену – Яру, что позволяет рекомендовать прамипексол для широкого применения у больных на ранних стадиях болезни Паркинсона.
Появление новой лекарственной формы прамипексола с замедленным высвобождением делает препарат удобным для применения и повышает приверженность пациентов лечению, что особенно важно на ранней стадии заболевания. Более постоянный уровень дофаминергической стимуляции (с теоретической точки зрения), обеспечиваемый агонистом дофаминовых рецепторов прамипексолом, может отдалять развитие моторных и немоторных флуктуаций, а также дискинезий.
Таким образом, представленные данные могут свидетельствовать в пользу применения прамипексола по сравнению с пирибедилом.

