Антимикробная терапия острого цистита в условиях роста антибиотикорезистености уропатогенов к фторхинолонам
- Аннотация
- Статья
- Ссылки
Социально-экономическое значение острого цистита обусловлено не только его широкой распространенностью, но и прямыми и непрямыми затратами на лечение, а также снижением качества жизни пациенток. Установлено, что около 15% всех назначений антимикробных препаратов в амбулаторных условиях – это назначения по поводу ИМП [2]. В США ежегодно расходуется более 1 млрд долларов на терапию ИМП [3]. Рациональный выбор антибактериальной терапии во многом определяет эффективность лечения ОЦ, приводит к быстрому исчезновению клинических и лабораторных симптомов заболевания и снижает риск рецидивов цистита в последующем.
Наряду с фармакодинамическими и фармакокинетическими параметрами при выборе препарата для терапии ОЦ важно учитывать не только его стоимость, но и соотношение «затраты/эффективность», а также то обстоятельство, что лечение ОЦ проводят преимущественно в амбулаторных условиях. В связи с этим препарат для лечения данной инфекции должен обладать благоприятным профилем безопасности и выпускаться в пероральной форме. Помимо вышеперечисленного, препарат выбора для лечения ОЦ должен иметь удобный режим дозирования для приема 1 или 2 раза в сутки – это позволяет достигать высокой приверженности пациентов к терапии, что является важным фактором ее эффективности.
Одной из отличительных особенностей антимикробных препаратов является изменение их активности с течением времени, обусловленное формированием у микроорганизмов устойчивости к ним. На сегодняшний день во многих странах отмечается рост резистентности уропатогенных микроорганизмов к фторхинолонам – препаратам выбора при лечении ОЦ. Так, по данным различных авторов, в США распространенность фторхинолонрезистентных штаммов уропатогенной Escherichia coli, выделенных от амбулаторных пациентов, варьирует в пределах 6,8–25,4% [4]. В ряде европейских стран наблюдается высокая распространенность штаммов уропатогенной E.coli, устойчивых к фторхинолонам, например, в Италии и Великобритании она составляет 11,7% и 9,3%, соответственно [5]. Высокая распространенность фторхинолонрезистентных штаммов уропатогенной E.coli зарегистрирована в Индии (31%) и Японии (26,4%) [6].
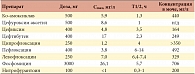
Тенденция роста резистентности уропатогенов к фторхинолонам, наблюдаемая в зарубежных странах, характерна и для некоторых регионов РФ. В ряде областей Центрального федерального округа к ципрофлоксацину устойчивы 10% выделенных штаммов уропатогенной E.coli [7]. В исследовании V. Vorobieva (2007) было показано, что в Архангельской области распространенность фторхинолонрезистентных штаммов уропатогенной E.coli, выделенных от амбулаторных пациентов с ИМП, составляет 17% (табл. 1) [8]. Высокий уровень резистентности основных уропатогенных микроорганизмов к фторхинолонам вызывает необходимость поиска альтернативных препаратов для терапии ИМП.
На сегодняшний день одной из перспективных групп антибиотиков для терапии ИМП являются цефалоспорины III поколения, которые обладают высокой активностью в отношении наиболее вероятных возбудителей амбулаторных ИМП – представителей семейства Enterobacteriacea. Антибиотики данной группы включены в большинство международных и национальных рекомендаций по лечению ИМП, а в ряде случаев они являются препаратами выбора [9]. Значительного роста резистентности внебольничных уропатогенов к цефалоспоринам III поколения не наблюдается, в отличие от фторхинолонов. Резистентность уропатогенной E.coli к цефиксиму в Европе варьирует в пределах 2,6–4,2% [10]. Низкий уровень резистентности к цефиксиму штаммов уропатогенной E.coli, выделенных от пациентов с неосложненными ИМП, был выявлен в исследовании отечественных ученых [7]. Так было показано, что МПК90 (минимальная подавляющая концентрация для 90% бактерий) для цефиксима составила 0,5 мг/л, МПК50 – 0,125 мг/л. (табл. 2). Также было установлено, что у пациентов с неосложненными ИМП не выделено ни одного штамма, резистентного к цефиксиму. Доля умеренно резистентных штаммов была низкой и составила 1,1% от общего количества исследованных бактерий (один штамм) (табл. 2).
Следует отметить, что наиболее существенной угрозой для широкого применения цефалоспоринов III поколения при лечении ИМП может стать распространение штаммов грамотрицательных бактерий, продуцирующих β-лактамазы расширенного спектра (БЛРС). Обзор данных зарубежной литературы позволяет сделать вывод о невысокой частоте выделения продуцентов БЛРС у пациентов с неосложненными ИМП – от 1,7% в Испании до 7% в Гон-Конге [11]. По данным многоцентрового исследования UTIAP-III (2005 г.), в котором не было выявлено штаммов E.coli со сниженной чувствительностью к цефалоспоринам II и III поколений, можно судить об отсутствии и крайне невысоком уровне продуцентов БЛРС при внебольничных неосложненных ИМП в России [12]. Правомерность этого заключения подтверждают данные исследования ARESC, в ходе которого установлено, что в настоящее время в Европе распространенность штаммов уропатогенной E.coli, продуцирующих БЛРС, составляет 1,7% [13].
Рациональный выбор препарата для терапии ИМП не может осуществляться без учета его фармакокинетических особенностей. Прежде всего, он должен обеспечивать высокие концентрации действующего вещества в моче, тканях и органах мочевого тракта [14]. На сегодняшний день количество пероральных препаратов, обладающих приемлемыми фармакокинетическими параметрами, ограничено. Для лечения ИМП наиболее подходящими являются амоксициллин/клавуланат, нитрофурантоин, фторхинолоны с высокой почечной экскрецией (ципро-, офло-, пефло-, левофлоксацин), пероральные цефалоспорины III (цефиксим, цефтибутен), фосфомицина трометамол. В таблице 3 представлены основные фармакокинетические параметры антибиотиков для перорального приема [15].
Из представленных пероральных β-лактамных антибиотиков лишь цефиксим и цефтибутен могут назначаться 1 раз в сутки, что в большинстве случаев позволяет достигнуть высокой комплаентности при лечении ИМП. Цефиксим создает высокие концентрации в моче, достигающие 164 мг/л (табл. 4) [16], и обладает наиболее длительным из пероральных цефалоспоринов III поколения периодом полувыведения (3,5 ч); наряду с этим уропатогены in vitro сохраняют высокую чувствительность к цефиксиму [7]. Следует отметить, что в серии клинических исследований была продемонстрирована высокая (> 90%) микробиологическая и клиническая эффективность цефиксима, назначаемого в дозе 400 мг 1 раз в сутки при лечении неосложненных ИМП [17]. Рациональный выбор антибиотика для терапии ИМП невозможен без оценки данных клинических исследований. Так, было показано, что наибольшей микробиологической эффективностью в лечении неосложненных ИМП среди β-лактамных антибиотиков обладают цефиксим и ко-амоксиклав (табл. 4).
Нами проведено сравнение безопасности и эффективности коротких курсов перорального цефалоспорина цефиксима (Супракс, «Гедеон Рихтер», Венгрия) и ципрофлоксацина (Ципролет, «Д-р Редди’с Лабораторис Лтд», Индия) при остром неосложненном цистите (ОНЦ). Проведено многоцентровое проспективное рандомизированное исследование, в котором участвовали женщины в возрасте 18-55 лет с клиническими проявлениями ОНЦ и бактериологическим подтверждением инфекции (микробное число > 105 КОЕ/мл). Пациенты, соответствующие критериям включения, были рандомизированы в соотношении 1:1 на две группы. Пациенты 1-й группы получали цефиксим в дозе 400 мг 1 раз в сутки в течение 5 дней, пациенты 2-й группы – ципрофлоксацин в дозе 250 мг на первом этапе (до проведения промежуточного статистического анализа) и 500 мг 2 раза в сутки в течение 5 дней на втором этапе (после проведения промежуточного статистического анализа). На 2-м (8-й день) и 3-м (28-й день) визите пациентам проводили физикальное исследование, оценивали жалобы, сведения о нежелательных явлениях, выполняли общеклинический и бактериологический анализы мочи. Бактериологическое исследование мочи проводили с использованием тест-системы Uricult TrioTM (Orion Diagnostica, Финляндия).
Всего в исследование было включено 104 пациента, из них 49 рандомизированы в группу 1 (терапия цефиксимом), 55 в группу 2 (терапия ципрофлоксацином). В рамках исследования проводился промежуточный статистический анализ сравнительной бактериологической эффективности изучаемых режимов терапии после достижения популяции включенных пациентов в количестве 42 человек. В ходе этого анализа достоверно установлена более низкая бактериологическая эффективность ципрофлоксацина 250 мг 2 раза в сутки по сравнению с таковой цефиксима 400 мг 1 раз в сутки. Частота эрадикации составила соответственно 55,6% и 100% в группах пациентов, получавших ципрофлоксацин и цефиксим, различия были статистически достоверны (p < 0,05). В связи с выявлением низкой микробиологической эффективности терапии ОНЦ ципрофлоксацином в стандартной дозе 250 мг 2 раза в сутки и достоверных различий в ранней микробиологической эффективности препаратов было принято решение увеличить разовую дозу ципрофлоксацина до 500 мг.
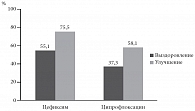
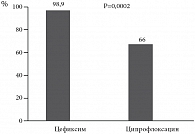
Выздоровление (полное исчезновение всех симптомов, регистрируемых на 1-м визите, ко 2-му визиту) наблюдалось у 55,1% пациентов 1-й группы (цефиксим 400 мг) и у 37,3% пациентов 2-й группы (ципрофлоксацин 250-500 мг) (p = 0,96), а улучшение – в 75,5% и 58,1%, соответственно (p = 0,08) (рис. 1). Эрадикация возбудителя (элиминация возбудителя, выделенного во время 1-го визита, при проведении исследования во время 2-го визита в отсутствии других клинически значимых возбудителей) отмечалась у 95,9% пациентов 1-й группы и 66% пациентов 2-й группы (разница статистически достоверна, p = 0,0002) (рис. 2). Отдаленные результаты терапии при бактериологической оценке не различались – стойкий бактериологический ответ у пациенток с эрадикацией возбудителя отмечался в 100% в обеих группах.
В ходе исследования зафиксировано 2 случая нежелательных явлений в виде бактериального вагиноза у пациенток, получавших цефиксим, и 11 случаев в группе пациенток, получавших ципрофлоксацин, – в виде крапивницы, диареи (n = 7), бактериального вагиноза (n = 2) и пиелонефрита (p = 0,02). Реакции, которые исследователи связывают с приемом препарата, послужили причиной отмены ципрофлоксацина (в случае возникновения крапивницы), а также госпитализации пациента в стационар (пиелонефрит). В нашем исследовании была выявлена неожиданно невысокая микробиологическая эффективность ципрофлоксацина, назначаемого в дозе 250 мг 2 раза в сутки, в лечении ОНЦ – частота эрадикации уропатогенов составила 55,6% против 100% при терапии цефиксимом. В связи с этим после проведения промежуточного статистистического анализа было принято решение о повышении дозы ципрофлоксацина в два раза. Таким образом, пациенты с рандомизационного номера 43 и далее получали ципрофлоксацин в дозе 500 мг 2 раза в сутки. Длительность курса терапии осталась без изменений.
Аналогичные данные о недостаточно высокой эффективности ципрофлоксацина при ИМП были получены в ряде других исследований. В одном из них было показано, что микробиологическая эффективность ципрофлоксацина, назначаемого в дозировке 500 мг 2 раза в сутки в течение 5 суток, при лечении неосложненной ИМП составляла 78%, что обусловлено высокой частотой встречаемости штаммов фторхинолонорезистентной E.coli, выявленной у 59% пациентов [26]. Следует отметить, что в настоящее время чувствительность уропатогенных микроорганизмов к фторхинолонам значительно варьирует в зависимости от региона (от 1,6% в Австрии до 4,2-12,9% в России) [5, 27, 28]. Нельзя исключить, что низкая эффективность ципрофлоксацина в нашем исследовании была обусловлена расширением распространенности уропатогенов, резистентных к фторхинолонам.
Необходимо учесть также тот факт, что в большинстве зарубежных исследований, в которых была отмечена высокая эффективность ципрофлоксацина, применялся оригинальный препарат. В нашем исследовании был использован наиболее распространенный в РФ генерик ципрофлоксацина [29]. Хотя формально считается, что оригинальный препарат и генерик (при условии их биоэквивалентности) не должны различаться по своей эффективности и безопасности, такой подход не лишен недостатков. Подтверждением тому являются требования проведения исследований клинической эквивалентности антибиотиков в ряде стран. Строго говоря, делать заключение о низкой эффективности ципрофлоксацина при лечении ОНЦ мы можем только по отношению к препарату конкретного производителя, использованному в нашем исследовании. Нельзя исключить, что эффективность оригинального ципрофлоксацина или генериков других производителей будет отличаться. Данные о высокой микробиологической эффективности цефиксима, полученные в нашем исследовании, согласуются с результатами зарубежных исследований, в которых было показано, что микробиологическая эффективность цефиксима, назначаемого при неосложненных ИМП в дозировке 400 мг 1 раз в сутки в течение 1–10 дней, варьирует в пределах 89,4–100% [24].
Заключение
В условиях роста устойчивости уропатогенной кишечной палочки к фторхинолонам отмечается снижение бактериологической эффективности ципрофлоксацина при ИМП. Назначение ципрофлоксацина в дозировке 250 и 500 мг 2 раза в сутки позволяет достичь эрадикации только в 55,6% и 66% случаев соответственно. В то же время назначение цефиксима в дозе 400 мг 1 раз в сутки в течение 5 дней является эффективным и безопасным режимом терапии ОНЦ, позволяющим в 95,9% случаев достичь эрадикации патогена, что сопровождается стойким бактериологическим ответом (отсутствием рецидива и реинфекции на 28-й день после завершения терапии у всех пациентов).Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.