Актуальные вопросы гиперпролактинемии в гинекологической практике. Репродуктивное здоровье женщины. Эндокринный фактор
- Аннотация
- Статья
- Ссылки





Актуальные вопросы гиперпролактинемии в гинекологической практике
Гиперпролактинемия – одно из наиболее частых проявлений гипоталамо-гипофизарной дисфункции.
Повышение содержания пролактина имеет различную этиологию, но все его варианты могут быть разделены на три основные категории: физиологическую, патологическую и фармакологическую (ятрогенную) гиперпролактинемию. Секреция пролактина у человека имеет пульсирующий характер (около 10 пиков секреции в течение дня) с постоянным повышением во время сна, независимо от того, когда это происходит – днем или ночью. В связи с этим забор крови для определения уровня этого гормона следует проводить не менее чем через час после пробуждения. Кроме того, у женщин репродуктивного возраста подъем пролактина наблюдается в периовуляторный период и в лютеиновую фазу цикла, поэтому для минимизации возможной ошибки целесообразно исследовать пролактин в середине первой фазы менструального цикла (5–8 день).
Во время беременности содержание пролактина значительно и прогрессивно возрастает (в десятки раз). Такая гиперпролактинемия является физиологической, поскольку основной функцией пролактина в этот период является подготовка молочных желез к лактации и приоритетной регуляции этой функции в послеродовом периоде. Исследовать уровень пролактина и ориентироваться на референтное значение во время беременности в широкой практике нецелесообразно, четких критериев нормы для этого показателя во время беременности на сегодняшний день нет. По той же причине контроль уровня пролактина во время беременности при наличии пролактин-секретирующей аденомы гипофиза также не оправдан, тем более что корреляции между уровнем пролактина и ростом опухоли до настоящего времени не обнаружено. Относительно информативным может быть лишь динамика его уровня. После родов базальная секреция пролактина быстро снижается в течение 3–4 недель до уровня, предшествующего беременности. При грудном вскармливании базальные уровни пролактина дольше остаются повышенными: акт сосания активирует афферентные нейрональные пути, вызывая увеличение секреции пролактина, длящееся около 30–45 минут после акта сосания. Со временем рефлекторный ответ нивелируется, и уровень пролактина между кормлениями возвращается к норме.
Помимо беременности, лактации и сна физиологическими причинами гиперпролактинемии являются различные стрессы (медицинские манипуляции, гипогликемия, острый инфаркт миокарда, половой акт, хирургические вмешательства). На секрецию пролактина существенно влияют различные фармакологические препараты, в том числе весьма распространенные (метоклопрамид, домперидон, различные антидепрессанты, эстрогены, опиаты и ряд других), что необходимо учитывать при выяснении причин повышенного содержания пролактина. Патологическими причинами гиперпролактинемии, наряду с пролактиномами и рядом других заболеваний гипофиза и гипоталамуса, могут служить первичный гипотиреоз (в 40% случаев), синдром поликистозных яичников (в 25–60% случаев), хронический простатит, хроническая почечная недостаточность, цирроз печени, рак шейки матки и ряд других состояний.
Основные клинические проявления гиперпролактинемии развиваются в результате влияния гиперпролактинемии на репродуктивную систему на различных ее уровнях, включая подавление выработки гонадотропин-рилизинг гормона в гипоталамусе, с последующей потерей пульсирующего характера секреции и преовуляторного пика лютеинизирующего гормона на уровне гипофиза. На уровне яичников гиперпролактинемия приводит к блокаде фолликулогенеза, ингибируя ароматазную активность в клетках гранулезы, подавляя яичниковый стероидогенез, что в конечном итоге способствует развитию гипоэстрогении и ановуляции. Клинически у женщин это проявляется нарушением менструального цикла (по типу олиго-, аменореи), снижением либидо, галактореей и/или бесплодием.
Метаболические эффекты гиперпролактинемии разнообразны. В период лактации они направлены на ее поддержание и ответственны за качество молока: под влиянием пролактина увеличиваются всасывание кальция в желудочно-кишечном тракте и мобилизация его из костной ткани. Пролактин также оказывает прямое стимулирующее влияние на β-клетки поджелудочной железы (инсулин содействует синтезу белка и жира в молоке). Центральные эффекты пролактина определяют формирование материнского поведения и стимуляцию аппетита. Описанные выше механизмы, являющиеся целесообразными в период лактации, при хронической гиперпролактинемии ассоциированы с развитием остеопороза и инсулинорезистентности – у 40–60% пациентов с гиперпролактинемией имеет место ожирение различной степени.
При обнаружении повышенного уровня пролактина для исключения спонтанных и/или связанных со стрессом подъемов необходимо повторить анализ дважды в разные дни. Кроме того, следует исключить возможные причины симптоматической гиперпролактинемии путем уточнения анамнеза, общеклинического обследования, биохимического анализа крови, определения уровня ТТГ и исключения влияния фармакологических факторов. Также следует помнить о феномене макропролактинемии. Определение макропролактина целесообразно при отсутствии эффекта от условно адекватной терапии, а также у пациентов с незначительной гиперпролактинемией при отсутствии выраженной симптоматики.
В настоящее время методом выбора в лечении гиперпролактинемии является медикаментозная терапия агонистами дофамина. Для врачей акушеров-гинекологов наиболее актуален вопрос планирования и ведения беременности у пациенток с гиперпролактинемией. Когда женщина репродуктивного возраста впервые начинает прием агонистов дофамина, она должна быть информирована о том, что беременность может наступить незамедлительно (даже до восстановления менструального цикла). Восстановление овуляции и/или наступление беременности в течение полугода регистрируется у 52% пациенток с синдромом гиперпролактинемии при терапии агонистом дофамина I поколения – бромокриптином и у 72% пациенток – на фоне лечения агонистом дофамина III поколения – каберголином (Достинекс). При увеличении продолжительности терапии каберголином до 10 месяцев восстановление фертильности наблюдается уже у 90% больных. Аксиомой для врача является планирование беременности на фоне подтвержденной нормопролактинемии. Во время беременности угрозу для женщины представляет не сам по себе феномен увеличения пролактина, а риск роста опухоли. У больных с пролактиномами, в том числе микроаденомами гипофиза, терапия агонистами дофамина должна быть продолжена даже после достижения нормопролактинемии в поддерживающей дозировке в течение 12 месяцев, после чего на фоне лечения агонистами дофамина (бромокриптином и каберголином) разрешают зачатие. Сразу после установления диагноза беременности препараты отменяют. В настоящее время появились данные о безопасности применения каберголина до и во время беременности, но эти данные касаются только Достинекса. Возможность зачатия на фоне терапии бромокриптином и каберголином и отмены медикаментозной терапии при подтверждении беременности (то есть препараты не нужно отменять заранее) подтверждается актуальными в настоящее время рекомендациями по диагностике и лечению пролактином Общества гипофизарных заболеваний (Guidelines of the Pituitary Soсiety for the diagnosis and management of prolactinomas)1.
Клиническое обследование пациенток с органической гиперпролактинемией в период беременности показано один раз в триместр, с обязательной оценкой полей зрения и состояния глазного дна во втором и третьем триместрах беременности. Риск роста опухоли не превышает 2–3%. Проведение магнитно-резонансной томографии (МРТ) у лиц с микроаденомами целесообразно после родов. У больных с макропролактиномами риск роста опухоли выше (15–30%), поэтому необходимо добиться нормализации уровня пролактина и уменьшения размеров опухоли и продолжать терапию агонистами дофамина в течение не менее 1–2 лет до зачатия. При наступлении беременности у таких пациенток необходимость медикаментозной терапии агонистами дофамина и МРТ определяется в индивидуальном порядке. Обязательным для этой группы больных являются ежемесячное клиническое обследование, исследование полей зрения и состояния глазного дна. При наличии признаков роста опухоли, сужении полей зрения показана медикаментозная терапия агонистами дофамина.
Дисгормональная гиперплазия молочных желез. Патогенетическая коррекция
Дисплазия молочной железы или фиброзно-кистозная мастопатия представляет собой группу гетерогенных заболеваний, характеризующихся широким спектром пролиферативных и регрессивных изменений ткани молочной железы с нарушенным соотношением эпителиального и соединительнотканного компонентов. Согласно действующей в России клинико-рентгенологической классификации мастопатии, существуют диффузная и узловая форма фиброзно-кистозной мастопатии. Диффузная форма в свою очередь делится на диффузную мастопатию с преобладанием кистозного компонента, диффузную мастопатию с преобладанием фиброзного компонента, диффузную мастопатию с преобладанием железистого компонента и смешанную форму. Причины возникновения заболеваний молочных желез у женщин самые разные – от отягощенной наследственности, эндокринных и острых воспалительных заболеваний до неблагоприятной экологической обстановки и отсутствия государственных программ ранней диагностики и профилактики заболеваний молочной железы. К неблагоприятным факторам репродуктивного анамнеза относятся раннее наступление менархе; позднее наступление менопаузы; отсутствие беременности и родов; прерывание беременности; отсутствие полноценной лактации. К неблагоприятным факторам гинекологического анамнеза относятся все прогестерон-дефицитные состояния и опухоли яичников. Такие эндокринные заболевания, как нарушения функции щитовидной железы, сахарный диабет типа 1 и 2, метаболический синдром, синдром поликистозных яичников и врожденная дисфункция коры надпочечников, также являются факторами риска диспластических заболеваний молочных желез. В формировании и развитии молочной железы участвует целый ряд гормонов. Самые известные – эстрогены, прогестерон и пролактин. Однако немаловажную роль в морфогенезе и функциональной дифференцировке эпителиальных клеток молочной железы играют также гормоны щитовидной железы; инсулин действует на клетки молочной железы опосредованно через инсулиноподобные факторы роста; кортизол способствует образованию рецепторов пролактина в молочных железах и стимулирует рост эпителиальных клеток в синергизме с пролактином.
Но решающая роль в заболевании молочных желез отводится прогестерон-дефицитным состояниям, при которых избыток эстрогенов (относительная или абсолютная гиперэстрогения) приводит к пролиферации эпителия альвеол, протоков, усилению активности фибробластов и вызывает пролиферацию соединительной ткани молочной железы. Остановимся на таких составляющих метаболического синдрома, как инсулинорезистентность и компенсаторная гиперинсулинемия, которые являются факторами развития диспластических заболеваний молочных желез. Инсулинорезистентность и гиперинсулинемия характерны для сахарного диабета типа 2. Они приводят к стимуляции инсулиноподобных факторов роста, взаимодействию их с рецепторами IGF-I в тканях молочных желез, усилению процессов клеточной пролиферации и развитию мастопатии. А вот сахарный диабет типа 1 – это аутоиммунное заболевание. При длительно существующем сахарном диабете типа 1 в молочных железах развивается «диабетическая» мастопатия (склеротический лимфоцитарный лобулит), имеющая аутоиммунную природу. У пациенток, страдающих сахарным диабетом типа 1, выявляют «диабетическую» мастопатию в 70% случаев. Лечение мастопатии без компенсации основного заболевания (нормализации уровня сахара в крови) неэффективно. Для синдрома поликистозных яичников характерны два патогенетических механизма развития мастопатии. Первый механизм – ановуляция, которая приводит к относительной гиперэстрогении и прогестерон-дефицитным состояниям, стимуляции клеточной пролиферации в тканях органов-мишеней и, в конечном итоге, к мастопатии. Второй механизм – наличие инсулинорезистентности и гиперинсулинемии обусловливает развитие мастопатии по той же схеме, что и у больных сахарным диабетом типа 2. Клиническая картина мастопатии у эндокринологических больных не имеет специфических проявлений. В основном, это боли в молочных железах, усиливающиеся перед менструацией; боли различного характера, отдающие в подмышечную область, в плечо, утихающие после окончания менструации; в редких случаях нарушения сна; канцерофобия. Что касается щитовидной железы, изменения в молочной железе чаще всего происходят при гипотиреозе. Гипофункция щитовидной железы повышает риск возникновения дисплазий молочных желез по сравнению со здоровыми женщинами в 3,8 раза. Лечение больных должно проводиться с учетом возраста, формы заболевания, характера нарушений менструального цикла, заинтересованности в сохранении репродуктивной функции или, наоборот, необходимости контрацепции, наличия соответствующих эндокринных, гинекологических заболеваний или экстрагенитальной патологии. В лечении диффузной формы мастопатии следует обратить особое внимание на компенсацию основного заболевания, сочетанное применение витамино- и энзимотерапии, иммуномодулирующих средств, нейролептиков, фито- и гормонотерапии. При гормональной терапии мастопатии наиболее патогенетически обосновано применение препаратов гестагенового ряда. При оральном пути введения наименьшими побочными влияниями обладают натуральный прогестерон, синтетический гестаген дигидрогестерон, а также синтетические гестагены нового поколения – дезогестрел, гестоден, дроспиренон, входящие в состав оральных контрацептивов, а также гестагены с трансдермальным способом введения. Однако назначать препараты следует индивидуально и с учетом детального предварительного обследования.
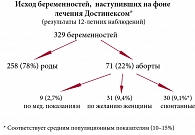
При гиперпролактинемии гиперпластические процессы в молочных железах отмечаются у 52% женщин. С одной стороны, повышение уровня пролактина может быть только маркером центральных нарушений в системе регуляции репродуктивной функции, с другой стороны, пролактин оказывает прямое стимулирующее влияние на развитие пролиферативных процессов в молочных железах. Как известно, частота всех форм гиперпролактинемии варьирует от 0,15 до 1,6% среди взрослой популяции. Причем в 80% случаев заболевание отмечается у женщин 25–40 лет, то есть самого репродуктивного возраста. В Эндокринологическом научном центре проводилось исследование влияния агонистов дофамина и, в том числе, влияния препарата III поколения Достинекса на структуру молочной железы с гиперпролактинемией. Наблюдение велось за 77 пациентками, которых лечили агонистами дофамина (и Достинексом – в дозе 0,5–3,5 мг в неделю в 2 приема) в течение 11–16 месяцев. Результаты исследования показали, что нормализация пролактина была достигнута у 72 пациенток. Существуют данные 2008 г. об исходах беременностей, наступивших на фоне лечения Достинексом. Цифры весьма позитивны: из 329 беременностей 258 (они были желанными) закончились родами. Частота спонтанного прерывания беременностей, индуцированных Достинексом, составила 9,1%, что соответствует средним показателям в популяции (10–15%). Полученные данные также свидетельствовали о том, что Достинекс не обладает тератогенным эффектом и не оказывает негативного влияния на здоровье матери. Несколько рекомендаций от эндокринологов. Для индукции овуляции у больных гиперпролактинемией рекомендуется использовать агонисты дофамина, которые следует отменить при наступлении беременности. Наличие ПРЛ-секретирующей аденомы не является показанием к искусственному прерыванию беременности, а всем беременным с гиперпролактинемией в анамнезе показано применение терапии гестагенами с момента диагностики беременности и до окончания первого триместра. Беременным с пролактиномами показано нейроофтальмологическое обследование 1 раз в 3 месяца. Роды у больных с гиперпролактинемией следует вести через родовые пути, наличие аденомы гипофиза не является показанием к кесареву сечению. Синдром гиперпролактинемии, независимо от генеза, не является показанием для подавления лактации. Пациентки с этим синдромом после родов должны находиться под систематическим наблюдением гинеколога и эндокринолога, им следует проводить магнитно-резонансную томографию головного мозга, а также необходимые гормональные исследования с определением уровня пролактина в сыворотке крови.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.