Алимта (пеметрексед) в лечении немелкоклеточного рака легкого III-IV стадии
- Аннотация
- Статья
- Ссылки

В последние годы появились противоопухолевые препараты, такие как таксол, таксотер, гемцитабин, навельбин, иринотекан, обладающие уникальным механизмом действия и достаточно высокой эффективностью при НМРЛ.
К ним следует отнести и новый многоцелевой антиметаболит из группы антифолатов – пеметрексед. Его появление вызвало большой интерес и открыло новые перспективы в лечении неоперабельных форм НМРЛ.
Алимта (пеметрексед) – новый противоопухолевый препарат, являющийся антагонистом фолатов, ингибирующим тимидилатсинтазу (TS), дигидрофолатредуктазу (DHFR) и глицинамидрибонуклеотидформилтрансферазу (GARFT), которые являются ключевыми фолат-зависимыми энзимами при биосинтезе тимидиновых и пуриновых нуклеотидов. Пеметрексед поступает в клетки с помощью переносчика восстановленных фолатов и белковых фолат-связывающих транспортных систем.
Поступая в клетку, Алимта быстро и эффективно превращается в полиглутаматные формы с помощью энзима фолилполиглутоматсинтетазы. Полиглутаматные формы задерживаются в клетках и являются более мощными ингибиторами тимидилатсинтазы и GARFT. Полиглутамация – это зависимый от времени и концентрации процесс, который встречается в опухолевых клетках и в меньшей степени – в нормальных тканях. У полиглутамированных метаболитов увеличен период полувыведения, вследствие чего увеличивается время действия препарата в опухолевых клетках. Таким образом, пеметрексед и его полиглутаматы (пеметрексед-Glu) конкурентно ингибируют ряд ключевых фолат-зависимых ферментов, вовлеченных в биосинтез ДНК и РНК (TS, DHFR и GARFT). Воздействуя на эти мишени, пеметрексед вызывает гибель опухолевых клеток.
Первоначально при лечении этим препаратом наблюдались случаи тяжелой, непредсказуемой и иногда фатальной токсичности (особенно миелосупрессивной и гастроинестинальной), которую связывали с дефицитом фолатов у больных.
Проведенный многофакторный анализ показал, что высокий уровень гомоцистеина и метилмалоновой кислоты в плазме коррелировали с возникновением нейтропении и диареи IV степени, что позволило предположить, что пониженные уровни фолиевой кислоты и витамина В12 могут способствовать развитию этих нежелательных явлений и возможному смертельному исходу из-за развития подобной токсичности. С целью снижения риска развития выраженной токсичности компанией Lilly было принято решение, что все больные, получающие Алимту, будут получать витамин В12 в виде внутримышечных инъекций в дозе 1000 мкг, начиная за 1-3 недели до лечения и продолжая в течение всего курса лечения через каждые три цикла и фолиевую кислоту ежедневно в низких дозах, равных 350-1000 мкг внутрь, начиная за 1-3 недели до лечения и продолжая в течение всего курса лечения и 3 недели после его окончания (1,2,19).
По результатам клинических исследований I фазы был выработан оптимальный режим применения пеметрекседа – 500 мг/м2 1 раз в 21 день (3). Также были проведены многочисленные исследования по изучению применения пеметрекседа в качестве монотерапии и в комбинации с препаратами платины в качестве первой линии лечения (6,7).
Алимта в I линии лечения
Было проведено 2 исследования II фазы, в которых изучались эффективность и токсичность Алимты в монорежиме у ранее не леченых пациентов с НМРЛ. У 4 из 8 пациентов с IIIВ стадией заболевания и у 3 из 25 с IV стадией была зарегистрирована частичная регрессия опухоли, общая эффективность составила 21,2% (4). Медиана выживаемости составила 3,8 месяца. Во втором исследовании из 57 пациентов объективный ответ был зарегистрирован у 9 (16%). Медиана выживаемости составила 8,4 месяца, медиана времени до прогрессирования – 5,6 месяца (5).
Платиносодержащие режимы комбинированной химиотерапии с включением Алимты
В исследованиях II фазы у больных НМРЛ изучались комбинации Алимты с цисплатином, карбоплатином и оксалиплатином.
Цисплатин + Алимта
У ранее не леченых пациентов Алимта вводилась в дозе 500 мг/м2, цисплатин – 75 мг/м2. В одном из исследований было включено 36 больных (с IIIB стадией – 18, с IV стадией – 18) (6). Общая эффективность составила 39%, медиана выживаемости – 10,9 месяца, 1-летняя выживаемость – 50%. Наиболее частыми проявлениями гематологической токсичности были нейтропения (21%) и анемия (5%) III-IV степени, негематологической – лихорадка II-III степени у 18 (50%) больных.
Во втором исследовании лечение проведено 31 пациенту (IIIB стадия – 5, IV – 26) (7). Общий эффект составил 45%. Медиана выживаемости – 8,9 мес., 1-летняя выживаемость – 49%. Наиболее частым проявлением негематологической токсичности была лихорадка II-III степени, отмечавшаяся у 21% пациентов. Из проявлений гематологической токсичности нейтропения III-IV степени выявлена у 11% больных, анемия III-IV степени – у 6%.
Карбоплатин или Оксалиплатин + Алимта
В исследование II фазы были включены 80 ранее не леченых больных с распространенным или метастатическим НМРЛ; рандомизация осуществлялась в две группы: в первой группе пеметрексед (500 мг/м2 на фоне витаминотерапии) применялся с карбоплатином AUC6, во второй – с оксалиплатином 120 мг/м2 1 раз в 3 недели. Объективный эффект в группе пеметрексед+карбоплатин были достигнуты у 31,6% больных, в группе пеметрексед+оксалиплатин – у 26,8% (различия не достоверны). В обеих группах медиана выживаемости составляла 10,5 месяца, медиана времени до прогрессирования в группе с оксалиплатином – 5,5 месяца, в группе с карбоплатином – 5,7 месяца (8).
В этом исследовании уровень тяжелой гематологической и негематологической токсичности был весьма умеренным по сравнению с результатами других исследований (9-12). Нейтропения III-IV степени выявлена у 7,3% больных в группе с оксалиплатином и 25,6% – в группе с карбоплатином. Самыми частыми проявлениями негематологической токсичности были рвота III степени – 7,3% в группе с оксалиплатином и лихорадка III степени – 7,7% в группе карбоплатина. Нейротоксичность как правило легкой и средней степени выраженности, чаще встречалась у больных, получавших оксалиплатин.
Неплатиновые комбинации – Винорельбин + Алимта
Алимта назначалась в дозе 500 мг/м2 в первый день на фоне введения фолиевой кислоты и витамина В12, винорельбин – 30 мг/м2 в 1,8 дни. Всего в исследование включено 35 больных. Полная регрессия была зарегистрирована у 1 больного, ЧР – у 12 больных. Объективный эффект составил 37,1%, медиана времени до прогрессирования – 3,8 месяца.
Наиболее частым проявлением гематологической токсичности была нейтропения. У 15 из 35 больных зарегистрирована нейтропения IV степени. Негематологическая токсичность III-IV степени в виде лихорадки отмечалась у 7 пациентов, одышка – у 5, тошнота – у 3 (13).
Гемцитабин + Алимта
Гемцитабин широко применяется при лечении НМРЛ как в монотерапии, так и в комбинациях с другими препаратами.
Adjei с соавт. (14) провели исследование II фазы по оценке комбинации Алимты и гемцитабина. Гемцитабин вводился по 1250 мг/м2 в 1 и 8 дни цикла, Алимта – 500 мг/м2 в восьмой день. Продолжительность цикла – 21 день. В исследование включено 53 больных. Частичная регрессия опухоли отмечена у 9 (17%) больных. Медиана продолжительности ремиссии составила 3,3 месяца. У 29 (54,7%) пациентов была достигнута стабилизация заболевания сроком 4 месяца и более. Медиана выживаемости составила 11,3 месяца, 1-летняя выживаемость – 44% (15). Чаще всего токсичность проявлялась в виде нейтропении (III степень – 29%, IV степень – 34%). Тромбоцитопения III степени отмечена у 5% больных. Наиболее частым видом негематологической токсичности была лихорадка III степени, отмечавшаяся у 23% больных. Несмотря на относительно невысокую непосредственную эффективность, эта комбинация характеризуется достаточно высокими уровнями общей и безрецидивной выживаемости и умеренной токсичностью. Эти параметры являются важными показателями эффективности лечения. Таким образом, схема Алимта+гемцитабин может использоваться как альтернативная при диссеминированном НМРЛ.
С появлением целого спектра противоопухолевых препаратов, эффективных при НМРЛ, встал вопрос о возможности и целесообразности проведения II линии химиотерапии при лекарственной резистентности опухоли, первичной или развивающейся в процессе лечения.
До последнего времени в качестве стандартной химиотерапии II линии, по результатам двух исследований III фазы (Tax 317 и Tax 320) был принят доцетаксел в дозе 75 мг/м2 и одобрен FDA и EMEA (16,17). Эффективность составила 6,7%, время до прогрессирования 2,1 мес., общая выживаемость – 5,7 мес., и 1-летняя выживаемость – 32%. Эти данные показали необходимость изучения новых противоопухолевых препаратов в качестве второй линии лечения НМРЛ.
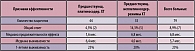
В различных клинических исследованиях по изучению противоопухолевой эффективности Алимты была показана достаточно хорошая ее переносимость. Препарат прошел исследования по II и III фазе в качестве второй линии химиотерапии. Препаратом сравнения был выбран доцетаксел в стандартном режиме. В рандомизированное исследование, проведенное Смитом и соавт. (18), был включен 81 пациент с прогрессированием на I линии лечения или с прогрессированием не более чем через 3 месяца после окончания лечения. Критериями включения являлись планируемая продолжительность жизни более 8 недель, наличие измеряемых очагов в двух проекциях, ECOG 0-1. Пациенты получали пеметрексед 500 мг/м2 в виде 10- минутной инфузии 1 раз в 21 день и были разделены по предшествующей терапии на платиносодержащие режимы (n=44) и неплатиносодержащие (n=35). Все пациенты получали премедикацию дексаметазоном раз в 12 часов, начиная за 24 часа до начала лечения с последующими четырьмя приемами после лечения. Во время проведения данного исследования назначение фолиевой кислоты и витамина В12 рутинно не применялось. В таблице 1 представлены результаты данного исследования. Частота ответа составила 8,9% Частота ответа была выше в группе пациентов, не получавших препараты платины (14,3% по сравнению с 4,5%), однако медиана выживаемости в этой группе составила всего 4 месяца по сравнению с 6,4 в группе с предшествующим лечением препаратами платины.
Из побочных явлений у 35% пациентов отмечалась нейтропения III-IV степени. Также было зарегистрировано 3 случая смерти от нейтропении, осложнившейся сепсисом. Пероральное профилактическое использование дексаметазона привело к снижению частоты появления сыпи III степени, которая было отмечена всего у 4 пациентов. Полученные положительные результаты II фазы инициировали дальнейшее проведение III фазы исследования по сравнению пеметрекседа и стандартного режима доцетаксела в качестве второй линии химиотерапии НМРЛ.
С марта 2001 года по февраль 2002 года Ханна и соавт. включили в регистрационное мультицентровое исследование по изучению пеметрекседа в качестве второй линии монотерапии НМРЛ 571 пациента, это на настоящий момент самое большое исследование III фазы (20). Пациенты получали пеметрексед 500 мг/м2 в/в или доцетаксел 75 мг/м2 в/в раз в 21 день. В группе пеметрекседа больным проводилась премедикация кортикостероидами и сопроводительная терапия фолиевой кислотой и витамином В12, в группе с доцетакселом только кортикостероиды. 90% пациентов ранее уже были пролечены препаратами платины, 28% получали таксаны. Задачей первичной оценки эффективности лечения была общая выживаемость, вторичной – различные виды токсичности, частота лечебного ответа, время до прогрессирования. Различий по эффективности в группах выявлено не было, данные представлены в таблице 2.
Медиана выживаемости составила 8,3 месяцев в группе пеметрекседа по сравнению с 7,9 месяцами в группе доцетаксела. Общий ответ составил 9,1% и 8,8% соответственно. Различий по уменьшению симптомов заболевания в двух группах также выявлено не было. Были выявлены статистически значимые преимущества по профилю токсичности при применении пеметрекседа. У пациентов, получавших доцетаксел, по сравнению с группой пеметрекседа, чаще отмечалась нейтропения III-IV степени (40,2% по сравнению с 5,3% р<0,001), фебрильная нейтропения (12,7% и 1,9%, соотв. р<0,001), инфекционные осложнения с фебрильной нейтропенией (3,3% и 0% соотв., р=0,004) и алопеция (37,7% и 6,4% соотв., р<0,001). И соответственно выше была потребность в применении КСФ в группе доцетаксела (19,2% и 2,6%, соотв. р<0,001). Частота внеплановых госпитализаций в связи с фебрильной нейтропенией или другими побочными явлениями была выше также в группе доцетаксела (13,4% и 1,5% р<0,001, 40,6% и 31,7%, р=0,092 соответственно). По данным проведенных исследований можно сделать вывод о высокой эффективности и низком профиле токсичности пеметрекседа по сравнению с доцетакселом в качестве второй линии лечения НМРЛ.
Заключение
Таким образом, на сегодняшний день Алимта (пеметрексед) новый мультитаргетный антифолат, кардинально отличающийся по механизму действия от большинства цитостатических препаратов, применяющихся в лечении НМРЛ. Отсутствие перекрестной резистентности дает большие преимущества при комбинировании пеметрекседа с другими препаратами и применения его как в качестве первой линии лечения, так и в качестве второй линии химиотерапии. По данным рандомизированного исследования (Ханна и соавт.), Алимта и доцетаксел в стандартном 3-недельном режиме показали одинаковую эффективность, однако пациенты в группе с Алимтой показали более низкий профиль гематологической и негематологической токсичности и соответственно более высокие показатели качества жизни. Назначение перорально фолиевой кислоты ежедневно и витамина В12 внутримышечно 1 раз в 9 недель, вне зависимости от уровня витаминов в сыворотке крови, позволило исследователям адекватно оценить эффективность и профиль токсичности данного режима. По полученным данным в 2004 году пеметрексед был одобрен FDA в качестве монотерапии второй линии химиотерапии НМРЛ и может считаться общепринятым стандартом лечения данной группы пациентов.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.