Анализ встречаемости аллергенов, вызывающих анафилаксию у детей, в разных регионах России
- Аннотация
- Статья
- Ссылки
- English
Цель – оценить частоту выявления анафилактогенов в России в зависимости от возраста больных и влияние аллергологического обследования на пищевые ограничения.
Материал и методы. Проведено онлайн-анкетирование 341 участника пациентских сообществ, у детей которых в анамнезе имели место острые тяжелые аллергические реакции на пищевые аллергены (анафилактогены) с вовлечением двух органов-мишеней и более.
Результаты. В исследуемой когорте (n = 341) преобладали мальчики – 59,8% (p < 0,05), соответственно девочек было 40,2%. Средний возраст больных составил 5 [3; 8] лет. В зависимости от возраста пациенты с анафилаксией были распределены следующим образом: до трех лет (включительно) – 33,1%, с четырех до шести лет (включительно) – 32,0%, с семи до 11 лет – 24,0%, 12 лет и старше – 10,9%. Клинические симптомы пищевой анафилаксии со стороны кожи отмечены у 90,3% детей, дыхательной системы – у 69,5%, желудочно-кишечного тракта – у 55,4%, сердечно-сосудистой системы и мозга – у 30,2%.
Согласно данным опроса, в России в перечень аллергенов, вызвавших анафилаксию, вошли молоко – 54,8%, яйца – 41,6%, рыба – 25,9%, древесные орехи – 23,8%, пшеница – 17,6%, другие морепродукты – 8,8%. Остальные аллергены были не установлены. Не употребляли из-за страха развития аллергической реакции молоко – 4,7%, яйца – 8,8%, пшеницу – 4,4%, рыбу – 19,7%, моллюски и креветки – 56,2%, древесные орехи – 37,0%.
Мультиплексные анализы достоверно повышали осведомленность об аллергенных триггерах и позволяли уменьшить количество пациентов, ограничивающих себя в питании. После проведения многокомпонентного теста резко снижалась частота неясных реакций на продукты, которые ранее не были введены в пищу: для морепродуктов – с 81,2 до 15,7%, для арахиса – с 79,7 до 18,8%, для древесных орехов – с 79,4 до 18,3% c достоверными различиями во всех случаях (p = 0,0001).
На показатели частоты использования мультиплексной молекулярной диагностики достоверно влиял возраст пациентов. Так, в возрасте от нуля до трех лет обследованы 16,9% детей, с четырех до шести лет – 39,4%, с семи до 11 лет – 32,4%, 12 лет и старше – 11,3% детей (p = 0,035). Обеспеченность пациентов адреналином составила 27,6%. Эпинефрин в ампулах был в наличии у 19,6%, в автоинъекторе – у 5,6%. Еще 2,4% не указали форму выпуска лекарства.
Выводы. В Российской Федерации анафилаксия остается плохо изученной проблемой. Спектр аллергенов существенно отличается от таковых в других странах. Существует потребность в более тщательном изучении региональных особенностей встречаемости анафилактогенов.
Использование мультиплексных тестов необходимо для диагностики причин острых анафилактических реакций и профилактики неоправданных пищевых ограничений.
Цель – оценить частоту выявления анафилактогенов в России в зависимости от возраста больных и влияние аллергологического обследования на пищевые ограничения.
Материал и методы. Проведено онлайн-анкетирование 341 участника пациентских сообществ, у детей которых в анамнезе имели место острые тяжелые аллергические реакции на пищевые аллергены (анафилактогены) с вовлечением двух органов-мишеней и более.
Результаты. В исследуемой когорте (n = 341) преобладали мальчики – 59,8% (p < 0,05), соответственно девочек было 40,2%. Средний возраст больных составил 5 [3; 8] лет. В зависимости от возраста пациенты с анафилаксией были распределены следующим образом: до трех лет (включительно) – 33,1%, с четырех до шести лет (включительно) – 32,0%, с семи до 11 лет – 24,0%, 12 лет и старше – 10,9%. Клинические симптомы пищевой анафилаксии со стороны кожи отмечены у 90,3% детей, дыхательной системы – у 69,5%, желудочно-кишечного тракта – у 55,4%, сердечно-сосудистой системы и мозга – у 30,2%.
Согласно данным опроса, в России в перечень аллергенов, вызвавших анафилаксию, вошли молоко – 54,8%, яйца – 41,6%, рыба – 25,9%, древесные орехи – 23,8%, пшеница – 17,6%, другие морепродукты – 8,8%. Остальные аллергены были не установлены. Не употребляли из-за страха развития аллергической реакции молоко – 4,7%, яйца – 8,8%, пшеницу – 4,4%, рыбу – 19,7%, моллюски и креветки – 56,2%, древесные орехи – 37,0%.
Мультиплексные анализы достоверно повышали осведомленность об аллергенных триггерах и позволяли уменьшить количество пациентов, ограничивающих себя в питании. После проведения многокомпонентного теста резко снижалась частота неясных реакций на продукты, которые ранее не были введены в пищу: для морепродуктов – с 81,2 до 15,7%, для арахиса – с 79,7 до 18,8%, для древесных орехов – с 79,4 до 18,3% c достоверными различиями во всех случаях (p = 0,0001).
На показатели частоты использования мультиплексной молекулярной диагностики достоверно влиял возраст пациентов. Так, в возрасте от нуля до трех лет обследованы 16,9% детей, с четырех до шести лет – 39,4%, с семи до 11 лет – 32,4%, 12 лет и старше – 11,3% детей (p = 0,035). Обеспеченность пациентов адреналином составила 27,6%. Эпинефрин в ампулах был в наличии у 19,6%, в автоинъекторе – у 5,6%. Еще 2,4% не указали форму выпуска лекарства.
Выводы. В Российской Федерации анафилаксия остается плохо изученной проблемой. Спектр аллергенов существенно отличается от таковых в других странах. Существует потребность в более тщательном изучении региональных особенностей встречаемости анафилактогенов.
Использование мультиплексных тестов необходимо для диагностики причин острых анафилактических реакций и профилактики неоправданных пищевых ограничений.


Введение
Анафилаксия представляет серьезную угрозу жизни. В настоящее время эта проблема охватывает все больше взрослых и детей в разных регионах мира. Кроме того, повышается частота встречаемости анафилаксии в раннем детском возрасте [1].
Глобальная заболеваемость анафилаксией составляет от 50 до 112 на 100 тыс. человеко-лет, в течение жизни – от 0,3 до 5,1% [2]. Разброс данных о распространенности анафилаксии в мире зависит от региональных особенностей ее учета, а также используемого определения анафилаксии.
Причинами анафилаксии могут быть многие виды аллергенов. В педиатрии лидерство принадлежит пищевым аллергенам.
Спектр аллергенов, вызвавших анафилаксию, может различаться в зависимости от возраста, страны проживания и, видимо, от особенностей питания семьи [3].
Первичная заболеваемость в Европе составляет 1,5–7,9 на 100 тыс. человек в год. Согласно данным метаанализа, проведенного экспертами Европейской академии аллергологии и клинической иммунологии (European Academy of Allergy and Clinical Immunology – EAACI), распространенность анафилаксии у детей достигает 0,1%. Максимальный прирост заболеваемости (314 на 100 тыс. человек в год) был выявлен в возрастной группе до четырех лет. Установлено, что 0,3% лиц в какой-то момент жизни будут испытывать анафилаксию [4].
Официальные данные о распространенности анафилаксии в России отсутствуют. При кодировании анафилаксии без развития шокового состояния в зависимости от преимущественных симптомов тяжелой аллергической реакции могут использоваться такие диагнозы, как аллергическая крапивница (код L50.0 по Международной классификации болезней десятого пересмотра), ангиоотек с шоком или без него (код T78.0-4), аллергический дерматит в разных сочетаниях (коды L20, L27.2, L23.6, L24.6 и L25.4), нежелательные реакции на пищу, обострение бронхиальной астмы (код J45), аллергический гастроэнтерит (код K52.2). Указанные коды не включаются в отчет Минздрава России и не могут быть предоставлены для анализа. Следовательно, проблема анафилаксии не актуализирована и маскируется под другие заболевания, ее исследования носят несистемный характер [5].
Собственный опыт свидетельствует о том, что частота встречаемости анафилаксии в России увеличивается. Согласно результатам обследования 79 детей c атопическим дерматитом в возрасте до двух лет, о симптомах пищевой анафилаксии сообщалось в 6,3% случаев [6].
В зарубежной литературе указывается, что смертность от пищевой анафилаксии составляет 0,03–0,32 случая на 1 млн человеко-лет [2, 4]. Согласно отечественным источникам, от анафилаксии при аллергии на пищу умирает меньше пациентов, чем при лекарственной аллергии, но в семь раз больше, чем при аллергии на укусы насекомых. Пищевые аллергены становятся причиной тяжелых реакций примерно у трети госпитализированных в стационар по поводу анафилаксии [5].
Своевременное выявление аллергена необходимо для профилактики острых реакций после контакта с аллергеном, напротив, раннее введение продуктов в пищу стимулирует развитие толерантности и предотвращает новые случаи аллергии [7]. В связи с упомянутыми фактами необходимы: более тщательное изучение проблемы анафилаксии, разработка эффективных методов профилактики острых реакций, стимулирование толерантности путем ранней интервенции пищевых продуктов.
Целью настоящей работы стала оценка частоты выявления анафилактогенов в России в зависимости от возраста пациентов и влияния аллергологического обследования на пищевые ограничения.
Материал и методы
Обсервационное исследование выполнено одномоментным способом. Проведено онлайн-анкетирование родителей (опекунов) детей с тяжелыми аллергическими реакциями на пищу из всех регионов России.
В опросе участвовали члены пациентских сообществ «Аллергомамы», «Дети на диете», «Pro_dermatit», посчитавших, что у их детей были тяжелые пищевые реакции.
После проведения анализа ответов выбраны дети с острыми тяжелыми реакциями на пищевые аллергены, согласно критериям анафилаксии Всемирной организации по борьбе с аллергией (World Allergy Organization – WAO).
Опросник для родителей (опекунов) содержал вопросы, касающиеся клинической картины анафилаксии, триггерных аллергенов и обеспеченности адреналином.
Опрос проводился с помощью сервиса Yandex Forms.
Статистическая обработка данных выполнена в JASP [8].
Ограничения исследования
Среди ограничений исследования следует отметить включение детей с сохраняющейся анафилаксией, отсутствие данных о детях, выработавших толерантность, меньшее количество родителей старших школьников, что может быть связано как с переносимостью аллергена, так и с тем, что они не являются активными пользователями форумов (выборка из пользователей социальной сети для пациентов).
Результаты
Из 392 респондентов были отобраны лица с достоверно тяжелыми реакциями на пищу с вовлечением двух и более систем организма.
По результатам анкетирования, количество детей с вероятной по критериям WAO анафилаксией составило 341.
В нашей выборке достоверно преобладали лица мужского пола. Так, мальчиков было 59,8%, девочек – 40,2%. Тест χ2 больше критического значения, p < 0,05.
В разных возрастных группах соотношение мальчиков и девочек было следующим: среди детей от нуля до трех лет – 51,3 vs 48,7%, с четырех до шести лет – 62,4 vs 37,6%, с семи до 11 лет – 63,4 vs 36,6, 12 лет и старше – 70,3 vs 29,7%. Во всех возрастных группах отмечалось преобладание лиц мужского пола с трендом на увеличение различий.
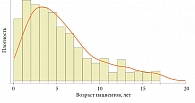
Возрастные особенности анафилаксии в общей группе прослеживались довольно четко. Основное количество пациентов – дети дошкольного возраста. Большинство (72,4%) респондентов на момент заполнения анкеты указали возраст ребенка с анафилаксией до семи лет. Распределение пациентов асимметричное, смещено влево к первому году жизни.
Средний возраст больных на момент опроса составил 5,7 ± 3,9 года, медиана – 5 [3; 8] лет.
Плотность распределения по возрасту представлена на рисунке. До пяти лет распространенность анафилаксии в выборке была примерно одинаковой, с увеличением возраста наблюдалось снижение встречаемости заболевания.
При категоризации пациентов по возрасту с шагом три года получены четыре группы. Деление выбрано по социальным показаниям: в три года дети поступают в детский сад, в семь лет – в школу, в 12 лет становятся старшими школьниками.
В нашей когорте распределение пациентов с анафилаксией выглядело следующим образом: от нуля до трех лет (включительно) – 33,1%, с четырех до шести лет – 32,0%, с семи до 11 лет – 24,0%, 12 лет и старше – 10,9%.
Клиническая картина
Симптомокомплекс анафилаксии включает поражение сразу нескольких органов-мишеней. Поскольку внезапная пищевая реакция обычно происходит вне медицинского наблюдения, справедливо ожидать, что родители смогут заметить только явные, сильные симптомы. Рассмотрим преимущественный клинический фенотип анафилаксии с поправкой на это допущение.
Кожные проявления в виде крапивницы и ангиоотека отметили 90,3%. Вторым по частоте ответом были респираторные нарушения – 69,5%. При острых аллергических болезнях родители фиксировали у детей кашель, свистящие хрипы или удушье. Третьими по значимости и частоте встречаемости стали симптомы со стороны пищеварительного тракта. Путь попадания анафилактогена в организм объясняет высокую частоту поражения органов пищеварения. Жалобы со стороны желудочно-кишечного тракта (ЖКТ) в виде рвоты, боли в животе, изменения стула отметили 55,4% опрошенных.
Возможность элиминации аллергена в виде рвоты, перемешивание с другой пищей, воздействие пищеварительных ферментов и барьерные свойства эпителия ЖКТ препятствуют попаданию аллергена в кровь, его быстрому распространению и развитию общих системных реакций. В поддержание этой гипотезы следует отметить, что сердечно-сосудистые проявления встречались значительно реже, особенно с учетом того, что обязательным критерием выставления диагноза «шок» является значимое снижение артериального давления. Вопрос об измерении давления в момент анафилаксии не задавался, так как дома обычно отсутствуют тонометры с детскими манжетами.
Симптомы поражения сердечно-сосудистой системы в виде снижения давления, вялости, бледности, нарушения работы сердца суммарно указали 22,6%. Симптоматика со стороны центральной нервной системы, проявляющаяся головной болью, снижением или потерей сознания, головокружением, судорогами, по мнению родителей, отмечалась у 7,6% детей.
Разделить мозговую симптоматику и снижение давления сложно. В патогенезе судорог и обморока при анафилаксии могут наблюдаться сочетанные нарушения. Рецепторы к гистамину представлены в центральной нервной системе, однако велика роль и нарушения мозгового кровообращения вследствие прямого спазма сосудов головного мозга и системной гипотонии [9]. При объединении групп пациентов с условными симптомами поражения центральной нервной и сердечно-сосудистой систем суммарно треть (30,2%) опрошенных отметили указанные выше жалобы.
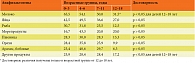
Распределение симптомов анафилаксии по разным возрастным группам представлено в табл. 1. Так, во всех возрастных группах частота встречаемости разных проявлений анафилаксии примерно одинаковая, за исключением мозговой симптоматики, которая чаще встречалась у подростков (p < 0,05).
Аллергены, вызывающие анафилаксию
Традиционно считается, что основными анафилактогенами являются арахис, орехи, морепродукты, молоко, яйца, рыба. Ограничением опроса стало то, что достоверно родители могут указывать аллергены, на которые произошла реакция, однако если продукт еще не был введен, он находится в зоне риска реакции («серой зоне»). Поэтому мы просили особо указать продукты, которые не были введены в пищу по причине страха анафилаксии.
В группе опрошенных произошедшую анафилаксию на молоко отметили 54,8%, еще 4,7% боялись давать детям молочные продукты.
Анафилаксия на яйца указана 41,6% опрошенных. При этом еще 8,8% отнесли этот аллерген к «серой зоне», так как их дети не пробовали пищу, содержащую куриные яйца.
Рыба была релевантным аллергеном для 25,9%, аллергеном «серой зоны» для 19,7%. Остальные морепродукты (ракообразные и моллюски) указали как триггер 8,8%, опасались вводить их в рацион 56,2%. Это самый высокий показатель в нашем опросе.
Пшеница как триггер тяжелых реакций встречалась в 17,6% ответов. Не использовали глютеносодержащие продукты и не знали о реакции на них только 4,4%.
Бобовые и орехи в качестве триггера острых реакций отметило меньшее число опрошенных. Однако величина «серой зоны» в отношении данных аллергенов оказалась выше. Арахис в качестве причины пищевой анафилаксии указали 18,8% респондентов. Опасения по поводу употребления этого продукта выразили 40,6%. Древесные орехи (фундук, миндаль, кешью, фисташка и др.) вызывали анафилаксию у 23,8% детей. Возможность развития такой реакции у детей и, следовательно, опасения по поводу введения орехов в пищу отметили 37,0% респондентов.
Полная информация о триггерах анафилаксии в разных возрастных группах представлена в табл. 2.
Пищевые аллергены, которые находятся в «серой зоне», – важная проблема, снижающая качество жизни пациентов. Под данным термином мы понимаем аллергены продуктов, которые ранее не употреблялись. Возможные реакции пациента на эти продукты неясны, оценить их частоту без обследования или пробного кормления невозможно. Игнорирование аллергенов «серой зоны» может существенно исказить итоговую структуру встречаемости аллергенов.
При опросе установлено, что часто употребляемые продукты (молоко, яйца, пшеница) не представляли сложности в отношении выявляемости реакций на них. В среднем около 5% респондентов не определились в отношении реакции на эти аллергены. Редко употребляемые аллергены (орехи и морепродукты) были причиной опасений в значительном числе случаев (табл. 3).
В ходе опроса также уточнялось, сколько пациентов получили полноценное обследование с помощью мультиплексных анализов (аллергочипа), охватывающих большое количество предполагаемых аллергенов.
Установлено, что молекулярную диагностику прошли только 20,8% пациентов. В связи с неполной диагностикой у большинства больных оставались сомнения о возможности употребления в пищу статистически часто выявляемых в качестве аллергенов продуктов.
Введение в план обследования мультиплексных анализов резко повышало качество диагностики. Согласно данным опроса, после их проведения резко снизилась частота неясных реакций на продукты, которые ранее не были введены в пищу: для морепродуктов – с 81,2 до 15,7%, для арахиса – с 79,7 до 18,8%, для древесных орехов – с 79,4 до 18,3% c достоверными различиями во всех случаях (p = 0,0001).
Возраст достоверно влиял на показатели частоты использования мультиплексных анализов. Так, в возрасте до трех лет с помощью аллергочипа обследованы 16,9% детей, с четырех до шести лет – 39,4%, с семи до 11 лет – 32,4%, 12 лет и старше – 11,3% детей (p = 0,035). Небольшая частота обследованных в возрасте до трех лет и старше 11 лет может быть связана с тем, что в раннем возрасте обычно используют другие методы диагностики, а у подростков заболевание было диагностировано до широкого распространения мультиплексных анализов.
Обеспеченность адреналином
Обеспеченность адреналином больных пищевой анафилаксией в Российской Федерации остается низкой. Так, у 27,6% пациентов от всех опрошенных был препарат эпинефрина: в ампулах (19,6%), в автоинъекторе (5,6%). Остальные 2,4% не указали лекарственную форму. Следует отметить, что эпинефрин, препарат Эпиджект® (производство MEDA, Epiject®), зарегистрирован в РФ, но официально не продается.
Максимальная обеспеченность адреналином наблюдалась в дошкольном возрасте. Так, им были обеспечены 18 детей в возрасте от нуля до трех лет, 32 ребенка в возрасте от четырех до шести лет, 29 детей от семи до 11 лет, восемь детей в возрасте 12 лет и старше.
Обсуждение результатов
Данные европейского регистра NORA свидетельствуют о том, что в Европе анафилактические реакции выявляются и учитываются лучше. В России на момент написания статьи не было действующего регистра тяжелой пищевой аллергии и анафилаксии.
В нашем исследовании основную часть пациентов составляли дети раннего возраста. В Европе наблюдается похожая ситуация – среди пациентов преобладают дети дошкольного возраста [10]. В Японии зафиксирован еще больший возрастной сдвиг в сторону больных трех-четырех лет [11]. На такое разделение анафилаксии по возрастам могут влиять ряд факторов. Помимо естественно вытекающей гипотезы о возрастающей заболеваемости детей на такое распределение могут влиять механизмы формирования толерантности. Так, пищевая аллергия склонна к угасанию с течением времени [12]. По мнению пациентов, к 12 годам молоко, яйца и пшеница как причины анафилаксии встречаются несколько реже. Однако следует учитывать, что оральная провокация этим детям не проводилась. Поэтому определить, в каком возрасте и у какой доли детей реально не выработалась толерантность, невозможно. Очевидно, неуточненная часть пациентов сохраняла пищевые привычки элиминации аллергена и не собиралась вводить его в рацион. Подобный подход характерен не только для России, но и для европейских стран.
Некоторые авторы относят к анафилаксии исключительно состояния, при которых артериальное давление снижается более чем на 30%, не разделяя таким образом понятия «анафилаксия» (острая системная аллергическая реакция с вовлечением двух систем организма и более) и «анафилактический шок» (системная аллергическая реакция с обязательным нарушением гемодинамики), что приводит к неточностям в статистике, диагностике и подходах к лечению [13].
Родителям сложно оценить степень острой гипотензии при аллергических реакциях. В отличие от термометров тонометры с детскими манжетами практически не встречаются в быту, поэтому доказательства снижения давления до осмотра врача всегда будут иметь косвенный характер. Известен подход Брайтоновской коллаборации по анафилаксии, когда клинические признаки анафилаксии разделяются на уровни с первого по пятый (симптомы выстроены от более вероятных реакций к сомнительным). Согласно данному правилу, вовлечение двух из четырех систем может свидетельствовать о достоверном наличии именно системной аллергической реакции [14]. Основываясь на рекомендациях WAO и EAACI, полагаем, что все острые системные реакции с вовлечением любых двух систем организма нужно считать потенциально угрожающими жизни, поскольку степень тяжести реакции зависит от принятой дозы аллергена и нарушение гемодинамики может проявиться спустя некоторое время после всасывания аллергена [15]. Определение триптазы является дополнительным критерием заболевания. Однако оно не получило широкого распространения в РФ, поскольку значимо в первые часы после заболевания и сложно выполнимо в условиях реальной клинической практики [16].
В клинической картине анафилаксии у детей всех возрастных групп преобладали кожные и респираторные реакции. Наиболее редко регистрировались сердечно-сосудистые осложнения. Полученные нами результаты поддерживают утверждение о преобладании кожных форм при развитии анафилаксии и акцентируют внимание на важности симптомов со стороны ЖКТ и органов дыхания. Симптомы со стороны ЖКТ, как правило рвота, помогают элиминировать аллерген из организма. Непрямое попадание аллергена на барьерные ткани, активность протеолитических ферментов ЖКТ могут объяснять меньшую частоту смертельных случаев при возникновении пищевой анафилаксии по сравнению с инсектной, лекарственной [17]. Практическая значимость полученных результатов заключается в том, что знание преобладающих типичных симптомов пищевой анафилаксии позволит своевременно распознать состояние.
Новым является преобладание мальчиков в исследуемой когорте. Однако выборка не позволяет сделать однозначные выводы о преобладании лиц мужского пола среди генеральной популяции с педиатрической анафилаксией. Противоположные результаты получены у взрослых. Согласно данным L. Salvati и соавт., тяжелая пищевая и лекарственная аллергия была более характерна для женщин [18]. В работе M. Somiya и соавт. среди тех, у кого развилась лекарственная анафилаксия на вакцины против COVID-19, также преобладали женщины – 88,1–94,0% [19]. W. Chen и соавт. предположили, что гормональная дисрегуляция у половозрелых женщин может быть причиной более частого и тяжелого течения заболевания [20]. Эстрогены способствуют активации тучных клеток и аллергической сенсибилизации, прогестерон подавляет выброс гистамина, но поддерживает синтез иммуноглобулина E. Напротив, мужские половые гормоны (дегидроэпиандростерон) являются антагонистами Th2-ответа [20]. В детском возрасте влияние женских половых гормонов минимально. При анализе факторов риска смертельного исхода при анафилаксии P.J. Turner и соавт. выявили, что лица мужского пола умирали чаще, в том числе дети [21]. Согласно данным общего регистра анафилаксии, проанализированным W. Francuzik и соавт., в Европе в допубертатном периоде половых различий не отмечено, после такового более тяжелые реакции фиксировались у мужчин [22]. Данный вопрос требует дальнейшего изучения, особенно в отношении влияния взросления и физиологических изменений иммунной системы на формирование толерантности [23]. Нами установлено, что с возрастом частота анафилаксии имеет тенденцию к снижению, поэтому роль пубертатных гормональных изменений представляет определенный научный интерес.
Важным компонентом управления риском возникновения анафилаксии является точная аллергологическая диагностика. Развитие аллергии предотвращает своевременное введение продуктов, позволяющее сформироваться ранней естественной толерантности к аллергенам [24]. Оптимальная стратегия при назначении диетических рекомендаций таким пациентам – исключение только причинно-значимого аллергена и адекватное употребление других продуктов. Статистические вероятности частоты встречаемости аллергии не должны быть основанием для исключения продукта.
В нашем исследовании 2022 г. оценивалось сочетание пищевой аллергии, анафилаксии и атопического дерматита у детей раннего возраста. В качестве триггера пищевых реакций преобладали яйца [6]. В настоящей работе достоверно чаще других аллергенов встречалось молоко. Ведущая роль молока и яиц обусловлена частым употреблением этих продуктов в российских семьях, что приводит к ингаляционным и трансэпидермальным путям сенсибилизации у детей [25]. По этой же причине минимальна роль арахиса. В России это бобовое редко используется в кулинарии и употребляется в целом виде в отличие от США, где популярны паста и масло из арахиса. Редкость анафилаксии на бобовые и арахис является региональной особенностью и новой информацией, полученной при изучении аллергенов, вызывающих анафилаксию.
Особый интерес представляет вопрос целесообразности использования мультиплексных анализов при анафилаксии. Согласно нашим данным, пациенты, как правило, сенсибилизированы более чем к одному аллергену [5, 6, 25].
Подход, при котором назначается широкий спектр диагностических исследований, способствует выявлению редких аллергенных триггеров [26]. Большое значение имеют отрицательные результаты. Отсутствие гиперчувствительности при определении специфического иммуноглобулина E и/или при кожном тестировании позволяет исключить реакции немедленного типа с высокой степенью достоверности, а значит, провести безопасное пробное кормление и введение продукта в рацион [27]. Полученные нами данные свидетельствуют, что выполнившие обследование реже ограничивали свой рацион. Такой подход позволяет использовать диагностику пищевой аллергии как элемент направленной стратегии и разрабатывать безопасную диету для пациентов. В случае выявления анафилаксии на один продукт авторы рекомендуют обследовать больных на полный спектр наиболее часто встречающихся аллергенов. После получения отрицательных результатов необходимо как можно быстрее вводить частые аллергены в пищу с соблюдением норм безопасности.
В настоящем исследовании установлен факт низкой обеспеченности адреналином в России – около 28%.
Со стороны врачей существуют необъективные препятствия к назначению эпинефрина. Так, согласно данным D. Munblit и соавт., только 10% врачей, опрошенных в РФ, были готовы назначить этот препарат [28]. Обеспеченность адреналином в мире варьируется в зависимости от региона. Она наиболее высока в странах США и Европы, в которых отмечается повышенная частота встречаемости анафилаксии. Так, после выписки из отделения неотложной помощи более половины больных получают рекомендацию по использованию эпинефрина [29]. Объективная недоступность в стране автоинъектора с эпинефрином препятствует самостоятельному оказанию помощи при анафилаксии и, как следствие, повышает риск смертельного исхода.
Наличие у 6% пациентов из нашей выборки автоинъекторов, вероятно, связано с ввозом этих медицинских девайсов из других стран.
Заключение
Анафилаксия является значимой проблемой педиатрической практики по причине роста распространенности и возможности смертельного исхода. Врачи должны быть осведомлены об особенностях клинической картины анафилаксии у детей и учитывать относительную редкость сердечно-сосудистых осложнений. У детей очень часто кожные проявления сочетаются с респираторной симптоматикой и рвотой (спастической болью в животе).
Наиболее распространенными пищевыми аллергенами в РФ являются молоко, яйца, рыба, пшеница и древесные орехи.
Проблема анафилаксии не актуализирована для здравоохранения РФ. Пациенты не получают информации о пищевой аллергии, ее прогнозах и доказанных диетических и клинических рекомендациях. Отмечаются тотальная необеспеченность пациентов адреналином, отсутствие современных методов обследования.
Благодарность
Выражаем благодарность Е. Савковской, Н. Гоцелюк, Ю. Прищепе, Т. Зверевой, И. Калининой и всем участникам сообществ «Аллергомамы», «Дети на диете» и «Pro_dermatit».
S.S. Masalskiy, PhD, Yu.S. Smolkin, MD, PhD, Prof.
Medical University ‘Reaviz’, Moscow
Academy of Postgraduate Education of the Federal Scientific and Clinical Center of the Federal Medical-Biological Agency
Contact person: Sergey S. Masalskiy, masalsky@live.com
The prevalence of anaphylaxis in the Russian Federation and its allergenic triggers are poorly studied. Regional characteristics of the allergen spectrum determine differences in its manifestation.
Objective – to evaluate the frequency of detection of anaphylactogens in Russia depending on the age of patients and the impact of allergological examination on dietary restrictions.
Material and methods. Survey of 341 participants of patient communities (online) with a history of acute severe allergic reactions to food allergens (anaphylactogens) involving 2 or more target organs.
Results. In the study cohort (n = 341), boys accounted for 59.8% (p < 0.05). Accordingly, there were 40.2% girls.
The median age of all children was 5 [3; 8] years. The age profile of patients with anaphylaxis: under 3 years of age – 33.1%, from 3 to 6 years – 32.0%, from 7 to 11 years – 24.0%, from 11 years and older – 10.9%.
Clinical signs of food anaphylaxis in children are characterized by: skin symptoms – 90.3%, respiratory system – 69.5%, gastrointestinal tract – 55.4%, cardiovascular and cerebral symptoms in summary – 30.2%.
Spectrum of sensitization in the Russian Federation according to the survey: milk – 54.8%, egg – 41.6%, fish – 25.9%, tree nuts – 23.8%, wheat – 17.6%, other seafood – 8.8%. Foods excluded from the diet and not consumed due to fear of reaction: milk – 4.7%, egg – 8.8%, wheat – 4.4%, fish – 19.7%, shellfish and shrimp – 56.2%, tree nuts – 37.0%. The use of multiplex testing reliably increases awareness of allergenic triggers and reduces the number of patients who restrict their diet. Following the allergy blood test, the incidence of unclear reactions to foods to the diet decreased dramatically: for seafood – from 81.2 to 15.7%, for peanuts – from 79.7 to 18.8%, for tree nuts – from 79.4 to 18.3% c significant differences in all cases (p = 0.0001).
Age significantly influenced the frequency of multiplex molecular diagnostics: 16.9% of children under 3 years of age, 39.4% of children 4–7 years of age, 32.4% of children 7–11 years of age, and 11.3% of children over 12 years of age (p = 0.035).
Epinephrine availability among patients was 27,6%. 19.6% had epinephrine in the form of ampules and 5.6% had epinephrine in the form of autoinjector.
Conclusions. Anaphylaxis in the Russian Federation remains a poorly studied problem. The spectrum of allergens differs significantly from other regions of the world. There is an urgent need for a more thorough study of regional variations in the occurrence of anaphylactogens. The use of multiplex tests is necessary to diagnose the causes of acute anaphylactic reactions and to prevent unjustified food restrictions.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.